文档内容
长沙市 2023 年新高考适应性考试
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写
在答题卡上,写在本试卷上无效。
3.考试结束后,将本试题卷和答题卡一并交回。
一、选择题:本题共 10 小题,每小题 3 分,共30 分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.湖南省有众多国家级非物质文化遗产,如湘绣、醴陵彩瓷、苗银锻造工艺、安化黑
茶等。下列说法错误的是( )
A.技艺精湛的湘绣,绣线分为丝线、绒线、织花线、金银线等,其中丝线的主要成
分是蛋白质
B.陶瓷的生产以黏土和石灰石为主要原料
C.苗族银饰锻制工艺需要使用较多的银质材料,银质材料在常温下化学性质比较稳定
D.安化黑茶制作中的发酵工序涉及了氧化还原反应
2.下列化学用语或图示表达不正确的是( )
A.原子核内中子数为20的氯原子20Cl B.H O的VSEPR模型
17 2
C.二氧化碳的电子式: D.p-pπ键电子云轮廓图
3.下列实验装置、试剂选用或操作正确的是( )
1 2 3 4
A.用图1所示装置制备并干燥收集NH
3
B.用图2所示装置收集SO
2
C.用图3所示装置制备氢氧化铁胶体
D.用图4所示装置除去CO气体中的CO
2
化学试题第1页(共8页)4.下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子
方程式正确的是( )
选项 离子组 加入试剂 加入试剂后发生的离子反应
A Fe2+、NO、NH NaHSO 3Fe2++NO+4H+=3Fe3++NO+2HO
3 4 4 3 2
B Ca2+、HCO、Cl 少量NaOH Ca2++2HCO+2OH=2HO+CaCO + CO2
3 3 2 3 3
C K+、HCO、AlO 通入少量CO 2AlO+3HO+ CO =2AlOH + CO2
3 2 2 2 2 2 3 3
D NH、Al3+、SO2 少量BaOH 2NH+ SO2+Ba2++2OH-=2NH HO+ BaSO
4 4 2 4 4 3 2 4
A.A B.B C.C D.D
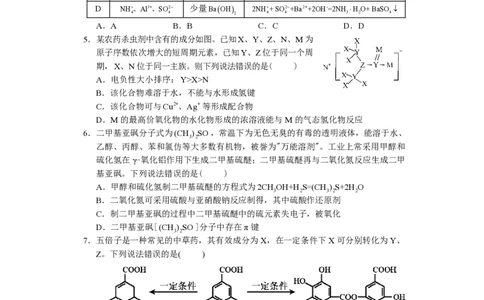
5.某农药杀虫剂中含有的成分如图。已知X、Y、Z、N、M为
原子序数依次增大的短周期元素,已知Y、Z位于同一个周
期,X、N位于同一主族。则下列说法错误的是( )
A.电负性大小排序:Y>X>N
B.该化合物难溶于水,不能与水形成氢键
C.该化合物可与Cu2+、Ag+等形成配合物
D.M的最高价氧化物的水化物形成的浓溶液能与M的气态氢化物反应
6.二甲基亚砜分子式为(CH ) SO,常温下为无色无臭的有毒的透明液体,能溶于水、
3 2
乙醇、丙醇、苯和氯仿等大多数有机物,被誉为"万能溶剂"。工业上常采用甲醇和
硫化氢在 γ-氧化铝作用下生成二甲基硫醚;二甲基硫醚再与二氧化氮反应生成二甲
基亚砜。下列说法错误的是( )
A.甲醇和硫化氢制二甲基硫醚的方程式为2CH OH+H S=(CH ) S+2H O
3 2 3 2 2
B.二氧化氮可采用硫酸与亚硝酸钠反应制得,其中硫酸作还原剂
C.制二甲基亚砜的过程中二甲基硫醚中的硫元素失电子,被氧化
D.二甲基亚砜[(CH ) SO]分子中存在π键
3 2
7.五倍子是一种常见的中草药,其有效成分为X,在一定条件下X可分别转化为Y、
Z。下列说法错误的是( )
A.不能用酸性KMnO 鉴别X和Y
4
B.Y可以和水形成氢键
C.Z中所有碳原子不一定在同一平面上
D.1molZ与NaOH溶液反应时,最多可消耗7molNaOH
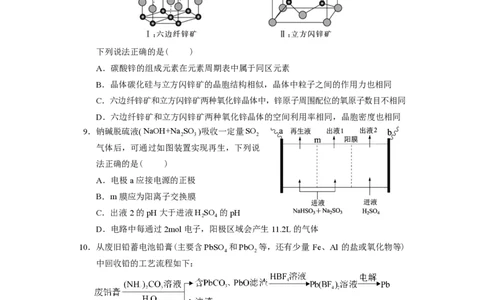
化学试题第2页(共8页)8.医学上利用碳酸锌(ZnCO )为原料,通过热分解来制备氧化锌,同时产生CO 。氧
3 2
化锌有六边纤锌矿和立方闪锌矿两种常见晶体结构,晶胞结构如图所示。
下列说法正确的是( )
A.碳酸锌的组成元素在元素周期表中属于同区元素
B.晶体碳化硅与立方闪锌矿的晶胞结构相似,晶体中粒子之间的作用力也相同
C.六边纤锌矿和立方闪锌矿两种氧化锌晶体中,锌原子周围配位的氧原子数目不相同
D.六边纤锌矿和立方闪锌矿两种氧化锌晶体的空间利用率相同,晶胞密度也相同
9.钠碱脱硫液(NaOH+Na SO )吸收一定量SO
2 3 2
气体后,可通过如图装置实现再生,下列说
法正确的是( )
A.电极a应接电源的正极
B.m膜应为阳离子交换膜
C.出液2的pH大于进液H SO 的pH
2 4
D.电路中每通过2mol电子,阳极区域会产生11.2L的气体
10.从废旧铅蓄电池铅膏(主要含PbSO 和PbO 等,还有少量 Fe、Al 的盐或氧化物等)
4 2
中回收铅的工艺流程如下:
下列说法正确的是( )
A.PbSO 和(NH ) CO 溶液反应的离子方程式:Pb2 CO2 PbCO
4 4 2 3 3 3
B.H O 的主要作用是作氧化剂,氧化Fe2+
2 2
C.对于BF离子,其中心原子的杂化方式为sp2
4
D.电解时,阳极、阴极材料可分别用石墨、铅
化学试题第3页(共8页)二、选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一个或
两个选项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
11.偶联反应(布赫瓦尔德-哈特维希反应)是合成芳胺的重要方法,反应机理如图(图中
Ar表示芳香烃基, 表示为副反应)。下列说法正确的是( )
A.该变化过程中涉及到的有机反应类型仅限于取代和加成反应
B.该体系中3、5和8都是中间体
C.理论上1 mol 最多能消耗1mol
D.若原料用 和 ,则可能得到的产物为 、 和
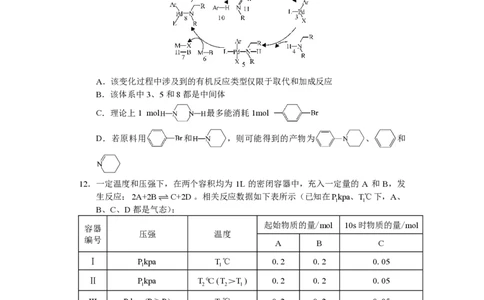
12.一定温度和压强下,在两个容积均为 1L 的密闭容器中,充入一定量的 A 和 B,发
生反应:2A+2BC+2D。相关反应数据如下表所示(已知在Pkpa、T℃下,A、
1 1
B、C、D都是气态):
起始物质的量/mol 10s时物质的量/mol
容器
压强 温度
编号
A B C
Ⅰ Pkpa T℃ 0.2 0.2 0.05
1 1
Ⅱ Pkpa T ℃ (T>T ) 0.2 0.2 0.05
1 2 2 1
III Pkpa (P>P) T℃ 0.2 0.2 0.05
2 2 1 1
下列说法正确的是( )
A.该反应的H>0
B.在容器III中,A、B中至少有一种呈非气态
C.10s时,容器Ⅱ中的反应一定处于平衡状态
D.若起始时,向容器Ⅱ中充入0.08molA、0.1molB、0.04molC和0.1molD,反应
将向正反应方向进行
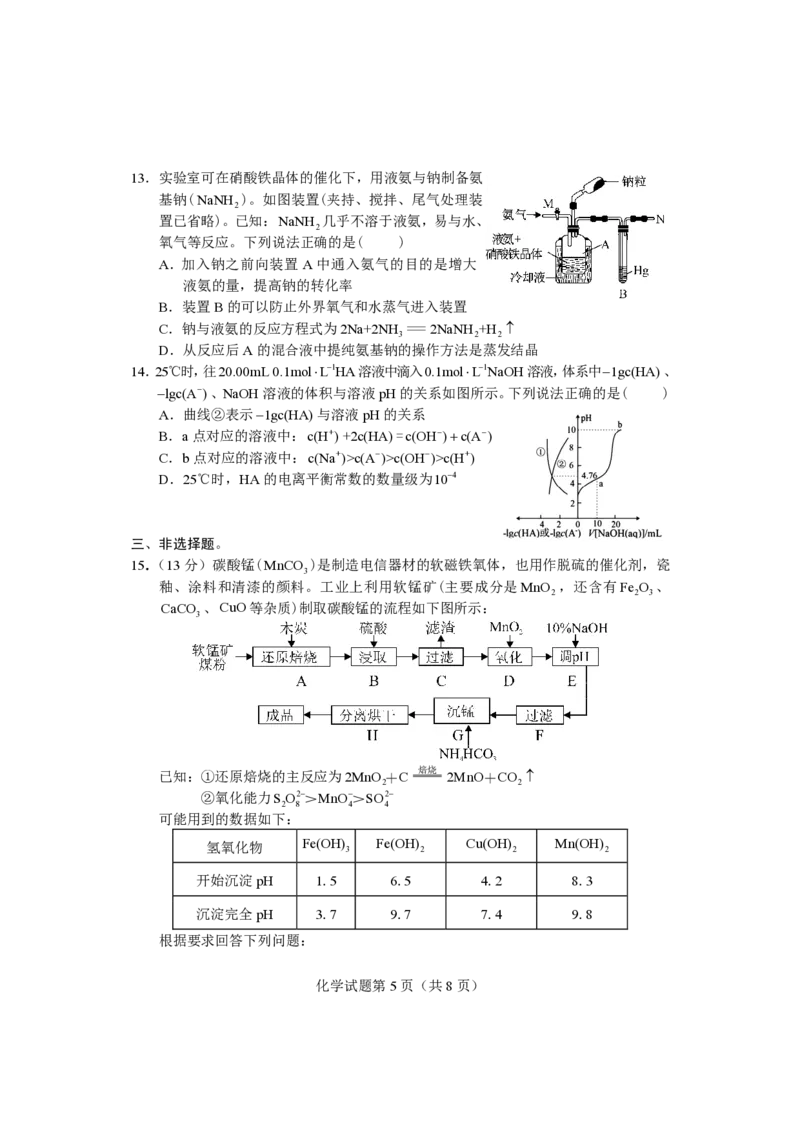
化学试题第4页(共8页)13.实验室可在硝酸铁晶体的催化下,用液氨与钠制备氨
基钠(NaNH )。如图装置(夹持、搅拌、尾气处理装
2
置已省略)。已知:NaNH 几乎不溶于液氨,易与水、
2
氧气等反应。下列说法正确的是( )
A.加入钠之前向装置 A中通入氨气的目的是增大
液氨的量,提高钠的转化率
B.装置B的可以防止外界氧气和水蒸气进入装置
C.钠与液氨的反应方程式为2Na+2NH =2NaNH +H
3 2 2
D.从反应后A的混合液中提纯氨基钠的操作方法是蒸发结晶
14.25℃时,往20.00mL 0.1molL1HA溶液中滴入0.1molL1NaOH溶液,体系中1gc(HA)、
lgc(A)、NaOH溶液的体积与溶液pH的关系如图所示。下列说法正确的是( )
A.曲线②表示1gc(HA)与溶液pH的关系
B.a点对应的溶液中:c(H+) +2c(HA)=c(OH)c(A)
C.b点对应的溶液中:c(Na+)>c(A)>c(OH)>c(H+)
D.25℃时,HA的电离平衡常数的数量级为104
三、非选择题。
15.(13 分)碳酸锰(MnCO )是制造电信器材的软磁铁氧体,也用作脱硫的催化剂,瓷
3
釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO ,还含有Fe O 、
2 2 3
CaCO 、CuO等杂质)制取碳酸锰的流程如下图所示:
3
已知:①还原焙烧的主反应为2MnO+C 焙烧 2MnO+CO
2 2
②氧化能力S O2>MnO>SO2
2 8 4 4
可能用到的数据如下:
氢氧化物 Fe(OH) Fe(OH) Cu(OH) Mn(OH)
3 2 2 2
开始沉淀pH 1.5 6.5 4.2 8.3
沉淀完全pH 3.7 9.7 7.4 9.8
根据要求回答下列问题:
化学试题第5页(共8页)(1)基态锰原子的价层电子排布式为______,S O2中存在过氧键(-O-O-),请问
2 8
S O2中S的化合价为______。
2 8
(2)在实验室进行步骤A操作时,可能用到的主要仪器为______。
A. 坩埚 B.蒸发皿 C.烧杯
(3)步骤E中调节3.7<pH<8.3,其目的是______。
(4)步骤G发生的离子方程式为______,若Mn2+恰好沉淀完全时测得溶液中CO2的
3
浓度为2.210-6molL1,则K (MnCO )=______。
sp 3
(5)实验室可以用Na S O 溶液来检验Mn2+是否完全发生反应,请写出对应的离子
2 2 8
方程式___________。
16.(14 分)2021 年中国政府工作报告中提出碳
中和目标:在 2030 年前达到最高值,2060 年前
达到碳中和。因此对二氧化碳的综合利用显得尤
为重要。
(1)通过电解的方式可实现对二氧化碳的综
合利用。2022 年 7 月香港中文大学王莹教授研
发新型电解槽实现二氧化碳回收转化效率达到
60%以上。
Pd-Cu 双金属催化剂在某介质中催化CO 转化为CH CH OH转化示意图如上,请
2 3 2
写出其电极反应方程式:_______。
(2)在席夫碱(含“—RC===N—”
的有机物)修饰的纳米金催化剂上,
CO 直接催化加氢成甲酸。其反应历程
2
如下图所示,其中吸附在催化剂表面上
的物质用*标注。
该历程中起决速步骤的化学方程式为是
______;
(3)通过使用不同新型催化剂,实现
二 氧 化 碳 加 氢 合 成 转 化 为 二 甲 醚
(CH OCH )也有广泛的应用。
3 3
反应Ⅰ:CO (g)+3H (g)CH OH(g)+H O(g) ΔH=49.01 kJmol1
2 2 3 2
反应Ⅱ:2CH OH(g)CH OCH (g)+H O(g) ΔH=24.52 kJmol1
3 3 3 2
反应Ⅲ:CO (g)+H (g)CO(g)+H O(g) ΔH=41.17 kJmol1
2 2 2
①2CO (g)+6H (g)CH OCH (g)+3H O(g) ΔH=______kJmol-1
2 2 3 3 2
②起始压强为4.0MPa、恒压条件下,通入氢气和二氧
化碳的n(H )/n(CO )=4的情况下,不同温度下CO 的平衡
2 2 2
转化率和产物的选择性(选择性是指生成某物质消耗的
CO 占CO 消耗总量的百分比)如下图所示:
2 2
当温度超过 290℃,CO 的平衡转化率随温度升
2
高而增大的原因是______。
化学试题第6页(共8页)在上图中,在 2000C 时,若经过 0.2s 该平衡体系即达到平衡。计算CO 分压的
2
平均变化速率为______MPa/s;此时对于反应 I 的K ______MPa2(保留三位有效
P
数字)
17.(14 分)某化学兴趣小组为了探究在相同条件下,草酸根(C O2)的还原性是否强
2 4
于Fe2+,进行了如下三个实验。
【实验1】通过Fe3+和C O2在溶液中的反应比较Fe2+和C O2的还原性强弱。实验操作
2 4 2 4
与现象如下:
在避光处,向10 mL 0.5 molL1FeCl 溶液中缓慢加入0.5molL1K C O 溶液至过量,
3 2 2 4
搅拌,充分反应后,冰水浴冷却,过滤后得到翠绿色溶液和翠绿色晶体,并留存翠绿色
溶液a待用。
已知:I.草酸(H C O )为二元弱酸。
2 2 4
II.三水三草酸合铁酸钾[K Fe(C O ) 3H O]为翠绿色晶体,光照易分解。其水
3 2 4 3 2
溶液中存在:[Fe(C O ) ]3 Fe3 3C O2 K 6.31021
2 4 3 2 4
请回答:
(1)实验室配制FeCl 溶液时若不加盐酸一起进行配制,常常得到红褐色的溶液,请
3
用离子方程式说明原因_______。
(2)取实验 1 中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫
酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是______。
(3)经检验,翠绿色晶体为K Fe(C O ) 3H O。为了确认实验1中是否发生了氧化
3 2 4 3 2
还原反应,取少量翠绿色溶液a,向其中滴加______(填序号)未见明显现象。
A.少量KSCN溶液 B.少量K [Fe(CN) ]溶液 C.少量HCl溶液
3 6
该小组据此判断氧化还原没有发生。请简述未发生氧化还原反应的原因______。
【实验 2】通过比较H O 与Fe2+、C O2反应的难易,判断二者还原性的强弱。实验操
2 2 2 4
作与现象如下:
① 向1 mL 0.5 molL1 FeSO 溶液中加入1 mL 0.5 molL-1 K C O 溶液,过滤,立即
4 2 2 4
产生黄色沉淀;
② 洗涤①中的黄色沉淀(已知:FeC O 2H O为黄色固体,微溶于水,可溶于强
2 4 2
酸),向其中加入过量的 6% H O 溶液,振荡,静置,反应剧烈放热,产生大量的红褐
2 2
色沉淀和无色气体;
③ 待充分反应后,向其中加入稀硫酸,调节pH约为4,得到翠绿色溶液。
请回答:
(4)证明Fe2+被氧化的实验现象是______。
(5)以上现象能否说明C O2没有被氧化。请判断并说明理由:______。
2 4
化学试题第7页(共8页)【实验3】利用电化学装置进行实验,其装置如右图:
(6)用FeC1 溶液、K C O 溶液和其他试
3 2 2 4
剂,设计右图的装置进行实验比较Fe2+和C O2
2 4
的还原性强弱,一段时间的实验后,该小组依
据实验所观察到的现象做出了C O2比Fe2+ 还
2 4
原性强的实验结论。则下列实验现象描述能支
持这一结论的有:______。(填序号)
A.电流表指针发生偏转
B.取左侧烧杯内溶液滴加氢氧化钠溶液,出现红褐色沉淀
C.取左侧烧杯内溶液滴加K [Fe(CN) ]溶液,有蓝色沉淀生成
3 6
D.右侧烧杯的电极附近有无色气泡生成,经实验,该气体能使澄清石灰水变浑浊。
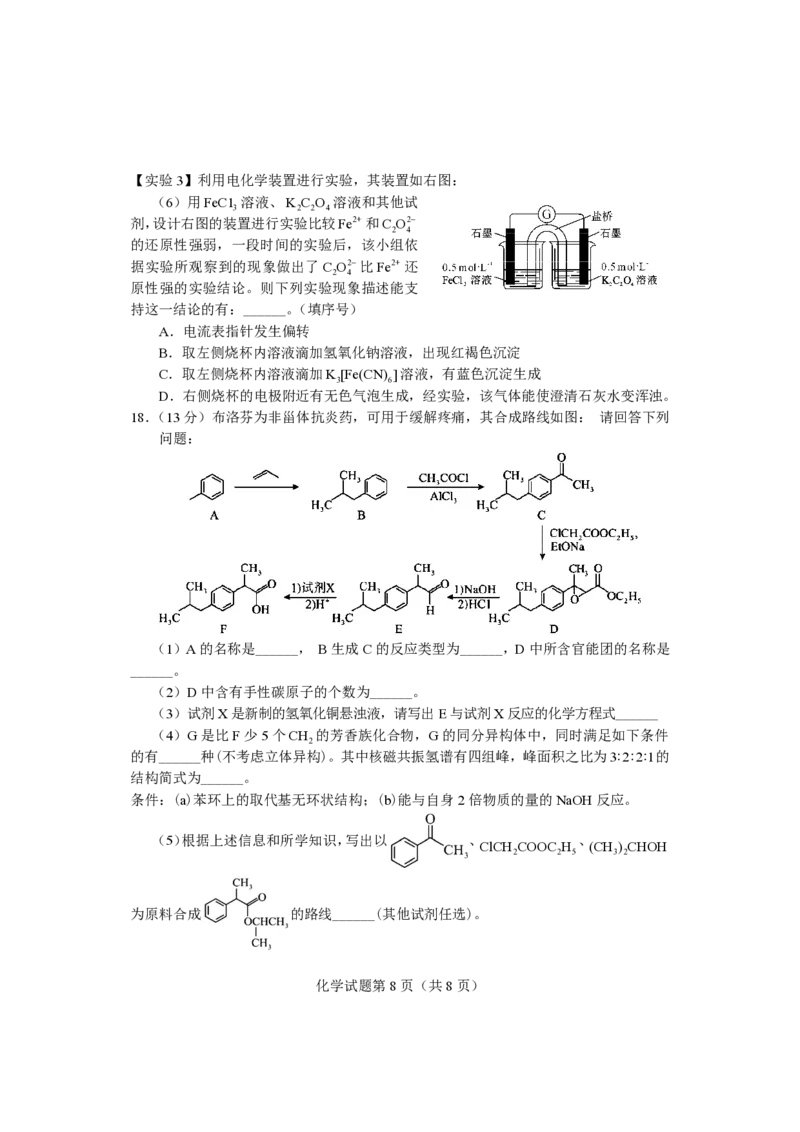
18.(13分)布洛芬为非甾体抗炎药,可用于缓解疼痛,其合成路线如图: 请回答下列
问题:
(1)A的名称是______, B生成C的反应类型为______,D中所含官能团的名称是
______。
(2)D中含有手性碳原子的个数为______。
(3)试剂X是新制的氢氧化铜悬浊液,请写出E与试剂X反应的化学方程式______
(4)G是比F少5个CH 的芳香族化合物,G的同分异构体中,同时满足如下条件
2
的有______种(不考虑立体异构)。其中核磁共振氢谱有四组峰,峰面积之比为3:2:2:1的
结构简式为______。
条件:(a)苯环上的取代基无环状结构;(b)能与自身2倍物质的量的NaOH反应。
(5)根据上述信息和所学知识,写出以 、 、
ClCH COOC H (CH ) CHOH
2 2 5 3 2
为原料合成 的路线______(其他试剂任选)。
化学试题第8页(共8页)