文档内容
微专题 06 “四型”和“四法”破解
与量有关离子方程式书写
1.(2022·浙江·统考高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH ·H O= +2H O
3 2 2
2.(2022·全国·高考真题)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司方法一、“连续反应型”离子方程式的书写——“分步分析”法
两种或两种以上的反应物发生反应后所得产物,当其中一种反应物过量时,过量的该反应
物能与其中的一种生成物继续反应,则按照反应顺序分别写出有关的反应方程式。
如向AlCl3
溶液中加入过量NaOH溶液,
可按照反应顺序分别写出两步反应:
①2OH-+CO 2 =CO 3 2-+H 2 O,②CO 3 2-+CO 2 +H 2 O=2HCO 3 - ,由①+②可得:
OH -+CO 2 =HCO 3 - 。
方法二、“离子配比型”离子方程式的书写——“少定多变”法
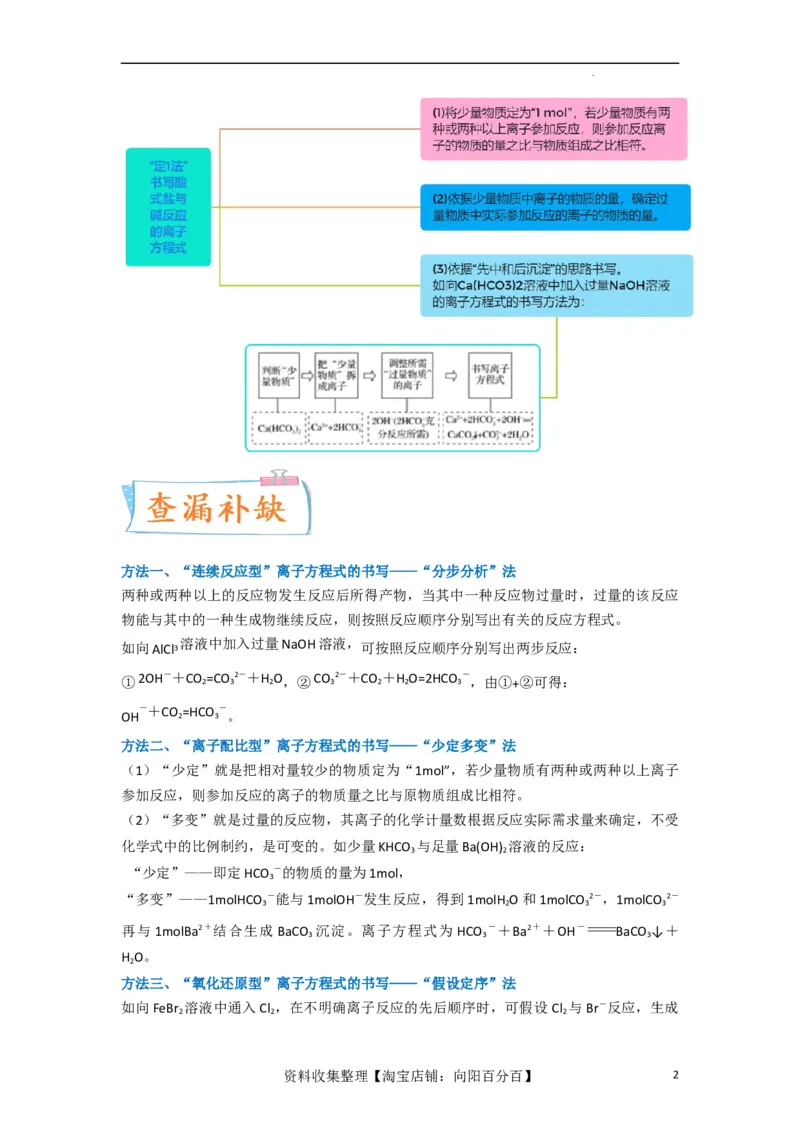
(1)“少定”就是把相对量较少的物质定为“1mol”,若少量物质有两种或两种以上离子
参加反应,则参加反应的离子的物质量之比与原物质组成比相符。
(2)“多变”就是过量的反应物,其离子的化学计量数根据反应实际需求量来确定,不受
化学式中的比例制约,是可变的。如少量KHCO 与足量Ba(OH) 溶液的反应:
3 2
“少定”——即定HCO -的物质的量为1mol,
3
“多变”——1molHCO -能与1molOH-发生反应,得到1molH O和1molCO 2-,1molCO 2-
3 2 3 3
再与 1molBa2+结合生成 BaCO 沉淀。离子方程式为 HCO -+Ba2++OH- BaCO ↓+
3 3 3
H O。
2
方法三、“氧化还原型”离子方程式的书写——“假设定序”法
如向FeBr 溶液中通入Cl ,在不明确离子反应的先后顺序时,可假设 Cl 与Br-反应,生成
2 2 2
资料收集整理【淘宝店铺:向阳百分百】 2
学科网(北京)股份有限公司的溴单质还要氧化Fe2+生成Fe3+,这样即可确定Cl 先与Fe2+后与Br-反应,然后再根据量
2
的关系书写。
(1)①FeBr 溶液中通入少量Cl 2Fe2+ + Cl == 2Fe3+ + 2Cl-
2 2 2
②FeBr 溶液中通入与其等物质的量的氯气 2Fe2+ + 2Br- + 2Cl == 2Fe3+ + Br + 4Cl-
2 2 2
③FeBr 溶液中通入足量的氯气 2Fe2+ + 4Br- + 3Cl == 2Fe3+ + 2Br + 6Cl-
2 2 2
方法四、“反应先后型”离子方程式的书写——“强先弱后”法
一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因为
反应次序不同而跟用量有关,又可称为竞争型。依据“竞争反应,强者优先”的规律,解
决离子反应的先后顺序问题,先确定出反应先后的离子,再分步书写出离子方程式。
如:向含有H+、Al3+、NH +的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依
4
次为
①H+ + OH- =H O
2
②Al3++3OH-= Al(OH) ↓
3
③NH + + OH- =NH .H O
4 3 2
④Al(OH)3+OH-=AlO2-+2H2O,
1.(2021·全国·高考真题)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
2.(2019·浙江·高考真题)能正确表示下列离子方程式是
A.KI溶液久置空气中变黄色:4I-+O +2 H O = 2 I +4 OHˉ
2 2 2
B.少量三氧化硫与氨水反应:SO +NH ·H O = NH ++HSO -
3 3 2 4 4
C.Na与CuSO 水溶液反应:2Na+Cu2+ =Cu +2Na+
4
D.(NH ) SO 和FeSO 混合溶液与足量NaOH反应:Fe2++2 OHˉ= Fe(OH) ↓
4 2 4 4 2
1.(2023·全国·高三专题练习)指反应生成的离子因又能跟剩余(过量)的反应物继续反应
而跟用量有关。
(1) 通入 溶液中:
资料收集整理【淘宝店铺:向阳百分百】 3
学科网(北京)股份有限公司碱过量:_______;
碱不足:_______。
(2) 溶液与稀盐酸反应:
稀盐酸不足:_______;
稀盐酸过量:_______。
(3)铝盐溶液与强碱溶液反应:
铝盐过量:_______;
强碱过量:_______。
(4) 溶液与强酸溶液反应:
过量:_______;
强酸过量:_______。
(5) 通入 溶液中:
过量:_______;
不足:_______。
2.向含有OH-,CO 2-,AlO -的溶液中,逐滴加入稀盐酸至过量,因为结合质子的能力:
3 2
OH->AlO - > CO 2-,故反应的离子方程式依次为
2 3
(1)
(2)
(3)
(4)
3.按用量要求书写下列离子方程式
Ba(OH) 溶液与NaHSO 溶液的反应
2 4
n[Ba(OH) ]∶n(NaHSO )=1∶1
2 4
_____________________________________________________________,
此时溶液呈________性;
n[Ba(OH) ]∶n(NaHSO )=1∶2
2 4
____________________________________________________________,
此 时 溶 液 呈 ________ 性 , 若 向 该 溶 液 中 再 加 Ba(OH) 溶 液 , 离 子 方 程 式 为
2
___________________________________________________________。
4.①少量铁粉加入到足量稀硝酸中:
_______________________________________________________________;
②n(Fe)∶n[HNO (稀)]=1∶3:
3
______________________________________________________________;
③足量铁粉加入到少量稀硝酸中:
资料收集整理【淘宝店铺:向阳百分百】 4
学科网(北京)股份有限公司___________________________________________________________。
1.(2022秋·河南焦作)下列离子方程式中正确的是
A.H SO 与Ba(OH) 溶液反应:Ba2++OH-+H++ =BaSO ↓+H O
2 4 2 4 2
B.Ca(HCO ) 与过量Ca(OH) 溶液反应:Ca2++HCO +OH-=CaCO ↓+H O
3 2 2 3 2
C.向NaOH溶液中加入过量Ca(HCO ) 溶液,有白色沉淀生成:Ca2++2HCO +2OH-
3 2
=CaCO ↓+2H O+
3 2
D.醋酸与NaOH溶液反应:H++OH-=H O
2
2.(2023·安徽宣城·统考一模)下列离子方程式表示正确的是
A.向KOH溶液中通入少量、过量H S的离子方程式均为:H S+2OH-=S2-+2H O
2 2 2
B.向FeBr 溶液中通少量、过量Cl 的离子方程式均为:2Fe2++2Br-+2Cl =2Fe3++Br +4Cl-
2 2 2 2
C.向NaHCO 溶液中加入少量、过量Ba(OH) 溶液的离子方程式均为:Ba2++OH-+HCO
3 2
=BaCO ↓+H O
3 2
D.向C H ONa溶液中通入少量、过量CO 的离子方程式均为:H O+CO +C H O-→HCO
6 5 2 2 2 6 5
+C H OH
6 5
3.(2023春·江苏南京)向含等物质的量浓度的FeI 、FeBr 混合溶液中通入一定量的氯气
2 2
后,再滴加少量的KSCN溶液,溶液变红。则下列离子方程式书写不合理的是
A.2I-+2Fe2++2Cl =2Fe3++I +4Cl-
2 2
B.2Br-+2I-+2Fe2++3Cl =I +Br +2Fe3++6Cl-
2 2 2
C.2Br-+4I-+2Fe2++4Cl =2I +Br +2Fe3++8Cl-
2 2 2
D.2Fe2++4I-+3Cl =2Fe3++2I +6Cl-
2 2
4.(2023·全国·模拟预测)下列离子方程式正确的是
A.足量的CO 通入饱和碳酸钠溶液中:CO +CO +H O=2HCO
2 2 2
B.酸性条件下KIO 溶液与KI溶液反应生成I :5I-+IO +3H O=3I +6OH-
3 2 2 2
C.向NH Al(SO ) 溶液中滴入Ba(OH) 使SO 恰好完全反应:2Ba2++4OH-+Al3++2SO
4 4 2 2
=BaSO ↓+AlO +2H O
4 2
D.NH HSO 溶液中逐滴加入足量的Ba(OH) 溶液:NH +HSO +Ba2++2OH-
4 3 2
=BaSO ↓+NH ·H O+H O
3 3 2 2
5.(2023·上海·模拟预测)下列化学反应,相应的离子方程式一定正确的是
A.向 溶液中加入少量 溶液:
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司B. 溶液与一定量氯气反应,转移电子数为6.02×1023时:
C.将2.24L(标准状况)CO 通入500mL 0.3 mol·L-1 溶液中:
2
D.向 溶液通入少量SO :
2
6.(2023春·浙江杭州)下列指定反应的方程式不正确的是
A.向含有 和 的混合溶液中通入少量 :
B.同体积同浓度的 溶液与 溶液混合:
C.铜与浓硝酸溶液反应:
D.保存 溶液的试剂瓶用橡胶塞不用玻璃塞的原因是:
7.(2023·安徽马鞍山·统考二模)能正确表示下列反应的离子方程式为
A.新制氯水中加入少量CaCO : 2Cl +H O+CaCO =Ca2++2Cl-+CO ↑+2HClO
3 2 2 3 2
B.硫酸铜溶液中滴入几滴氨水: Cu2++4NH ·H O = [Cu(NH ) ]2++4H O
3 2 3 4 2
C.久置的H S溶液变浑浊: 2S2-+ O +4H+ = 2S↓+2H O
2 2 2
D.用铜电极电解硫酸铜溶液: 2Cu2+ +2H O 2Cu+O ↑+4H+
2 2
8.(2023春·浙江杭州)下列离子方程式的书写及评价均合理的是
选
离子方程式 评价
项
将 通入含 的溶液中: 正确; 过量,可
A
将 、 全部氧化
溶液与足量的 溶液反应: 正确;酸式盐与碱反
B
应生成正盐和水
将过量 通入饱和 溶液中: 正确;生成
C
溶液
正确; 与
溶液和 溶液等体积混合:
D 消耗的 的
物质的量之比为2:3
资料收集整理【淘宝店铺:向阳百分百】 6
学科网(北京)股份有限公司A.A B.B C.C D.D
9.(2023·全国·模拟预测)下列反应的离子方程式不正确的是
A.向MgSO 溶液中加入(NH ) CO 溶液生成Mg(OH) •MgCO :2Mg2++3CO
4 4 2 3 2 3
+2H O=Mg(OH) •MgCO ↓+2HCO
2 2 3
B.向CuSO 溶液中滴加过量的氨水:Cu2++2NH •H O=Cu(OH) ↓+2NH
4 3 2 2
C.向NaHSO 溶液中加入过量NaHSO 溶液:HSO +H+=H O+SO ↑
3 4 2 2
D.将等物质的量浓度的NH Al(SO ) 与Ba(OH) 溶液按体积比为1:2混合:NH +Al3++2SO
4 4 2 2
+2Ba2++4OH-=NH •H O+Al(OH) ↓+2BaSO ↓
3 2 3 4
10.(2023春·重庆沙坪坝·高三重庆八中校考阶段练习)下列表示对应化学反应的离子方
程式正确的是
A.将足量铁加入一定量稀硝酸中:3Fe+2NO +8H+=3Fe2++2NO↑+4H O
2
B.泡沫灭火器原理:2Al3++3CO +3H O=2Al(OH) ↓+3CO2↑
2 3
C.向Ca(ClO) 溶液中通入少量的SO :Ca2++ClO-+H O+SO =Cl-+CaSO ↓+2H+
2 2 2 2 4
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶1混合:Ba2++OH-+H++SO
2 4 4
=H O+BaSO ↓
2 4
11.(2023秋·上海杨浦)下列能用离子方程式:Ca2++2 +2OH-=CaCO ↓+ +2H O
3 2
表示的反应是
A.Ca(OH) 与少量的NH HCO B.Ca(OH) 与足量的NaHCO
2 4 3 2 3
C.Ca(HCO ) 与少量的KOH D.Ca(HCO ) 与足量的Ca(OH)
3 2 3 2 2
12.(2023秋·辽宁葫芦岛·高三统考期末)下列过程对应的离子反应方程式书写正确的是
A. 溶液与过量澄清石灰水混合:
B.明矾溶液与过量氨水混合:
C.用 溶液吸收少量 :
D.向水垢中滴加足量醋酸:
13.(2023·全国·高三专题练习)一种反应物的两种或两种以上的组成离子,都能跟另一种
反应物的组成离子反应,但因反应次序不同而跟用量有关,又可称为竞争型。
(1) 溶液与 溶液的反应:
不足:_______;
过量:_______。
(2)向含有 的溶液中,逐滴加入 溶液至过量,反应依次为:
_______;
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司_______;
_______;
_______。
(3)向 溶液中通 :
少量:_______;
过量:_______。
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司