文档内容
(新高考)小题必练12:化学平衡移动
主要考查化学平衡状态的特征和判断以及外界条件对化学平衡的影响、化学平衡常数表
达式及意义、化学平衡常数相关计算、判断典型反应的自发和非自发等内容。
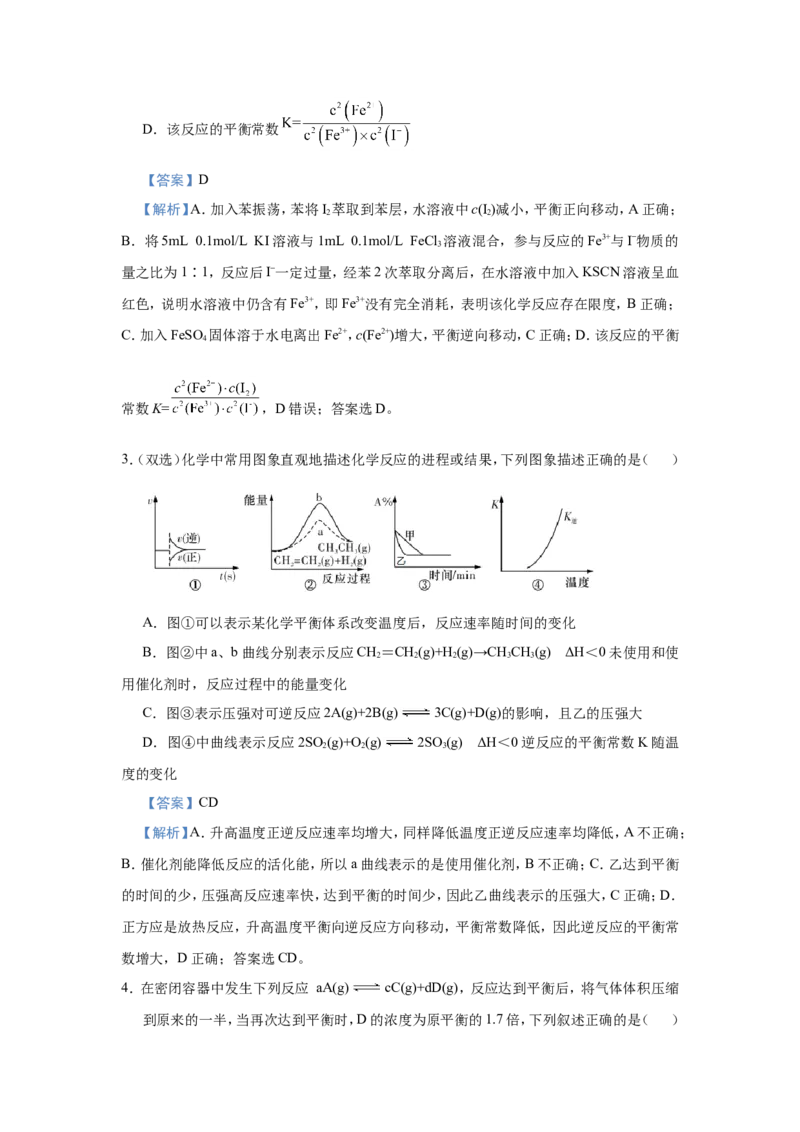
1.【2020年天津卷】已知[Co(H O) ]2+呈粉红色,[CoCl ]2−呈蓝色,[ZnCl ]2−为无色。现将CoCl
2 6 4 4 2
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H O) ]2++4Cl−
2 6
[CoCl ]2−+6HO,用该溶液做实验,溶液的颜色变化如下:
4 2
以下结论和解释正确的是( )
A.等物质的量的[Co(H O) ]2+和[CoCl ]2−中σ键数之比为3∶2
2 6 4
B.由实验①可推知ΔH<0
C.实验②是由于c(H O)增大,导致平衡逆向移动
2
D.由实验③可知配离子的稳定性:[ZnCl ]2−>[CoCl ]2−
4 4
【答案】D
【解析】A.1个[Co(H O) ]2+中含有18个σ键,1个[CoCl ]2-中含有4个σ键,等物质的量的
2 6 4
[Co(H O) ]2+和[CoCl ]2−所含σ键数之比为18∶4=9∶2,A错误;B.实验①将蓝色溶液置于冰
2 6 4
水浴中,溶液变为粉红色,说明降低温度平衡逆向移动,则逆反应为放热反应,正反应为吸热
反应,∆H>0,B错误;C.实验②加水稀释,溶液变为粉红色,加水稀释,溶液的体积增大,
[Co(H O) ]2+、[CoCl ]2−、Cl−浓度都减小,[Co(H O) ]2+、Cl−的化学计量数之和大于[CoCl ]2−的化
2 6 4 2 6 4
学计量数,则瞬时浓度商>化学平衡常数,平衡逆向移动,C错误;D.实验③加入少量ZnCl
2
固体,溶液变为粉红色,说明Zn2+与Cl−结合成更稳定的[ZnCl ]2−,导致溶液中c(Cl−)减小,平
4
衡逆向移动,则由此说明稳定性:[ZnCl ]2−>[CoCl ]2−,D正确;选D。
4 4
【点睛】本题有两个易错点:A项中[Co(H O) ]2+中不仅有Co2+与HO分子间的配位键,而
2 6 2且每个HO分子中还有两个O—H σ键;C项中HO为溶剂,视为纯液体,加水稀释,溶液体
2 2
积增大,相当于利用“对气体参与的反应,增大体积、减小压强,平衡向气体系数之和增大的
方向移动”来理解。
2.【2020年浙江选考】在干燥的HCl气流中加热MgCl ·6H O,能得到无水MgCl 。下列说法
2 2 2
不正确的是( )
A.MgCl ·nH O(s)=MgCl ·(n-1)H O(s)+HO(g) ΔH>0
2 2 2 2 2
B.MgCl ·2H O(s)=Mg(OH) (s)+2HCl(g),HCl气流可抑制反应进行
2 2 2
C.MgCl ·H O(s)=Mg(OH)Cl(s)+HCl(g),升高温度,反应更易发生
2 2
D.MgCl ·4H O(s)=MgCl ·2H O(s)+2HO(g),HCl气流可抑制反应进行
2 2 2 2 2
【答案】D
【解析】A项、MgCl ·nH O的失水反应是吸热反应,焓变ΔH>0,故A正确;B项、在HCl
2 2
气流中,能使MgCl ·2H O的水解平衡向逆反应方向移动,抑制反应进行,故B正确;C项、
2 2
MgCl ·H O的水解反应是吸热反应,升高温度,水解平衡向正反应方向移动,促进反应进行,
2 2
故C正确;D项、MgCl ·4H O的失水反应没有氯化氢生成,HCl气流对反应没有影响,故D
2 2
错误;故选D。
【点睛】MgCl ·6H O加热时MgCl 能水解,在HCl气流中能抑制其水解,但对失水反应没
2 2 2
有影响是解答易错点。
3.【2020年浙江选考】一定温度下,在2 L的恒容密闭容器中发生反应。A(g)+2B(g)
3C(g)反应过程中的部分数据如下表所示:
t/min
n/mol n(A) n(B) n(C)
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是( )
A.0~5min用A表示的平均反应速率为0.09mol·L−1·min−1
B.该反应在10min后才达到平衡
C.平衡状态时,c(C)=0.6mol·L−1D.物质B的平衡转化率为20%
【答案】C
【解析】A.v(C)= ,同一反应反应中反应速率之比等于计量
数之比,3v(A)=v(C),所以v(A)=0.03mol·L−1·min−1,故A错误;B.15min时,n(B)=1.6mol,消
耗了2.4mol-1.6mol=0.8mol,根据方程式可知这段时间内消耗A的物质的量为0.4mol,所以
15min时,n(A)=1.6mol,与10min时A的物质的量相同,说明10~15min这段时间内平衡没有
移动,但无法确定是10min时达到平衡,还是10min前已经达到平衡,故B错误;C.根据B
选项分析可知平衡时消耗的B为0.8mol,根据方程式可知生成C的物质的量为1.2mol,浓度
为 ,故C正确;D.物质B的平衡转化率为 ,故
D错误;故答案为C。
【点睛】同一反应中不同物质的速率之比等于化学计量数之比。
1.日本京东大学发明的UT-3循环是产生卤化物的典型反应,其反应之一为2CaO(s)+2Br (g)
2
2CaBr (s)+O (g),改变下列条件,能提高反应速率的是( )
2 2
A.升高温度 B.增大容器容积
C.恒温恒容条件下,充入一定量的He D.再加入一定量的CaO
【答案】A
【解析】A.升高温度,活化分子数增多,反应速率加快,故A正确;B.增大容器容积,气体
浓度减小,反应速率减小,故B错误;C.恒温恒容条件下,充入一定量的He,各反应物和生
成物浓度不变,反应速率不变,故C错误;D.CaO是固体,再加入一定量的CaO不改变浓度,
反应速率不变,故D错误;故选A。
2.5mL 0.1mol/L KI溶液与1mL 0.1mol/L FeCl 溶液发生反应:2Fe3+(aq)+2I−(aq) 2Fe2+
3
(aq)+I(aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限
度
C.加入FeSO 固体,平衡逆向移动
4D.该反应的平衡常数
【答案】D
【解析】A.加入苯振荡,苯将I 萃取到苯层,水溶液中c(I)减小,平衡正向移动,A正确;
2 2
B.将5mL 0.1mol/L KI溶液与1mL 0.1mol/L FeCl 溶液混合,参与反应的Fe3+与I−物质的
3
量之比为1∶1,反应后I−一定过量,经苯2次萃取分离后,在水溶液中加入KSCN溶液呈血
红色,说明水溶液中仍含有Fe3+,即Fe3+没有完全消耗,表明该化学反应存在限度,B正确;
C.加入FeSO 固体溶于水电离出Fe2+,c(Fe2+)增大,平衡逆向移动,C正确;D.该反应的平衡
4
常数K= ,D错误;答案选D。
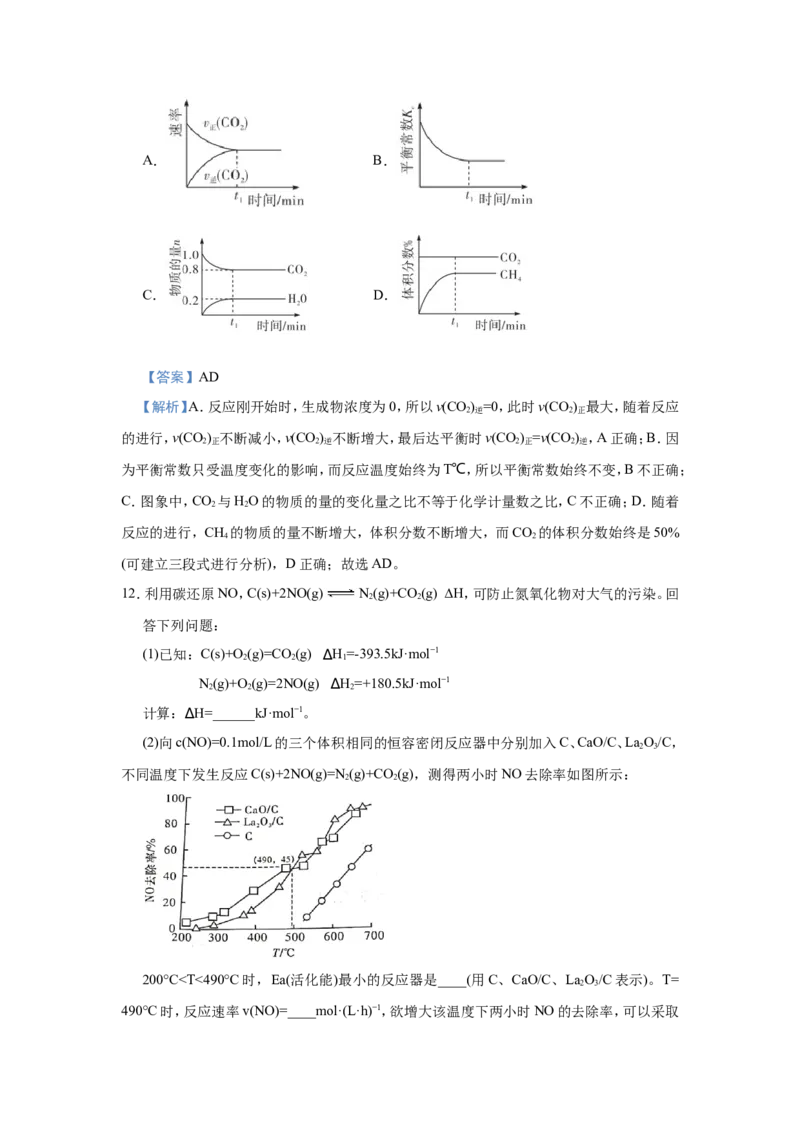
3.(双选)化学中常用图象直观地描述化学反应的进程或结果,下列图象描述正确的是( )
A.图①可以表示某化学平衡体系改变温度后,反应速率随时间的变化
B.图②中a、b曲线分别表示反应CH=CH(g)+H(g)→CH CH(g) ΔH<0未使用和使
2 2 2 3 3
用催化剂时,反应过程中的能量变化
C.图③表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(g)的影响,且乙的压强大
D.图④中曲线表示反应2SO (g)+O(g) 2SO (g) ΔH<0逆反应的平衡常数K随温
2 2 3
度的变化
【答案】CD
【解析】A.升高温度正逆反应速率均增大,同样降低温度正逆反应速率均降低,A不正确;
B.催化剂能降低反应的活化能,所以a曲线表示的是使用催化剂,B不正确;C.乙达到平衡
的时间的少,压强高反应速率快,达到平衡的时间少,因此乙曲线表示的压强大,C正确;D.
正方应是放热反应,升高温度平衡向逆反应方向移动,平衡常数降低,因此逆反应的平衡常
数增大,D正确;答案选CD。
4.在密闭容器中发生下列反应 aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩
到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.7倍,下列叙述正确的是( )A.A的转化率变小 B.平衡向正反应方向移动
C.D的物质的量变多 D.再次平衡时的逆反应速率小于原平衡的正反应速率
【答案】A
【解析】反应达到平衡后,将气体体积压缩到原来的一半,若平衡不移动,D的浓度变为原
来的2倍,而当再次达到平衡时,D的浓度为原平衡的1.7倍,说明体积减小、压强增大,平衡
向着逆向移动。A.由分析可知,平衡逆向移动,A的转化率变小,故A正确;B.根据分析可知
平衡向逆反应方向移动,故B错误;C.根据分析可知平衡向着逆向移动,D的物质的量减少,
故C错误;D.将气体体积压缩到原来的一半,虽然平衡逆向移动,但各物质的浓度依然变大,
所以再次平衡时的逆反应速率大于原平衡的正反应速率,故D错误;综上所述答案为A。
5.下列事实不能用勒夏特列原理解释的是( )
A.NaOH溶液使酯水解比稀HSO 使酯水解更彻底
2 4
B.实验室用排饱和食盐水的方法收集氯气
C.二氧化硫催化氧化时,通入过量氧气
D.压缩H(g)、I(g)和Hl(g)平衡体系,体系颜色加深
2 2
【答案】D
【解析】A.NaOH溶液使酯水解比稀HSO 使酯水解更彻底,是因为氢氧化钠消耗量酯水
2 4
解生成的酸,降低了反应物浓度,促进反应正向进行,能用勒夏特列原理解释,故不选A项;
B.氯气溶于水存在可逆反应Cl+H O HClO+HCl,饱和食盐水中含有大量氯离子,促进
2 2
平衡左移,抑制Cl 的溶解,能用勒夏特列原理解释,故不选B项;C.二氧化硫催化氧化时,
2
通入过量氧气,平衡右移,产率提高,能用勒夏特列原理解释,故不选C项;D.H+I =2HI,反
2 2
应前后体积不变,增加压强不能使平衡发生移动,混合气体颜色变深的原因是:I 的浓度增大,
2
不能用勒夏特列原理解释,故选D项;故选D。
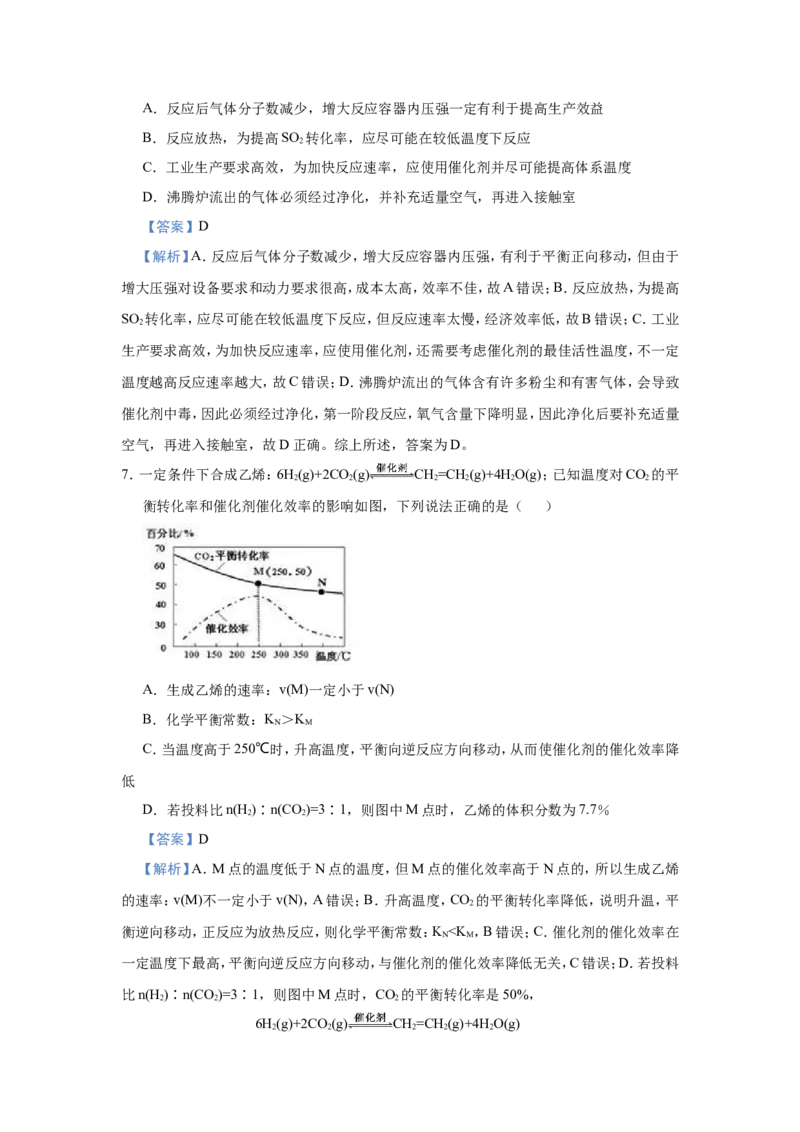
6.如图所示为接触法制硫酸的设备和工艺流程,其中关键步骤是SO 的催化氧化:2SO +O
2 2 2
2SO ΔH<0。下列说法正确的是( )
3A.反应后气体分子数减少,增大反应容器内压强一定有利于提高生产效益
B.反应放热,为提高SO 转化率,应尽可能在较低温度下反应
2
C.工业生产要求高效,为加快反应速率,应使用催化剂并尽可能提高体系温度
D.沸腾炉流出的气体必须经过净化,并补充适量空气,再进入接触室
【答案】D
【解析】A.反应后气体分子数减少,增大反应容器内压强,有利于平衡正向移动,但由于
增大压强对设备要求和动力要求很高,成本太高,效率不佳,故A错误;B.反应放热,为提高
SO 转化率,应尽可能在较低温度下反应,但反应速率太慢,经济效率低,故B错误;C.工业
2
生产要求高效,为加快反应速率,应使用催化剂,还需要考虑催化剂的最佳活性温度,不一定
温度越高反应速率越大,故C错误;D.沸腾炉流出的气体含有许多粉尘和有害气体,会导致
催化剂中毒,因此必须经过净化,第一阶段反应,氧气含量下降明显,因此净化后要补充适量
空气,再进入接触室,故D正确。综上所述,答案为D。
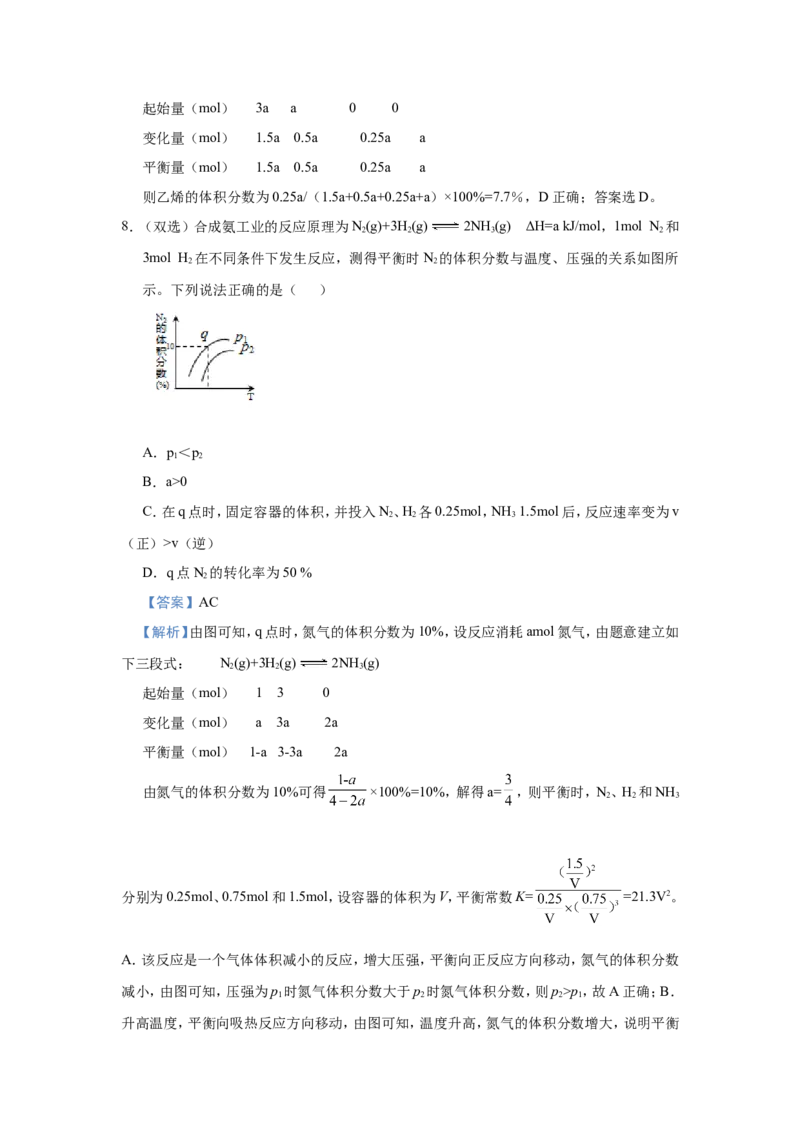
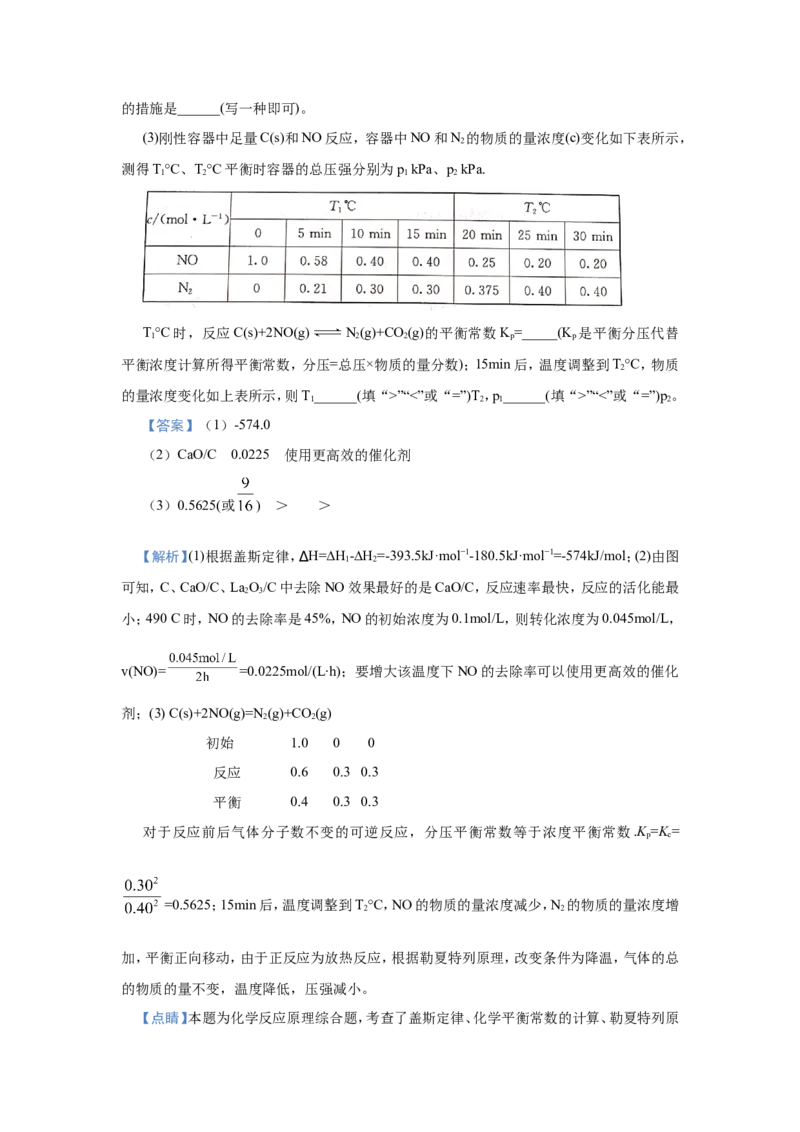
7.一定条件下合成乙烯:6H(g)+2CO (g) CH=CH (g)+4HO(g);已知温度对CO 的平
2 2 2 2 2 2
衡转化率和催化剂催化效率的影响如图,下列说法正确的是( )
A.生成乙烯的速率:v(M)一定小于v(N)
B.化学平衡常数:K >K
N M
C.当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降
低
D.若投料比n(H)∶n(CO)=3∶1,则图中M点时,乙烯的体积分数为7.7%
2 2
【答案】D
【解析】A.M点的温度低于N点的温度,但M点的催化效率高于N点的,所以生成乙烯
的速率:v(M)不一定小于v(N),A错误;B.升高温度,CO 的平衡转化率降低,说明升温,平
2
衡逆向移动,正反应为放热反应,则化学平衡常数:K 0
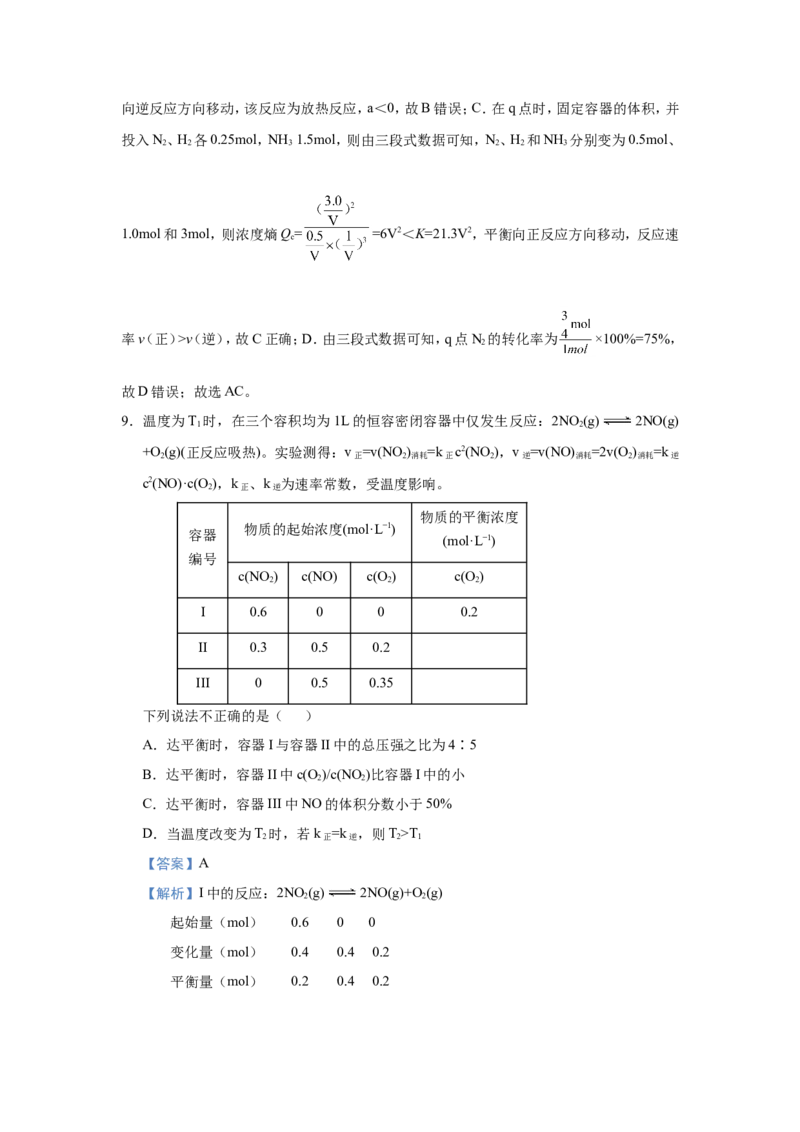
C.在q点时,固定容器的体积,并投入N、H 各0.25mol,NH 1.5mol后,反应速率变为v
2 2 3
(正)>v(逆)
D.q点N 的转化率为50 %
2
【答案】AC
【解析】由图可知,q点时,氮气的体积分数为10%,设反应消耗amol氮气,由题意建立如
下三段式: N(g)+3H(g) 2NH (g)
2 2 3
起始量(mol) 1 3 0
变化量(mol) a 3a 2a
平衡量(mol) 1-a 3-3a 2a
由氮气的体积分数为10%可得 ×100%=10%,解得a= ,则平衡时,N、H 和NH
2 2 3
分别为0.25mol、0.75mol和1.5mol,设容器的体积为V,平衡常数K= =21.3V2。
A.该反应是一个气体体积减小的反应,增大压强,平衡向正反应方向移动,氮气的体积分数
减小,由图可知,压强为p 时氮气体积分数大于p 时氮气体积分数,则p>p,故A正确;B.
1 2 2 1
升高温度,平衡向吸热反应方向移动,由图可知,温度升高,氮气的体积分数增大,说明平衡向逆反应方向移动,该反应为放热反应,a<0,故B错误;C.在q点时,固定容器的体积,并
投入N、H 各0.25mol,NH 1.5mol,则由三段式数据可知,N、H 和NH 分别变为0.5mol、
2 2 3 2 2 3
1.0mol和3mol,则浓度熵Q= =6V2<K=21.3V2,平衡向正反应方向移动,反应速
c
率v(正)>v(逆),故C正确;D.由三段式数据可知,q点N 的转化率为 ×100%=75%,
2
故D错误;故选AC。
9.温度为T 时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO (g) 2NO(g)
1 2
+O (g)(正反应吸热)。实验测得:v =v(NO) =k c2(NO ),v =v(NO) =2v(O ) =k
2 正 2 消耗 正 2 逆 消耗 2 消耗 逆
c2(NO)·c(O),k 、k 为速率常数,受温度影响。
2 正 逆
物质的平衡浓度
物质的起始浓度(mol·L−1)
容器
(mol·L−1)
编号
c(NO ) c(NO) c(O) c(O)
2 2 2
I 0.6 0 0 0.2
II 0.3 0.5 0.2
III 0 0.5 0.35
下列说法不正确的是( )
A.达平衡时,容器I与容器II中的总压强之比为4∶5
B.达平衡时,容器II中c(O)/c(NO)比容器I中的小
2 2
C.达平衡时,容器III中NO的体积分数小于50%
D.当温度改变为T 时,若k =k ,则T>T
2 正 逆 2 1
【答案】A
【解析】I中的反应:2NO (g) 2NO(g)+O (g)
2 2
起始量(mol) 0.6 0 0
变化量(mol) 0.4 0.4 0.2
平衡量(mol) 0.2 0.4 0.2化学平衡常数K= = =0.8;容器体积为1L,则平衡时I中气体总
物质的量=1L×(0.2+0.4+0.2)mol/L=0.8mol,恒容恒温时气体压强之比等于其物质的量之比,
如果平衡时I、II中压强之比为4∶5,则II中平衡时气体总物质的量为1mol,II中开始时浓度
商Qc= = = <0.8,则平衡正向移动,平衡正向移动导致混合气体
总物质的量之和增大,所以达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比小于4∶5,故A错误;
B.如果II中平衡时 c(NO )=c(O ),设参加反应的c(NO )=x mol/L,则0.3-x=0.2+0.5x,x= ,
2 2 2
平衡时c(NO )=c(O )= mol/L,c(NO)=0.5mol/L+ mol/L= mol/L
2 2
,II中Qc= = ≈1.3>0.8,说明II中平衡时应该存在c(NO )>c(O),
2 2
容器I中 =1,所以达平衡时,容器Ⅱ中 小于1,则比容器Ⅰ中的小,故B正确;
C.如果 III 中 NO 和氧气完全转化为二氧化氮,则 c(NO )=0.5mol/L,且容器中还有
2
c(O)=0.1mol/L剩余,与I相比,III是相当于增大压强,平衡逆向移动,二氧化氮和氧气之和
2
所占体积比大于50%,则达平衡时,容器Ⅲ中NO的体积分数小于50%,故C正确;D.v
正
=v(NO) =k c2(NO ),v =v(NO) =2v(O ) =k c2(NO)·c(O),达到平衡状态时正逆反应
2 消耗 正 2 逆 消耗 2 消耗 逆 2
速率相等,则k c2(NO )=k c2(NO)·c(O),且k =k ,则c2(NO )=c2(NO)·c(O),化学平衡常
正 2 逆 2 正 逆 2 2
数K等于1,该温度下的K大于0.8,且该反应的正反应是吸热反应,说明升高温度平衡正向
移动,所以T>T,故D正确;故答案为A。
2 1
10.已知C H(g)+H(g) C H(g) ΔH<0,在3个体积相等的恒容容器发生反应,结果如
2 4 2 2 6
下表。下列说法正确的是( )
起始物质的量/mol 平衡物质的量/mol
温
容器编号
度/K
H(g) C H(g) C H(g) C H(g)
2 2 4 2 6 2 6
Ⅰ T 0.10 0.10 0 0.05
1Ⅱ T 0.10 0.10 0.10
1
Ⅲ T 0 0 0.10 0.06
2
A.T”“<”或“=”)T,p______(填“>”“<”或“=”)p 。
1 2 1 2
【答案】(1)-574.0
(2)CaO/C 0.0225 使用更高效的催化剂
(3)0.5625(或 ) > >
【解析】(1)根据盖斯定律,∆H=∆H -∆H =-393.5kJ·mol−1-180.5kJ·mol−1=-574kJ/mol;(2)由图
1 2
可知,C、CaO/C、LaO/C中去除NO效果最好的是CaO/C,反应速率最快,反应的活化能最
2 3
小;490 C时,NO的去除率是45%,NO的初始浓度为0.1mol/L,则转化浓度为0.045mol/L,
v(NO)= =0.0225mol/(L∙h);要增大该温度下NO的去除率可以使用更高效的催化
剂;(3) C(s)+2NO(g)=N (g)+CO (g)
2 2
初始 1.0 0 0
反应 0.6 0.3 0.3
平衡 0.4 0.3 0.3
对于反应前后气体分子数不变的可逆反应,分压平衡常数等于浓度平衡常数.K =K=
p c
=0.5625;15min后,温度调整到T°C,NO的物质的量浓度减少,N 的物质的量浓度增
2 2
加,平衡正向移动,由于正反应为放热反应,根据勒夏特列原理,改变条件为降温,气体的总
的物质的量不变,温度降低,压强减小。
【点睛】本题为化学反应原理综合题,考查了盖斯定律、化学平衡常数的计算、勒夏特列原理进行图像的分析,难点为平衡常数的计算,巧用反应的化学方程式,进行了数据的处理,进
行计算得到平衡常数。
13.汽车发动机工作时会产生包括CO、NO 等多种污染气体,如何处理这些气体,对保护大
x
气环境意义重大,回答下列问题:
(1)已知:2NO (g) 2NO(g)+O (g) ΔH=+115.2kJ·mol−1
2 2 1
2O(g) 3O(g) ΔH=-286.6kJ·mol−1
3 2 2
写出臭氧与NO作用产生NO 和O 的热化学方程式_________________。
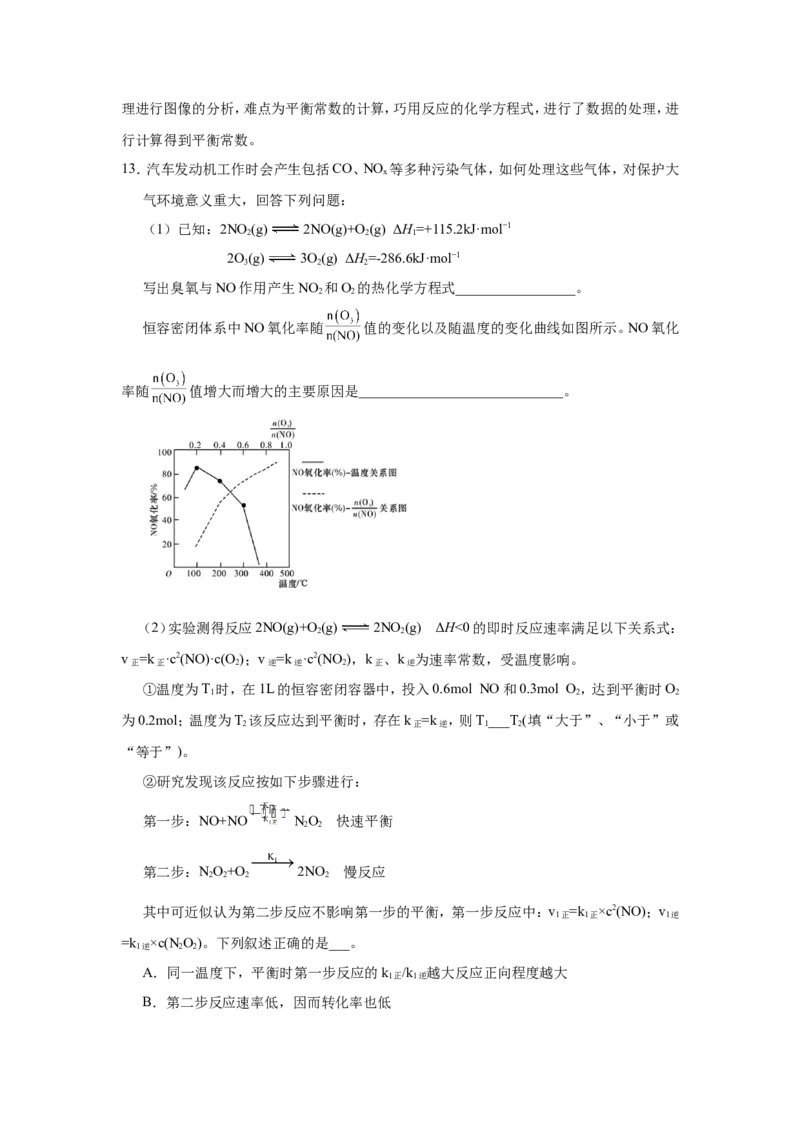
2 2
恒容密闭体系中NO氧化率随 值的变化以及随温度的变化曲线如图所示。NO氧化
率随 值增大而增大的主要原因是_____________________________。
(2)实验测得反应2NO(g)+O (g) 2NO (g) ΔH<0的即时反应速率满足以下关系式:
2 2
v =k ·c2(NO)·c(O);v =k ·c2(NO ),k 、k 为速率常数,受温度影响。
正 正 2 逆 逆 2 正 逆
①温度为T 时,在1L的恒容密闭容器中,投入0.6mol NO和0.3mol O,达到平衡时O
1 2 2
为0.2mol;温度为T 该反应达到平衡时,存在k =k ,则T___T(填“大于”、“小于”或
2 正 逆 1 2
“等于”)。
②研究发现该反应按如下步骤进行:
第一步:NO+NO NO 快速平衡
2 2
第二步:NO+O 2NO 慢反应
2 2 2 2
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v =k ×c2(NO);v
1正 1正 1逆
=k ×c(N O)。下列叙述正确的是___。
1逆 2 2
A.同一温度下,平衡时第一步反应的k /k 越大反应正向程度越大
1正 1逆
B.第二步反应速率低,因而转化率也低C.第二步的活化能比第一步的活化能低
D.整个反应的速率由第二步反应速率决定
(3)科学家研究出了一种高效催化剂,可以将CO和NO 两者转化为无污染气体,反应方
2
程式为:2NO (g)+4CO(g) 4CO(g)+N(g) ΔH<0
2 2 2
某温度下,向10L密闭容器中分别充入0.1mol NO 和0.2mol CO,发生上述反应,随着反
2
应的进行,容器内的压强变化如表所示:
时间/min 0 2 4 6 8 10 12
压强/kPa 75 73.4 71.95 70.7 69.7 68.75 68.75
回答下列问题:
①在此温度下,该反应达到平衡时,容器里气体的总物质的量为___,反应的平衡常数
K =___kPa−1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,K 为以分压表示的
p p
平衡常数,计算结果精确到小数点后2位);若保持温度不变,再将CO、CO 气体浓度分别增
2
加一倍,则平衡___(填“右移”或“左移”或“不移动”);
②若将温度降低,再次平衡后,与原平衡相比体系压强(p总)___(填“增大”、“减小”或
“不变”)。
【答案】(1)NO(g)+O (g) NO (g)+O(g) ΔH=-200.9kJ·mol−1 值增大,有利于平
3 2 2
衡NO(g)+O (g) NO (g)+O(g)正向移动
3 2 2
(2)小于 AD
(3)0.275mol 0.04 不移动 减小
【解析】(1)已知:2NO (g) 2NO(g)+O (g) ΔH=+115.2kJ·mol−1 ①;2O(g) 3O(g)
2 2 1 3 2
ΔH=-286.6kJ·mol−1 ②,利用盖斯定律可知,②式-①式后再除以2即得NO(g)+O (g)
2 3
NO (g)+O(g) , 则 对 应 的 热 效 应 ΔH= = =
2 2
-200.9kJ·mol−1,故答案为:NO(g)+O (g) NO (g)+O(g) ΔH=-200.9kJ·mol−1;根据平衡移
3 2 2
动原理,增大 的比值,O 浓度增加,有利于平衡NO(g)+O (g) NO (g)+O(g)正向移
3 3 2 2
动,使NO的氧化率增大,故答案为: 值增大,有利于平衡NO(g)+O (g) NO (g)
3 2
+O (g)正向移动;(2)①温度为T 时:
2 1
2NO(g)+O (g) 2NO (g)
2 2起始量(mol) 0.6 0.3 0
变化量(mol) 0.2 0.1 0.2
平衡量(mol) 0.4 0.2 0.2,
则温度为T 时,平衡常数K = =1.25,由于平衡时 = ,不难推出平衡常数
1 1 正 逆
等于速率常数之比,即:K = =1.25;温度为T 时,该反应存在K= =1,显然K