文档内容
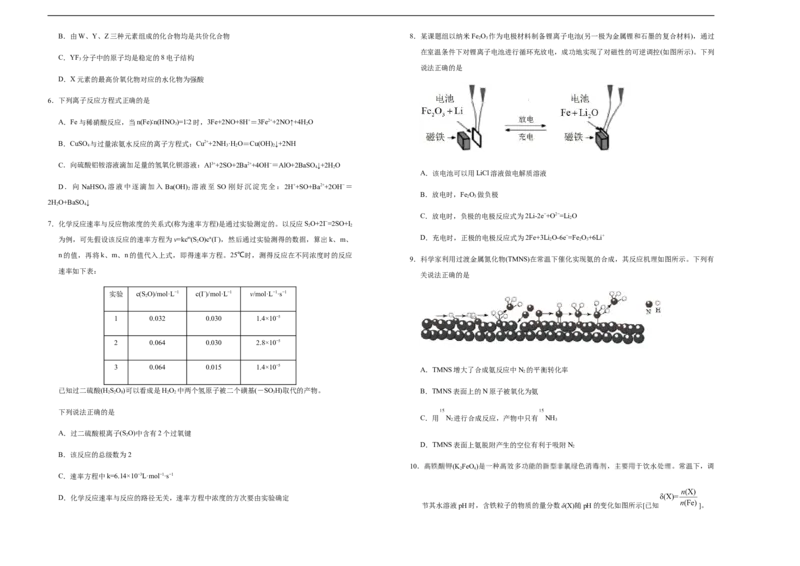
绝密 ★ 启用前 3.莽草酸是从中药八角茴香中提取的一种单体化合物,有抗炎、镇痛作用,其结构如图所示。关
于莽草酸的下列叙述中,正确的是
2021 年普通高等学校招生全国统一考试
班级
姓名
化 学
准考证号
注意事项:
考场号
A.分子式为C HO
此卷只 7 5 5
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己
装订座不位密号封
B.莽草酸只能发生取代反应、加成反应和氧化反应
的姓名、考生号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题的答案后,用铅笔把答题卡上对应题目的答案标号涂黑,
C.分子中所有原子可能在同一平面上
如需改动,用橡皮擦干净后,再选涂其他答案标号。写在试卷上无效。
D.1mol莽草酸与金属钠反应能产生标况下的氢气为44.8L
3.回答第Ⅱ卷时,将答案填写在答题卡上,写在试卷上无效。
4.考试结束,将本试卷和答题卡一并交回。 4.下列关于实验室制取SO 的实验,其中叙述正确的是
2
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cu 64
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.化学与生产和生活密切相关。下列有关说法不正确的是
A.甲图中可利用70%的浓硫酸和硫酸钠固体制取SO
2
A.古代记载文字的器物“丝帛”的主要成分属于天然有机高分子化合物
B.乙图中干燥SO
2
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.可用丙图中装置和药品收集二氧化硫并吸收尾气
C.酿酒过程中葡萄糖在酒化酶的作用下发生水解反应生成乙醇
D.可用丁图中装置和药品检验铜和浓硫酸反应生成的CuSO
4
D.“墨滴无声入水惊,如烟袅袅幻形生”中的墨滴具有胶体的性质
5.短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形成的化合物结构如图所示。在
2.设N 为阿伏加德罗常数的值,下列有关叙述正确的是
A 元素周期表中元素W是原子半径最小的元素,Z原子的最外层电子数是周期数的3倍,且W与
A.1L 0.1mol·L−1 Na SO 溶液中阴离子数目为0.1N X、Y、Z均可形成电子数相等的分子。下列说法正确的是
2 3 A
B.9.2g C HO含有共价键的数目为1.6N
2 6 A
C.N 个CO 分子形成的晶体中电子对数目为4N
A 2 A
D.1mol Na与足量O 反应,生成NaO和NaO 的混合物,钠失去电子数为2N
2 2 2 2 A
A.简单气态氢化物稳定性:Z<XB.由W、Y、Z三种元素组成的化合物均是共价化合物 8.某课题组以纳米Fe O 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过
2 3
在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图所示)。下列
C.YF 分子中的原子均是稳定的8电子结构
3
说法正确的是
D.X元素的最高价氧化物对应的水化物为强酸
6.下列离子反应方程式正确的是
A.Fe与稀硝酸反应,当n(Fe)∶n(HNO )=1∶2时,3Fe+2NO+8H+=3Fe2++2NO↑+4HO
3 2
B.CuSO 与过量浓氨水反应的离子方程式:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
C.向硫酸铝铵溶液滴加足量的氢氧化钡溶液:Al3++2SO+2Ba2++4OH−=AlO+2BaSO ↓+2H O
4 2
A.该电池可以用LiCl溶液做电解质溶液
D.向 NaHSO 溶液中逐滴加入 Ba(OH) 溶液至 SO 刚好沉淀完全:2H++SO+Ba2++2OH−=
4 2
B.放电时,Fe O 做负极
2 3
2HO+BaSO↓
2 4
C.放电时,负极的电极反应式为2Li-2e−+O2−=Li O
2
7.化学反应速率与反应物浓度的关系式(称为速率方程)是通过实验测定的。以反应SO+2I−=2SO+I
2 2
为例,可先假设该反应的速率方程为v=kcm(S 2 O)cn(I−),然后通过实验测得的数据,算出k、m、 D.充电时,正极的电极反应式为2Fe+3Li 2 O-6e−=Fe 2 O 3 +6Li+
n的值,再将k、m、n的值代入上式,即得速率方程。25℃时,测得反应在不同浓度时的反应
9.科学家利用过渡金属氮化物(TMNS)在常温下催化实现氨的合成,其反应机理如图所示。下列有
速率如下表:
关说法正确的是
实验 c(SO)/mol·L−1 c(I−)/mol·L−1 v/mol·L−1·s−1
2
1 0.032 0.030 1.4×10−5
2 0.064 0.030 2.8×10−5
3 0.064 0.015 1.4×10−5
A.TMNS增大了合成氨反应中N 的平衡转化率
2
已知过二硫酸(HSO)可以看成是HO 中两个氢原子被二个磺基(-SO H)取代的产物。 B.TMNS表面上的N原子被氧化为氨
2 2 8 2 2 3
下列说法正确的是
C.用 N 进行合成反应,产物中只有 NH
2 3
A.过二硫酸根离子(SO)中含有2个过氧键
2
D.TMNS表面上氨脱附产生的空位有利于吸附N
2
B.该反应的总级数为2
10.高铁酸钾(K FeO)是一种高效多功能的新型非氯绿色消毒剂,主要用于饮水处理。常温下,调
2 4
C.速率方程中k=6.14×10−3L·mol−1·s−1
D.化学反应速率与反应的路径无关,速率方程中浓度的方次要由实验确定
节其水溶液pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知 ]。下列说法正确的是 (1)过滤操作中需要用到的玻璃仪器有 ,上述过滤后可重复利用的物质为
(填物质名称)。
(2)“①氧化法”中Fe3+是反应的催化剂,反应产生了两种无毒气体,该氧化过程中的化学方程式
为 。
(3)“氧化”步骤中,酸性越强,草酸去除率越高,其原因是_______。为了使加入的17.5mg·L−1
的Fe3+催化效果达到最佳,废水酸化时应将pH调整至小于_______(已知lg2=0.3,1g5=0.7)。
(4)“②沉淀法”:将1.5mol PbSO 沉淀剂加到1L含有0.1mol·L−1草酸的模拟废水中。沉淀时发生
A.25℃,B点水电离出的c(H+)=1×10−4 4
的离子反应为PbSO (s)+HC O(aq) PbC O s)+2H+(aq)+SO(aq)。请计算此反应的平衡常数K=
4 2 2 4 2 4(
B.NaHFeO 溶液显碱性
4
__________。
C.常温下,HFeO(aq)+H+(aq) HFeO(aq)的平衡常数K<100
2 4 3
(5)干燥步骤温度过高会降低草酸产率,其原因是 。
D.KFeO 起杀菌消毒作用是因为其遇水生成了Fe(OH) 胶体
2 4 3
(6)已知在25℃时,亚硫酸的电离平衡常数为:K=1.54×10−2、K=1.02×10−7,向NaC O 溶液中
1 2 2 2 4
二、非选择题:本题共5小题,共70分。
通入少量的SO 气体,反应的离子方程式为 。
2
11.(14分)工业生产中会产生稀土草酸沉淀废水,其主要成分为盐酸和草酸(H C O)的混合溶液
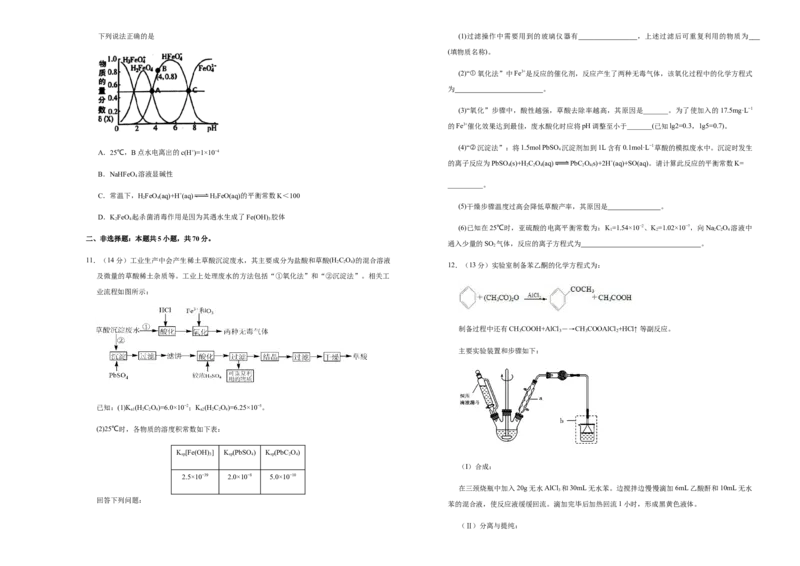
2 2 4 12.(13分)实验室制备苯乙酮的化学方程式为:
及微量的草酸稀土杂质等。工业上处理废水的方法包括“①氧化法”和“②沉淀法”。相关工
业流程如图所示:
制备过程中还有CH COOH+AlCl ―→CH COOAlCl +HCl↑ 等副反应。
3 3 3 2
主要实验装置和步骤如下:
已知:(1)K (H C O)=6.0×10−2;K (H C O)=6.25×10−5。
a1 2 2 4 a2 2 2 4
(2)25℃时,各物质的溶度积常数如下表:
K [Fe(OH) ] K (PbSO ) K (PbC O)
sp 3 sp 4 sp 2 4
(I)合成:
2.5×10−39 2.0×10−8 5.0×10−10
在三颈烧瓶中加入20g无水AlCl 和30mL无水苯。边搅拌边慢慢滴加6mL乙酸酐和10mL无水
3
回答下列问题:
苯的混合液,使反应液缓缓回流。滴加完毕后加热回流1小时,形成黑黄色液体。
(Ⅱ)分离与提纯:将冷却后的反应瓶置于冰水浴中,加入 15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,
无机相用乙醚萃取,与有机相合并,有机相用 10% NaOH溶液洗涤,分液,弃去无机层,有机层
用9mL水洗,分液,弃去无机层,有机层用 干燥,得到苯乙酮粗产品。
回答下列问题:
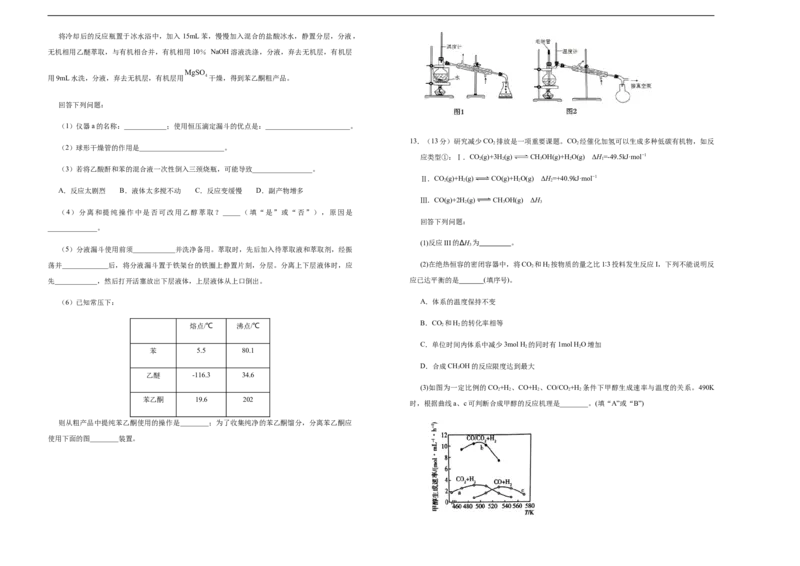
(1)仪器a的名称:____________;使用恒压滴定漏斗的优点是:________________________。
13.(13分)研究减少CO 排放是一项重要课题。CO 经催化加氢可以生成多种低碳有机物,如反
2 2
(2)球形干燥管的作用是________________________。
应类型①:Ⅰ.CO(g)+3H(g) CHOH(g)+H O(g) ΔH=-49.5kJ·mol−1
2 2 3 2 1
(3)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致_________________。
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH=+40.9kJ·mol−1
2 2 2 2
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
Ⅲ.CO(g)+2H(g) CHOH(g) ΔH
2 3 3
(4)分离和提纯操作中是否可改用乙醇萃取?_____(填“是”或“否”),原因是
回答下列问题:
______________。
(1)反应III的∆H 为 。
3
(5)分液漏斗使用前须____________并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振
荡并_____________后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应 (2)在绝热恒容的密闭容器中,将CO 和H 按物质的量之比1∶3投料发生反应I,下列不能说明反
2 2
先____________,然后打开活塞放出下层液体,上层液体从上口倒出。 应已达平衡的是 (填序号)。
(6)已知常压下: A.体系的温度保持不变
B.CO 和H 的转化率相等
熔点/℃ 沸点/℃ 2 2
C.单位时间内体系中减少3mol H 的同时有1mol HO增加
2 2
苯 5.5 80.1
D.合成CHOH的反应限度达到最大
3
乙醚 -116.3 34.6
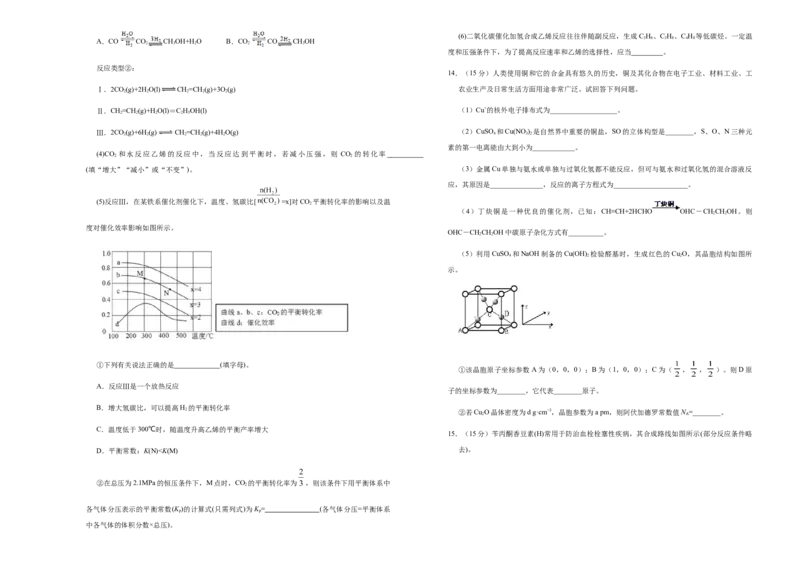
(3)如图为一定比例的CO+H 、CO+H 、CO/CO+H 条件下甲醇生成速率与温度的关系。490K
2 2 2 2 2
苯乙酮 19.6 202
时,根据曲线a、c可判断合成甲醇的反应机理是________。(填“A”或“B”)
则从粗产品中提纯苯乙酮使用的操作是________;为了收集纯净的苯乙酮馏分,分离苯乙酮应
使用下面的图________装置。(6)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H 、C H 、C H 等低碳烃。一定温
3 6 3 8 4 8
A.CO CO CHOH+H O B.CO CO CHOH
2 3 2 2 3
度和压强条件下,为了提高反应速率和乙烯的选择性,应当 。
反应类型②:
14.(15分)人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工
Ⅰ.2CO(g)+2HO(l) CH=CH (g)+3O(g) 农业生产及日常生活方面用途非常广泛。试回答下列问题。
2 2 2 2 2
Ⅱ.CH=CH (g)+HO(l)=C HOH(l) (1)Cu+的核外电子排布式为___________________。
2 2 2 2 5
Ⅲ.2CO(g)+6H(g) CH=CH (g)+4HO(g) (2)CuSO 和Cu(NO ) 是自然界中重要的铜盐,SO的立体构型是________,S、O、N三种元
2 2 2 2 2 4 3 2
素的第一电离能由大到小为____________。
(4)CO 和水反应乙烯的反应中,当反应达到平衡时,若减小压强,则 CO 的转化率
2 2
(填“增大”“减小”或“不变”)。 (3)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反
应,其原因是_______________,反应的离子方程式为_____________________。
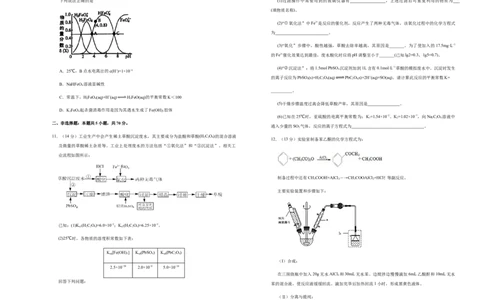
(5)反应Ⅲ,在某铁系催化剂催化下,温度、氢碳比[ =x]对CO 平衡转化率的影响以及温
2
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO OHC-CHCHOH。则
2 2
度对催化效率影响如图所示。
OHC-CHCHOH中碳原子杂化方式有__________。
2 2
(5)利用CuSO 和NaOH制备的Cu(OH) 检验醛基时,生成红色的Cu O,其晶胞结构如图所
4 2 2
示。
①下列有关说法正确的是 (填字母)。
①该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为( , , )。则D原
A.反应Ⅲ是一个放热反应
子的坐标参数为________,它代表________原子。
B.增大氢碳比,可以提高H 的平衡转化率
2 ②若Cu O晶体密度为d g·cm−3,晶胞参数为a pm,则阿伏加德罗常数值N =________。
2 A
C.温度低于300℃时,随温度升高乙烯的平衡产率增大
15.(15分)苄丙酮香豆素(H)常用于防治血栓栓塞性疾病,其合成路线如图所示(部分反应条件略
D.平衡常数:K(N)