文档内容
选择题突破六 B 组 能力提升练
1.(2024·黑龙江哈尔滨三校联考二模)下列有关物质的工业制备反应错误的是( )
A.侯氏制碱:NaCl+HO+NH +CO NaHCO ↓+NHCl
2 3 2 3 4
B.工业合成氨:N +3H 2NH
2 2 3
C.氯碱工业:2NaCl+2HO 2NaOH+H ↑+Cl↑
2 2 2
D.冶炼金属铝:2AlCl 2Al+3Cl ↑
3 2
2.(2024·浙江温州二模)侯氏制碱法利用CO、NH 及饱和NaCl溶液先制得NaHCO ,进一步生产
2 3 3
NaCO,下列说法不正确的是( )
2 3
A.生产中,向溶有CO 的饱和食盐水中通入NH ,可析出NaHCO 固体
2 3 3
B.将所得NaHCO 固体加热生产出纯碱
3
C.碳酸氢钠和碳酸钠的溶液均呈碱性,可用作食用碱或工业用碱
D.向新制氯水中加入少量碳酸氢钠,可提高氯水的漂白效果
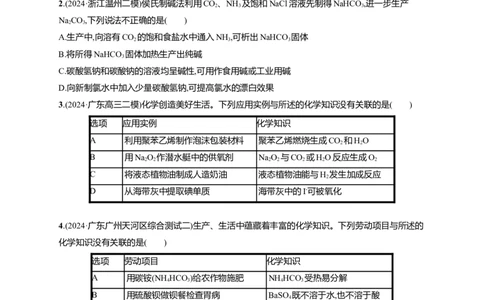
3.(2024·广东高三二模)化学创造美好生活。下列应用实例与所述的化学知识没有关联的是( )
选项 应用实例 化学知识
A 利用聚苯乙烯制作泡沫包装材料 聚苯乙烯燃烧生成CO 和HO
2 2
B 用NaO 作潜水艇中的供氧剂 NaO 与CO 或HO反应生成O
2 2 2 2 2 2 2
C 将液态植物油制成人造奶油 液态植物油能与H 发生加成反应
2
D 从海带灰中提取碘单质 海带灰中的I-可被氧化
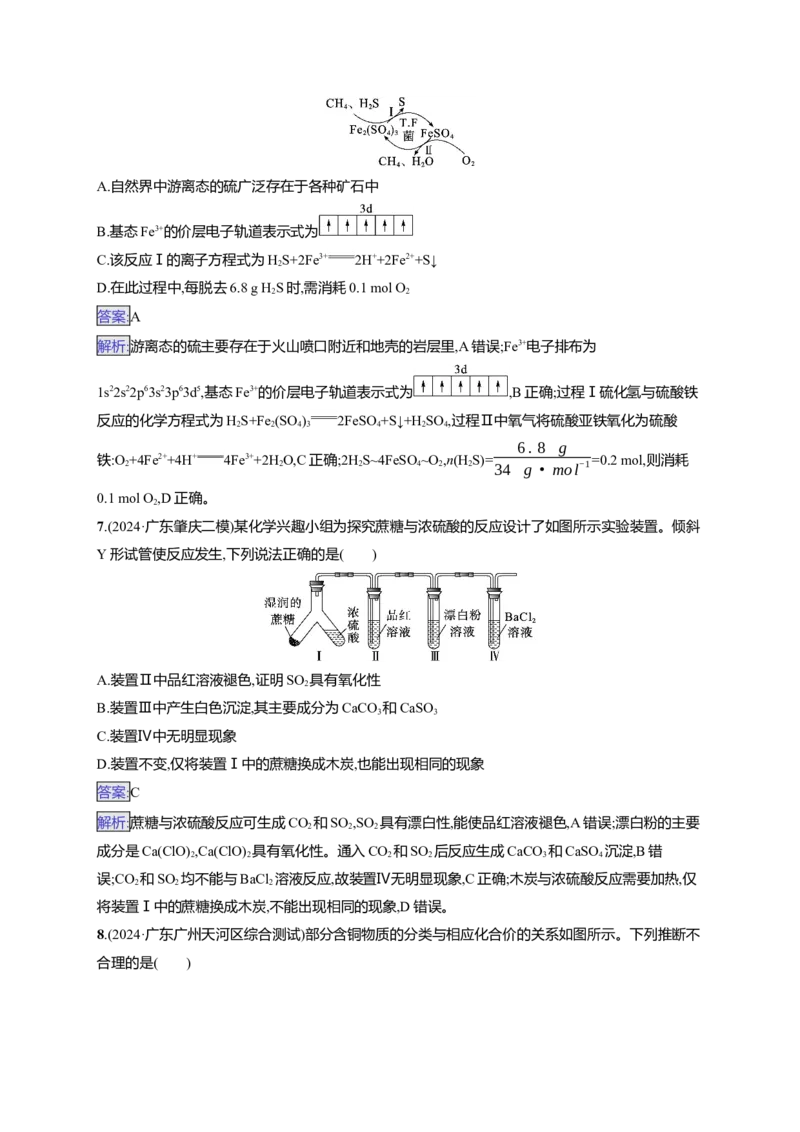
4.(2024·广东广州天河区综合测试二)生产、生活中蕴藏着丰富的化学知识。下列劳动项目与所述的
化学知识没有关联的是( )
选项 劳动项目 化学知识
A 用碳铵(NH HCO )给农作物施肥 NH HCO 受热易分解
4 3 4 3
B 用硫酸钡做钡餐检查胃病 BaSO 既不溶于水,也不溶于酸
4
C 用纯碱溶液清洗抽油烟机上的油渍 油脂在碱性条件下易水解
D 用活性炭清除冰箱中的异味 活性炭具有吸附性
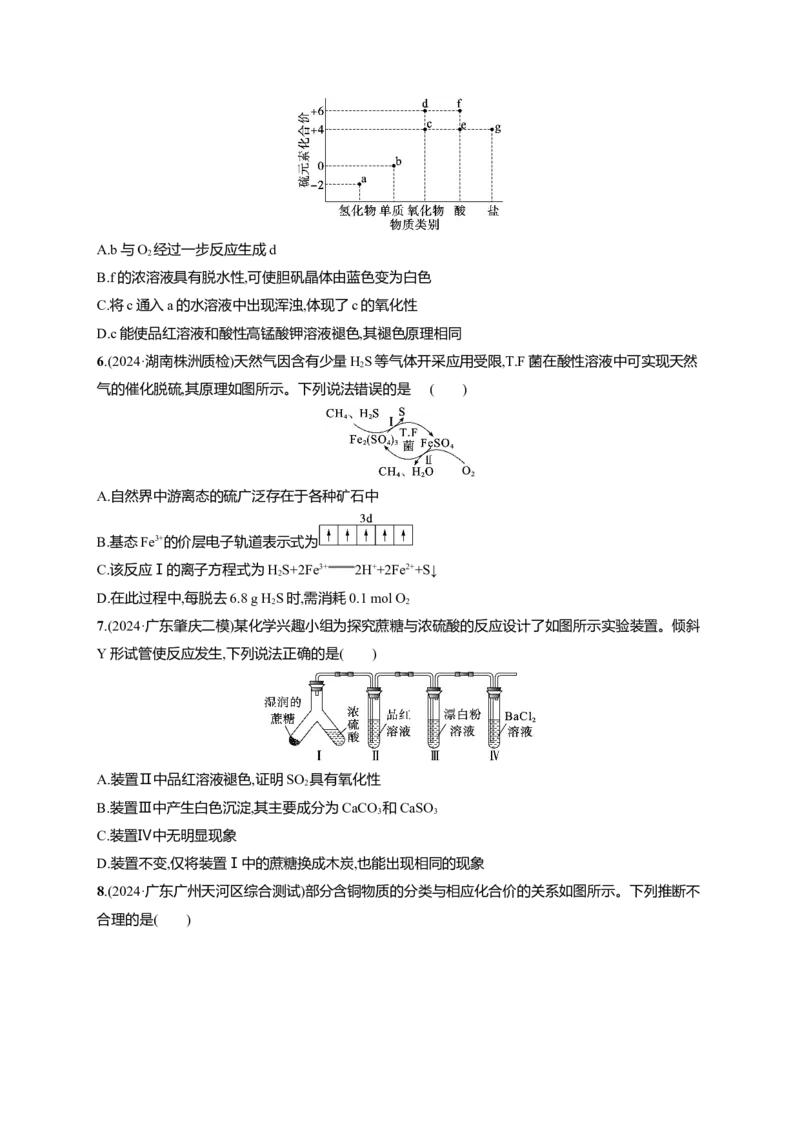
5.(2024·广东名校4月份联考)部分含硫物质的分类与相应化合价的关系如图所示。下列说法正确的
是 ( )A.b与O 经过一步反应生成d
2
B.f的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色
C.将c通入a的水溶液中出现浑浊,体现了c的氧化性
D.c能使品红溶液和酸性高锰酸钾溶液褪色,其褪色原理相同
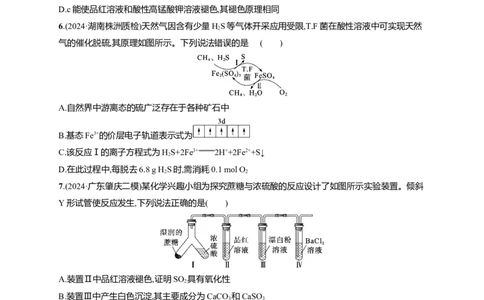
6.(2024·湖南株洲质检)天然气因含有少量HS等气体开采应用受限,T.F菌在酸性溶液中可实现天然
2
气的催化脱硫,其原理如图所示。下列说法错误的是 ( )
A.自然界中游离态的硫广泛存在于各种矿石中
B.基态Fe3+的价层电子轨道表示式为
C.该反应Ⅰ的离子方程式为HS+2Fe3+ 2H++2Fe2++S↓
2
D.在此过程中,每脱去6.8 g H S时,需消耗0.1 mol O
2 2
7.(2024·广东肇庆二模)某化学兴趣小组为探究蔗糖与浓硫酸的反应设计了如图所示实验装置。倾斜
Y形试管使反应发生,下列说法正确的是( )
A.装置Ⅱ中品红溶液褪色,证明SO 具有氧化性
2
B.装置Ⅲ中产生白色沉淀,其主要成分为CaCO 和CaSO
3 3
C.装置Ⅳ中无明显现象
D.装置不变,仅将装置Ⅰ中的蔗糖换成木炭,也能出现相同的现象
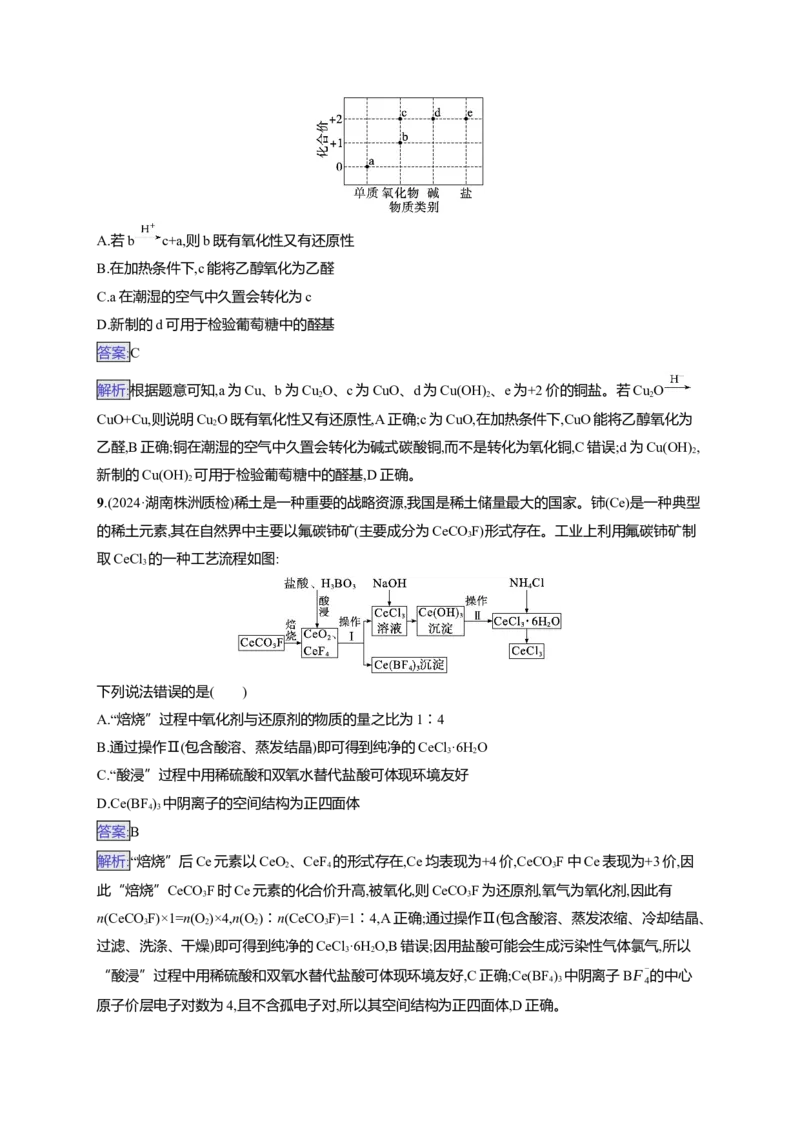
8.(2024·广东广州天河区综合测试)部分含铜物质的分类与相应化合价的关系如图所示。下列推断不
合理的是( )A.若b c+a,则b既有氧化性又有还原性
B.在加热条件下,c能将乙醇氧化为乙醛
C.a在潮湿的空气中久置会转化为c
D.新制的d可用于检验葡萄糖中的醛基
9.(2024·湖南株洲质检)稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈(Ce)是一种典型
的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为CeCO F)形式存在。工业上利用氟碳铈矿制
3
取CeCl 的一种工艺流程如图:
3
下列说法错误的是( )
A.“焙烧”过程中氧化剂与还原剂的物质的量之比为1∶4
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的CeCl ·6H O
3 2
C.“酸浸”过程中用稀硫酸和双氧水替代盐酸可体现环境友好
D.Ce(BF ) 中阴离子的空间结构为正四面体
4 3
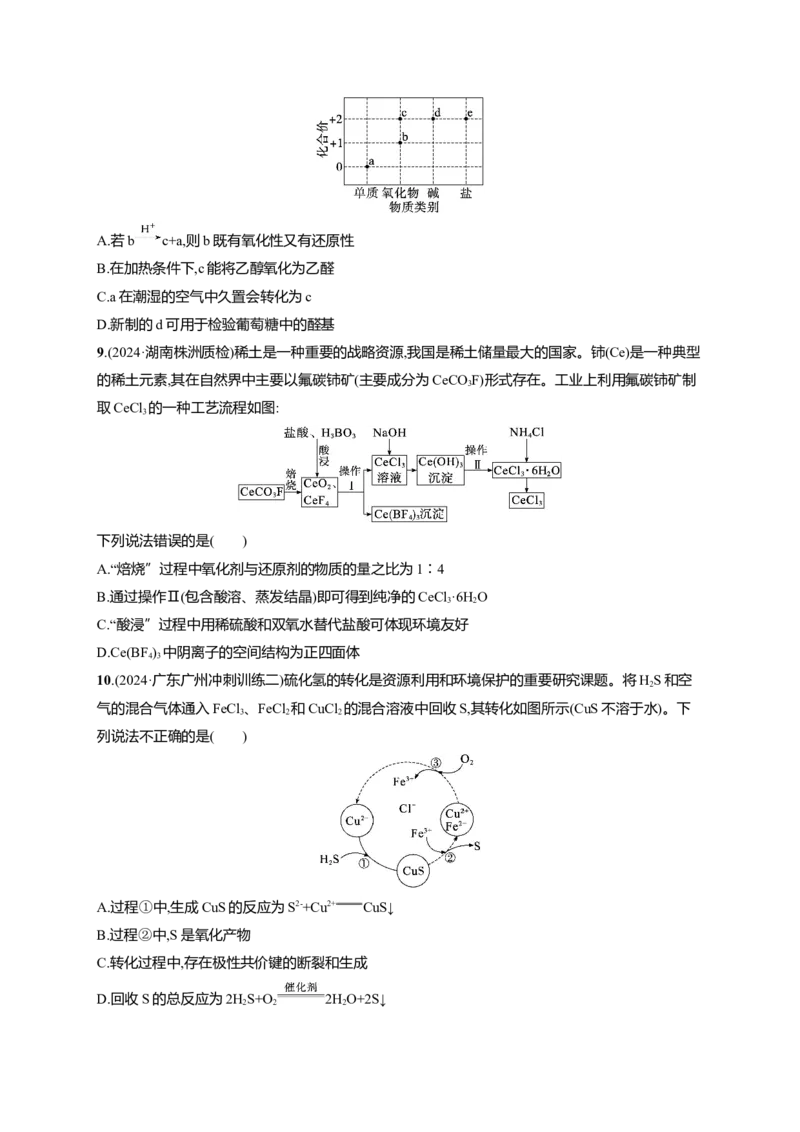
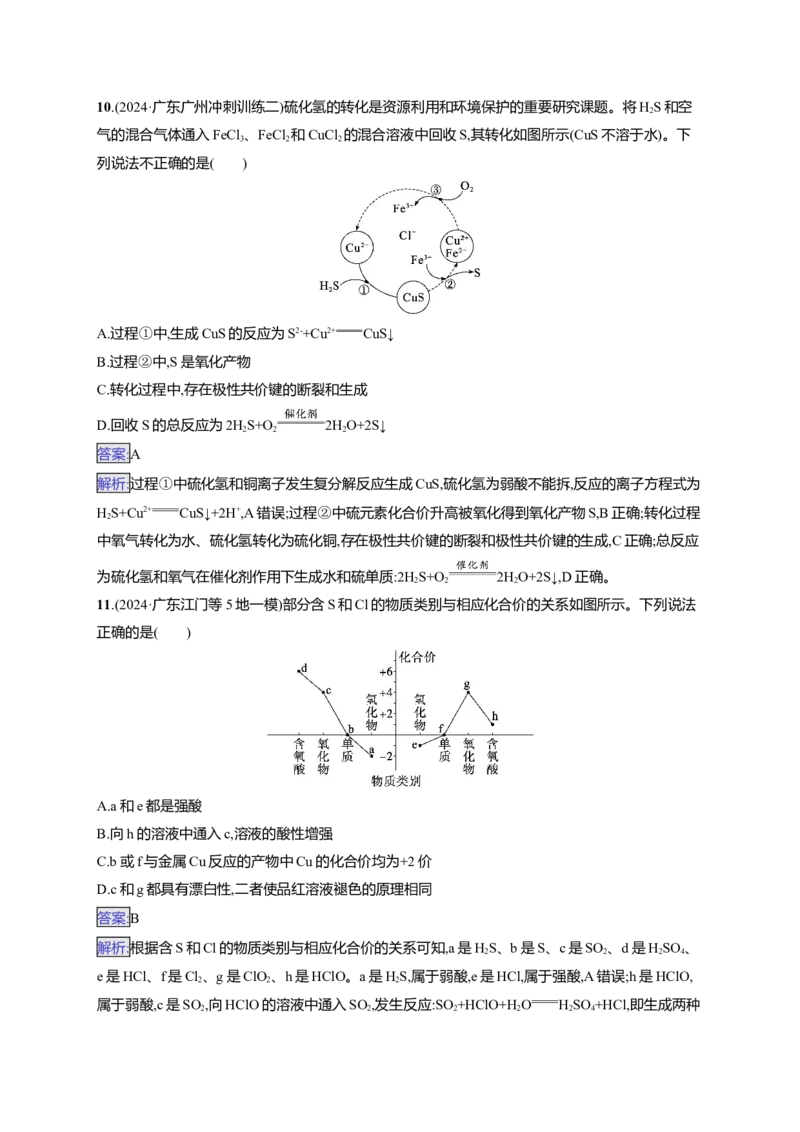
10.(2024·广东广州冲刺训练二)硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空
2
气的混合气体通入FeCl 、FeCl 和CuCl 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下
3 2 2
列说法不正确的是( )
A.过程①中,生成CuS的反应为S2-+Cu2+ CuS↓
B.过程②中,S是氧化产物
C.转化过程中,存在极性共价键的断裂和生成
D.回收S的总反应为2HS+O 2HO+2S↓
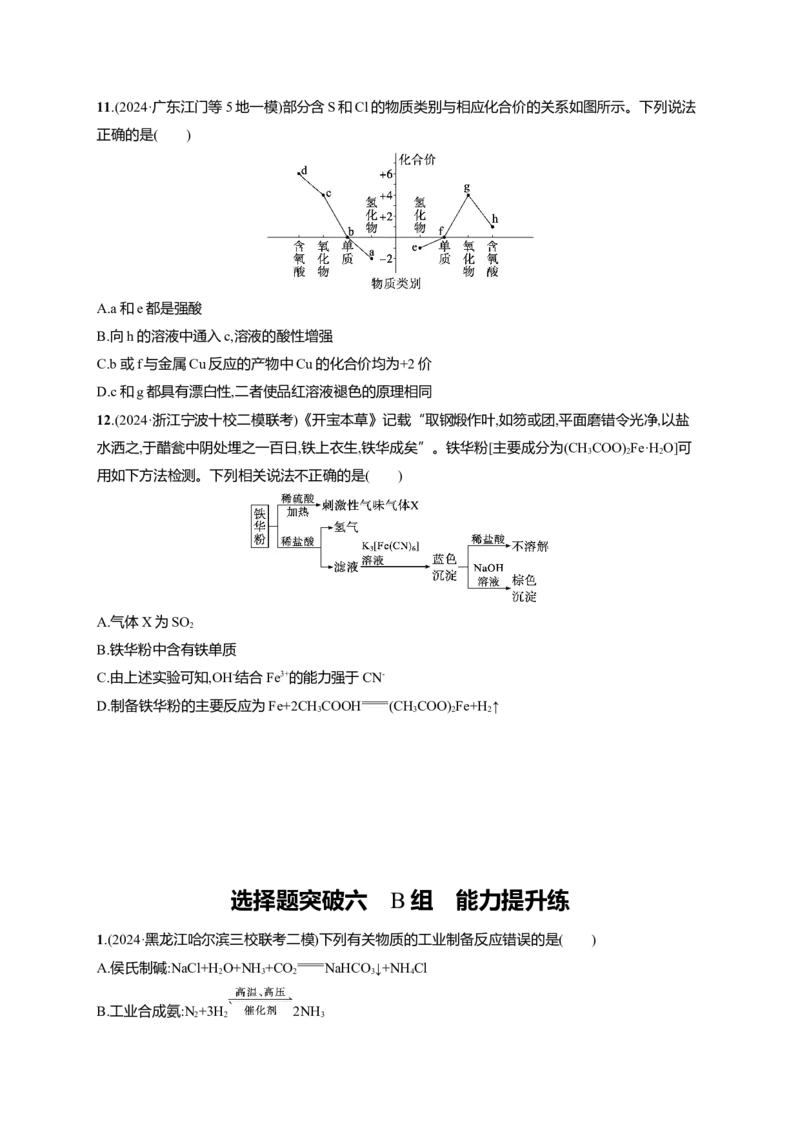
2 2 211.(2024·广东江门等5地一模)部分含S和Cl的物质类别与相应化合价的关系如图所示。下列说法
正确的是( )
A.a和e都是强酸
B.向h的溶液中通入c,溶液的酸性增强
C.b或f与金属Cu反应的产物中Cu的化合价均为+2价
D.c和g都具有漂白性,二者使品红溶液褪色的原理相同
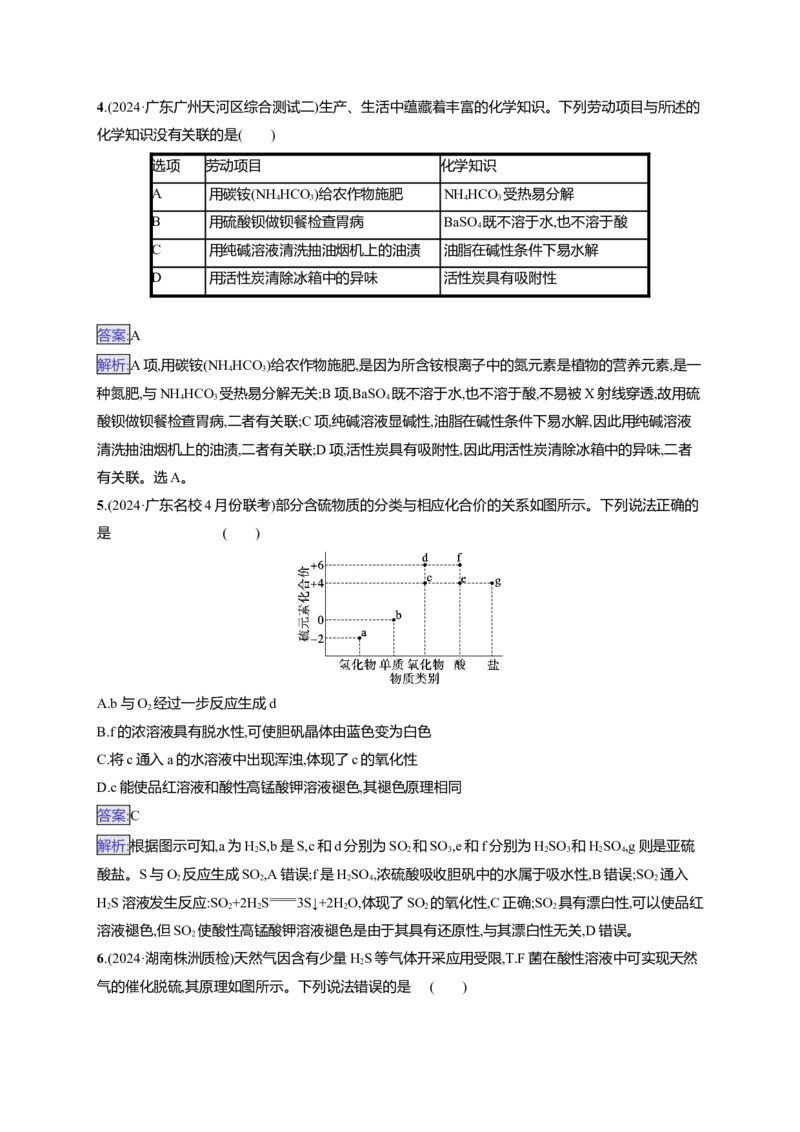
12.(2024·浙江宁波十校二模联考)《开宝本草》记载“取钢煅作叶,如笏或团,平面磨错令光净,以盐
水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要成分为(CHCOO) Fe·H O]可
3 2 2
用如下方法检测。下列相关说法不正确的是( )
A.气体X为SO
2
B.铁华粉中含有铁单质
C.由上述实验可知,OH-结合Fe3+的能力强于CN-
D.制备铁华粉的主要反应为Fe+2CH COOH (CHCOO) Fe+H ↑
3 3 2 2
选择题突破六 B 组 能力提升练
1.(2024·黑龙江哈尔滨三校联考二模)下列有关物质的工业制备反应错误的是( )
A.侯氏制碱:NaCl+HO+NH +CO NaHCO ↓+NHCl
2 3 2 3 4
B.工业合成氨:N +3H 2NH
2 2 3C.氯碱工业:2NaCl+2HO 2NaOH+H ↑+Cl↑
2 2 2
D.冶炼金属铝:2AlCl 2Al+3Cl ↑
3 2
答案:D
解析:侯氏制碱法是向饱和氯化钠溶液中通入氨气、二氧化碳气体生成碳酸氢钠固体,化学方程式为
NaCl+H O+NH +CO NaHCO ↓+NHCl,A正确;工业合成氨反应的化学方程式为N+3H
2 3 2 3 4 2 2
2NH ,B正确;氯碱工业是电解饱和食盐水,反应的化学方程式为2NaCl+2H O
3 2
2NaOH+H ↑+Cl↑,C正确;三氯化铝是共价化合物,熔融态不能电离出自由移动的离子,D错误。
2 2
2.(2024·浙江温州二模)侯氏制碱法利用CO、NH 及饱和NaCl溶液先制得NaHCO ,进一步生产
2 3 3
NaCO,下列说法不正确的是( )
2 3
A.生产中,向溶有CO 的饱和食盐水中通入NH ,可析出NaHCO 固体
2 3 3
B.将所得NaHCO 固体加热生产出纯碱
3
C.碳酸氢钠和碳酸钠的溶液均呈碱性,可用作食用碱或工业用碱
D.向新制氯水中加入少量碳酸氢钠,可提高氯水的漂白效果
答案:A
解析:二氧化碳在水中的溶解度较小、NH 极易溶于水,所以生产中应向溶有NH 的饱和食盐水中通
3 3
入过量CO,增大溶液中含碳粒子的浓度,析出NaHCO 固体,A错误;NaHCO 热稳定性不强,受热易分
2 3 3
解,将所得NaHCO 固体加热分解可生成碳酸钠,B正确;碳酸是二元弱酸,碳酸氢钠和碳酸钠为强碱弱
3
酸盐,均能水解,其溶液均呈碱性,可用作食用碱或工业用碱,C正确;向新制氯水中加入少量碳酸氢钠,
碳酸氢钠能和盐酸反应,促进氯气和水的反应正向进行,溶液中次氯酸的浓度增大,可提高氯水的漂白
效果,D正确。
3.(2024·广东高三二模)化学创造美好生活。下列应用实例与所述的化学知识没有关联的是( )
选项 应用实例 化学知识
A 利用聚苯乙烯制作泡沫包装材料 聚苯乙烯燃烧生成CO 和HO
2 2
B 用NaO 作潜水艇中的供氧剂 NaO 与CO 或HO反应生成O
2 2 2 2 2 2 2
C 将液态植物油制成人造奶油 液态植物油能与H 发生加成反应
2
D 从海带灰中提取碘单质 海带灰中的I-可被氧化
答案:A
解析:因为聚苯乙烯没有毒副作用,所以可制作泡沫包装材料,与聚苯乙烯燃烧生成CO 和HO没有关
2 2
联,A错误;由于NaO 与CO 或HO反应生成O,所以可用NaO 作潜水艇中的供氧剂,B正确;因为液
2 2 2 2 2 2 2
态植物油能与H 发生加成反应,所以可将液态植物油制成人造奶油,C正确;因为海带灰中的I-可被氧
2
化,所以可以用氧化剂氧化I-,从海带灰中提取碘单质,D正确。4.(2024·广东广州天河区综合测试二)生产、生活中蕴藏着丰富的化学知识。下列劳动项目与所述的
化学知识没有关联的是( )
选项 劳动项目 化学知识
A 用碳铵(NH HCO )给农作物施肥 NH HCO 受热易分解
4 3 4 3
B 用硫酸钡做钡餐检查胃病 BaSO 既不溶于水,也不溶于酸
4
C 用纯碱溶液清洗抽油烟机上的油渍 油脂在碱性条件下易水解
D 用活性炭清除冰箱中的异味 活性炭具有吸附性
答案:A
解析:A项,用碳铵(NH HCO )给农作物施肥,是因为所含铵根离子中的氮元素是植物的营养元素,是一
4 3
种氮肥,与NH HCO 受热易分解无关;B项,BaSO 既不溶于水,也不溶于酸,不易被X射线穿透,故用硫
4 3 4
酸钡做钡餐检查胃病,二者有关联;C项,纯碱溶液显碱性,油脂在碱性条件下易水解,因此用纯碱溶液
清洗抽油烟机上的油渍,二者有关联;D项,活性炭具有吸附性,因此用活性炭清除冰箱中的异味,二者
有关联。选A。
5.(2024·广东名校4月份联考)部分含硫物质的分类与相应化合价的关系如图所示。下列说法正确的
是 ( )
A.b与O 经过一步反应生成d
2
B.f的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色
C.将c通入a的水溶液中出现浑浊,体现了c的氧化性
D.c能使品红溶液和酸性高锰酸钾溶液褪色,其褪色原理相同
答案:C
解析:根据图示可知,a为HS,b是S,c和d分别为SO 和SO ,e和f分别为HSO 和HSO ,g则是亚硫
2 2 3 2 3 2 4
酸盐。S与O 反应生成SO ,A错误;f是HSO ,浓硫酸吸收胆矾中的水属于吸水性,B错误;SO 通入
2 2 2 4 2
HS溶液发生反应:SO+2H S 3S↓+2HO,体现了SO 的氧化性,C正确;SO 具有漂白性,可以使品红
2 2 2 2 2 2
溶液褪色,但SO 使酸性高锰酸钾溶液褪色是由于其具有还原性,与其漂白性无关,D错误。
2
6.(2024·湖南株洲质检)天然气因含有少量HS等气体开采应用受限,T.F菌在酸性溶液中可实现天然
2
气的催化脱硫,其原理如图所示。下列说法错误的是 ( )A.自然界中游离态的硫广泛存在于各种矿石中
B.基态Fe3+的价层电子轨道表示式为
C.该反应Ⅰ的离子方程式为HS+2Fe3+ 2H++2Fe2++S↓
2
D.在此过程中,每脱去6.8 g H S时,需消耗0.1 mol O
2 2
答案:A
解析:游离态的硫主要存在于火山喷口附近和地壳的岩层里,A错误;Fe3+电子排布为
1s22s22p63s23p63d5,基态Fe3+的价层电子轨道表示式为 ,B正确;过程Ⅰ硫化氢与硫酸铁
反应的化学方程式为HS+Fe (SO ) 2FeSO +S↓+H SO ,过程Ⅱ中氧气将硫酸亚铁氧化为硫酸
2 2 4 3 4 2 4
6.8 g
铁:O +4Fe2++4H+ 4Fe3++2H O,C正确;2H S~4FeSO ~O ,n(H S)= =0.2 mol,则消耗
2 2 2 4 2 2 34 g·mol-1
0.1 mol O,D正确。
2
7.(2024·广东肇庆二模)某化学兴趣小组为探究蔗糖与浓硫酸的反应设计了如图所示实验装置。倾斜
Y形试管使反应发生,下列说法正确的是( )
A.装置Ⅱ中品红溶液褪色,证明SO 具有氧化性
2
B.装置Ⅲ中产生白色沉淀,其主要成分为CaCO 和CaSO
3 3
C.装置Ⅳ中无明显现象
D.装置不变,仅将装置Ⅰ中的蔗糖换成木炭,也能出现相同的现象
答案:C
解析:蔗糖与浓硫酸反应可生成CO 和SO ,SO 具有漂白性,能使品红溶液褪色,A错误;漂白粉的主要
2 2 2
成分是Ca(ClO) ,Ca(ClO) 具有氧化性。通入CO 和SO 后反应生成CaCO 和CaSO 沉淀,B错
2 2 2 2 3 4
误;CO 和SO 均不能与BaCl 溶液反应,故装置Ⅳ无明显现象,C正确;木炭与浓硫酸反应需要加热,仅
2 2 2
将装置Ⅰ中的蔗糖换成木炭,不能出现相同的现象,D错误。
8.(2024·广东广州天河区综合测试)部分含铜物质的分类与相应化合价的关系如图所示。下列推断不
合理的是( )A.若b c+a,则b既有氧化性又有还原性
B.在加热条件下,c能将乙醇氧化为乙醛
C.a在潮湿的空气中久置会转化为c
D.新制的d可用于检验葡萄糖中的醛基
答案:C
解析:根据题意可知,a为Cu、b为Cu O、c为CuO、d为Cu(OH) 、e为+2价的铜盐。若Cu O
2 2 2
CuO+Cu,则说明Cu O既有氧化性又有还原性,A正确;c为CuO,在加热条件下,CuO能将乙醇氧化为
2
乙醛,B正确;铜在潮湿的空气中久置会转化为碱式碳酸铜,而不是转化为氧化铜,C错误;d为Cu(OH) ,
2
新制的Cu(OH) 可用于检验葡萄糖中的醛基,D正确。
2
9.(2024·湖南株洲质检)稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈(Ce)是一种典型
的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为CeCO F)形式存在。工业上利用氟碳铈矿制
3
取CeCl 的一种工艺流程如图:
3
下列说法错误的是( )
A.“焙烧”过程中氧化剂与还原剂的物质的量之比为1∶4
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的CeCl ·6H O
3 2
C.“酸浸”过程中用稀硫酸和双氧水替代盐酸可体现环境友好
D.Ce(BF ) 中阴离子的空间结构为正四面体
4 3
答案:B
解析:“焙烧”后Ce元素以CeO、CeF 的形式存在,Ce均表现为+4价,CeCO F中Ce表现为+3价,因
2 4 3
此“焙烧”CeCO F时Ce元素的化合价升高,被氧化,则CeCO F为还原剂,氧气为氧化剂,因此有
3 3
n(CeCOF)×1=n(O )×4,n(O )∶n(CeCOF)=1∶4,A正确;通过操作Ⅱ(包含酸溶、蒸发浓缩、冷却结晶、
3 2 2 3
过滤、洗涤、干燥)即可得到纯净的CeCl ·6H O,B错误;因用盐酸可能会生成污染性气体氯气,所以
3 2
“酸浸”过程中用稀硫酸和双氧水替代盐酸可体现环境友好,C正确;Ce(BF )
中阴离子BF-
的中心
4 3 4
原子价层电子对数为4,且不含孤电子对,所以其空间结构为正四面体,D正确。10.(2024·广东广州冲刺训练二)硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空
2
气的混合气体通入FeCl 、FeCl 和CuCl 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下
3 2 2
列说法不正确的是( )
A.过程①中,生成CuS的反应为S2-+Cu2+ CuS↓
B.过程②中,S是氧化产物
C.转化过程中,存在极性共价键的断裂和生成
D.回收S的总反应为2HS+O 2HO+2S↓
2 2 2
答案:A
解析:过程①中硫化氢和铜离子发生复分解反应生成CuS,硫化氢为弱酸不能拆,反应的离子方程式为
HS+Cu2+ CuS↓+2H+,A错误;过程②中硫元素化合价升高被氧化得到氧化产物S,B正确;转化过程
2
中氧气转化为水、硫化氢转化为硫化铜,存在极性共价键的断裂和极性共价键的生成,C正确;总反应
为硫化氢和氧气在催化剂作用下生成水和硫单质:2H S+O 2HO+2S↓,D正确。
2 2 2
11.(2024·广东江门等5地一模)部分含S和Cl的物质类别与相应化合价的关系如图所示。下列说法
正确的是( )
A.a和e都是强酸
B.向h的溶液中通入c,溶液的酸性增强
C.b或f与金属Cu反应的产物中Cu的化合价均为+2价
D.c和g都具有漂白性,二者使品红溶液褪色的原理相同
答案:B
解析:根据含S和Cl的物质类别与相应化合价的关系可知,a是HS、b是S、c是SO 、d是HSO 、
2 2 2 4
e是HCl、f是Cl、g是ClO 、h是HClO。a是HS,属于弱酸,e是HCl,属于强酸,A错误;h是HClO,
2 2 2
属于弱酸,c是SO ,向HClO的溶液中通入SO ,发生反应:SO+HClO+H O HSO +HCl,即生成两种
2 2 2 2 2 4强酸,则溶液酸性增强,B正确;b是S、f是Cl,两者与金属Cu反应的产物分别为Cu S、CuCl ,产物中
2 2 2
Cu的化合价分别为+1价、+2价,C错误;c是SO 、g是ClO ,SO 具有漂白性,是因为它能与某些有色
2 2 2
物质生成不稳定的无色物质,ClO 具有漂白性,是因为ClO 具有氧化性,二者使品红溶液褪色的原理
2 2
不相同,D错误。
12.(2024·浙江宁波十校二模联考)《开宝本草》记载“取钢煅作叶,如笏或团,平面磨错令光净,以盐
水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要成分为(CHCOO) Fe·H O]可
3 2 2
用如下方法检测。下列相关说法不正确的是( )
A.气体X为SO
2
B.铁华粉中含有铁单质
C.由上述实验可知,OH-结合Fe3+的能力强于CN-
D.制备铁华粉的主要反应为Fe+2CH COOH (CHCOO) Fe+H ↑
3 3 2 2
答案:A
解析:向铁华粉中加入稀硫酸并加热,产生的刺激性气味的气体X为醋酸蒸气,A错误;向铁华粉中加
入稀盐酸生成了氢气,有氢气生成说明铁华粉中含有铁单质,B正确;向铁华粉中加入稀盐酸得到的滤
液中含有Fe2+,Fe2+可与K[Fe(CN) ]反应产生KFe[Fe(CN) ]蓝色沉淀,氢氧根离子能与蓝色沉淀反应
3 6 6
生成棕色沉淀,说明有氢氧化铁沉淀生成,说明氢氧根离子结合铁离子的能力强于CN-,C正确;由题中
信息可知,制备铁华粉的主要反应方程式为Fe+2CH COOH (CHCOO) Fe+H ↑,D正确。
3 3 2 2