文档内容
选择题突破六 A 组 基础巩固练
题组一 常见无机物的性质与转化
1.(2024·海南省海南中学一模)铁、铜及其化合物之间的转化具有重要应用。下列说法错误的是(
)
A.常温下使用铁质容器盛装浓硫酸
B.氯化铁溶液在聚合物的基材上蚀刻出铜电路
C.电解精炼铜时,粗铜连电源的正极
D.向饱和FeCl 溶液中滴加稀氨水制备氢氧化铁胶体
3
2.(2024·北京卷)关于NaCO 和NaHCO 的下列说法中,不正确的是( )
2 3 3
A.两种物质的溶液中,所含微粒的种类相同
B.可用NaOH溶液使NaHCO 转化为NaCO
3 2 3
C.利用两者热稳定性差异,可从它们的固体混合物中除去NaHCO
3
D.室温下二者饱和溶液的pH差约为4,主要是由于它们的溶解度差异
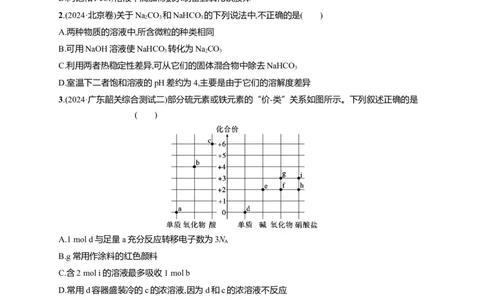
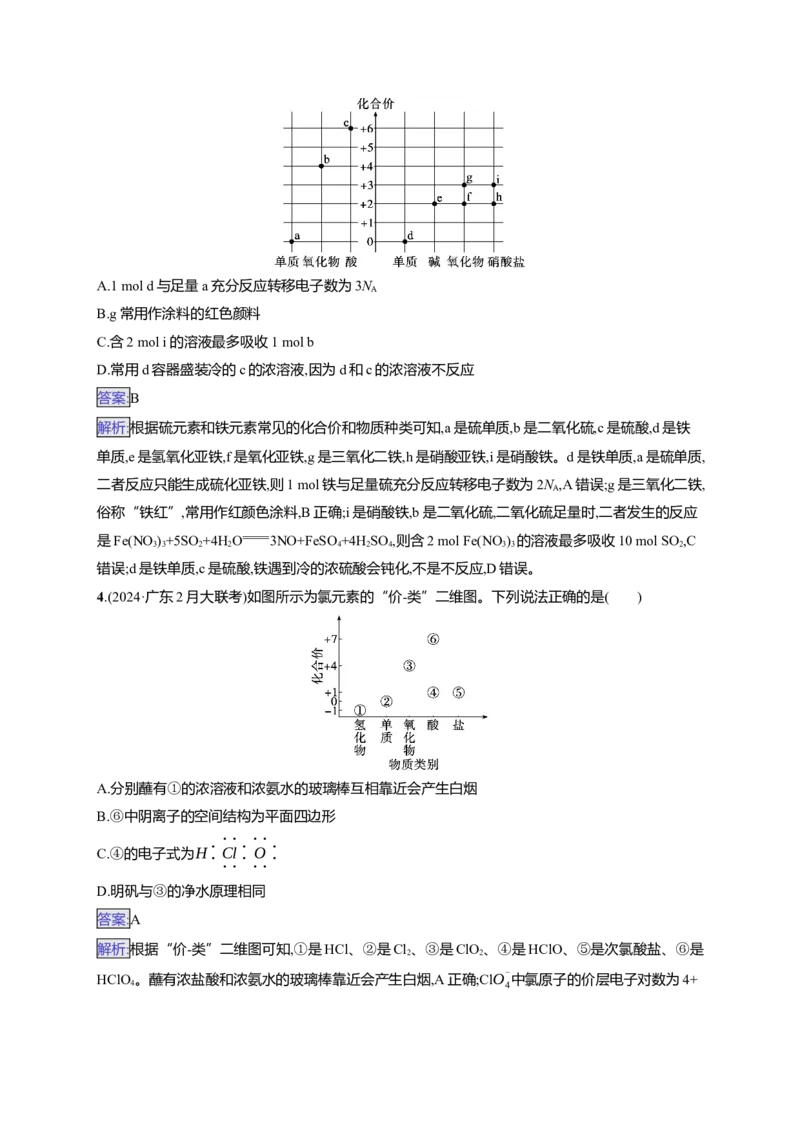
3.(2024·广东韶关综合测试二)部分硫元素或铁元素的“价-类”关系如图所示。下列叙述正确的是
( )
A.1 mol d与足量a充分反应转移电子数为3N
A
B.g常用作涂料的红色颜料
C.含2 mol i的溶液最多吸收1 mol b
D.常用d容器盛装冷的c的浓溶液,因为d和c的浓溶液不反应
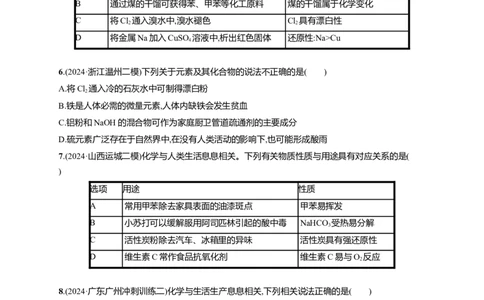
4.(2024·广东2月大联考)如图所示为氯元素的“价-类”二维图。下列说法正确的是( )
A.分别蘸有①的浓溶液和浓氨水的玻璃棒互相靠近会产生白烟B.⑥中阴离子的空间结构为平面四边形
·· ··
C.④的电子式为H·Cl· O ·
· · ·
·· ··
D.明矾与③的净水原理相同
题组二 常见物质的性质与应用
5.(2024·广东肇庆二模)下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A HCl的酸性强于CHCOOH 盐酸的pH一定小于醋酸溶液
3
B 通过煤的干馏可获得苯、甲苯等化工原料 煤的干馏属于化学变化
C 将Cl 通入溴水中,溴水褪色 Cl 具有漂白性
2 2
D 将金属Na加入CuSO 溶液中,析出红色固体 还原性:Na>Cu
4
6.(2024·浙江温州二模)下列关于元素及其化合物的说法不正确的是( )
A.将Cl 通入冷的石灰水中可制得漂白粉
2
B.铁是人体必需的微量元素,人体内缺铁会发生贫血
C.铝粉和NaOH的混合物可作为家庭厨卫管道疏通剂的主要成分
D.硫元素广泛存在于自然界中,在没有人类活动的影响下,也可能形成酸雨
7.(2024·山西运城二模)化学与人类生活息息相关。下列有关物质性质与用途具有对应关系的是(
)
选项 用途 性质
A 常用甲苯除去家具表面的油漆斑点 甲苯易挥发
B 小苏打可以缓解服用阿司匹林引起的酸中毒 NaHCO 受热易分解
3
C 活性炭粉除去汽车、冰箱里的异味 活性炭具有强还原性
D 维生素C常作食品抗氧化剂 维生素C易与O 反应
2
8.(2024·广东广州冲刺训练二)化学与生活生产息息相关,下列相关说法正确的是( )
A.为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
B.基于界面效应的新型开关中含有碲元素和钛元素,这两种元素均为过渡元素
C.燃料的脱硫、NO的催化转化都是减少温室效应的措施
D.氧化铁是质地疏松的红色固体,用作颜料为生活带来一抹红
9.(2024·山东济南3月模拟)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.Ag与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜
B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明HSO 酸性强于HCl
2 4
C.将CO 通入Ba(NO ) 溶液无明显现象,则将SO 通入Ba(NO ) 溶液也无明显现象
2 3 2 2 3 2D.向NaClO溶液中滴加酚酞溶液,溶液先变红后褪色,证明NaClO在溶液中发生了水解反应
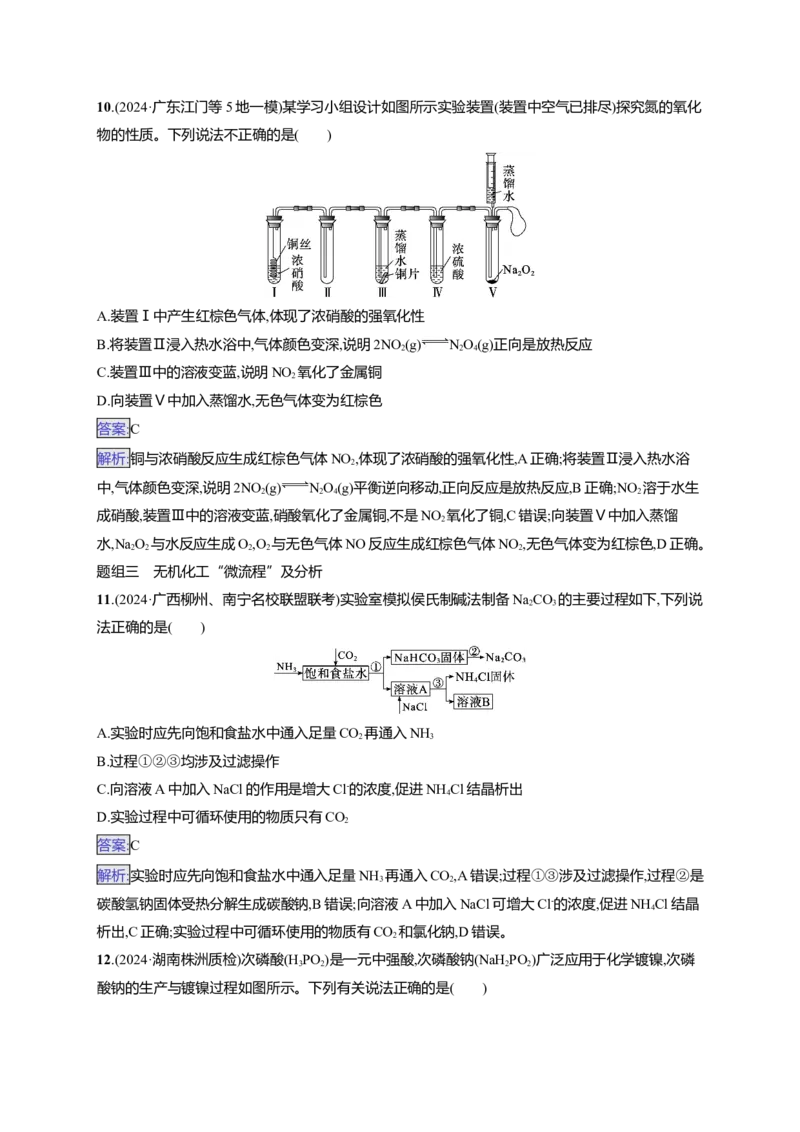
10.(2024·广东江门等5地一模)某学习小组设计如图所示实验装置(装置中空气已排尽)探究氮的氧化
物的性质。下列说法不正确的是( )
A.装置Ⅰ中产生红棕色气体,体现了浓硝酸的强氧化性
B.将装置Ⅱ浸入热水浴中,气体颜色变深,说明2NO (g) NO(g)正向是放热反应
2 2 4
C.装置Ⅲ中的溶液变蓝,说明NO 氧化了金属铜
2
D.向装置Ⅴ中加入蒸馏水,无色气体变为红棕色
题组三 无机化工“微流程”及分析
11.(2024·广西柳州、南宁名校联盟联考)实验室模拟侯氏制碱法制备NaCO 的主要过程如下,下列说
2 3
法正确的是( )
A.实验时应先向饱和食盐水中通入足量CO 再通入NH
2 3
B.过程①②③均涉及过滤操作
C.向溶液A中加入NaCl的作用是增大Cl-的浓度,促进NH Cl结晶析出
4
D.实验过程中可循环使用的物质只有CO
2
12.(2024·湖南株洲质检)次磷酸(H PO )是一元中强酸,次磷酸钠(NaH PO )广泛应用于化学镀镍,次磷
3 2 2 2
酸钠的生产与镀镍过程如图所示。下列有关说法正确的是( )
A.Ni2+的核外电子有26种空间运动状态
B.“碱溶”时氧化剂与还原剂的物质的量之比为3∶1
C.PH
、PO3- 、P(正四面体结构)中的键角:PO3-
>PH>P
3 4 4 4 3 4
D.次磷酸铵与足量氢氧化钠共热:N H+ 4+H 2 P O 2 - +3OH- NH 3 +3H 2 O+P O 2 3-
13.(2024·黑龙江大庆实验中学模拟)下列有关物质的工业制备过程,在给定条件下能实现的是( )
A.冶炼铝:铝土矿 Na[Al(OH)] 无水AlCl Al
4 3B.工业制硝酸:NH NO NO HNO
3 2 3
C.海带提碘:海带 海带灰 I(aq) I
2 2
D.工业制硫酸:S SO HSO
3 2 4
选择题突破六 A 组 基础巩固练
题组一 常见无机物的性质与转化
1.(2024·海南省海南中学一模)铁、铜及其化合物之间的转化具有重要应用。下列说法错误的是(
)
A.常温下使用铁质容器盛装浓硫酸
B.氯化铁溶液在聚合物的基材上蚀刻出铜电路
C.电解精炼铜时,粗铜连电源的正极
D.向饱和FeCl 溶液中滴加稀氨水制备氢氧化铁胶体
3
答案:D
解析:常温下浓硫酸可以使铁钝化,所以常温下可以使用铁质容器盛装浓硫酸,A正确;氯化铁溶液在
聚合物的基材上蚀刻出铜电路的反应为2Fe3++Cu Cu2++2Fe2+,B正确;电解精炼铜时,粗铜作阳极,
应连电源的正极,C正确;将饱和FeCl 溶液滴入沸水中才能制备氢氧化铁胶体,D错误。
3
2.(2024·北京卷)关于NaCO 和NaHCO 的下列说法中,不正确的是( )
2 3 3
A.两种物质的溶液中,所含微粒的种类相同
B.可用NaOH溶液使NaHCO 转化为NaCO
3 2 3
C.利用两者热稳定性差异,可从它们的固体混合物中除去NaHCO
3
D.室温下二者饱和溶液的pH差约为4,主要是由于它们的溶解度差异
答案:D
解析:NaCO 和NaHCO
的溶液中均存在HO、HCO、H+、OH-、Na+、CO2- 、HCO-
,A正确;向
2 3 3 2 2 3 3 3
NaHCO 溶液加入NaOH会发生反应NaOH+NaHCO NaCO+H O,B正确;NaHCO 受热易分解
3 3 2 3 2 3
可转化为NaCO,而NaCO 受热不易分解,利用二者热稳定性差异,可从它们的固体混合物中除去
2 3 2 3
NaHCO ,C正确;室温下NaCO 和NaHCO
饱和溶液的pH相差较大的主要原因是CO2-
的水解程度
3 2 3 3 3
远大于HCO-
,D错误。
3
3.(2024·广东韶关综合测试二)部分硫元素或铁元素的“价-类”关系如图所示。下列叙述正确的是
( )A.1 mol d与足量a充分反应转移电子数为3N
A
B.g常用作涂料的红色颜料
C.含2 mol i的溶液最多吸收1 mol b
D.常用d容器盛装冷的c的浓溶液,因为d和c的浓溶液不反应
答案:B
解析:根据硫元素和铁元素常见的化合价和物质种类可知,a是硫单质,b是二氧化硫,c是硫酸,d是铁
单质,e是氢氧化亚铁,f是氧化亚铁,g是三氧化二铁,h是硝酸亚铁,i是硝酸铁。d是铁单质,a是硫单质,
二者反应只能生成硫化亚铁,则1 mol铁与足量硫充分反应转移电子数为2N ,A错误;g是三氧化二铁,
A
俗称“铁红”,常用作红颜色涂料,B正确;i是硝酸铁,b是二氧化硫,二氧化硫足量时,二者发生的反应
是Fe(NO )+5SO+4H O 3NO+FeSO +4H SO ,则含2 mol Fe(NO) 的溶液最多吸收10 mol SO ,C
3 3 2 2 4 2 4 3 3 2
错误;d是铁单质,c是硫酸,铁遇到冷的浓硫酸会钝化,不是不反应,D错误。
4.(2024·广东2月大联考)如图所示为氯元素的“价-类”二维图。下列说法正确的是( )
A.分别蘸有①的浓溶液和浓氨水的玻璃棒互相靠近会产生白烟
B.⑥中阴离子的空间结构为平面四边形
·· ··
C.④的电子式为H·Cl· O ·
· · ·
·· ··
D.明矾与③的净水原理相同
答案:A
解析:根据“价-类”二维图可知,①是HCl、②是Cl、③是ClO 、④是HClO、⑤是次氯酸盐、⑥是
2 2
HClO。蘸有浓盐酸和浓氨水的玻璃棒靠近会产生白烟,A正确;ClO-
中氯原子的价层电子对数为4+
4 47+1-2×4 ·· ··
=4、没有孤电子对,故其空间结构是正四面体,B错误;HClO的电子式为H· O ·Cl· ,C
2 · · ·
·· ··
错误;明矾和ClO 均可用作净水剂,明矾水解生成的氢氧化铝胶体可以吸附水中的悬浮物,达到净水
2
的目的,二氧化氯净水是利用其强氧化性杀死水中的细菌和病毒,原理不同,D错误。
题组二 常见物质的性质与应用
5.(2024·广东肇庆二模)下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A HCl的酸性强于CHCOOH 盐酸的pH一定小于醋酸溶液
3
B 通过煤的干馏可获得苯、甲苯等化工原料 煤的干馏属于化学变化
C 将Cl 通入溴水中,溴水褪色 Cl 具有漂白性
2 2
D 将金属Na加入CuSO 溶液中,析出红色固体 还原性:Na>Cu
4
答案:B
解析:A项,HCl为一元强酸,CH COOH为一元弱酸,酸性:HCl>CH COOH,陈述Ⅰ正确;浓度相同时溶
3 3
液的pH:盐酸<醋酸;未告诉浓度关系,无法比较两者pH的相对大小,陈述Ⅱ错误。B项,煤的干馏是隔
绝空气加强热的过程,可获得苯、甲苯等化工原料,该过程属于化学变化,陈述Ⅰ、Ⅱ均正确,也有因
果关系。C项,将氯气通入溴水中,氯气会少量溶于水,溴水不会褪色,氯气也不具备漂白性,陈述Ⅰ、
Ⅱ均错误。D项,将金属Na加入CuSO 溶液中生成氢氧化铜蓝色沉淀、硫酸钠及氢气,陈述Ⅰ错误;
4
故选B。
6.(2024·浙江温州二模)下列关于元素及其化合物的说法不正确的是( )
A.将Cl 通入冷的石灰水中可制得漂白粉
2
B.铁是人体必需的微量元素,人体内缺铁会发生贫血
C.铝粉和NaOH的混合物可作为家庭厨卫管道疏通剂的主要成分
D.硫元素广泛存在于自然界中,在没有人类活动的影响下,也可能形成酸雨
答案:A
解析:向冷的石灰乳中通入氯气可制得漂白粉,A错误;铁是人体必需的微量元素,人体内缺铁易造成
造血原料不足而发生贫血,B正确;利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等
淤积物的腐蚀,同时产生的氢气增加管道内的气压,利于疏通,C正确;硫元素广泛存在于自然界中,火
山喷发时岩浆中的硫化物和硫酸盐会随着岩浆喷出,在没有人类活动的影响下,也可能形成酸雨,D正
确。
7.(2024·山西运城二模)化学与人类生活息息相关。下列有关物质性质与用途具有对应关系的是(
)
选项 用途 性质A 常用甲苯除去家具表面的油漆斑点 甲苯易挥发
B 小苏打可以缓解服用阿司匹林引起的酸中毒 NaHCO 受热易分解
3
C 活性炭粉除去汽车、冰箱里的异味 活性炭具有强还原性
D 维生素C常作食品抗氧化剂 维生素C易与O 反应
2
答案:D
解析:甲苯是有机溶剂,油漆的主要成分是有机化合物,油漆可溶解于甲苯,与甲苯易挥发无关,A错误;
碳酸氢钠可以与酸反应,所以能缓解酸中毒,与NaHCO 受热易分解无关,B错误;活性炭除去异味利用
3
了炭粉的吸附性,与还原性无关,C错误;维生素C保鲜食品,是因为维生素C易与O 反应,消耗O,避
2 2
免食品腐败,D正确。
8.(2024·广东广州冲刺训练二)化学与生活生产息息相关,下列相关说法正确的是( )
A.为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
B.基于界面效应的新型开关中含有碲元素和钛元素,这两种元素均为过渡元素
C.燃料的脱硫、NO的催化转化都是减少温室效应的措施
D.氧化铁是质地疏松的红色固体,用作颜料为生活带来一抹红
答案:D
解析:生石灰或硅胶能吸收水,但是不能吸收氧气,不能防止月饼等富脂食品因被氧化而变质,为防止
食物氧化变质,应当用铁粉作为抗氧化剂,A错误;碲为第五周期第ⅥA族元素,不是过渡元素,B错误;
脱硫、NO的催化转化可减少硫和氮的氧化物的排放,可以减少酸雨等污染,但不能减少温室效应,C
错误;氧化铁是质地疏松的红色固体(Fe O),用作颜料为生活带来一抹红,D正确。
2 3
9.(2024·山东济南3月模拟)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.Ag与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜
B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明HSO 酸性强于HCl
2 4
C.将CO 通入Ba(NO ) 溶液无明显现象,则将SO 通入Ba(NO ) 溶液也无明显现象
2 3 2 2 3 2
D.向NaClO溶液中滴加酚酞溶液,溶液先变红后褪色,证明NaClO在溶液中发生了水解反应
答案:D
解析:实验室通常用稀硝酸清洗银镜,稀硝酸成本更低,A错误;加热浓硫酸与NaCl固体反应的化学方
程式为HSO (浓)+2NaCl 2HCl↑+Na SO ,反应能发生是由于HCl为挥发性酸,不断离开反应体系,
2 4 2 4
使得反应不断进行,与HSO 和HCl的酸性强弱无关,B错误;将SO 通入Ba(NO ) 溶液中,SO 被氧化
2 4 2 3 2 2
为硫酸根离子,会生成BaSO 白色沉淀,C错误;向NaClO溶液中滴加酚酞溶液,溶液先变红后褪色,是
4
由于次氯酸根离子发生水解反应ClO-+H O HClO+OH-,使溶液呈碱性,由于生成的次氯酸具有漂
2
白性,所以溶液变红后又褪色,D正确。10.(2024·广东江门等5地一模)某学习小组设计如图所示实验装置(装置中空气已排尽)探究氮的氧化
物的性质。下列说法不正确的是( )
A.装置Ⅰ中产生红棕色气体,体现了浓硝酸的强氧化性
B.将装置Ⅱ浸入热水浴中,气体颜色变深,说明2NO (g) NO(g)正向是放热反应
2 2 4
C.装置Ⅲ中的溶液变蓝,说明NO 氧化了金属铜
2
D.向装置Ⅴ中加入蒸馏水,无色气体变为红棕色
答案:C
解析:铜与浓硝酸反应生成红棕色气体NO ,体现了浓硝酸的强氧化性,A正确;将装置Ⅱ浸入热水浴
2
中,气体颜色变深,说明2NO (g) NO(g)平衡逆向移动,正向反应是放热反应,B正确;NO 溶于水生
2 2 4 2
成硝酸,装置Ⅲ中的溶液变蓝,硝酸氧化了金属铜,不是NO 氧化了铜,C错误;向装置Ⅴ中加入蒸馏
2
水,Na O 与水反应生成O,O 与无色气体NO反应生成红棕色气体NO ,无色气体变为红棕色,D正确。
2 2 2 2 2
题组三 无机化工“微流程”及分析
11.(2024·广西柳州、南宁名校联盟联考)实验室模拟侯氏制碱法制备NaCO 的主要过程如下,下列说
2 3
法正确的是( )
A.实验时应先向饱和食盐水中通入足量CO 再通入NH
2 3
B.过程①②③均涉及过滤操作
C.向溶液A中加入NaCl的作用是增大Cl-的浓度,促进NH Cl结晶析出
4
D.实验过程中可循环使用的物质只有CO
2
答案:C
解析:实验时应先向饱和食盐水中通入足量NH 再通入CO,A错误;过程①③涉及过滤操作,过程②是
3 2
碳酸氢钠固体受热分解生成碳酸钠,B错误;向溶液A中加入NaCl可增大Cl-的浓度,促进NH Cl结晶
4
析出,C正确;实验过程中可循环使用的物质有CO 和氯化钠,D错误。
2
12.(2024·湖南株洲质检)次磷酸(H PO )是一元中强酸,次磷酸钠(NaH PO )广泛应用于化学镀镍,次磷
3 2 2 2
酸钠的生产与镀镍过程如图所示。下列有关说法正确的是( )A.Ni2+的核外电子有26种空间运动状态
B.“碱溶”时氧化剂与还原剂的物质的量之比为3∶1
C.PH
、PO3- 、P(正四面体结构)中的键角:PO3-
>PH>P
3 4 4 4 3 4
D.次磷酸铵与足量氢氧化钠共热:N H+ 4+H 2 P O 2 - +3OH- NH 3 +3H 2 O+P O 2 3-
答案:C
解析:Ni2+的核外电子排布式为1s22s22p63s23p63d8,核外电子的空间运动状态有14种,A错误;“碱溶”
时发生反应P+3NaOH+3HO 3NaH PO +PH↑,氧化剂P 与还原剂P 的物质的量之比为1∶3,B
4 2 2 2 3 4 4
错误;PH、PO3-
、P
中P的价层电子对数均为4,均为sp3杂化,PO3-
为5原子的正四面体结构,键角
3 4 4 4
为109°28',P 为4原子的正四面体结构,键角为60°,PH 中P含有1个孤电子对,空间结构为三角锥形,
4 3
由于孤电子对对成键电子对的斥力较大,所以键角PO3-
>PH>P ,C正确;次磷酸铵为正盐,与足量氢氧
4 3 4
化钠共热发生反应的离子方程式为N
H+
4+OH- NH
3
↑+H
2
O,D错误。
13.(2024·黑龙江大庆实验中学模拟)下列有关物质的工业制备过程,在给定条件下能实现的是( )
A.冶炼铝:铝土矿 Na[Al(OH)] 无水AlCl Al
4 3
B.工业制硝酸:NH NO NO HNO
3 2 3
C.海带提碘:海带 海带灰 I(aq) I
2 2
D.工业制硫酸:S SO HSO
3 2 4
答案:B
解析:AlCl 是共价化合物,熔融时不导电,不能用电解熔融AlCl 的方法冶炼Al,A不正确;工业制硝酸
3 3
时,先将NH 催化氧化制得NO,再将NO用O 进一步氧化为NO ,NO 与一定量空气混合通入水中,便
3 2 2 2
可制得HNO,B正确;海带提碘时,先将海带灼烧成灰,灰分用水溶解,再通入Cl 氧化,从而可制得含I
3 2 2
的溶液,但乙醇与水互溶,不能作萃取剂,所以不能通过乙醇萃取I,C不正确;工业制硫酸时,以硫黄为
2
原料,将硫黄燃烧只能生成SO ,不能生成SO ,D不正确。
2 3