文档内容
选择题标准练(四)
1.(2024·安徽合肥第三次质检)化学科学是现代科学技术发展的重要基础科学。下列说法正确的是
( )
A.5G时代某三维存储器能储存海量数据,其半导体衬底材料是SiO
2
B.铁磁流体液态机器人中驱动机器人运动的磁铁的主要成分是Fe O
2 3
C.三苯基铋在石墨烯中加热得到铋纳米球胶体,铋纳米球的直径在1 nm以下
D.氨硼烷(BHNH )作为一种储氢材料备受关注,氨硼烷分子中只存在极性共价键
3 3
2.(2024·黑龙江齐齐哈尔一模)V O-WO/TiO 催化剂能催化NH 脱除烟气中的NO,反应的化学方程
2 5 3 2 3
式为4NH (g)+O(g)+4NO(g) 4N(g)+6HO(g)。下列说法正确的是( )
3 2 2 2
A.N 的电子式为N︙︙N
2
B.H O的VSEPR模型名称为直线形
2
C.Ti的价层电子的轨道表示式为
D.NH 是极性分子,分子中N原子处在3个H原子所组成的三角形的中心
3
3.(2024·辽宁锦州质检)给定条件下,下列物质间的转化均能实现的是( )
A.NH ·H O (NH )SO (NH )SO
3 2 4 2 3 4 2 4
B.NaCl(饱和aq) NaHCO (s) NaCO(s)
3 2 3
C.Fe Fe O Fe(NO )
3 4 3 3
D.CuSO Cu(OH) Cu O
4 2 2
4.(2024·广东深圳一模)化学处处呈现美。下列说法不正确的是( )
A.金刚石中的碳原子采取sp3杂化形成空间网状结构
B.FeSO 溶液与K[Fe(CN) ]溶液反应生成蓝色KFe[Fe(CN) ]沉淀
4 3 6 6
C.缺角的NaCl晶体在饱和NaCl溶液中变为完美立方体块,体现晶体的自范性
D.绚烂烟花的产生是电子由基态跃迁到激发态时,能量以光的形式释放引起的
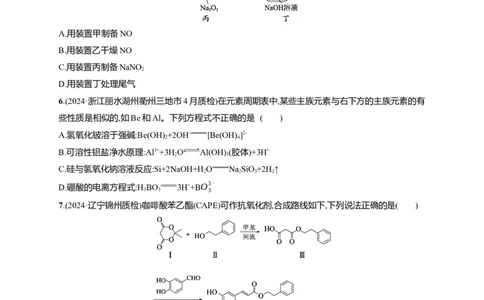
5.(2024·辽宁锦州质检)实验室通过反应:2NO+Na O 2NaNO 制备NaNO 。下列实验装置不能达
2 2 2 2
到实验目的的是( )A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO
2
D.用装置丁处理尾气
6.(2024·浙江丽水湖州衢州三地市4月质检)在元素周期表中,某些主族元素与右下方的主族元素的有
些性质是相似的,如Be和Al。下列方程式不正确的是 ( )
A.氢氧化铍溶于强碱:Be(OH) +2OH- [Be(OH) ]2-
2 4
B.可溶性铝盐净水原理:Al3++3H O Al(OH) (胶体)+3H+
2 3
C.硅与氢氧化钠溶液反应:Si+2NaOH+H O NaSiO+2H ↑
2 2 3 2
D.硼酸的电离方程式:H BO
3H++BO3-
3 3 3
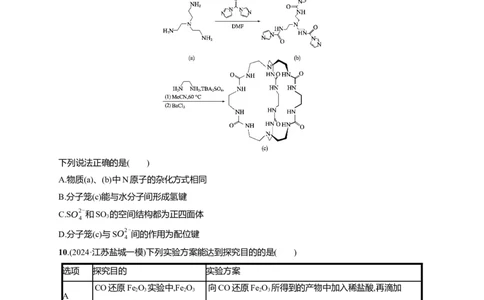
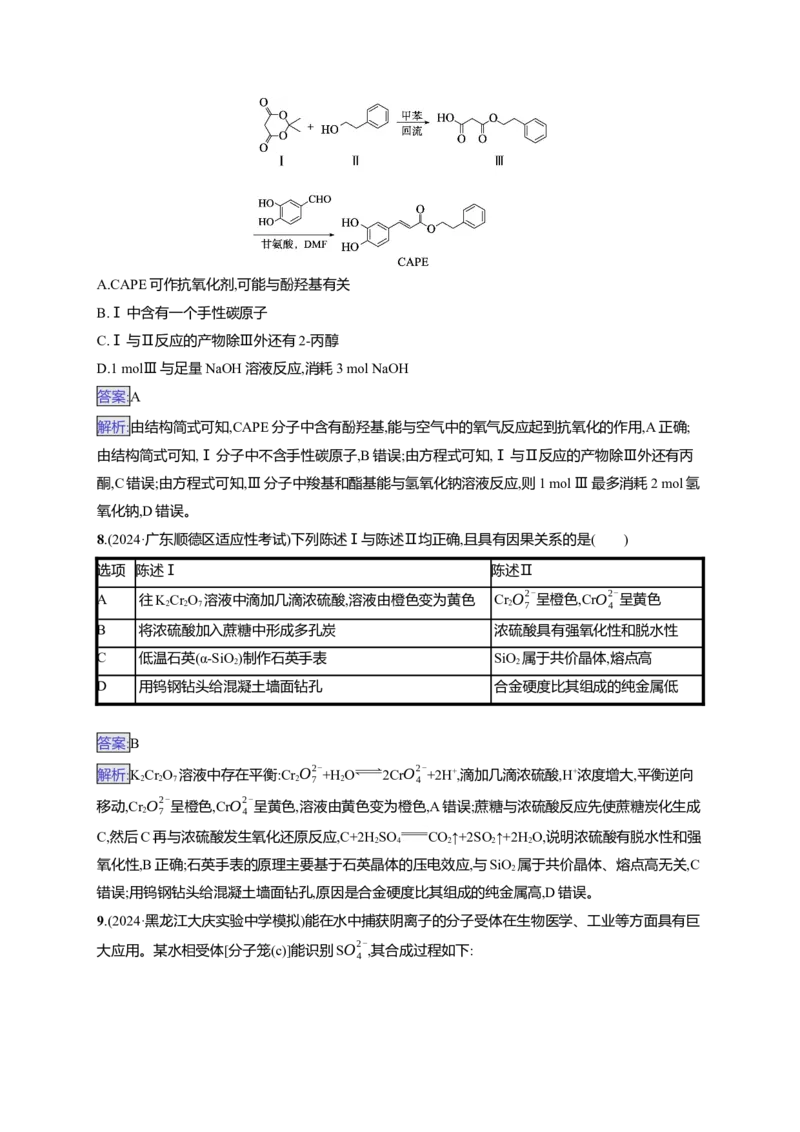
7.(2024·辽宁锦州质检)咖啡酸苯乙酯(CAPE)可作抗氧化剂,合成路线如下,下列说法正确的是( )
A.CAPE可作抗氧化剂,可能与酚羟基有关
B.Ⅰ中含有一个手性碳原子
C.Ⅰ与Ⅱ反应的产物除Ⅲ外还有2-丙醇
D.1 molⅢ与足量NaOH溶液反应,消耗3 mol NaOH
8.(2024·广东顺德区适应性考试)下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述ⅡA 往KCr O 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色
CrO2- 呈橙色,CrO2-
呈黄色
2 2 7 2 7 4
B 将浓硫酸加入蔗糖中形成多孔炭 浓硫酸具有强氧化性和脱水性
C 低温石英(α-SiO)制作石英手表 SiO 属于共价晶体,熔点高
2 2
D 用钨钢钻头给混凝土墙面钻孔 合金硬度比其组成的纯金属低
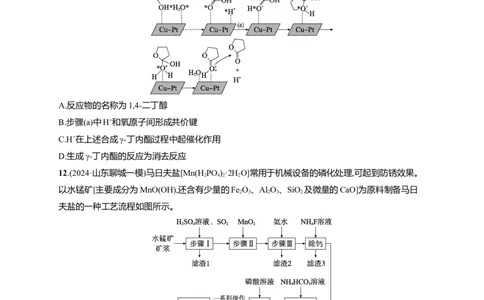
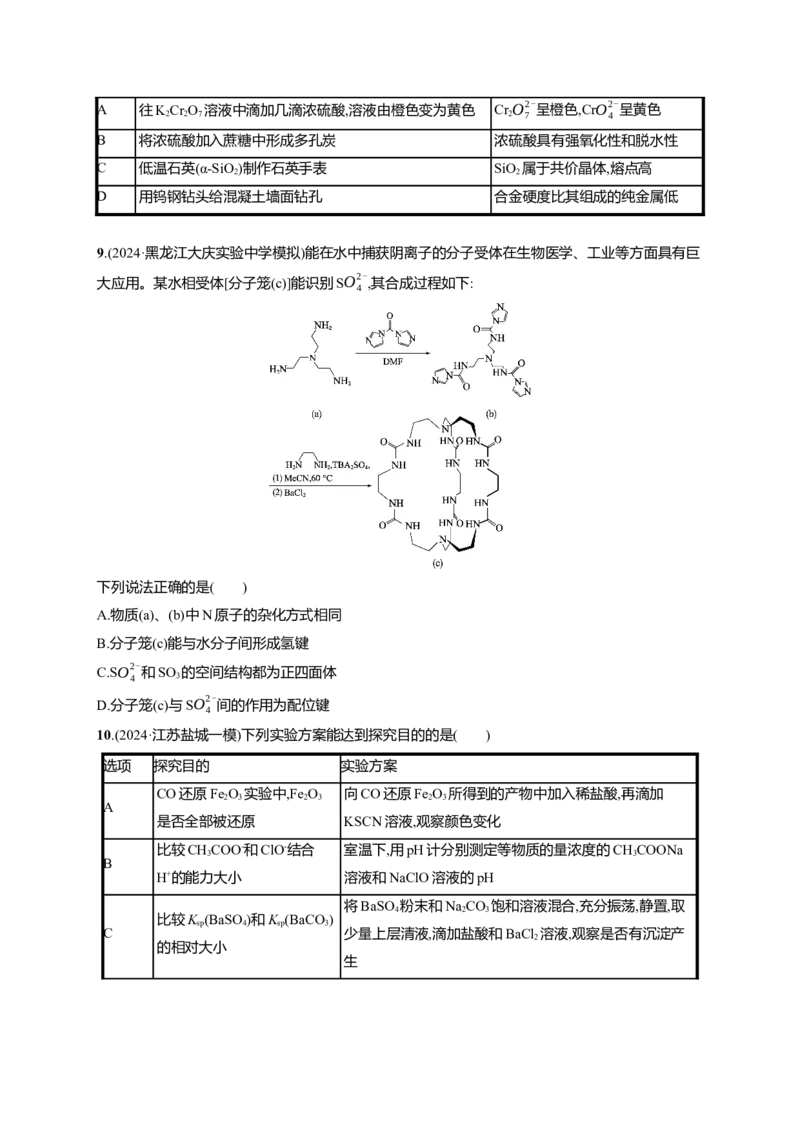
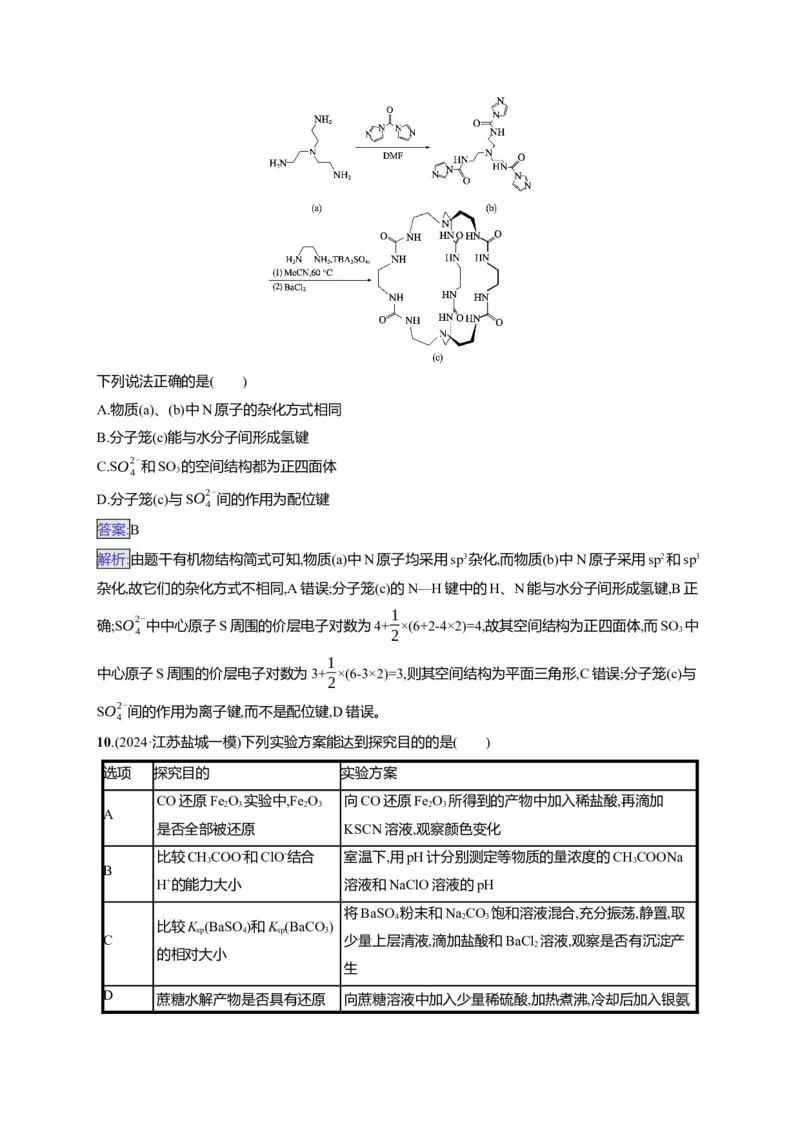
9.(2024·黑龙江大庆实验中学模拟)能在水中捕获阴离子的分子受体在生物医学、工业等方面具有巨
大应用。某水相受体[分子笼(c)]能识别SO2-
,其合成过程如下:
4
下列说法正确的是( )
A.物质(a)、(b)中N原子的杂化方式相同
B.分子笼(c)能与水分子间形成氢键
C.SO2-
和SO 的空间结构都为正四面体
4 3
D.分子笼(c)与SO2-
间的作用为配位键
4
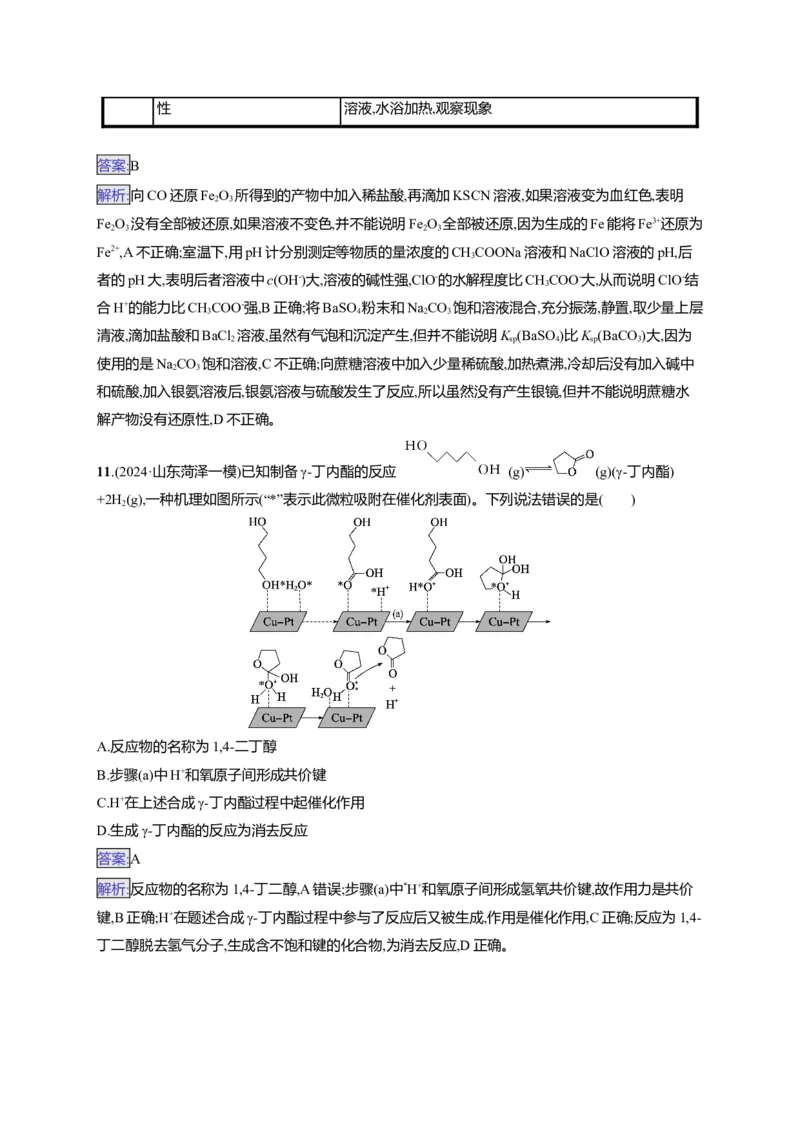
10.(2024·江苏盐城一模)下列实验方案能达到探究目的的是( )
选项 探究目的 实验方案
CO还原Fe O 实验中,Fe O 向CO还原Fe O 所得到的产物中加入稀盐酸,再滴加
2 3 2 3 2 3
A
是否全部被还原 KSCN溶液,观察颜色变化
比较CHCOO-和ClO-结合 室温下,用pH计分别测定等物质的量浓度的CHCOONa
3 3
B
H+的能力大小 溶液和NaClO溶液的pH
将BaSO 粉末和NaCO 饱和溶液混合,充分振荡,静置,取
4 2 3
比较K (BaSO)和K (BaCO)
sp 4 sp 3
C 少量上层清液,滴加盐酸和BaCl 溶液,观察是否有沉淀产
2
的相对大小
生蔗糖水解产物是否具有还原 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨
D
性 溶液,水浴加热,观察现象
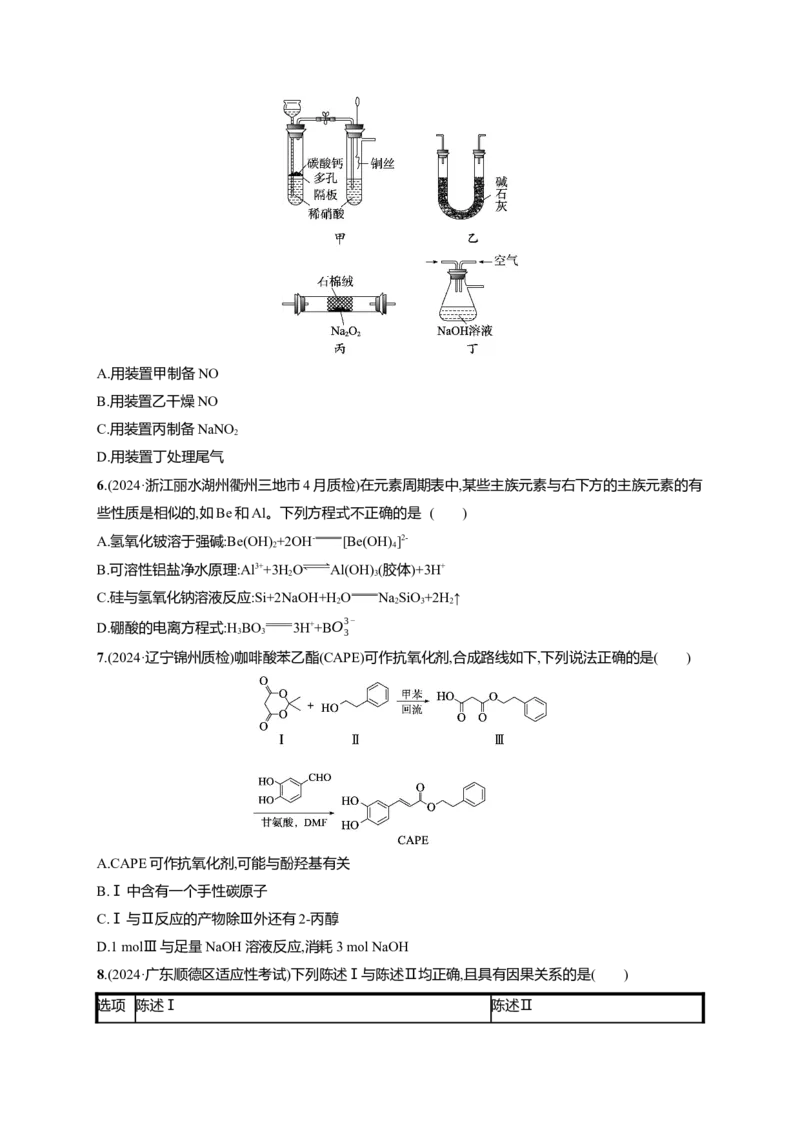
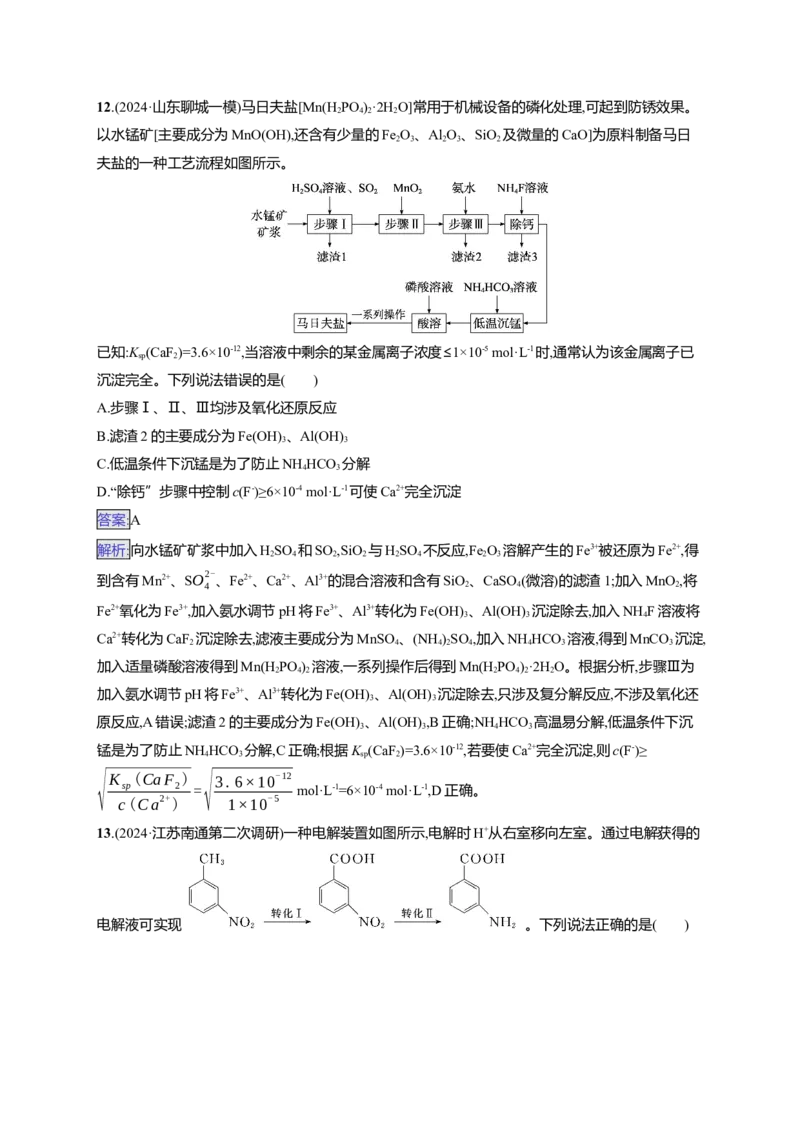
11.(2024·山东菏泽一模)已知制备γ-丁内酯的反应 (g) (g)(γ-丁内酯)
+2H (g),一种机理如图所示(“*”表示此微粒吸附在催化剂表面)。下列说法错误的是( )
2
A.反应物的名称为1,4-二丁醇
B.步骤(a)中H+和氧原子间形成共价键
C.H+在上述合成γ-丁内酯过程中起催化作用
D.生成γ-丁内酯的反应为消去反应
12.(2024·山东聊城一模)马日夫盐[Mn(H PO )·2H O]常用于机械设备的磷化处理,可起到防锈效果。
2 4 2 2
以水锰矿[主要成分为MnO(OH),还含有少量的Fe O、Al O、SiO 及微量的CaO]为原料制备马日
2 3 2 3 2
夫盐的一种工艺流程如图所示。
已知:K (CaF )=3.6×10-12,当溶液中剩余的某金属离子浓度≤1×10-5 mol·L-1时,通常认为该金属离子已
sp 2
沉淀完全。下列说法错误的是( )
A.步骤Ⅰ、Ⅱ、Ⅲ均涉及氧化还原反应
B.滤渣2的主要成分为Fe(OH) 、Al(OH)
3 3
C.低温条件下沉锰是为了防止NH HCO 分解
4 3
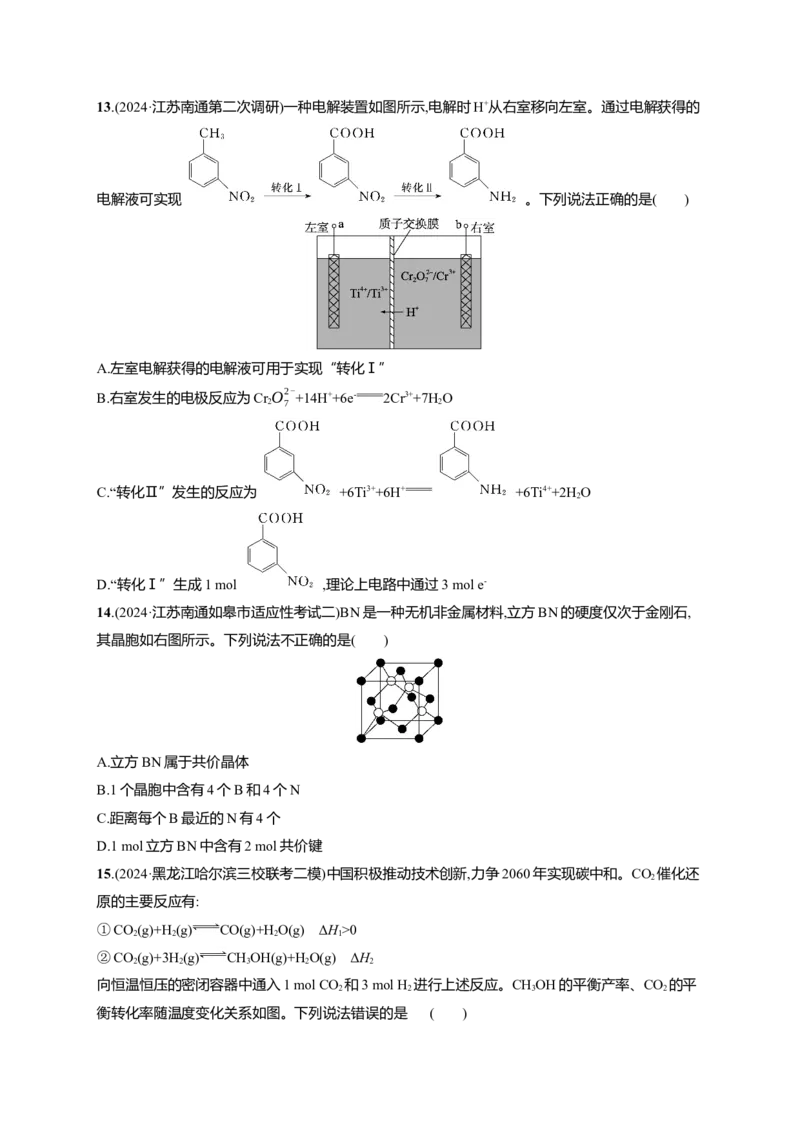
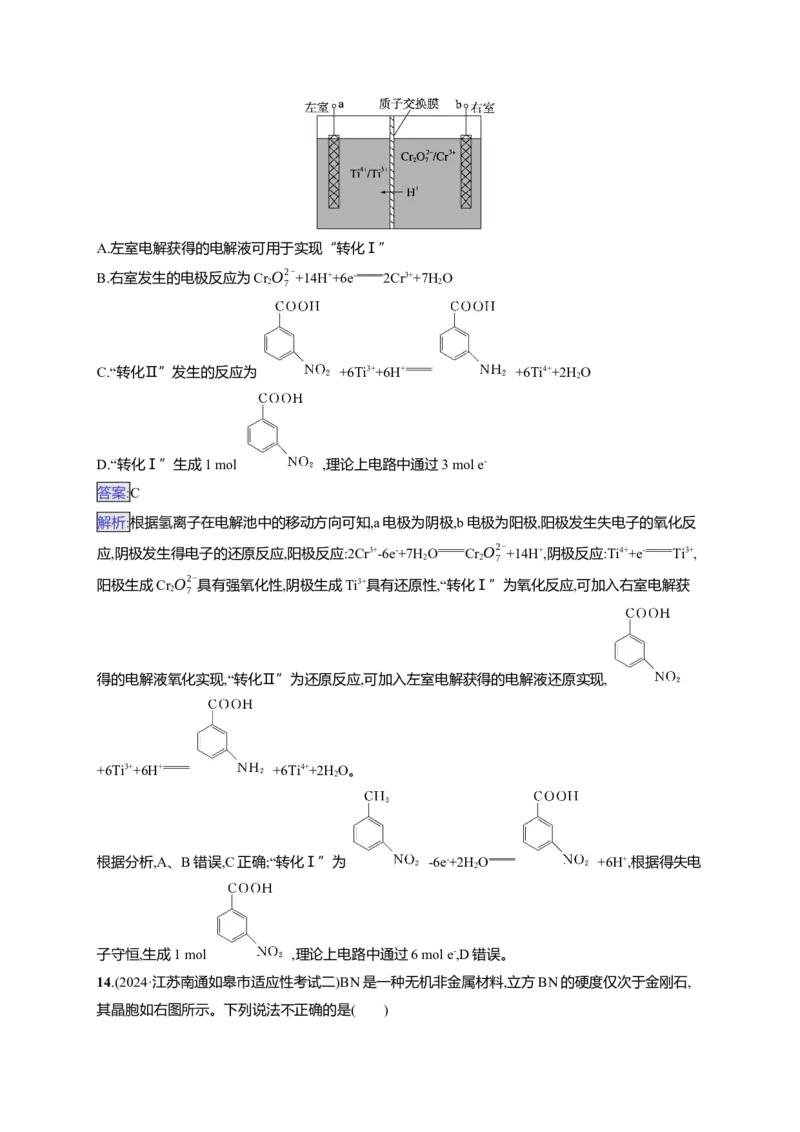
D.“除钙”步骤中控制c(F-)≥6×10-4 mol·L-1可使Ca2+完全沉淀13.(2024·江苏南通第二次调研)一种电解装置如图所示,电解时H+从右室移向左室。通过电解获得的
电解液可实现 。下列说法正确的是( )
A.左室电解获得的电解液可用于实现“转化Ⅰ”
B.右室发生的电极反应为CrO2-
+14H++6e- 2Cr3++7H O
2 7 2
C.“转化Ⅱ”发生的反应为 +6Ti3++6H+ +6Ti4++2H O
2
D.“转化Ⅰ”生成1 mol ,理论上电路中通过3 mol e-
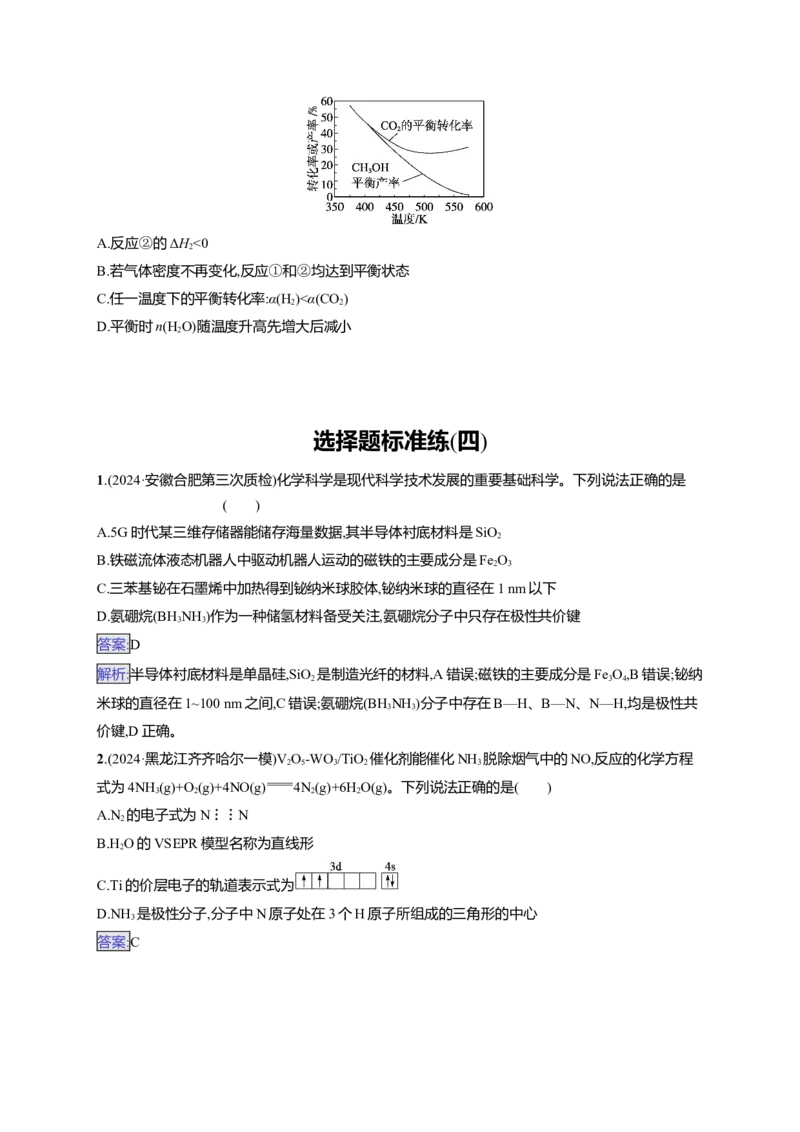
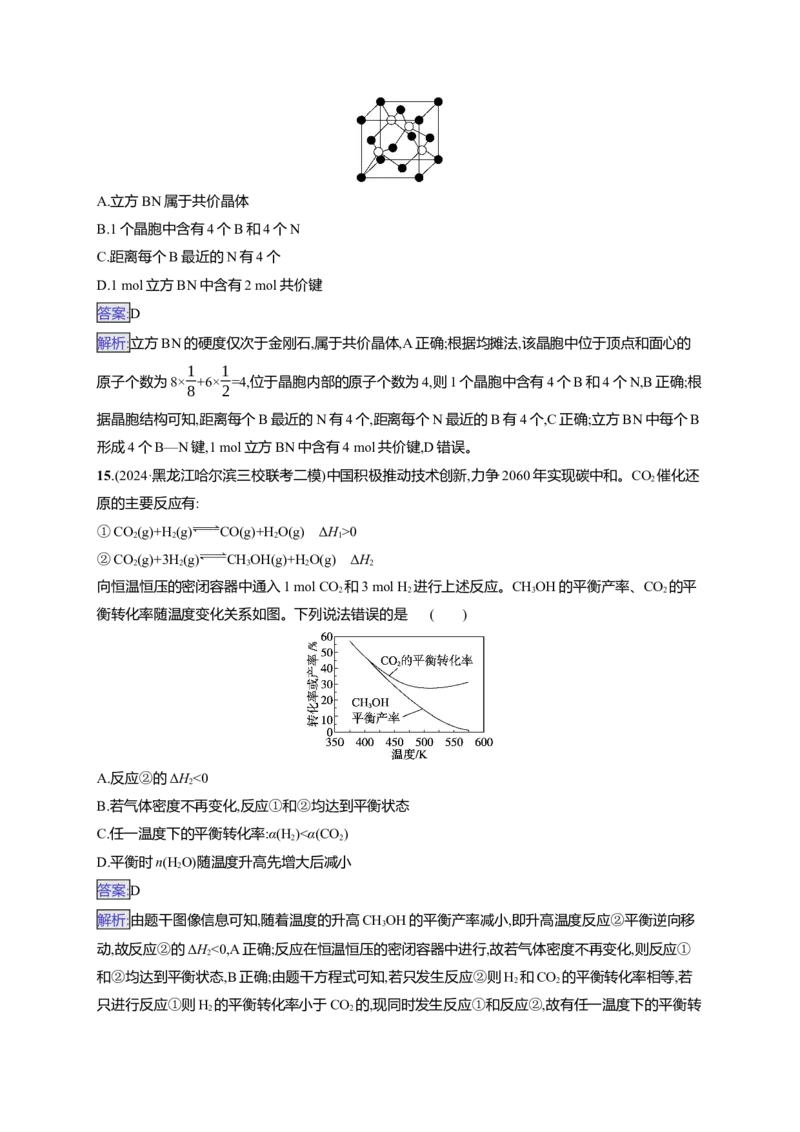
14.(2024·江苏南通如皋市适应性考试二)BN是一种无机非金属材料,立方BN的硬度仅次于金刚石,
其晶胞如右图所示。下列说法不正确的是( )
A.立方BN属于共价晶体
B.1个晶胞中含有4个B和4个N
C.距离每个B最近的N有4个
D.1 mol立方BN中含有2 mol共价键
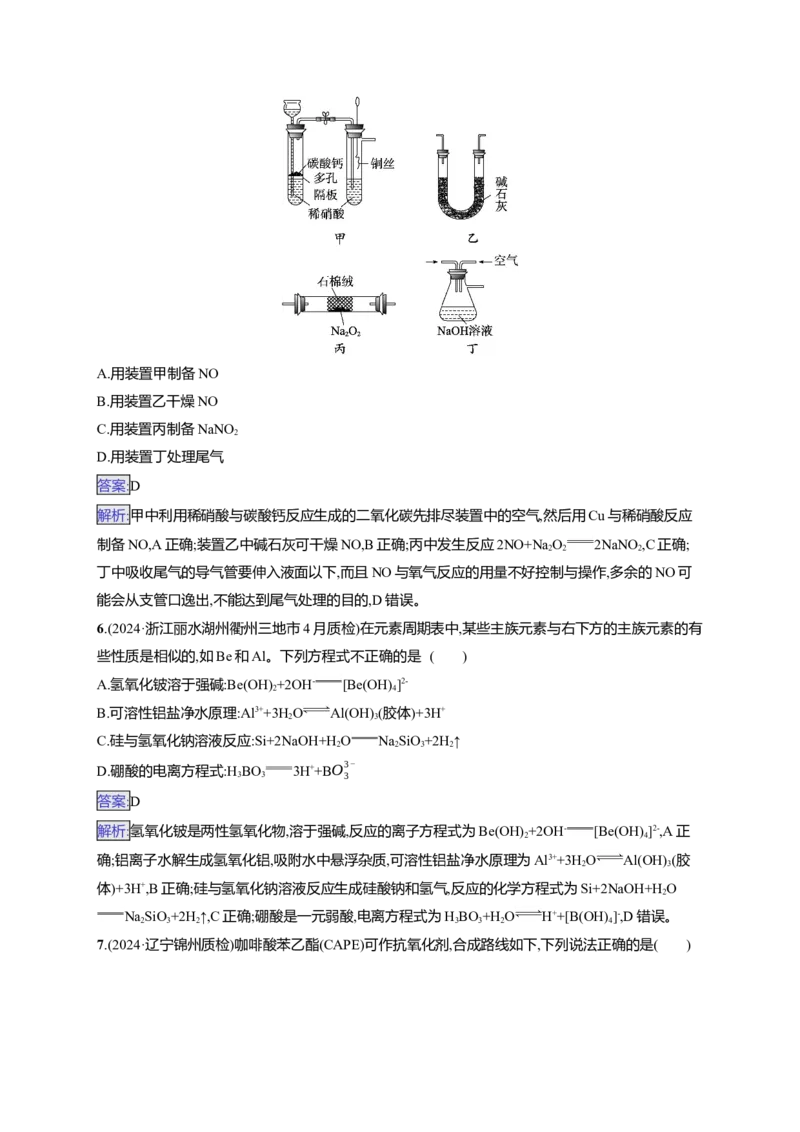
15.(2024·黑龙江哈尔滨三校联考二模)中国积极推动技术创新,力争2060年实现碳中和。CO 催化还
2
原的主要反应有:
①CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2 1
②CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 2
向恒温恒压的密闭容器中通入1 mol CO 和3 mol H 进行上述反应。CHOH的平衡产率、CO 的平
2 2 3 2
衡转化率随温度变化关系如图。下列说法错误的是 ( )A.反应②的ΔH<0
2
B.若气体密度不再变化,反应①和②均达到平衡状态
C.任一温度下的平衡转化率:α(H )<α(CO)
2 2
D.平衡时n(H O)随温度升高先增大后减小
2
选择题标准练(四)
1.(2024·安徽合肥第三次质检)化学科学是现代科学技术发展的重要基础科学。下列说法正确的是
( )
A.5G时代某三维存储器能储存海量数据,其半导体衬底材料是SiO
2
B.铁磁流体液态机器人中驱动机器人运动的磁铁的主要成分是Fe O
2 3
C.三苯基铋在石墨烯中加热得到铋纳米球胶体,铋纳米球的直径在1 nm以下
D.氨硼烷(BHNH )作为一种储氢材料备受关注,氨硼烷分子中只存在极性共价键
3 3
答案:D
解析:半导体衬底材料是单晶硅,SiO 是制造光纤的材料,A错误;磁铁的主要成分是Fe O,B错误;铋纳
2 3 4
米球的直径在1~100 nm之间,C错误;氨硼烷(BHNH )分子中存在B—H、B—N、N—H,均是极性共
3 3
价键,D正确。
2.(2024·黑龙江齐齐哈尔一模)V O-WO/TiO 催化剂能催化NH 脱除烟气中的NO,反应的化学方程
2 5 3 2 3
式为4NH (g)+O(g)+4NO(g) 4N(g)+6HO(g)。下列说法正确的是( )
3 2 2 2
A.N 的电子式为N︙︙N
2
B.H O的VSEPR模型名称为直线形
2
C.Ti的价层电子的轨道表示式为
D.NH 是极性分子,分子中N原子处在3个H原子所组成的三角形的中心
3
答案:C解析:N 的电子式为
· N︙︙N·
,A错误;H O的VSEPR模型名称为四面体形,B错误;Ti的价层电子的
2 · · 2
轨道表示式为 ,C正确;NH 是极性分子,分子的空间结构为三角锥形,N原子处在三
3
角锥形的锥顶,3个H原子位于锥底,D错误。
3.(2024·辽宁锦州质检)给定条件下,下列物质间的转化均能实现的是( )
A.NH ·H O (NH )SO (NH )SO
3 2 4 2 3 4 2 4
B.NaCl(饱和aq) NaHCO (s) NaCO(s)
3 2 3
C.Fe Fe O Fe(NO )
3 4 3 3
D.CuSO Cu(OH) Cu O
4 2 2
答案:C
解析:NH ·H O与过量的SO 反应,生成NH HSO ,A错误;NaCl与CO 不反应,侯氏制碱法是先在饱和
3 2 2 4 3 2
食盐水中通入氨气再通入CO,B错误;Fe与水蒸气反应生成四氧化三铁,四氧化三铁再与稀硝酸反应
2
生成硝酸铁,C正确;蔗糖无醛基,不能与氢氧化铜在加热条件下生成氧化亚铜,D错误。
4.(2024·广东深圳一模)化学处处呈现美。下列说法不正确的是( )
A.金刚石中的碳原子采取sp3杂化形成空间网状结构
B.FeSO 溶液与K[Fe(CN) ]溶液反应生成蓝色KFe[Fe(CN) ]沉淀
4 3 6 6
C.缺角的NaCl晶体在饱和NaCl溶液中变为完美立方体块,体现晶体的自范性
D.绚烂烟花的产生是电子由基态跃迁到激发态时,能量以光的形式释放引起的
答案:D
解析:金刚石是共价晶体,为空间网状结构,1个C原子与周围的4个C原子形成单键,其价层电子对数
为4,VSEPR模型为正四面体,采取sp3杂化,A正确;FeSO 与K[Fe(CN) ]反应生成KFe[Fe(CN) ]和
4 3 6 6
KSO ,KFe[Fe(CN) ]为蓝色沉淀,B正确;晶体具有规则的几何形状,有自范性,则缺角的NaCl晶体在饱
2 4 6
和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性,C正确;绚烂烟花的产生原理是焰色
试验,电子吸收能量,由基态跃迁到激发态,再由激发态跃迁到能量较低的激发态或基态时放出热量,
能量以光的形式释放,D错误。
5.(2024·辽宁锦州质检)实验室通过反应:2NO+Na O 2NaNO 制备NaNO 。下列实验装置不能达
2 2 2 2
到实验目的的是( )A.用装置甲制备NO
B.用装置乙干燥NO
C.用装置丙制备NaNO
2
D.用装置丁处理尾气
答案:D
解析:甲中利用稀硝酸与碳酸钙反应生成的二氧化碳先排尽装置中的空气,然后用Cu与稀硝酸反应
制备NO,A正确;装置乙中碱石灰可干燥NO,B正确;丙中发生反应2NO+Na O 2NaNO ,C正确;
2 2 2
丁中吸收尾气的导气管要伸入液面以下,而且NO与氧气反应的用量不好控制与操作,多余的NO可
能会从支管口逸出,不能达到尾气处理的目的,D错误。
6.(2024·浙江丽水湖州衢州三地市4月质检)在元素周期表中,某些主族元素与右下方的主族元素的有
些性质是相似的,如Be和Al。下列方程式不正确的是 ( )
A.氢氧化铍溶于强碱:Be(OH) +2OH- [Be(OH) ]2-
2 4
B.可溶性铝盐净水原理:Al3++3H O Al(OH) (胶体)+3H+
2 3
C.硅与氢氧化钠溶液反应:Si+2NaOH+H O NaSiO+2H ↑
2 2 3 2
D.硼酸的电离方程式:H BO
3H++BO3-
3 3 3
答案:D
解析:氢氧化铍是两性氢氧化物,溶于强碱,反应的离子方程式为Be(OH) +2OH- [Be(OH) ]2-,A正
2 4
确;铝离子水解生成氢氧化铝,吸附水中悬浮杂质,可溶性铝盐净水原理为Al3++3H O Al(OH) (胶
2 3
体)+3H+,B正确;硅与氢氧化钠溶液反应生成硅酸钠和氢气,反应的化学方程式为Si+2NaOH+H O
2
NaSiO+2H ↑,C正确;硼酸是一元弱酸,电离方程式为HBO+H O H++[B(OH) ]-,D错误。
2 3 2 3 3 2 4
7.(2024·辽宁锦州质检)咖啡酸苯乙酯(CAPE)可作抗氧化剂,合成路线如下,下列说法正确的是( )A.CAPE可作抗氧化剂,可能与酚羟基有关
B.Ⅰ中含有一个手性碳原子
C.Ⅰ与Ⅱ反应的产物除Ⅲ外还有2-丙醇
D.1 molⅢ与足量NaOH溶液反应,消耗3 mol NaOH
答案:A
解析:由结构简式可知,CAPE分子中含有酚羟基,能与空气中的氧气反应起到抗氧化的作用,A正确;
由结构简式可知,Ⅰ分子中不含手性碳原子,B错误;由方程式可知,Ⅰ与Ⅱ反应的产物除Ⅲ外还有丙
酮,C错误;由方程式可知,Ⅲ分子中羧基和酯基能与氢氧化钠溶液反应,则1 mol Ⅲ最多消耗2 mol氢
氧化钠,D错误。
8.(2024·广东顺德区适应性考试)下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 往KCr O 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色
CrO2- 呈橙色,CrO2-
呈黄色
2 2 7 2 7 4
B 将浓硫酸加入蔗糖中形成多孔炭 浓硫酸具有强氧化性和脱水性
C 低温石英(α-SiO)制作石英手表 SiO 属于共价晶体,熔点高
2 2
D 用钨钢钻头给混凝土墙面钻孔 合金硬度比其组成的纯金属低
答案:B
解析:KCr O
溶液中存在平衡:CrO2-
+H O
2CrO2-
+2H+,滴加几滴浓硫酸,H+浓度增大,平衡逆向
2 2 7 2 7 2 4
移动,CrO2- 呈橙色,CrO2-
呈黄色,溶液由黄色变为橙色,A错误;蔗糖与浓硫酸反应先使蔗糖炭化生成
2 7 4
C,然后C再与浓硫酸发生氧化还原反应,C+2HSO CO↑+2SO↑+2H O,说明浓硫酸有脱水性和强
2 4 2 2 2
氧化性,B正确;石英手表的原理主要基于石英晶体的压电效应,与SiO 属于共价晶体、熔点高无关,C
2
错误;用钨钢钻头给混凝土墙面钻孔,原因是合金硬度比其组成的纯金属高,D错误。
9.(2024·黑龙江大庆实验中学模拟)能在水中捕获阴离子的分子受体在生物医学、工业等方面具有巨
大应用。某水相受体[分子笼(c)]能识别SO2-
,其合成过程如下:
4下列说法正确的是( )
A.物质(a)、(b)中N原子的杂化方式相同
B.分子笼(c)能与水分子间形成氢键
C.SO2-
和SO 的空间结构都为正四面体
4 3
D.分子笼(c)与SO2-
间的作用为配位键
4
答案:B
解析:由题干有机物结构简式可知,物质(a)中N原子均采用sp3杂化,而物质(b)中N原子采用sp2和sp3
杂化,故它们的杂化方式不相同,A错误;分子笼(c)的N—H键中的H、N能与水分子间形成氢键,B正
1
确;SO2-
中中心原子S周围的价层电子对数为4+ ×(6+2-4×2)=4,故其空间结构为正四面体,而SO 中
4 2 3
1
中心原子S周围的价层电子对数为3+ ×(6-3×2)=3,则其空间结构为平面三角形,C错误;分子笼(c)与
2
SO2-
间的作用为离子键,而不是配位键,D错误。
4
10.(2024·江苏盐城一模)下列实验方案能达到探究目的的是( )
选项 探究目的 实验方案
CO还原Fe O 实验中,Fe O 向CO还原Fe O 所得到的产物中加入稀盐酸,再滴加
2 3 2 3 2 3
A
是否全部被还原 KSCN溶液,观察颜色变化
比较CHCOO-和ClO-结合 室温下,用pH计分别测定等物质的量浓度的CHCOONa
3 3
B
H+的能力大小 溶液和NaClO溶液的pH
将BaSO 粉末和NaCO 饱和溶液混合,充分振荡,静置,取
4 2 3
比较K (BaSO)和K (BaCO)
sp 4 sp 3
C 少量上层清液,滴加盐酸和BaCl 溶液,观察是否有沉淀产
2
的相对大小
生
D
蔗糖水解产物是否具有还原 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨性 溶液,水浴加热,观察现象
答案:B
解析:向CO还原Fe O 所得到的产物中加入稀盐酸,再滴加KSCN溶液,如果溶液变为血红色,表明
2 3
Fe O 没有全部被还原,如果溶液不变色,并不能说明Fe O 全部被还原,因为生成的Fe能将Fe3+还原为
2 3 2 3
Fe2+,A不正确;室温下,用pH计分别测定等物质的量浓度的CHCOONa溶液和NaClO溶液的pH,后
3
者的pH大,表明后者溶液中c(OH-)大,溶液的碱性强,ClO-的水解程度比CHCOO-大,从而说明ClO-结
3
合H+的能力比CHCOO-强,B正确;将BaSO 粉末和NaCO 饱和溶液混合,充分振荡,静置,取少量上层
3 4 2 3
清液,滴加盐酸和BaCl 溶液,虽然有气泡和沉淀产生,但并不能说明K (BaSO)比K (BaCO)大,因为
2 sp 4 sp 3
使用的是NaCO 饱和溶液,C不正确;向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后没有加入碱中
2 3
和硫酸,加入银氨溶液后,银氨溶液与硫酸发生了反应,所以虽然没有产生银镜,但并不能说明蔗糖水
解产物没有还原性,D不正确。
11.(2024·山东菏泽一模)已知制备γ-丁内酯的反应 (g) (g)(γ-丁内酯)
+2H (g),一种机理如图所示(“*”表示此微粒吸附在催化剂表面)。下列说法错误的是( )
2
A.反应物的名称为1,4-二丁醇
B.步骤(a)中H+和氧原子间形成共价键
C.H+在上述合成γ-丁内酯过程中起催化作用
D.生成γ-丁内酯的反应为消去反应
答案:A
解析:反应物的名称为1,4-丁二醇,A错误;步骤(a)中*H+和氧原子间形成氢氧共价键,故作用力是共价
键,B正确;H+在题述合成γ-丁内酯过程中参与了反应后又被生成,作用是催化作用,C正确;反应为1,4-
丁二醇脱去氢气分子,生成含不饱和键的化合物,为消去反应,D正确。12.(2024·山东聊城一模)马日夫盐[Mn(H PO )·2H O]常用于机械设备的磷化处理,可起到防锈效果。
2 4 2 2
以水锰矿[主要成分为MnO(OH),还含有少量的Fe O、Al O、SiO 及微量的CaO]为原料制备马日
2 3 2 3 2
夫盐的一种工艺流程如图所示。
已知:K (CaF )=3.6×10-12,当溶液中剩余的某金属离子浓度≤1×10-5 mol·L-1时,通常认为该金属离子已
sp 2
沉淀完全。下列说法错误的是( )
A.步骤Ⅰ、Ⅱ、Ⅲ均涉及氧化还原反应
B.滤渣2的主要成分为Fe(OH) 、Al(OH)
3 3
C.低温条件下沉锰是为了防止NH HCO 分解
4 3
D.“除钙”步骤中控制c(F-)≥6×10-4 mol·L-1可使Ca2+完全沉淀
答案:A
解析:向水锰矿矿浆中加入HSO 和SO ,SiO 与HSO 不反应,Fe O 溶解产生的Fe3+被还原为Fe2+,得
2 4 2 2 2 4 2 3
到含有Mn2+、SO2-
、Fe2+、Ca2+、Al3+的混合溶液和含有SiO、CaSO(微溶)的滤渣1;加入MnO ,将
4 2 4 2
Fe2+氧化为Fe3+,加入氨水调节pH将Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀除去,加入NH F溶液将
3 3 4
Ca2+转化为CaF 沉淀除去,滤液主要成分为MnSO 、(NH )SO ,加入NH HCO 溶液,得到MnCO 沉淀,
2 4 4 2 4 4 3 3
加入适量磷酸溶液得到Mn(H PO ) 溶液,一系列操作后得到Mn(H PO )·2H O。根据分析,步骤Ⅲ为
2 4 2 2 4 2 2
加入氨水调节pH将Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀除去,只涉及复分解反应,不涉及氧化还
3 3
原反应,A错误;滤渣2的主要成分为Fe(OH) 、Al(OH) ,B正确;NHHCO 高温易分解,低温条件下沉
3 3 4 3
锰是为了防止NH HCO 分解,C正确;根据K (CaF )=3.6×10-12,若要使Ca2+完全沉淀,则c(F-)≥
4 3 sp 2
√K (CaF ) √3.6×10-12
sp 2 = mol·L-1=6×10-4 mol·L-1,D正确。
c(Ca2+) 1×10-5
13.(2024·江苏南通第二次调研)一种电解装置如图所示,电解时H+从右室移向左室。通过电解获得的
电解液可实现 。下列说法正确的是( )A.左室电解获得的电解液可用于实现“转化Ⅰ”
B.右室发生的电极反应为CrO2-
+14H++6e- 2Cr3++7H O
2 7 2
C.“转化Ⅱ”发生的反应为 +6Ti3++6H+ +6Ti4++2H O
2
D.“转化Ⅰ”生成1 mol ,理论上电路中通过3 mol e-
答案:C
解析:根据氢离子在电解池中的移动方向可知,a电极为阴极,b电极为阳极,阳极发生失电子的氧化反
应,阴极发生得电子的还原反应,阳极反应:2Cr3+-6e-+7H O
CrO2-
+14H+,阴极反应:Ti4++e- Ti3+,
2 2 7
阳极生成CrO2-
具有强氧化性,阴极生成Ti3+具有还原性,“转化Ⅰ”为氧化反应,可加入右室电解获
2 7
得的电解液氧化实现,“转化Ⅱ”为还原反应,可加入左室电解获得的电解液还原实现,
+6Ti3++6H+ +6Ti4++2H O。
2
根据分析,A、B错误,C正确;“转化Ⅰ”为 -6e-+2H O +6H+,根据得失电
2
子守恒,生成1 mol ,理论上电路中通过6 mol e-,D错误。
14.(2024·江苏南通如皋市适应性考试二)BN是一种无机非金属材料,立方BN的硬度仅次于金刚石,
其晶胞如右图所示。下列说法不正确的是( )A.立方BN属于共价晶体
B.1个晶胞中含有4个B和4个N
C.距离每个B最近的N有4个
D.1 mol立方BN中含有2 mol共价键
答案:D
解析:立方BN的硬度仅次于金刚石,属于共价晶体,A正确;根据均摊法,该晶胞中位于顶点和面心的
1 1
原子个数为8× +6× =4,位于晶胞内部的原子个数为4,则1个晶胞中含有4个B和4个N,B正确;根
8 2
据晶胞结构可知,距离每个B最近的N有4个,距离每个N最近的B有4个,C正确;立方BN中每个B
形成4个B—N键,1 mol立方BN中含有4 mol共价键,D错误。
15.(2024·黑龙江哈尔滨三校联考二模)中国积极推动技术创新,力争2060年实现碳中和。CO 催化还
2
原的主要反应有:
①CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2 1
②CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 2
向恒温恒压的密闭容器中通入1 mol CO 和3 mol H 进行上述反应。CHOH的平衡产率、CO 的平
2 2 3 2
衡转化率随温度变化关系如图。下列说法错误的是 ( )
A.反应②的ΔH<0
2
B.若气体密度不再变化,反应①和②均达到平衡状态
C.任一温度下的平衡转化率:α(H )<α(CO)
2 2
D.平衡时n(H O)随温度升高先增大后减小
2
答案:D
解析:由题干图像信息可知,随着温度的升高CHOH的平衡产率减小,即升高温度反应②平衡逆向移
3
动,故反应②的ΔH<0,A正确;反应在恒温恒压的密闭容器中进行,故若气体密度不再变化,则反应①
2
和②均达到平衡状态,B正确;由题干方程式可知,若只发生反应②则H 和CO 的平衡转化率相等,若
2 2
只进行反应①则H 的平衡转化率小于CO 的,现同时发生反应①和反应②,故有任一温度下的平衡转
2 2化率:α(H )<α(CO),C正确;CH OH的平衡产率随温度的升高一直在减小,而CO 的平衡转化率先减小
2 2 3 2
后增大,说明温度较低时以反应②为主,随着温度升高平衡逆向移动,H O的物质的量减小,而温度较高
2
时,以反应①为主,温度升高平衡正向移动,H O的物质的量增大,即平衡时n(H O)随温度升高先减小
2 2
后增大,D错误。