文档内容
第 28 讲 常见气体的实验室制备、净化和收集
[复习目标] 1.了解常见气体的制备原理、装置及改进。2.能根据气体的性质及制备原理设
计实验流程。
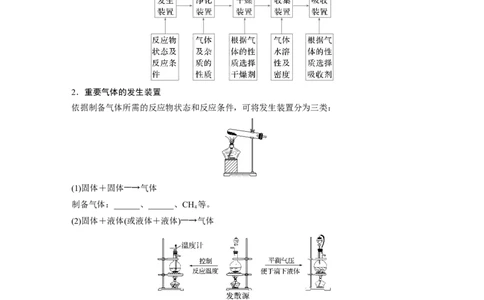
1.气体制备实验的基本思路
2.重要气体的发生装置
依据制备气体所需的反应物状态和反应条件,可将发生装置分为三类:
(1)固体+固体――→气体
制备气体:______、______、CH 等。
4
(2)固体+液体(或液体+液体)――→气体
制备气体:Cl、C H 等。
2 2 4
(3)固体+液体(不加热)―→气体
制备气体:选择合适的药品和装置能制取中学化学中常见的气体。
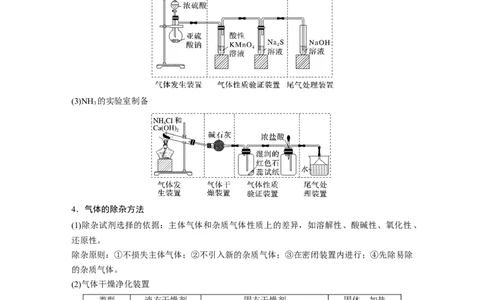
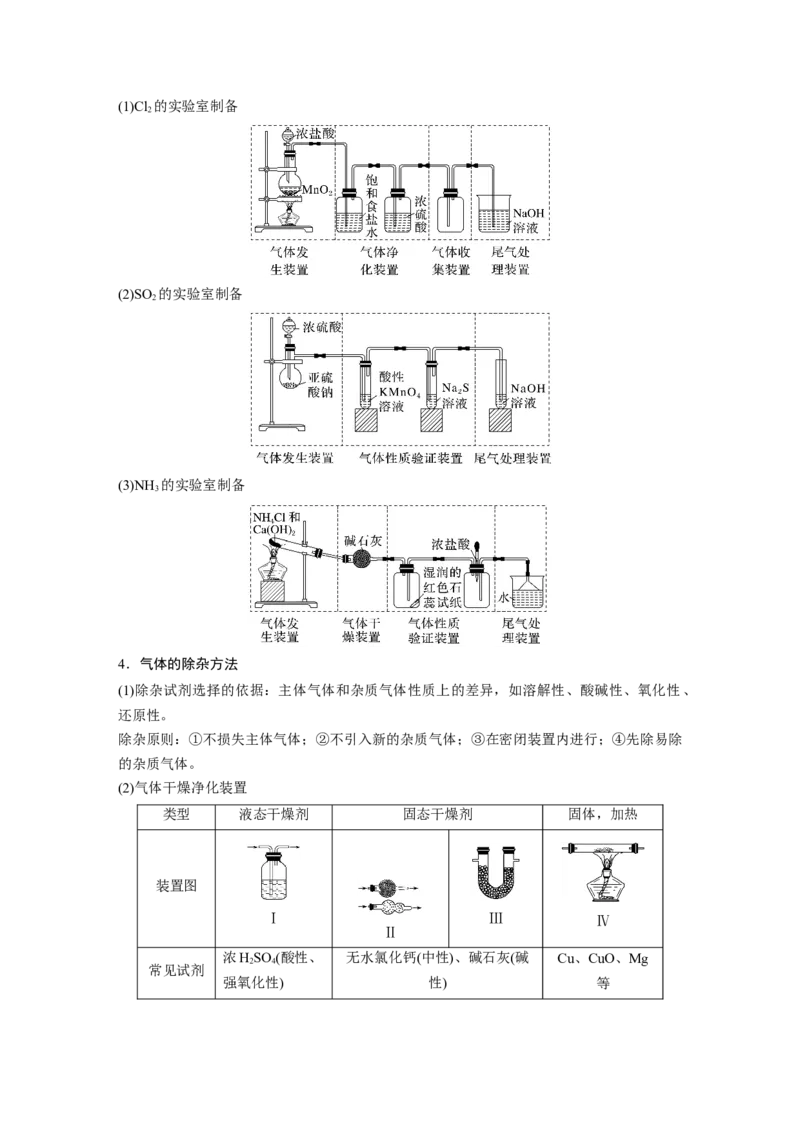
3.常见气体典型制备装置举例(1)Cl 的实验室制备
2
(2)SO 的实验室制备
2
(3)NH 的实验室制备
3
4.气体的除杂方法
(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、
还原性。
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除
的杂质气体。
(2)气体干燥净化装置
类型 液态干燥剂 固态干燥剂 固体,加热
装置图
Ⅰ Ⅲ Ⅳ
Ⅱ
浓HSO (酸性、 无水氯化钙(中性)、碱石灰(碱 Cu、CuO、Mg
2 4
常见试剂
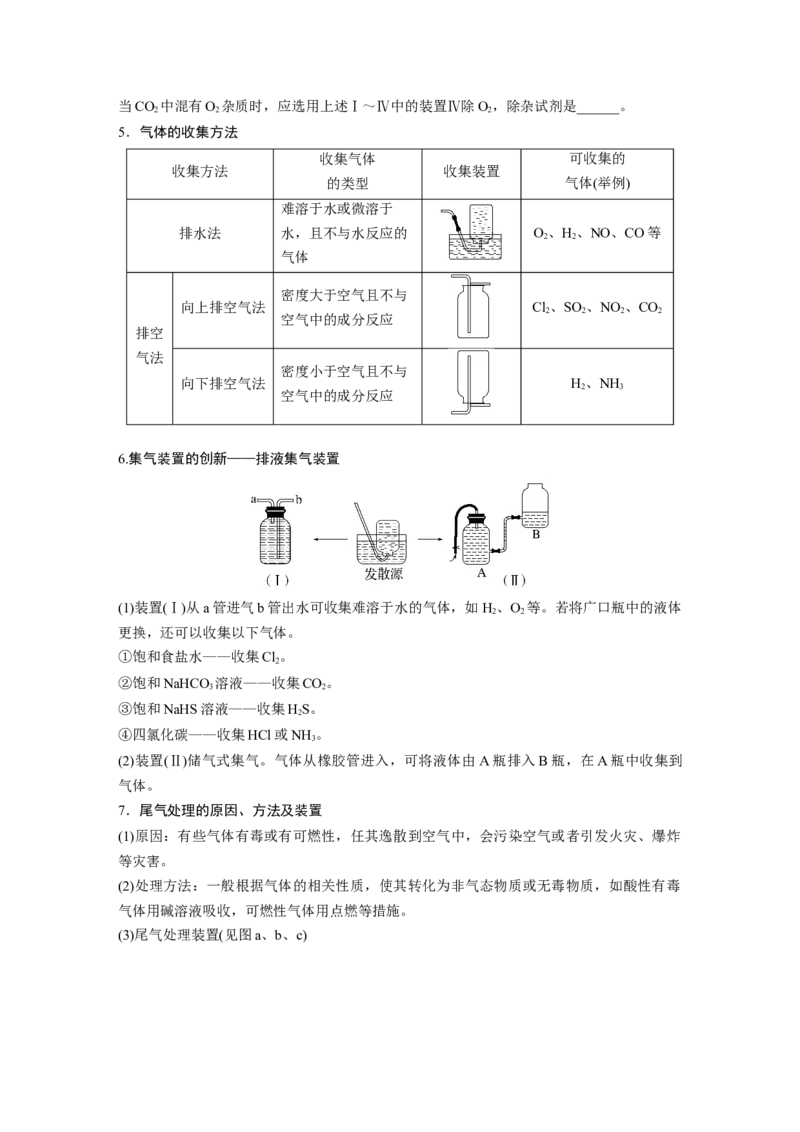
强氧化性) 性) 等当CO 中混有O 杂质时,应选用上述Ⅰ~Ⅳ中的装置Ⅳ除O,除杂试剂是______。
2 2 2
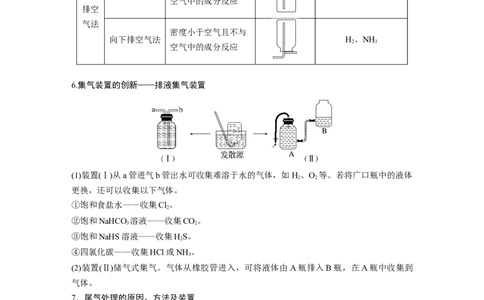
5.气体的收集方法
收集气体 可收集的
收集方法 收集装置
的类型 气体(举例)
难溶于水或微溶于
排水法 水,且不与水反应的 O、H、NO、CO等
2 2
气体
密度大于空气且不与
向上排空气法 Cl、SO 、NO 、CO
2 2 2 2
空气中的成分反应
排空
气法
密度小于空气且不与
向下排空气法 H、NH
2 3
空气中的成分反应
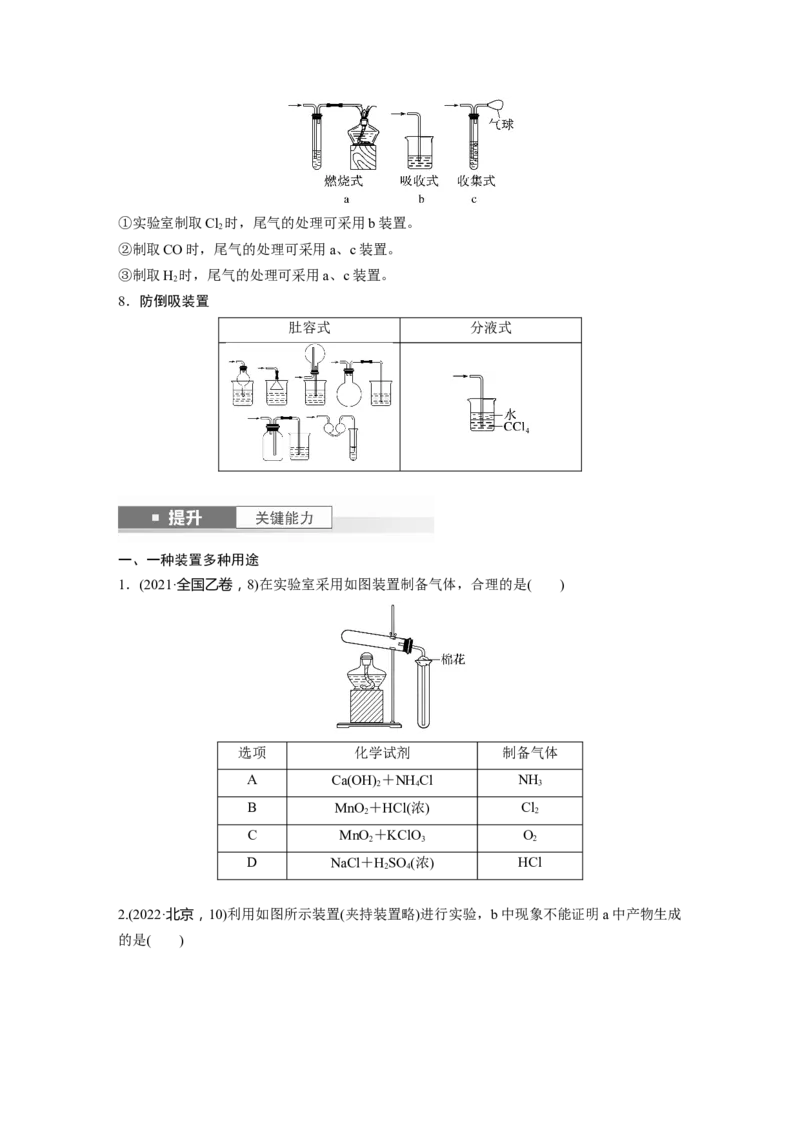
6.集气装置的创新——排液集气装置
(1)装置(Ⅰ)从a管进气b管出水可收集难溶于水的气体,如H、O 等。若将广口瓶中的液体
2 2
更换,还可以收集以下气体。
①饱和食盐水——收集Cl。
2
②饱和NaHCO 溶液——收集CO。
3 2
③饱和NaHS溶液——收集HS。
2
④四氯化碳——收集HCl或NH 。
3
(2)装置(Ⅱ)储气式集气。气体从橡胶管进入,可将液体由A瓶排入B瓶,在A瓶中收集到
气体。
7.尾气处理的原因、方法及装置
(1)原因:有些气体有毒或有可燃性,任其逸散到空气中,会污染空气或者引发火灾、爆炸
等灾害。
(2)处理方法:一般根据气体的相关性质,使其转化为非气态物质或无毒物质,如酸性有毒
气体用碱溶液吸收,可燃性气体用点燃等措施。
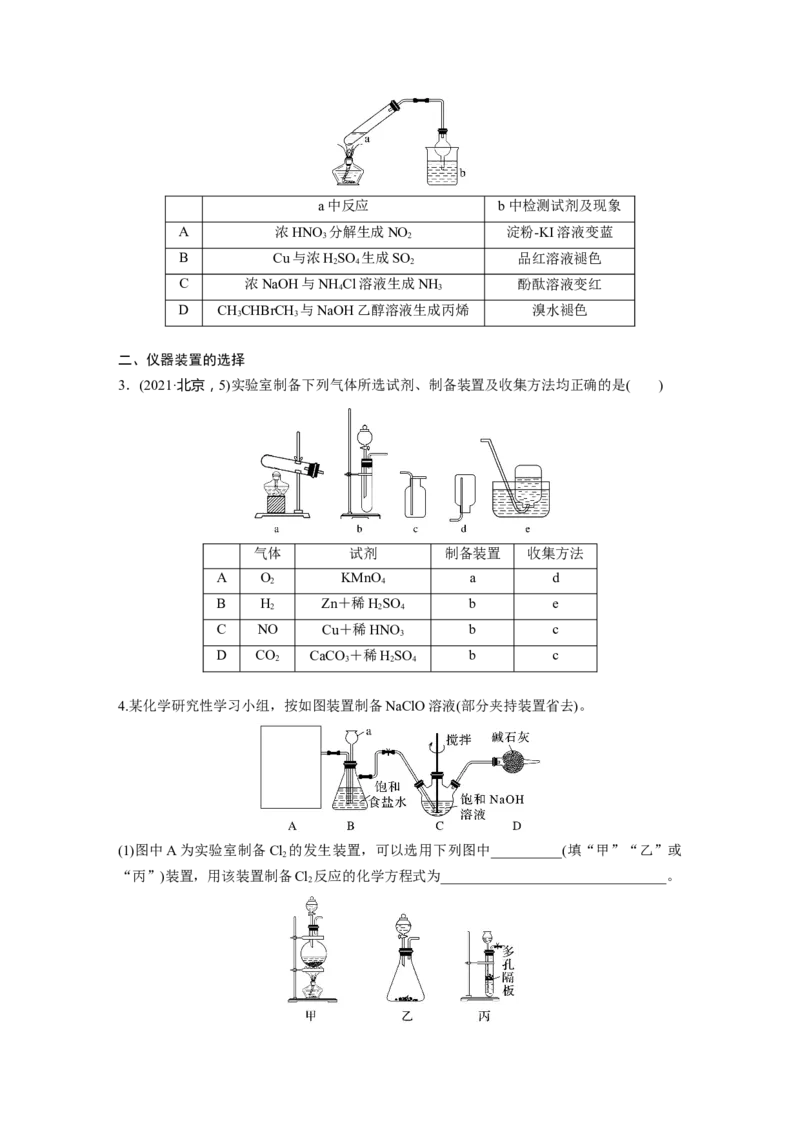
(3)尾气处理装置(见图a、b、c)①实验室制取Cl 时,尾气的处理可采用b装置。
2
②制取CO时,尾气的处理可采用a、c装置。
③制取H 时,尾气的处理可采用a、c装置。
2
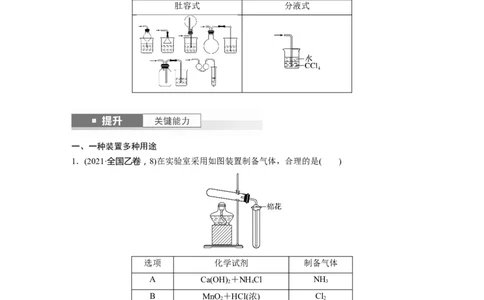
8.防倒吸装置
肚容式 分液式
一、一种装置多种用途
1.(2021·全国乙卷,8)在实验室采用如图装置制备气体,合理的是( )
选项 化学试剂 制备气体
A Ca(OH) +NH Cl NH
2 4 3
B MnO +HCl(浓) Cl
2 2
C MnO +KClO O
2 3 2
D NaCl+HSO (浓) HCl
2 4
2.(2022·北京,10)利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成
的是( )a中反应 b中检测试剂及现象
A 浓HNO 分解生成NO 淀粉-KI溶液变蓝
3 2
B Cu与浓HSO 生成SO 品红溶液褪色
2 4 2
C 浓NaOH与NH Cl溶液生成NH 酚酞溶液变红
4 3
D CHCHBrCH 与NaOH乙醇溶液生成丙烯 溴水褪色
3 3
二、仪器装置的选择
3.(2021·北京,5)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是( )
气体 试剂 制备装置 收集方法
A O KMnO a d
2 4
B H Zn+稀HSO b e
2 2 4
C NO Cu+稀HNO b c
3
D CO CaCO +稀HSO b c
2 3 2 4
4.某化学研究性学习小组,按如图装置制备NaClO溶液(部分夹持装置省去)。
(1)图中A为实验室制备Cl 的发生装置,可以选用下列图中__________(填“甲”“乙”或
2
“丙”)装置,用该装置制备Cl 反应的化学方程式为________________________________。
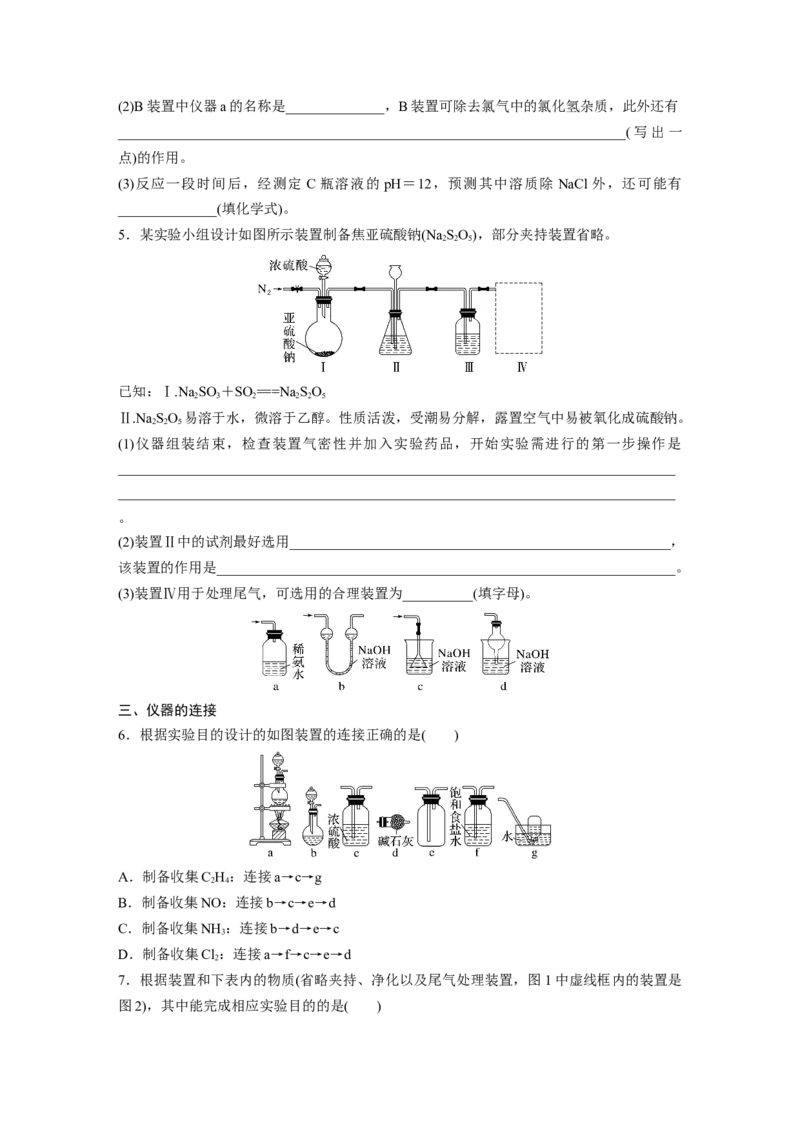
2(2)B装置中仪器a的名称是______________,B装置可除去氯气中的氯化氢杂质,此外还有
________________________________________________________________________(写出一
点)的作用。
(3)反应一段时间后,经测定 C瓶溶液的 pH=12,预测其中溶质除 NaCl外,还可能有
______________(填化学式)。
5.某实验小组设计如图所示装置制备焦亚硫酸钠(Na SO),部分夹持装置省略。
2 2 5
已知:Ⅰ.Na SO +SO ===NaSO
2 3 2 2 2 5
Ⅱ.Na SO 易溶于水,微溶于乙醇。性质活泼,受潮易分解,露置空气中易被氧化成硫酸钠。
2 2 5
(1)仪器组装结束,检查装置气密性并加入实验药品,开始实验需进行的第一步操作是
_______________________________________________________________________________
_______________________________________________________________________________
。
(2)装置Ⅱ中的试剂最好选用______________________________________________________,
该装置的作用是_________________________________________________________________。
(3)装置Ⅳ用于处理尾气,可选用的合理装置为__________(填字母)。
三、仪器的连接
6.根据实验目的设计的如图装置的连接正确的是( )
A.制备收集C H:连接a→c→g
2 4
B.制备收集NO:连接b→c→e→d
C.制备收集NH :连接b→d→e→c
3
D.制备收集Cl:连接a→f→c→e→d
2
7.根据装置和下表内的物质(省略夹持、净化以及尾气处理装置,图1中虚线框内的装置是
图2),其中能完成相应实验目的的是( )实验目的、试剂和操作
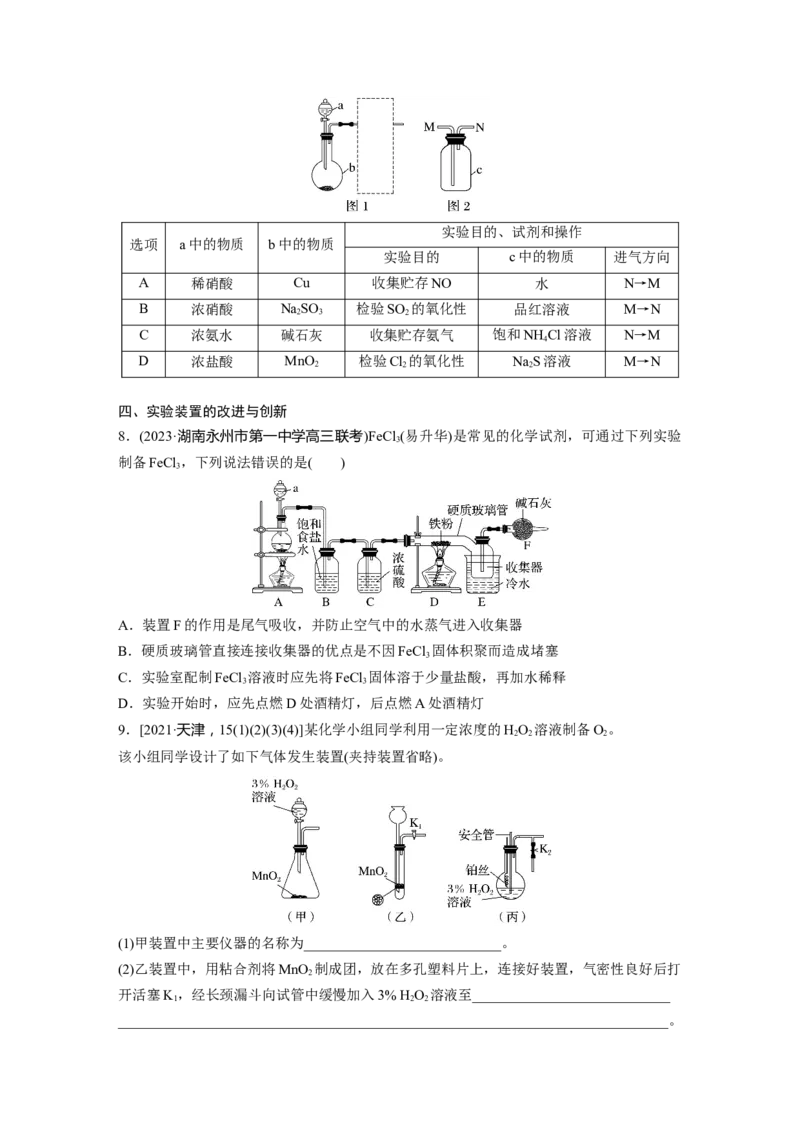
选项 a中的物质 b中的物质
实验目的 c中的物质 进气方向
A 稀硝酸 Cu 收集贮存NO 水 N→M
B 浓硝酸 NaSO 检验SO 的氧化性 品红溶液 M→N
2 3 2
C 浓氨水 碱石灰 收集贮存氨气 饱和NH Cl溶液 N→M
4
D 浓盐酸 MnO 检验Cl 的氧化性 NaS溶液 M→N
2 2 2
四、实验装置的改进与创新
8.(2023·湖南永州市第一中学高三联考)FeCl (易升华)是常见的化学试剂,可通过下列实验
3
制备FeCl ,下列说法错误的是( )
3
A.装置F的作用是尾气吸收,并防止空气中的水蒸气进入收集器
B.硬质玻璃管直接连接收集器的优点是不因FeCl 固体积聚而造成堵塞
3
C.实验室配制FeCl 溶液时应先将FeCl 固体溶于少量盐酸,再加水稀释
3 3
D.实验开始时,应先点燃D处酒精灯,后点燃A处酒精灯
9.[2021·天津,15(1)(2)(3)(4)]某化学小组同学利用一定浓度的HO 溶液制备O。
2 2 2
该小组同学设计了如下气体发生装置(夹持装置省略)。
(1)甲装置中主要仪器的名称为____________________________。
(2)乙装置中,用粘合剂将MnO 制成团,放在多孔塑料片上,连接好装置,气密性良好后打
2
开活塞K,经长颈漏斗向试管中缓慢加入3% H O 溶液至____________________________
1 2 2
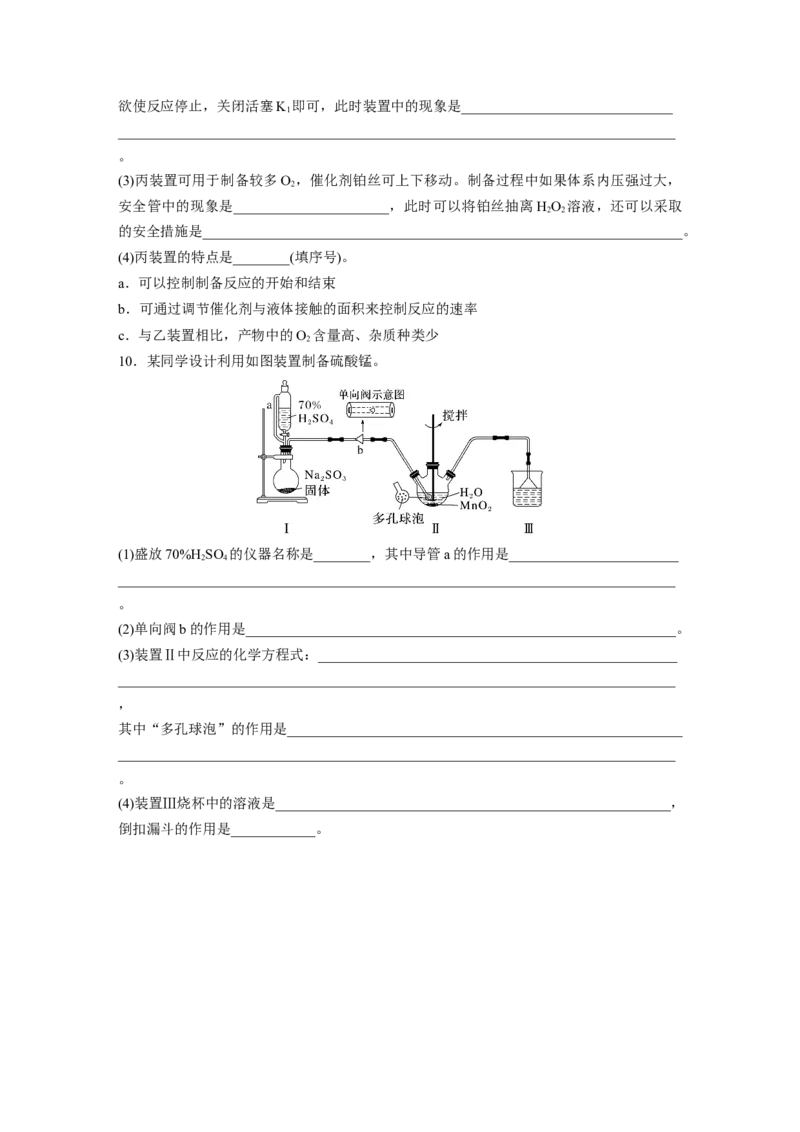
______________________________________________________________________________。欲使反应停止,关闭活塞K 即可,此时装置中的现象是______________________________
1
_______________________________________________________________________________
。
(3)丙装置可用于制备较多O ,催化剂铂丝可上下移动。制备过程中如果体系内压强过大,
2
安全管中的现象是______________________,此时可以将铂丝抽离HO 溶液,还可以采取
2 2
的安全措施是____________________________________________________________________。
(4)丙装置的特点是________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的O 含量高、杂质种类少
2
10.某同学设计利用如图装置制备硫酸锰。
(1)盛放70%H SO 的仪器名称是________,其中导管a的作用是________________________
2 4
_______________________________________________________________________________
。
(2)单向阀b的作用是_____________________________________________________________。
(3)装置Ⅱ中反应的化学方程式:___________________________________________________
_______________________________________________________________________________
,
其中“多孔球泡”的作用是________________________________________________________
_______________________________________________________________________________
。
(4)装置Ⅲ烧杯中的溶液是________________________________________________________,
倒扣漏斗的作用是____________。