文档内容
微专题18 金属及其化合物制备流程(Co)
钴:元素符号Co,原子序数27,原子量58.93,外围电子排布3d74s2,位于第四周期Ⅷ族。
主要氧化数+1、+3、+4。
一、物理性质:
金属,硬而有延展性,具有铁磁性,密度8.9克/厘米3,熔点1495℃,沸点2870℃。
二、化学性质:
常温下不跟空气,水反应。白热时燃烧生成四氧化三钴,也能分解水蒸气。能跟卤素直
接化合。能溶解于盐酸、硫酸和硝酸中。能被氢氟酸,氨水和氢氧化钠溶液缓慢侵蚀。
三、用途:
用于制超硬耐热合金、磁性合金和切削工具用合金。同位素60Co是一种放射源,用于医
疗、科研和生产中。1735年瑞典人布朗特煅烧钻矿得到钴。主要钴矿有辉钴矿、砷钴矿。
先将钴矿转化为氧化钴,然后用铝还原制取钴。
四、钴的提取工艺
自然界中的钴矿很少单独存在,主要伴生于镍矿、铜矿、黄铁矿和砷矿床中,而且含量
较少,提取起来相对比较困难。钴矿资源主要有镍钴硫化矿和氧化矿,铜钴矿,砷钴矿,
含钴黄铁矿四种类型。钴冶炼特点表现为原料品位低,提取流程长,提取方法多。
1.从镍、铜硫的吹炼渣中提钴:含钴吹炼渣在鼓风炉或电炉中经还原硫化熔炼,获得钴
合金或钴锍。经磁选富集后加压酸浸,使钴进入溶液。溶液经净化后加入草酸使钴生产
草酸钴沉淀,草酸钴经煅烧即可产出精制氧化钴产品。
2.从镍精炼净化渣中提钴:镍电解精炼过程中阳极液净化产出的钴渣是重要的提钴原料。
钴渣经还原硫酸浸出使钴呈硫酸钴进入溶液,溶液用黄钠铁矾法除铁,萃取法除铜,锌,
锰等杂质和镍钴分离获得纯净的氯化钴溶液,籍此可生产氧化钴产品,或经电积获取金
属钴产品。
3.从含钴黄铁矿中提取钴:含钴黄铁矿经浮选可产出含钴0.3%~0。5%的钴硫精矿。钴
硫精矿经硫酸化焙烧,使精矿中的钴,镍,铜等有价元素转变为可溶性的硫酸盐。焙砂
用水浸或酸浸使钴,镍,铜等转入溶液。浸出液经净化除杂除去铁,铜,锌,锰等杂质,
再经镍钴分离得到纯净的钴溶液,电积生产金属钴。4.从砷钴矿提取钴:砷钴矿经焙烧或熔炼使砷以As O 挥发脱除,得到焙砂或钴锍经酸
2 3
浸使钴进入溶液,溶液经除铁,砷和铜,锌,锰等杂质后进入镍钴分离。净化后的钴溶
液再根据市场需要生产金属钴或氧化钴产品。
钴大多伴生在其他矿物中而且成分复杂,因此钴的冶炼方法繁多,流程复杂。钴的冶炼
一般分成三个步骤:
一是把钴从矿石中转入溶液,或制成粗钴合金或钴锍,再转入溶液;
二是除杂净化;
三是提取金属。
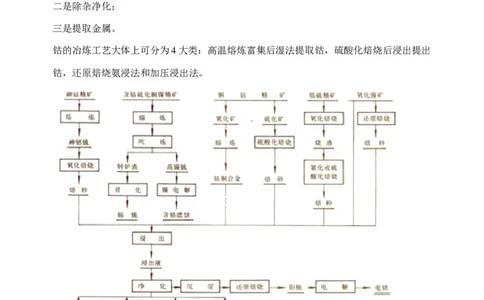
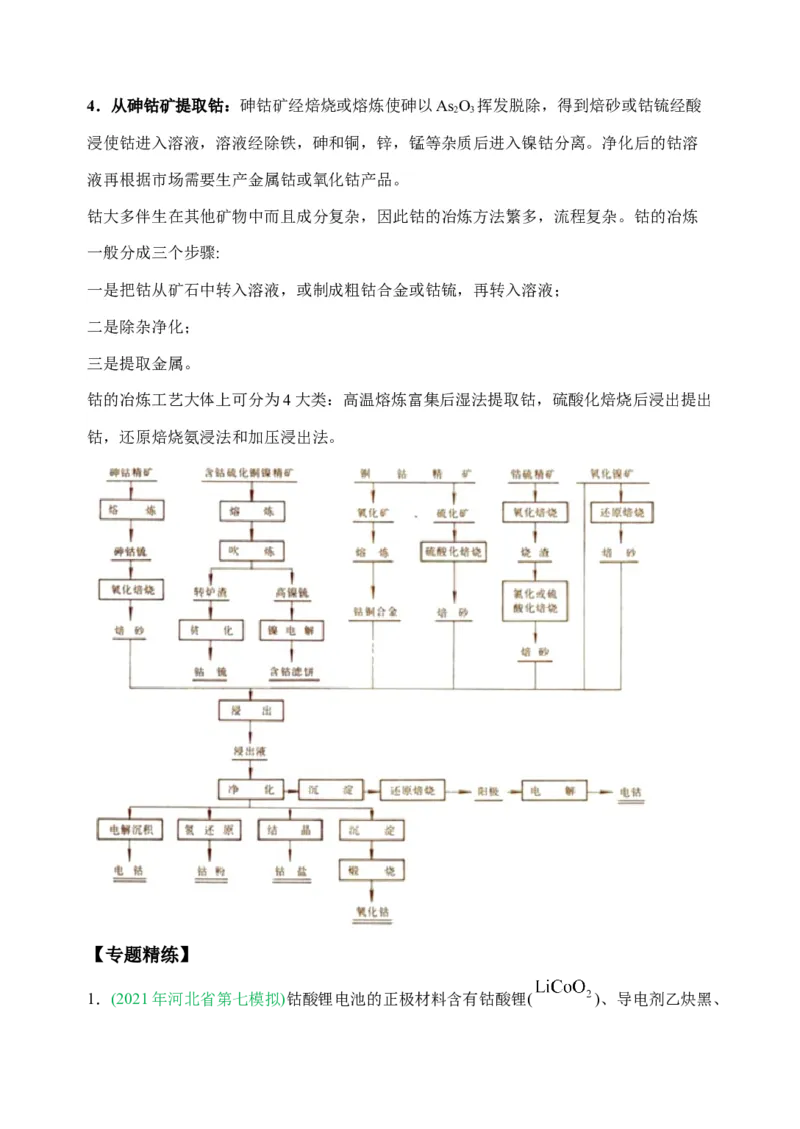
钴的冶炼工艺大体上可分为4大类:高温熔炼富集后湿法提取钴,硫酸化焙烧后浸出提出
钴,还原焙烧氨浸法和加压浸出法。
【专题精练】
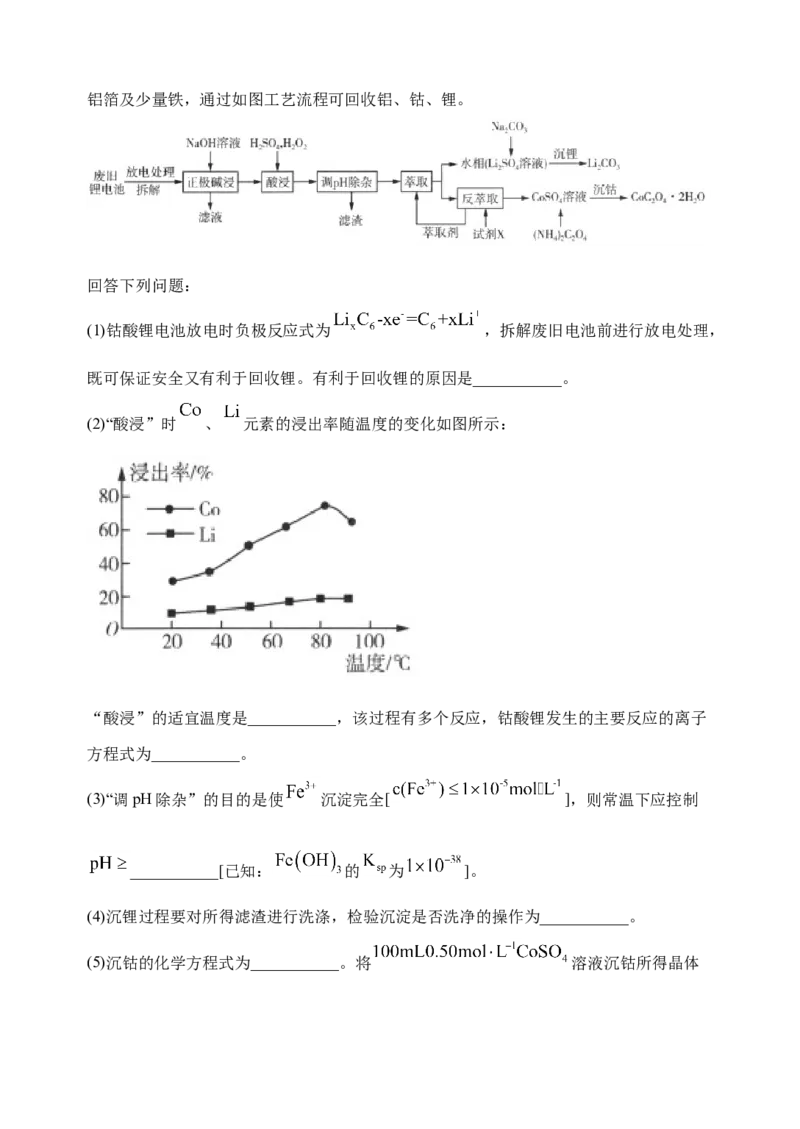
1.(2021年河北省第七模拟)钴酸锂电池的正极材料含有钴酸锂( )、导电剂乙炔黑、铝箔及少量铁,通过如图工艺流程可回收铝、钴、锂。
回答下列问题:
(1)钴酸锂电池放电时负极反应式为 ,拆解废旧电池前进行放电处理,
既可保证安全又有利于回收锂。有利于回收锂的原因是___________。
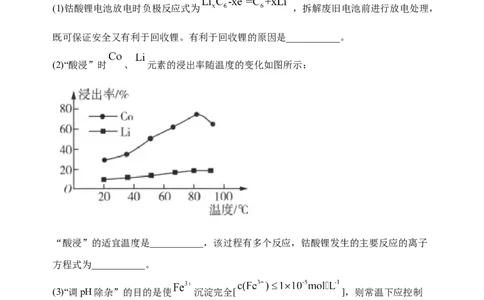
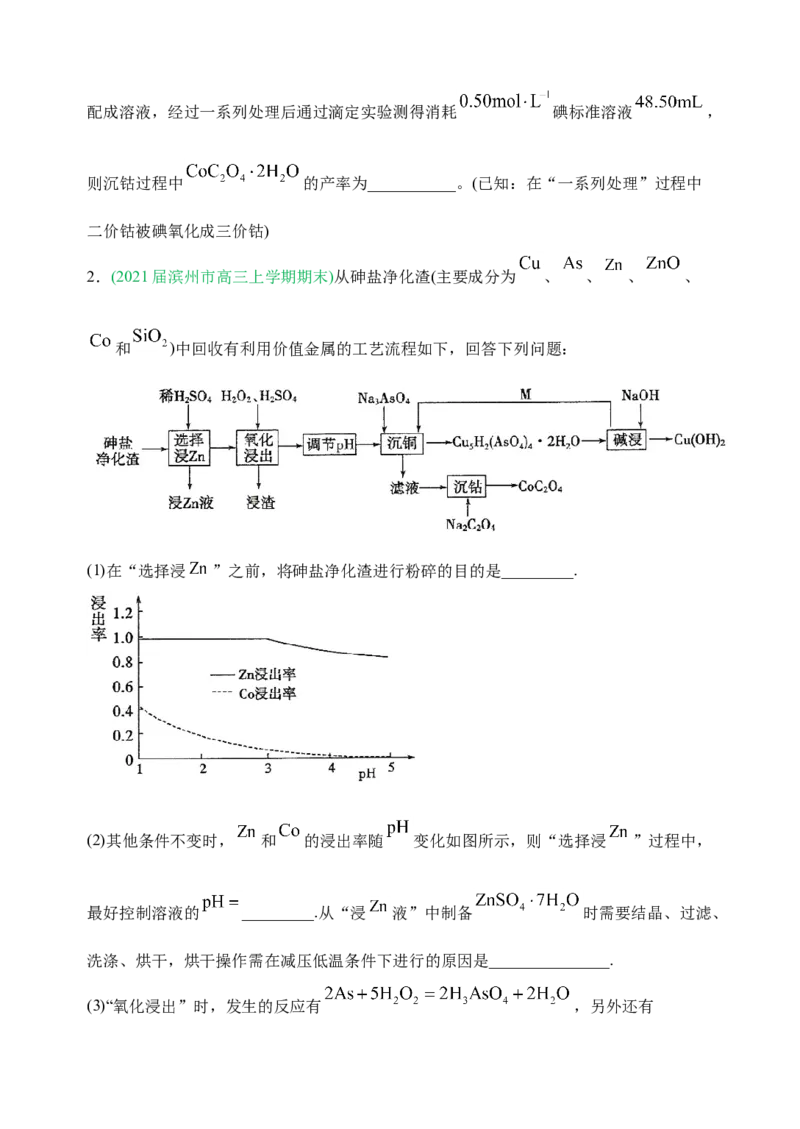
(2)“酸浸”时 、 元素的浸出率随温度的变化如图所示:
“酸浸”的适宜温度是___________,该过程有多个反应,钴酸锂发生的主要反应的离子
方程式为___________。
(3)“调pH除杂”的目的是使 沉淀完全[ ],则常温下应控制
___________[已知: 的 为 ]。
(4)沉锂过程要对所得滤渣进行洗涤,检验沉淀是否洗净的操作为___________。
(5)沉钴的化学方程式为___________。将 溶液沉钴所得晶体配成溶液,经过一系列处理后通过滴定实验测得消耗 碘标准溶液 ,
则沉钴过程中 的产率为___________。(已知:在“一系列处理”过程中
二价钴被碘氧化成三价钴)
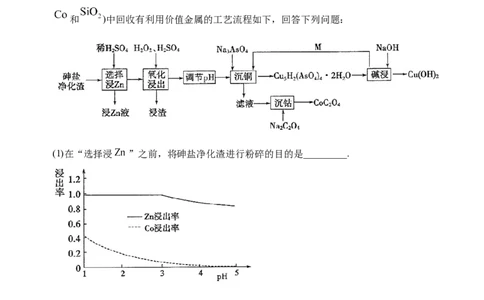
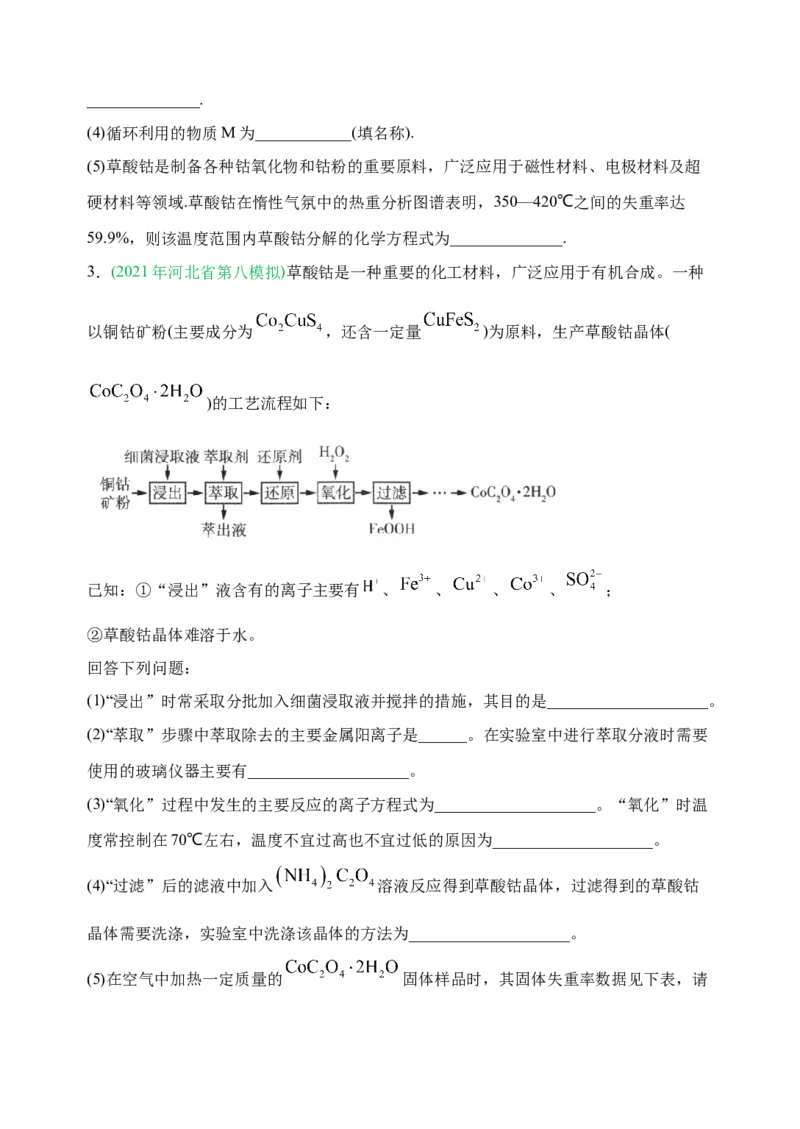
2.(2021届滨州市高三上学期期末)从砷盐净化渣(主要成分为 、 、 、 、
和 )中回收有利用价值金属的工艺流程如下,回答下列问题:
(1)在“选择浸 ”之前,将砷盐净化渣进行粉碎的目的是_________.
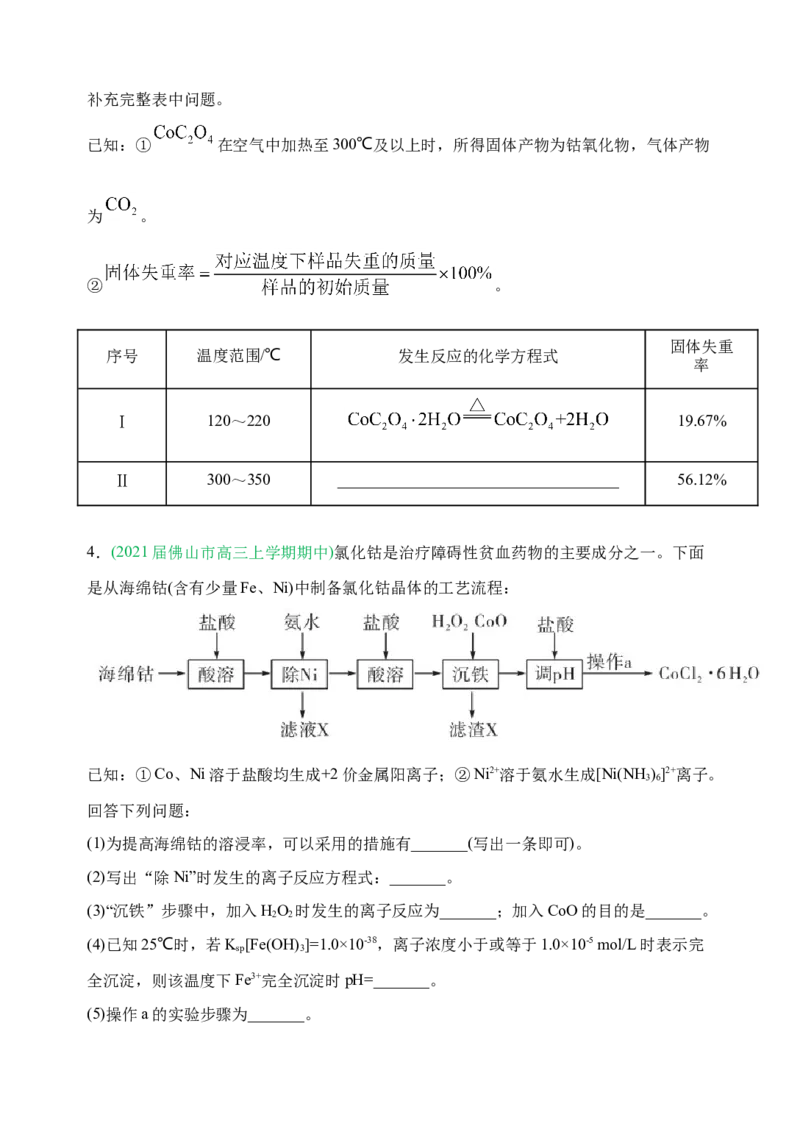
(2)其他条件不变时, 和 的浸出率随 变化如图所示,则“选择浸 ”过程中,
最好控制溶液的 _________.从“浸 液”中制备 时需要结晶、过滤、
洗涤、烘干,烘干操作需在减压低温条件下进行的原因是_______________.
(3)“氧化浸出”时,发生的反应有 ,另外还有______________.
(4)循环利用的物质M为____________(填名称).
(5)草酸钴是制备各种钴氧化物和钴粉的重要原料,广泛应用于磁性材料、电极材料及超
硬材料等领域.草酸钴在惰性气氛中的热重分析图谱表明,350—420℃之间的失重率达
59.9%,则该温度范围内草酸钴分解的化学方程式为______________.
3.(2021年河北省第八模拟)草酸钴是一种重要的化工材料,广泛应用于有机合成。一种
以铜钴矿粉(主要成分为 ,还含一定量 )为原料,生产草酸钴晶体(
)的工艺流程如下:
已知:①“浸出”液含有的离子主要有 、 、 、 、 ;
②草酸钴晶体难溶于水。
回答下列问题:
(1)“浸出”时常采取分批加入细菌浸取液并搅拌的措施,其目的是____________________。
(2)“萃取”步骤中萃取除去的主要金属阳离子是______。在实验室中进行萃取分液时需要
使用的玻璃仪器主要有____________________。
(3)“氧化”过程中发生的主要反应的离子方程式为____________________。“氧化”时温
度常控制在70℃左右,温度不宜过高也不宜过低的原因为____________________。
(4)“过滤”后的滤液中加入 溶液反应得到草酸钴晶体,过滤得到的草酸钴
晶体需要洗涤,实验室中洗涤该晶体的方法为____________________。
(5)在空气中加热一定质量的 固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:① 在空气中加热至300℃及以上时,所得固体产物为钴氧化物,气体产物
为 。
② 。
固体失重
序号 温度范围/℃ 发生反应的化学方程式
率
Ⅰ 120~220 19.67%
Ⅱ 300~350 ___________________________________ 56.12%
4.(2021届佛山市高三上学期期中)氯化钴是治疗障碍性贫血药物的主要成分之一。下面
是从海绵钴(含有少量Fe、Ni)中制备氯化钴晶体的工艺流程:
已知:①Co、Ni溶于盐酸均生成+2价金属阳离子;②Ni2+溶于氨水生成[Ni(NH )]2+离子。
3 6
回答下列问题:
(1)为提高海绵钴的溶浸率,可以采用的措施有_______(写出一条即可)。
(2)写出“除Ni”时发生的离子反应方程式:_______。
(3)“沉铁”步骤中,加入HO 时发生的离子反应为_______;加入CoO的目的是_______。
2 2
(4)已知25℃时,若K [Fe(OH) ]=1.0×10-38,离子浓度小于或等于1.0×10-5 mol/L时表示完
sp 3
全沉淀,则该温度下Fe3+完全沉淀时pH=_______。
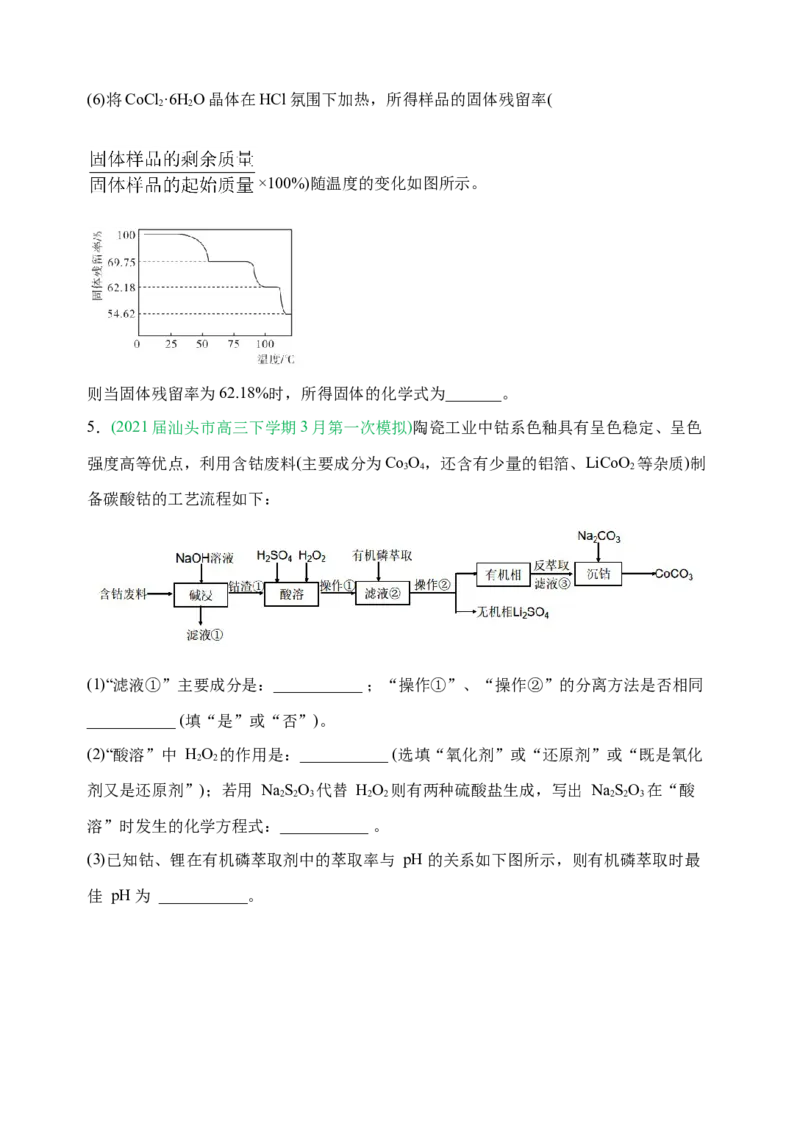
(5)操作a的实验步骤为_______。(6)将CoCl ·6H O晶体在HCl氛围下加热,所得样品的固体残留率(
2 2
×100%)随温度的变化如图所示。
则当固体残留率为62.18%时,所得固体的化学式为_______。
5.(2021届汕头市高三下学期3月第一次模拟)陶瓷工业中钴系色釉具有呈色稳定、呈色
强度高等优点,利用含钴废料(主要成分为Co O,还含有少量的铝箔、LiCoO 等杂质)制
3 4 2
备碳酸钴的工艺流程如下:
(1)“滤液①”主要成分是:___________ ;“操作①”、“操作②”的分离方法是否相同
___________ (填“是”或“否”)。
(2)“酸溶”中 HO 的作用是:___________ (选填“氧化剂”或“还原剂”或“既是氧化
2 2
剂又是还原剂”);若用 NaSO 代替 HO 则有两种硫酸盐生成,写出 NaSO 在“酸
2 2 3 2 2 2 2 3
溶”时发生的化学方程式:___________ 。
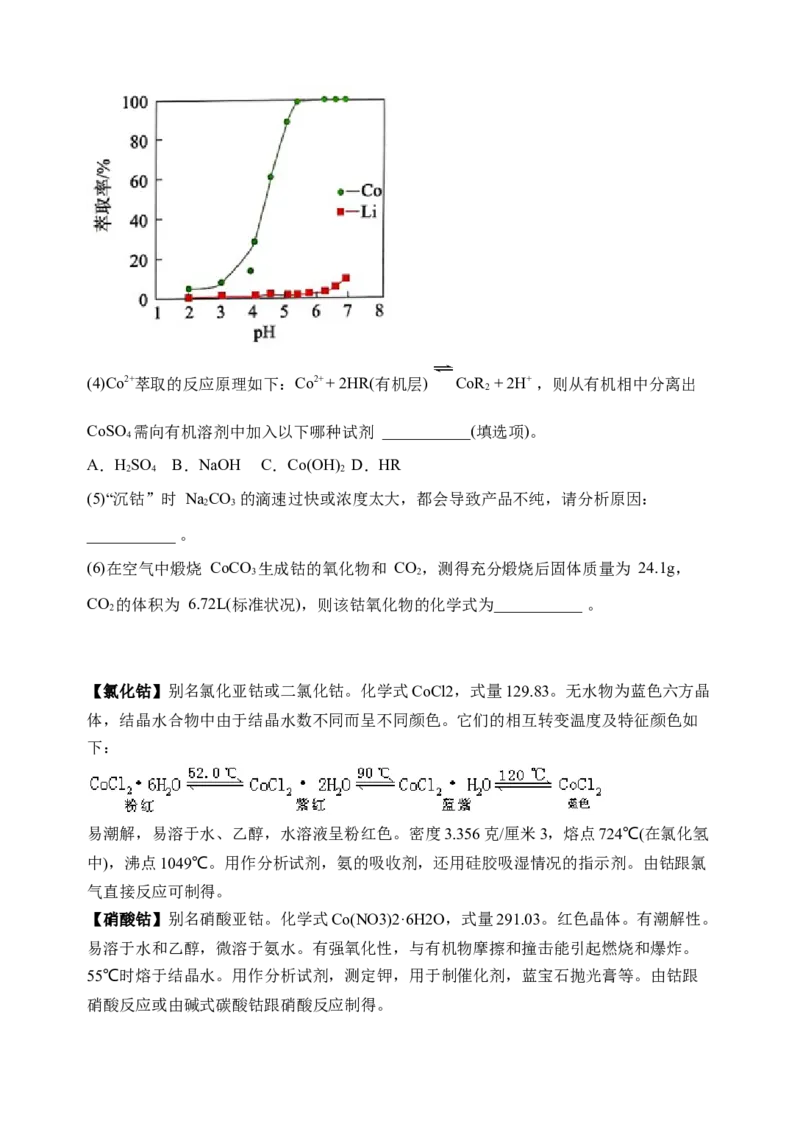
(3)已知钴、锂在有机磷萃取剂中的萃取率与 pH 的关系如下图所示,则有机磷萃取时最
佳 pH 为 ___________。(4)Co2+萃取的反应原理如下:Co2+ + 2HR(有机层) CoR + 2H+ ,则从有机相中分离出
2
CoSO 需向有机溶剂中加入以下哪种试剂 ___________(填选项)。
4
A.HSO B.NaOH C.Co(OH) D.HR
2 4 2
(5)“沉钴”时 NaCO 的滴速过快或浓度太大,都会导致产品不纯,请分析原因:
2 3
___________ 。
(6)在空气中煅烧 CoCO 生成钴的氧化物和 CO,测得充分煅烧后固体质量为 24.1g,
3 2
CO 的体积为 6.72L(标准状况),则该钴氧化物的化学式为___________ 。
2
【氯化钴】别名氯化亚钴或二氯化钴。化学式CoCl2,式量129.83。无水物为蓝色六方晶
体,结晶水合物中由于结晶水数不同而呈不同颜色。它们的相互转变温度及特征颜色如
下:
易潮解,易溶于水、乙醇,水溶液呈粉红色。密度3.356克/厘米3,熔点724℃(在氯化氢
中),沸点1049℃。用作分析试剂,氨的吸收剂,还用硅胶吸湿情况的指示剂。由钴跟氯
气直接反应可制得。
【硝酸钴】别名硝酸亚钴。化学式Co(NO3)2·6H2O,式量291.03。红色晶体。有潮解性。
易溶于水和乙醇,微溶于氨水。有强氧化性,与有机物摩擦和撞击能引起燃烧和爆炸。
55℃时熔于结晶水。用作分析试剂,测定钾,用于制催化剂,蓝宝石抛光膏等。由钴跟
硝酸反应或由碱式碳酸钴跟硝酸反应制得。【氧化高钴】别名三氧化二钴,化学式Co2O3,式量165.86。灰黑色结晶性粉末。溶于
热盐酸或热稀硫酸,分别放出氯气和氧气。不溶于水和醇。熔点895℃(分解)。用作分析
试剂,氧化剂,催化剂。还用于制取钴或钴盐。在空气中加热碳酸钴可制得三氧化二钴。
【三氧化二钴】见氧化高钴条。