文档内容
微专题17 金属及其化合物制备流程(Zn)
锌:素符号Zn,原子序数30,原子量65.38,外围电子排布3d10s2,位于第四周期ⅡB族。
主要化合价+2。
一、物理性质:
银白略带蓝色有光泽金属,硬度2.5,有延展性,良好的传热、导电性,密度为7.14克/厘
米3,熔点419.58℃,沸点907℃。
二、化学性质:
化学性质比较活泼。室温时在空气中较稳定。在潮湿空气中生成一层灰色碱式碳酸锌,
可作保护膜。锌燃烧时有蓝绿色火焰。高温时跟水蒸汽反应放出氢气。加热时可跟卤素,
硫等反应。易与酸反应,但高纯锌反应慢,若加入少量硫酸铜溶液,或跟铜、镍、铂等
金属接触时,反应加快。溶于强碱溶液,生成锌酸盐,如:
Zn+2NaOH=Na ZnO+H ↑
2 2 2
溶于氨水和铵盐溶液中,如:
Zn+2NH Cl=Zn(NH )Cl+H ↑
4 3 2 2 2
三、用途:
主要用于制合金、金属表面镀锌,还用于制于电池、焰火、作催化剂和还原剂。我国明
代以前已发现并使用锌。主要矿物有闪锌矿ZnS、菱锌矿ZnCO 等。先将矿石煅烧变成
3
氧化锌,再用焦炭还原氧化锌制得。
*最后附有锌的化合物
四、工业制备:
锌的冶炼方法
锌的冶炼有两种工艺:火法冶炼和湿法冶炼。
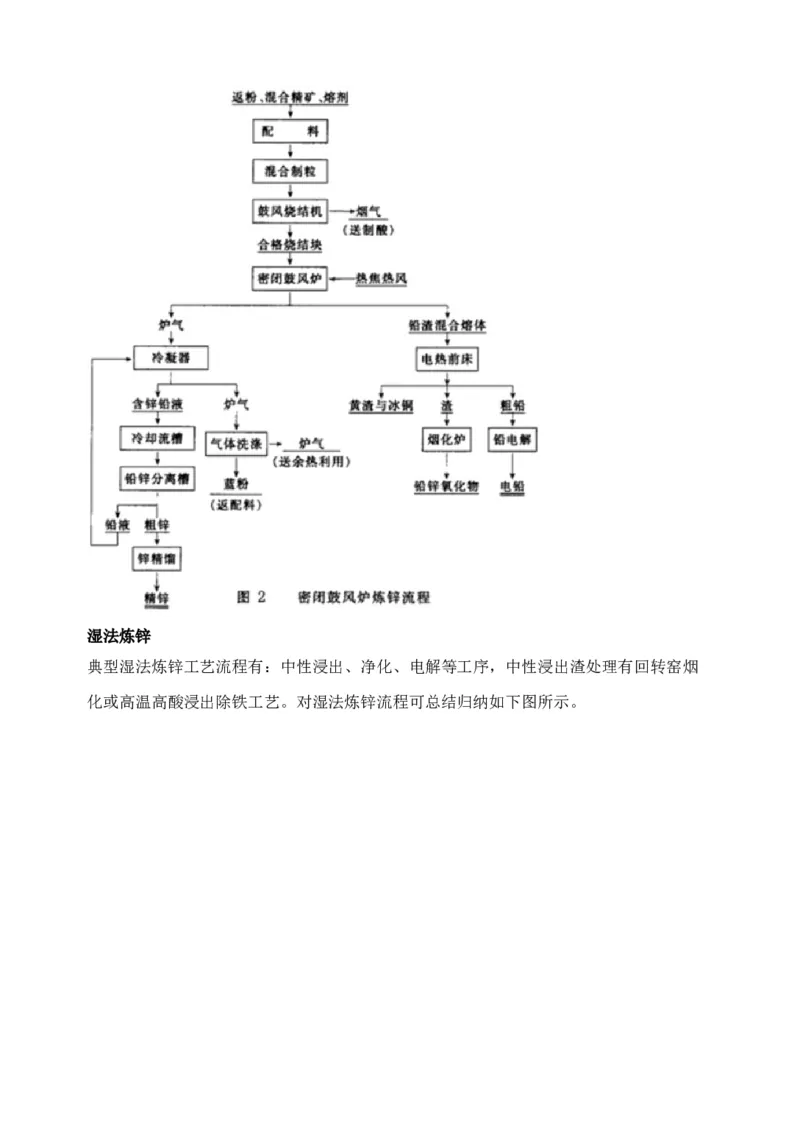
密闭鼓风炉炼铅锌是世界上最主要的几乎是唯一的火法炼锌方法。
湿法炼锌是当今世界最主要的炼锌方法,其产量占世界总锌产量的85%以上。近期世界
新建和扩建的生产能力均采用湿法炼锌工艺。
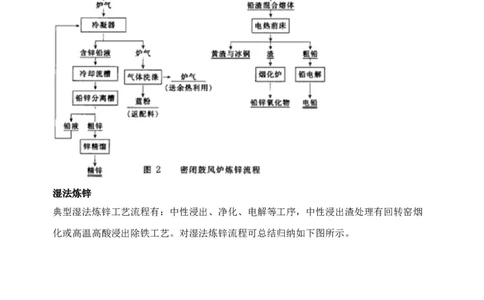
火法炼锌
在高温下,用碳作还原剂从氧化锌物料中还原提取金属锌的过程被称为火法炼锌。
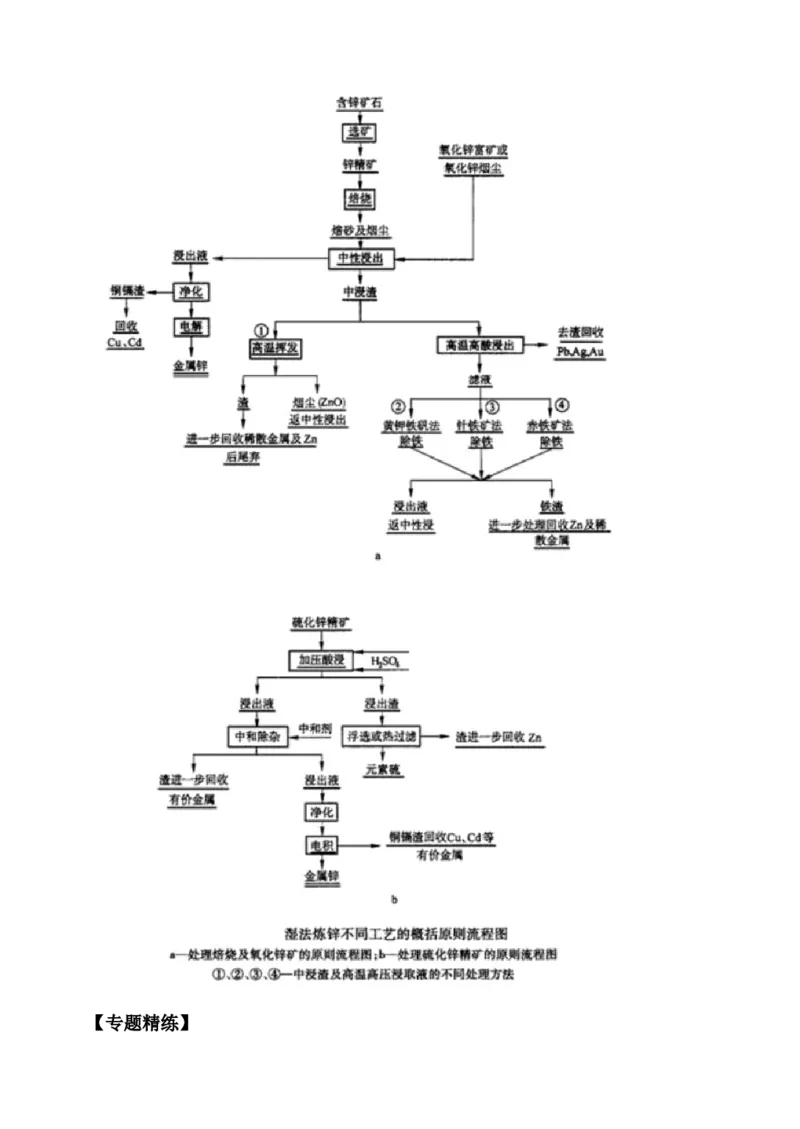
密闭鼓风炉炼锌工艺流程图如下:湿法炼锌
典型湿法炼锌工艺流程有:中性浸出、净化、电解等工序,中性浸出渣处理有回转窑烟
化或高温高酸浸出除铁工艺。对湿法炼锌流程可总结归纳如下图所示。【专题精练】1.(2020届高考化学二轮复习大题精准训练)氧化锌工业品广泛应用于橡胶、涂料、陶瓷、
化工、医药、玻璃和电子等行业,随着工业的飞速发展,我国对氧化锌的需求量日益增
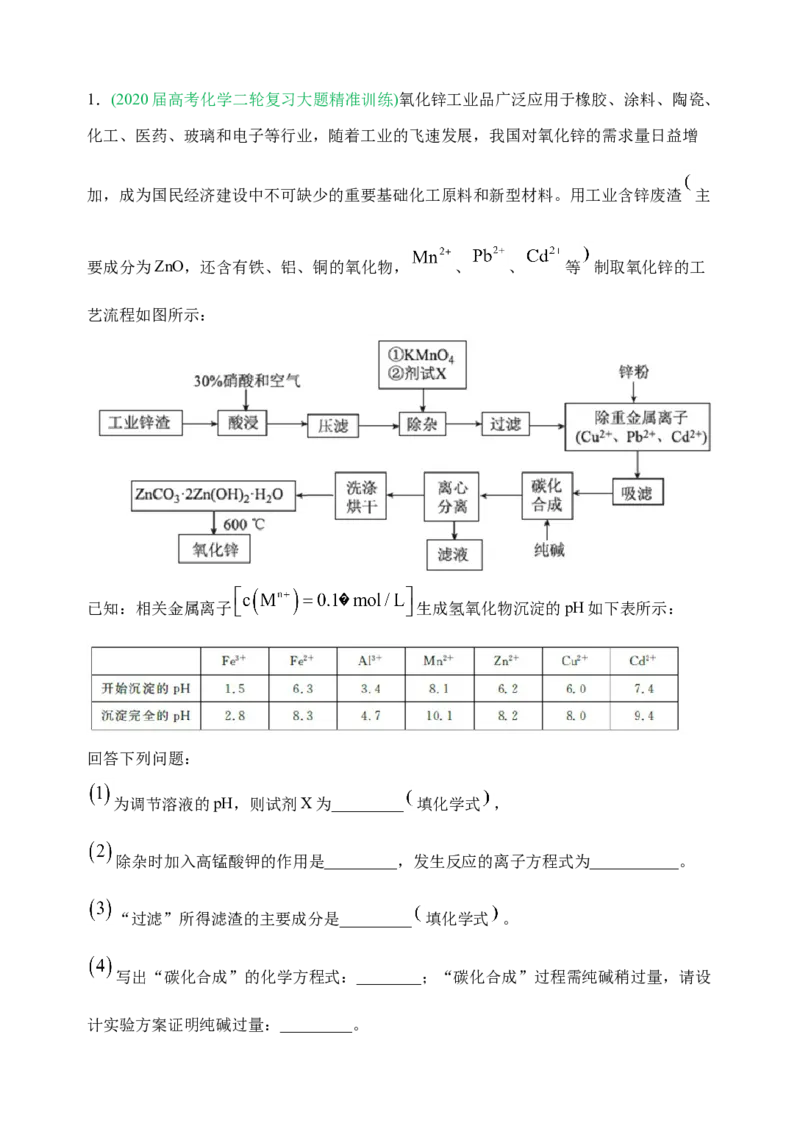
加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。用工业含锌废渣 主
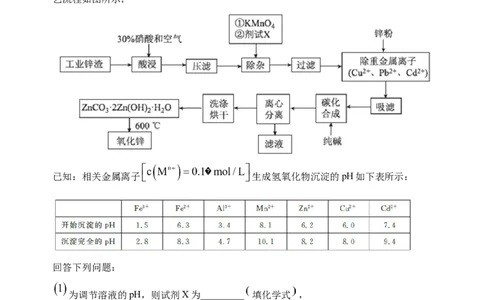
要成分为ZnO,还含有铁、铝、铜的氧化物, 、 、 等 制取氧化锌的工
艺流程如图所示:
已知:相关金属离子 生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
为调节溶液的pH,则试剂X为_________ 填化学式 ,
除杂时加入高锰酸钾的作用是_________,发生反应的离子方程式为___________。
“过滤”所得滤渣的主要成分是_________ 填化学式 。
写出“碳化合成”的化学方程式:________;“碳化合成”过程需纯碱稍过量,请设
计实验方案证明纯碱过量:_________。【答案】 或 或 除去
、 、
或
静置,取少许上层清液继续滴加纯碱溶液,若无沉淀产生,则证明纯碱过量 或静置,取
少许上层清液滴加 溶液,若有白色沉淀产生,则证明纯碱过量
【详解】
加入试剂X的目的是调节溶液的pH,使 、 生成沉淀除去,为不引入新的杂
质离子,可加入ZnO、 、 等;
加入高锰酸钾的作用是将 转化为 沉淀,除去 ,反应的离子方程式
为 ;
由 、 知,“过滤”所得滤渣的主要成分是 、 、 ;
“碳化合成”时加入 ,产物为 ,反应的化学方程式为 或
过量时 ;若 不足时,溶液中还有 ,继续滴加 溶液有沉淀产
生,或 过量时,可检验溶液中的 ,具体方法为:静置,取少许上层清液继
续滴加纯碱溶液,若无沉淀产生,则证明纯碱过量 或静置,取少许上层清液滴加
溶液,若有白色沉淀产生,则证明纯碱过量 。
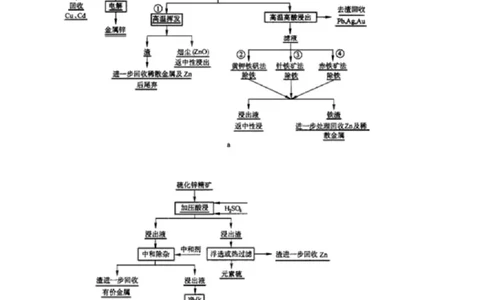
2.(2020届高三化学二轮选修大题必练)硫化锌 是一种重要的化工原料,难溶于水,
可由炼锌的废渣锌灰制取,其工艺流程如图所示。
为提高锌灰的浸取率,不宜采用的方法是______ 填序号 。
研磨 多次浸取 升高温度 加压 搅拌
步骤Ⅱ中 的作用是______,所得滤渣的主要成分是______ 写化学式 。
步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为______。步骤Ⅳ还可以回收 来制取 。
检验ZnS固体是否洗涤干净的方法是______。
可由等物质的量的 和 在高温、催化剂条件下制取,化学反应方程
式为______。
若步骤Ⅱ加入的 为b mol,步骤Ⅲ所得Cd为d mol,最后得到V L,c
的 溶液。则理论上所用锌灰中含有锌元素的质量为______。
【答案】 调节溶液的pH,使 水解 而除去 、
Zn 取最后的洗涤液少许于试管,滴加几滴 溶液,若出现
浑浊则未洗净,反之则已洗净
【详解】
锌灰与硫酸反应得含有镉离子、锌离子、铁离子、亚铁离子等的溶液,加入双氧水将二
价铁离子氧化为三价铁离子,用碳酸锌调节平衡pH使 完全沉淀,过滤后得到
含有镉离子、锌离子的溶液Ⅰ和滤渣 、 ;步骤Ⅲ中可得Cd单质,为避
免引入新的杂质,试剂X应为锌,过滤后得溶液Ⅱ为硫酸锌溶液,硫酸锌溶液中加入硫
化钠可得硫酸钠和硫化锌。搅拌、适当升温、将废渣碾细成粉末、搅拌、多次浸取等都可提高锌灰的浸取率,加
压对锌灰的浸取率无影响,故选④;
根据上面的分析可知,用碳酸锌调节平衡pH使 完全沉淀,反应的离子方程
式为 、 ,所以步骤Ⅱ
所得滤渣为 、 ;
向含有镉离子、锌离子的溶液Ⅰ中加入锌,即可置换出Cd单质,又不引入新的杂质;
检验ZnS固体是否洗涤干净也就是检验最后一次洗涤液中是否含有硫酸根,具体
操作为:取最后的洗涤液少许于试管,滴加几滴 溶液,若出现浑浊则未洗净,反
之则已洗净;
等物质的量的 和 在高温、催化剂条件下生成 ,根据元素守恒可知,
该化学反应方程式为: ;
步骤Ⅲ所得Cd为d mol,则用于置换镉的锌的物质的量为d mol,硫酸钠的物质的量
为: ,所以硫酸锌的物质的量为cV mol,根据锌元素守恒可知,
样品中锌元素的物质的量为: mol,所以锌灰中含有锌元素的质量为:。
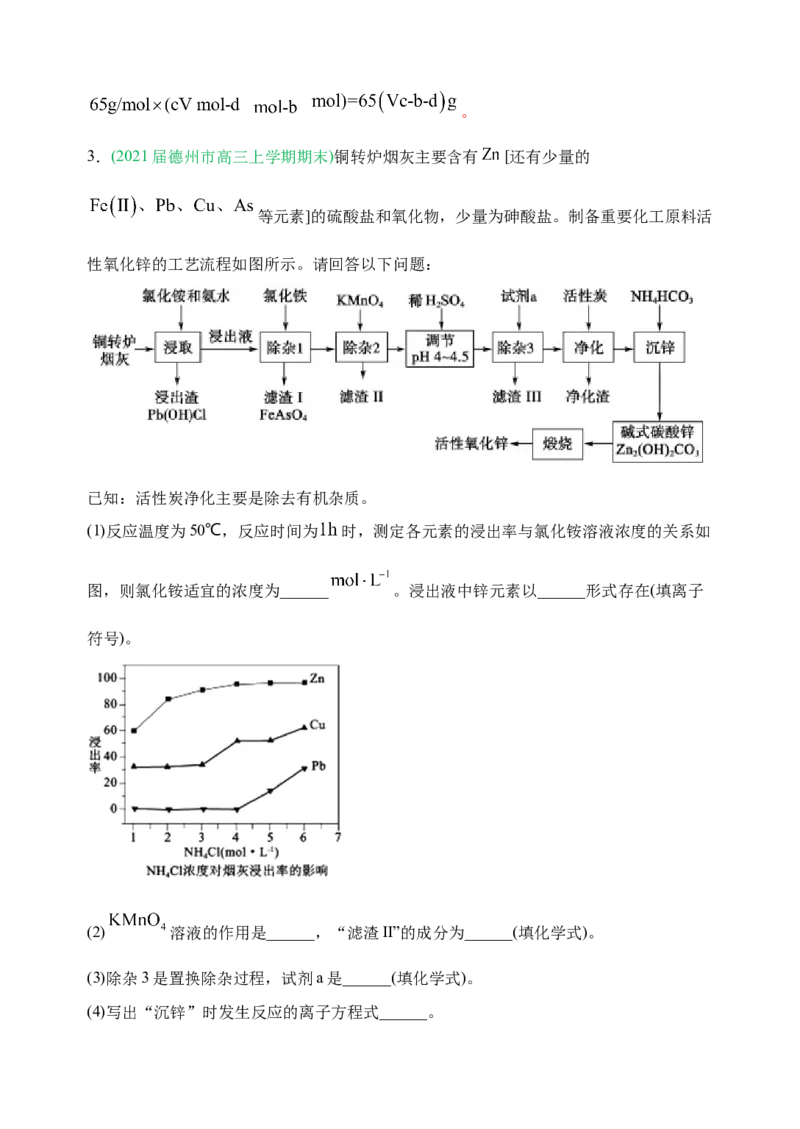
3.(2021届德州市高三上学期期末)铜转炉烟灰主要含有 [还有少量的
等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活
性氧化锌的工艺流程如图所示。请回答以下问题:
已知:活性炭净化主要是除去有机杂质。
(1)反应温度为50℃,反应时间为 时,测定各元素的浸出率与氯化铵溶液浓度的关系如
图,则氯化铵适宜的浓度为______ 。浸出液中锌元素以______形式存在(填离子
符号)。
(2) 溶液的作用是______,“滤渣II”的成分为______(填化学式)。
(3)除杂3是置换除杂过程,试剂a是______(填化学式)。
(4)写出“沉锌”时发生反应的离子方程式______。(5)取 活性氧化锌样品配成待测液,加入3、4滴指示剂,再加入适量六亚甲基四胺,
用 标准液进行滴定,消耗标准液 。已知:与 标
准液 相当的以克表示的氧化锌质量为0.08139,则样品中氧
化锌的质量分数为______(用含a的代数式表示)。
【答案】(1)4 (2) 将 氧化为 (3)
(4) (5)
【详解】
(1)加入氯化铵时,主要是为了除去Pb杂质,从图中可以看出,Pb的浸出率为0时,氯化
铵适宜的浓度为4 。浸出液中Zn2+与氨水反应的产物进入滤液中,则锌元素以
形式存在。答案为:4; ;
(2)加入KMnO 的目的是除去溶液中的铁元素,所以它将Fe2+氧化为Fe3+再转化为沉淀,
4
自身被还原为MnO ,从而得出加入KMnO 的作用是将 氧化为 ,“滤渣II”的成
2 4
分为 。答案为:将 氧化为 ; ;
(3)除杂3是置换除杂过程,则试剂a应能将Cu2+从溶液中置换出来,且不引入新的杂质,
所以a应是 。答案为: ;
(4)“沉锌”时,加入NH HCO ,最终Zn2+转化为Zn(OH) CO 沉淀,发生反应的离子方程
4 3 2 2 3
式 。答案为:;
(5)依题意知,与 标准液 相当的以克表示的
氧化锌质量为0.08139,则100mL 标准液相当于氧化锌的质量为
=8.319g,则样品中氧化锌的质量分数为
= 。答案为: 。
4.(2013年新课标Ⅱ卷)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业
级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如图:
工业ZnO 浸出液 滤液 滤
液 滤饼 ZnO
提示:在本实验条件下,Ni(Ⅱ)不能被氧化,高锰酸钾的还原产物是MnO
2
回答下列问题:
(1)反应②中除掉的杂质离子是_______,发生反应的离子方程式为 _______。
加高锰酸钾溶液前,若pH较低,对除杂的影响是_______。
(2)反应③的反应类型为_______,过滤得到的滤渣中,除了过量的锌外还有_______。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是_______。
(4)反应④中产物的成分可能是ZnCO ·xZn(OH) .取干操后的滤饼11.2g,煅烧后可得到产
3 2
品8.1 g. 则x等于_______。
【答案】(1)Fe2+和Mn2+ MnO +3Fe2++7H O=3Fe(OH)↓+MnO+5H+;2MnO +3Mn2+
2 3 2
+2H O=5MnO ↓+4H+ 铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质 (2) 置
2 2换反应 镍 (3) 取少量水洗液于试管中,滴入1-2滴稀硝酸,再滴入硝酸钡溶液,若
无白色沉淀生成,则说明沉淀已经洗涤干净 (4) 1
【详解】
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方
程式为。加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去
铁和锰杂质。
(2)反应③为锌与镍离子的反应,反应类型为置换反应,得到的滤渣中,除了过量的锌外
还有金属镍。
(3)检验沉淀是否洗涤干净的方法是取少量水洗液于试管中,滴入1-2滴稀硝酸酸化,再滴
入硝酸钡溶液,若无白色沉淀生成,说明没有硫酸根离子,则说明沉淀已经洗涤干净
(4)根据关系式ZnCO ·xZn(OH) _______ (x+1)ZnO
3 2
125+99x 81(x+1)
11.2g 8.1g
解得:x=1
【氧化锌】化学式ZnO,式量81.37。俗名锌白。白色六方晶体或粉末。密度5.606克/厘
米3,熔点1975℃,难溶于水。加热时变黄,冷却后仍为白色。两性氧化物,溶于酸生成
锌盐,溶于强碱溶液生成锌酸盐。还能溶于氯化铵溶液。用作油漆颜料、橡胶填料、制
药、粘合剂、釉药、橡皮膏。由锌在空气中燃烧制得。
【硫酸锌】常见的是七水合硫酸锌ZnSO4·7H2O,俗称皓矾,式量287.54。无色晶体,密
度 1.957克/厘米3,熔点100℃,易溶于水。280℃时失去结晶水成无水物(白色固体)。
600℃时分解成氧化锌。溶于水,水溶液显酸性。用作媒染剂、收敛剂、杀菌剂、木材防
腐剂、纸张漂白剂、饲料填加剂、镀锌、治疗缺锌的药剂。由锌与稀硫酸反应制得。
【氯化锌】化学式 ZnCl,式量136.28。白色固体,密度2.91克/厘米3,熔点283℃,沸
点732℃。易潮解,易溶于水。高温时浓的氯化锌溶液有溶解金属氧化物的能力。用作媒
染剂、有抗合成的脱水剂和催化剂,牙科用作粘合剂,用于饲料添加剂。还用于镀锌、
制干电池、石油炼制、焊药水。用盐酸溶解锌或氧化锌制得,经干燥脱水得无水物。【氢氧化锌】化学式Zn(OH)2,式量99.38。无色斜方晶体。密度3.053克/厘米3,难溶
于水。125℃时分解为氧化锌和水。是两性氢氧化物。溶于强酸生成锌盐。溶于强碱生成
锌酸盐。和氢氧化铝不同,能溶于氨水中生成锌氨络离子:
Zn(OH)2+4NH3=[Zn(NH3)4]2++20H-
甭缋用作橡胶填加剂、外科药膏。由锌盐溶液加入适量强碱溶液制得。
【锌白】见氧化锌条。
【硫化锌】化学式ZnS,式量97.43。白色或微黄色粉末。α变体为无色六方晶体,密度
3.98克/厘米3,熔点1700±28℃(202.66千帕——20大气压);β变体为无色立方晶体,密
度4.102克/厘米3,于1020℃转化为α型。不溶于水、易溶于酸。见阳光色变暗。久置潮
湿空气中转变为硫酸锌。若在晶体ZnS中加入微量的Cu、Mn、Ag做活化剂,经光照后,
能发出不同颜色的荧光。用作分析试剂、涂料、制油漆、白色和不透明玻璃,充填橡胶、
塑料,以及用于制备荧光粉。由硫跟锌共热制得。
【磷化锌】化学式Zn3P2,式量258.08。深灰色四方晶体。有恶臭。密度 4.55克/厘米
3,熔点高于420℃。干燥时较稳定。在空气中易吸水分解,放出剧毒的磷化氢气体。不
溶于醇,可溶于酸。跟水反应可生成磷化氢和联膦P2H4的混和物,这混和物在空气中能
自燃。用作杀鼠剂,也可用作海上照明灯。由锌粉跟红磷在500~600℃时反应制得。
【硝酸锌】化学式Zn(NO3)2·6H2O,式量297.47。无色晶体。易潮解,易溶于水和乙醇,
水溶液显酸性。36.4℃熔于结晶水。105℃时失去结晶水。有氧化性,与有机物摩擦或撞
击能引起燃烧或爆炸。用作分析试剂和制药。将氧化锌溶于硝酸制得。
【锌钡白】俗称立德粉。是硫化锌跟硫酸钡的混合晶体。是一种优良的白色颜料。由硫
酸锌溶液跟硫化钡溶液混合制得:
ZnSO4(溶液)+BaS(溶液)=ZnS·BaSO4↓
【皓矾】见硫酸锌条。