文档内容
微专题突破15 化学计算考点透视二
一、选择题
1.(2024·江苏省南通市、盐城市二模)向某二价金属M的M(OH) 的溶液中加入过量的NaHCO
2 3
溶液,生成了MCO 沉淀,过滤,洗涤、干燥后将沉淀置于足量的稀盐酸中,充分反应后,在标准状况下
3
收集到V L气体。如要计算金属M的相对原子质量,你认为还必需提供下列哪项数据
A.M(OH) 溶液的物质的量浓度
2
B.与MCO 反应的盐酸的物质的量浓度
3
C.MCO 的质量
3
D.题给条件充足,不需要再补充数据
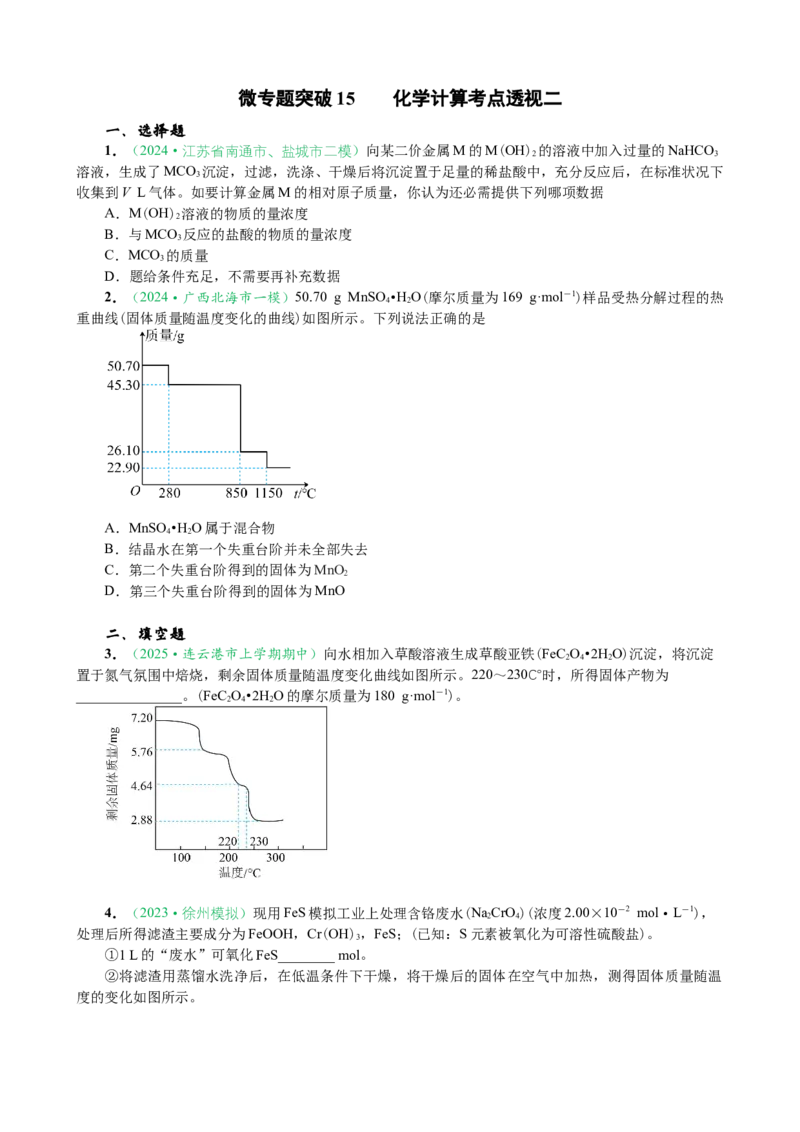
2.(2024·广西北海市一模)50.70 g MnSO •HO(摩尔质量为169 g·mol-1)样品受热分解过程的热
4 2
重曲线(固体质量随温度变化的曲线)如图所示。下列说法正确的是
A.MnSO •HO属于混合物
4 2
B.结晶水在第一个失重台阶并未全部失去
C.第二个失重台阶得到的固体为MnO
2
D.第三个失重台阶得到的固体为MnO
二、填空题
3.(2025·连云港市上学期期中)向水相加入草酸溶液生成草酸亚铁(FeC O•2HO)沉淀,将沉淀
2 4 2
置于氮气氛围中焙烧,剩余固体质量随温度变化曲线如图所示。220~230℃时,所得固体产物为
_______________。(FeC O•2HO的摩尔质量为180 g·mol-1)。
2 4 2
4.(2023·徐州模拟)现用FeS模拟工业上处理含铬废水(NaCrO)(浓度2.00×10-2 mol·L-1),
2 4
处理后所得滤渣主要成分为FeOOH,Cr(OH),FeS;(已知:S元素被氧化为可溶性硫酸盐)。
3
①1 L的“废水”可氧化FeS________ mol。
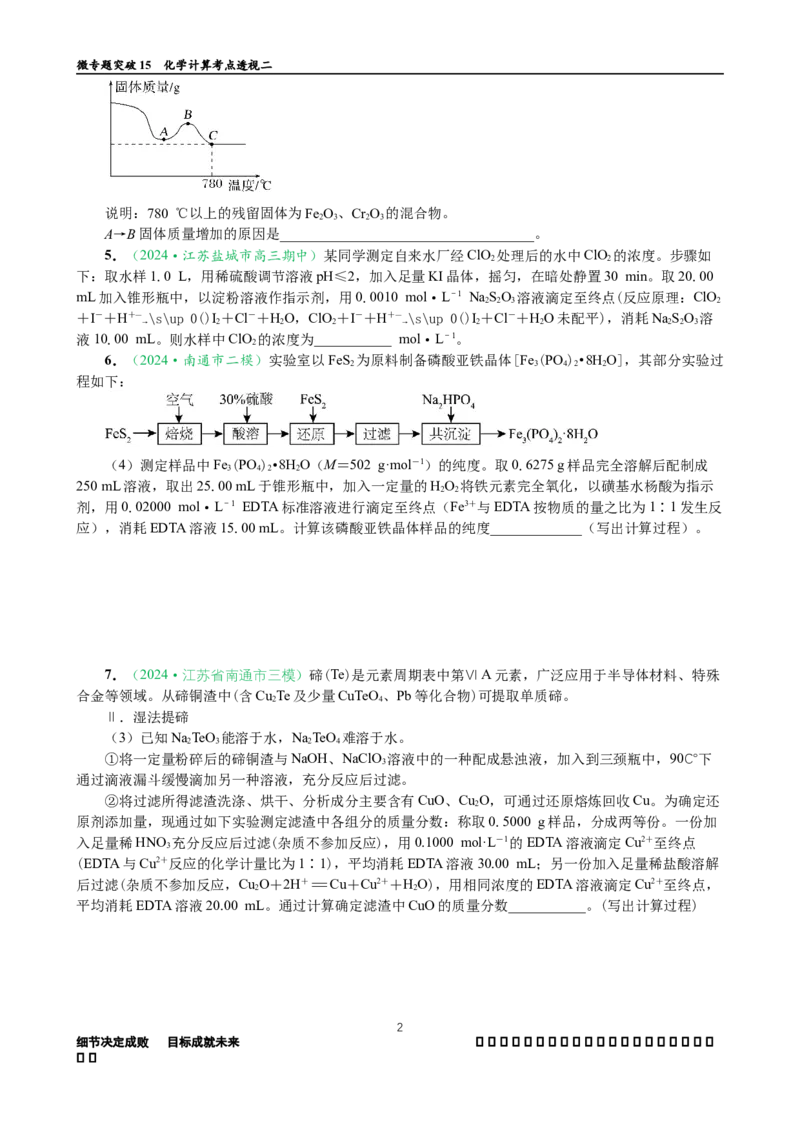
②将滤渣用蒸馏水洗净后,在低温条件下干燥,将干燥后的固体在空气中加热,测得固体质量随温
度的变化如图所示。微专题突破15 化学计算考点透视二
说明:780 ℃以上的残留固体为Fe O、Cr O 的混合物。
2 3 2 3
A→B固体质量增加的原因是____________________________________。
5.(2024·江苏盐城市高三期中)某同学测定自来水厂经ClO 处理后的水中ClO 的浓度。步骤如
2 2
下:取水样1.0 L,用稀硫酸调节溶液pH≤2,加入足量KI晶体,摇匀,在暗处静置30 min。取20.00
mL加入锥形瓶中,以淀粉溶液作指示剂,用0.0010 mol·L-1 NaSO 溶液滴定至终点(反应原理:ClO
2 2 3 2
+I-+H+— \s\up 0()I+Cl-+HO,ClO+I-+H+— \s\up 0()I+Cl-+HO未配平),消耗NaSO 溶
→ 2 2 2 → 2 2 2 2 3
液10.00 mL。则水样中ClO 的浓度为___________ mol·L-1。
2
6.(2024·南通市二模)实验室以FeS 为原料制备磷酸亚铁晶体[Fe (PO )•8HO],其部分实验过
2 3 4 2 2
程如下:
(4)测定样品中Fe (PO )•8HO(M=502 g·mol-1)的纯度。取0.6275 g样品完全溶解后配制成
3 4 2 2
250 mL溶液,取出25.00 mL于锥形瓶中,加入一定量的HO 将铁元素完全氧化,以磺基水杨酸为指示
2 2
剂,用0.02000 mol·L-1 EDTA标准溶液进行滴定至终点(Fe3+与EDTA按物质的量之比为1∶1发生反
应),消耗EDTA溶液15.00 mL。计算该磷酸亚铁晶体样品的纯度_____________(写出计算过程)。
7.(2024·江苏省南通市三模)碲(Te)是元素周期表中第ⅥA元素,广泛应用于半导体材料、特殊
合金等领域。从碲铜渣中(含Cu Te及少量CuTeO 、Pb等化合物)可提取单质碲。
2 4
Ⅱ.湿法提碲
(3)已知NaTeO 能溶于水,NaTeO 难溶于水。
2 3 2 4
①将一定量粉碎后的碲铜渣与NaOH、NaClO 溶液中的一种配成悬浊液,加入到三颈瓶中,90℃下
3
通过滴液漏斗缓慢滴加另一种溶液,充分反应后过滤。
②将过滤所得滤渣洗涤、烘干、分析成分主要含有CuO、Cu O,可通过还原熔炼回收Cu。为确定还
2
原剂添加量,现通过如下实验测定滤渣中各组分的质量分数:称取0.5000 g样品,分成两等份。一份加
入足量稀HNO 充分反应后过滤(杂质不参加反应),用0.1000 mol·L-1的EDTA溶液滴定Cu2+至终点
3
(EDTA与Cu2+反应的化学计量比为1∶1),平均消耗EDTA溶液30.00 mL;另一份加入足量稀盐酸溶解
后过滤(杂质不参加反应,Cu O+2H+=Cu+Cu2++HO),用相同浓度的EDTA溶液滴定Cu2+至终点,
2 2
平均消耗EDTA溶液20.00 mL。通过计算确定滤渣中CuO的质量分数___________。(写出计算过程)
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找8.(2023·南京模拟)纳米氧化锌是一种新型无机功能材料。以氧化锌烟灰(含ZnO及少量Fe O、
2 3
FeO、MnO、CuO)为原料制备纳米氧化锌的工艺流程如图:
如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算)。
金属离子 Fe3+ Fe2+ Cu2+ Zn2+ Mn2+
开始沉淀的pH 1.5 6.3 6.0 6.2 8.1
完全沉淀的pH 2.8 8.3 8.0 8.2 10.1
(1)“浸取”过程中盐酸不宜过量太多,其可能原因是
_________________________________________________________。
(2)“滤渣1”的成分是MnO 、Fe(OH) 。“氧化除杂”过程中KMnO 与Mn2+发生反应的离子方
2 3 4
程式为_______________________________________________,溶液pH范围应控制在________________。
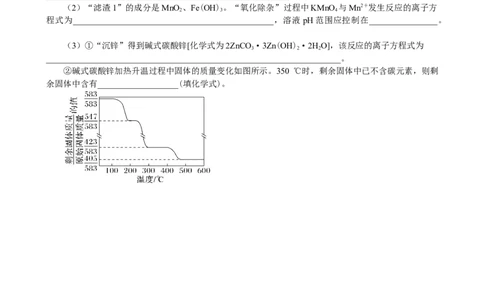
(3)①“沉锌”得到碱式碳酸锌[化学式为2ZnCO ·3Zn(OH)·2HO],该反应的离子方程式为
3 2 2
_____________________________________________________________________。
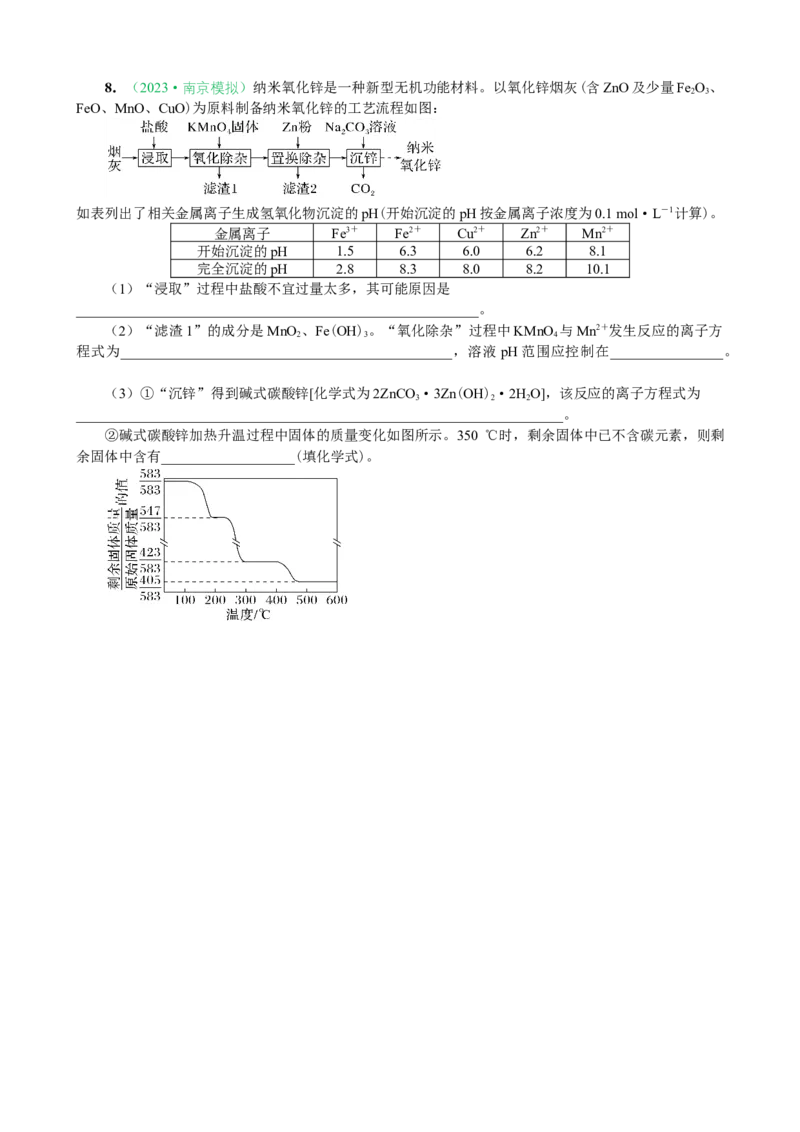
②碱式碳酸锌加热升温过程中固体的质量变化如图所示。350 ℃时,剩余固体中已不含碳元素,则剩
余固体中含有___________________(填化学式)。