文档内容
易错专题 09 反应热的表示与计算
聚焦易错点:
►易错点一 热化学方程式的书写
►易错点二 反应热的计算
典例精讲
易错点一 热化学方程式的书写
【易错典例】
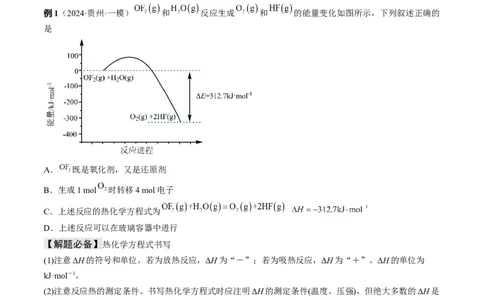
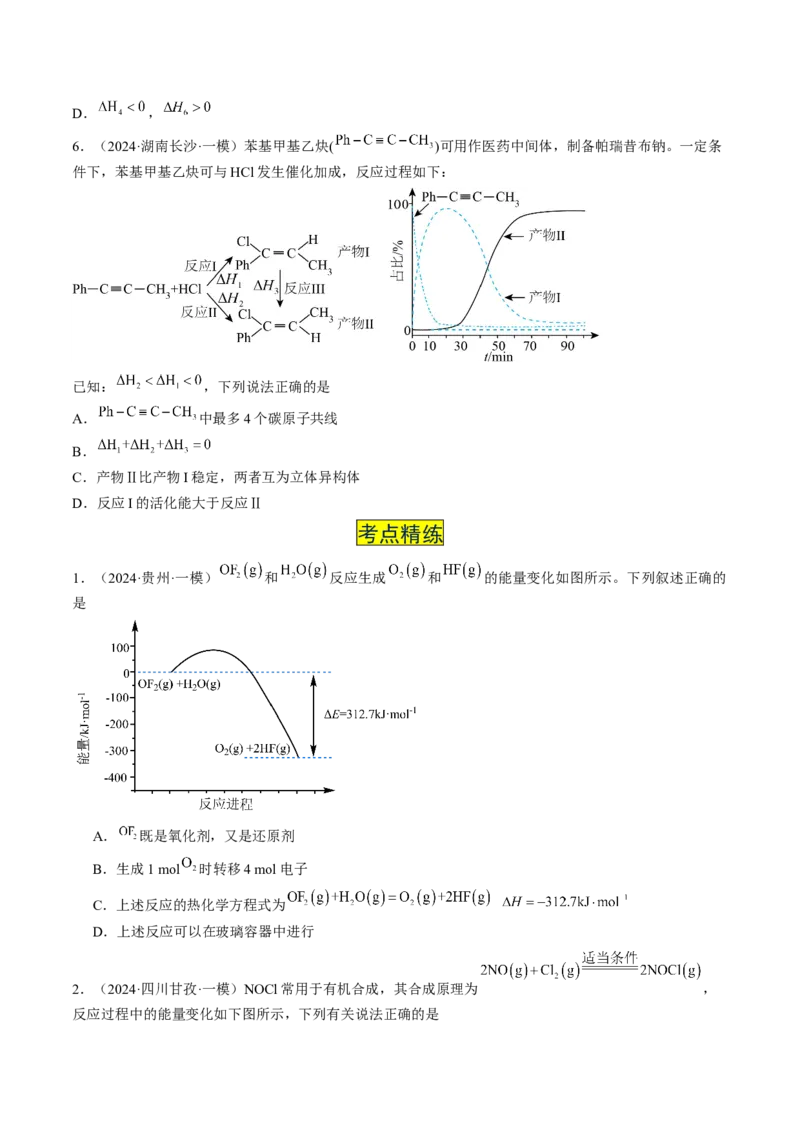
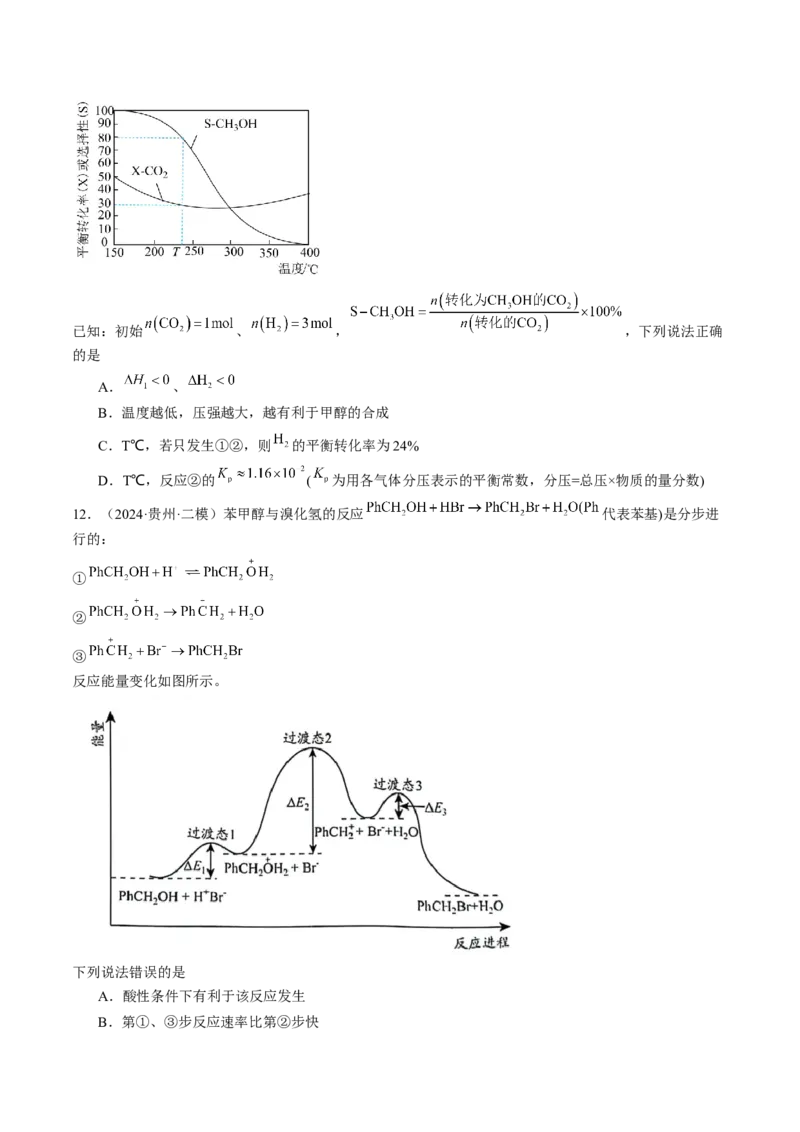
例1(2024·贵州·一模) 和 反应生成 和 的能量变化如图所示,下列叙述正确的
是
A. 既是氧化剂,又是还原剂
B.生成1 mol 时转移4 mol电子
C.上述反应的热化学方程式为
D.上述反应可以在玻璃容器中进行
【解题必备】热化学方程式书写
(1)注意ΔH的符号和单位。若为放热反应,ΔH为“-”;若为吸热反应,ΔH为“+”。ΔH的单位为
kJ·mol-1。
(2)注意反应热的测定条件。书写热化学方程式时应注明ΔH的测定条件(温度、压强),但绝大多数的ΔH是
在25 ℃、101 kPa下测定的,此时可不注明温度和压强。
(3)注意热化学方程式中的化学计量数。热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物
质的量,并不表示物质的分子数或原子数,因此化学计量数可以是整数,也可以是分数。
(4)注意物质的聚集状态。反应物和生成物的聚集状态不同,反应热ΔH不同。因此,必须注明物质的聚集
状态才能完整地体现出热化学方程式的意义。气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。热化
学方程式中不用“↑”和“↓”。
(5)注意ΔH的数值与符号。热化学方程式中的ΔH的值应是表示反应已完成的热量变化。由于ΔH与反应
完成的物质的量有关,所以热化学方程式中化学式前面的化学计量数必须与ΔH相对应,如果化学计量数
加倍,则ΔH也要加倍。逆反应的反应热与正反应的反应热数值相等,但符号相反。(6)注意燃烧热和中和热。燃烧热是指在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热
量,中和热是指在稀溶液中,强酸跟强碱发生中和反应生成1 mol液态HO时的反应热。
2
【变式突破】
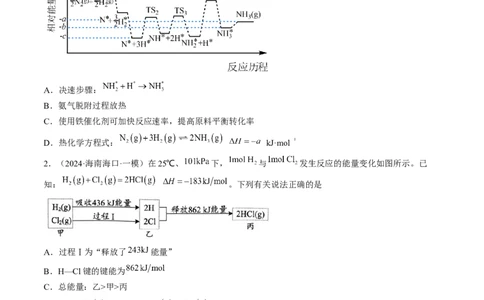
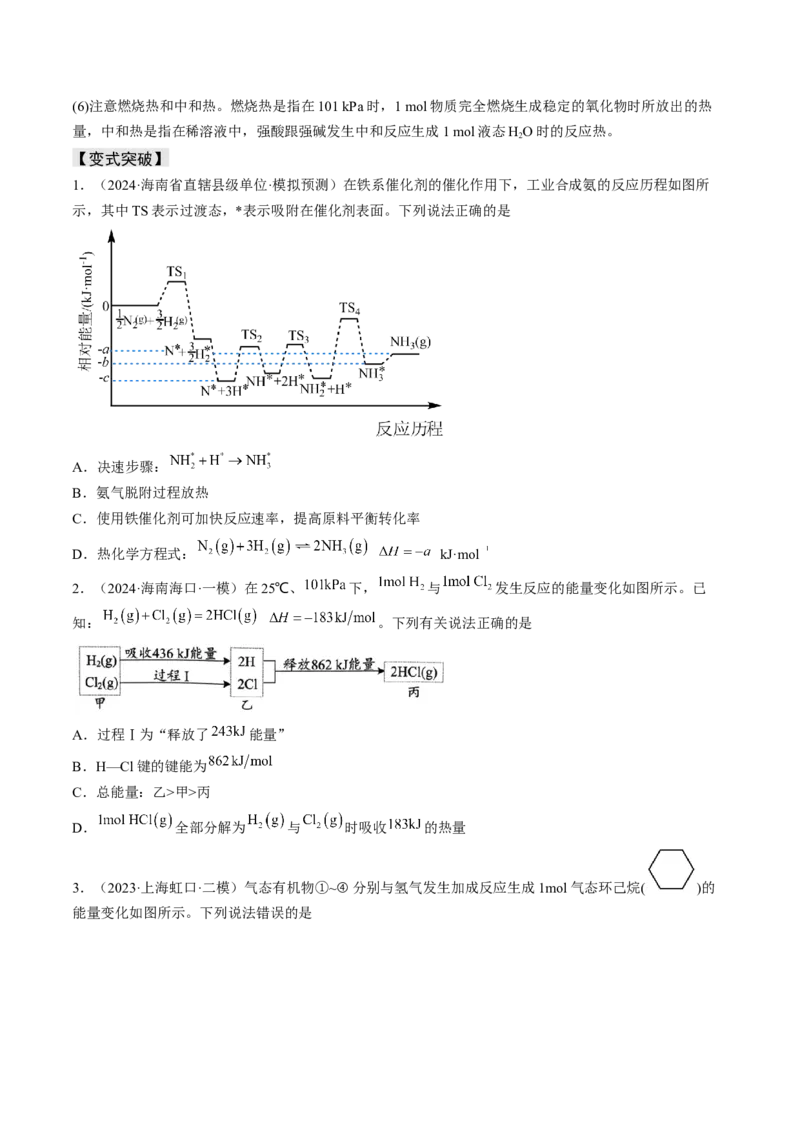
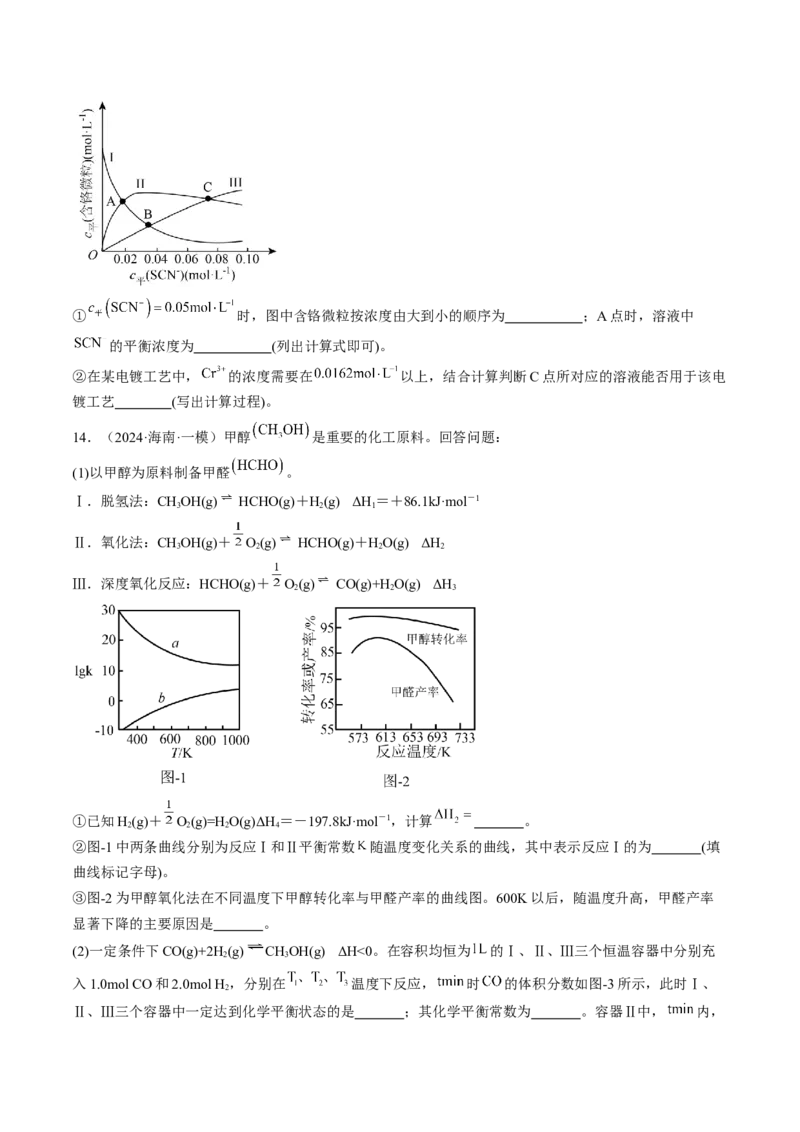
1.(2024·海南省直辖县级单位·模拟预测)在铁系催化剂的催化作用下,工业合成氨的反应历程如图所
示,其中TS表示过渡态,*表示吸附在催化剂表面。下列说法正确的是
A.决速步骤:
B.氨气脱附过程放热
C.使用铁催化剂可加快反应速率,提高原料平衡转化率
D.热化学方程式: kJ·mol
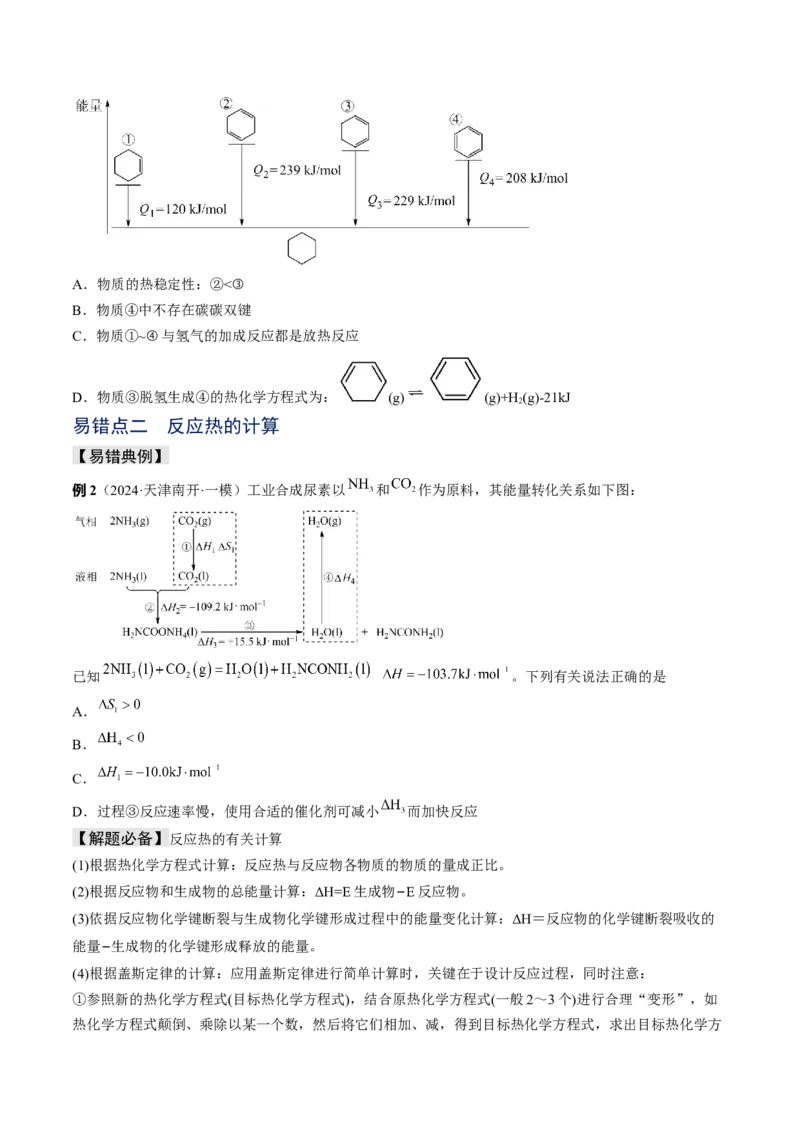
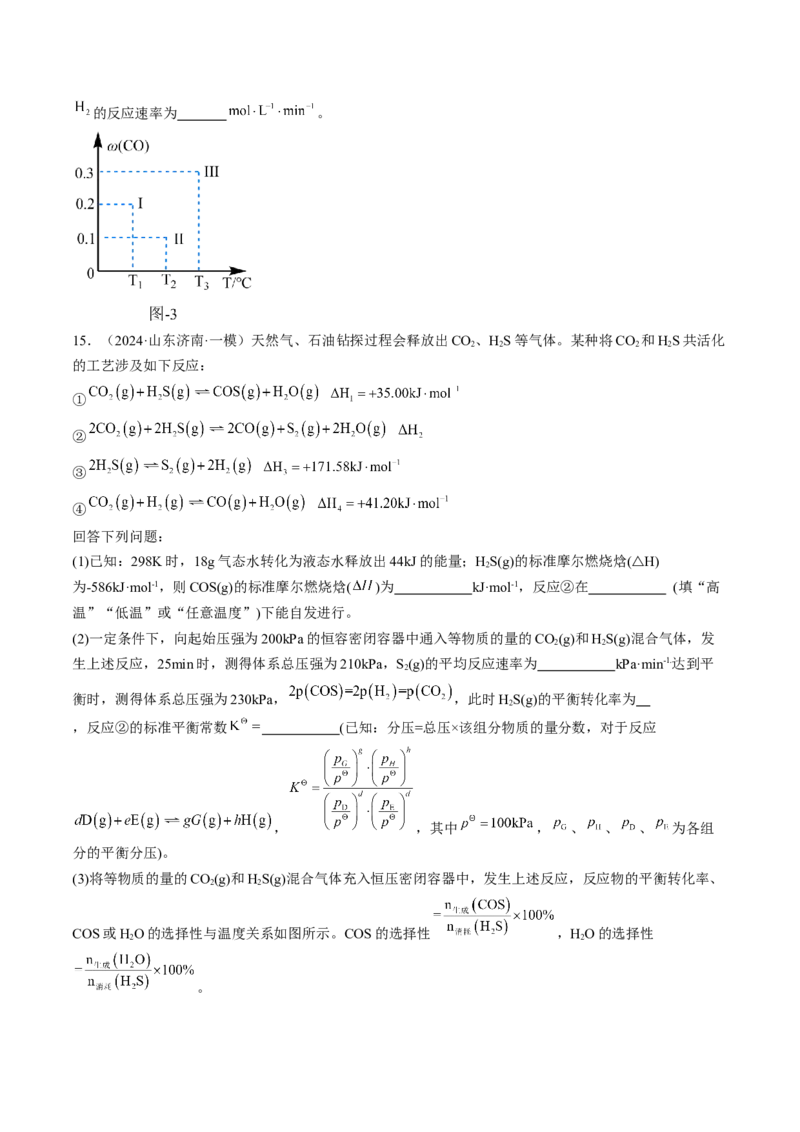
2.(2024·海南海口·一模)在25℃、 下, 与 发生反应的能量变化如图所示。已
知: 。下列有关说法正确的是
A.过程Ⅰ为“释放了 能量”
B.H—Cl键的键能为
C.总能量:乙>甲>丙
D. 全部分解为 与 时吸收 的热量
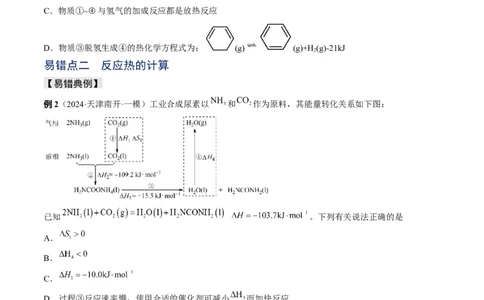
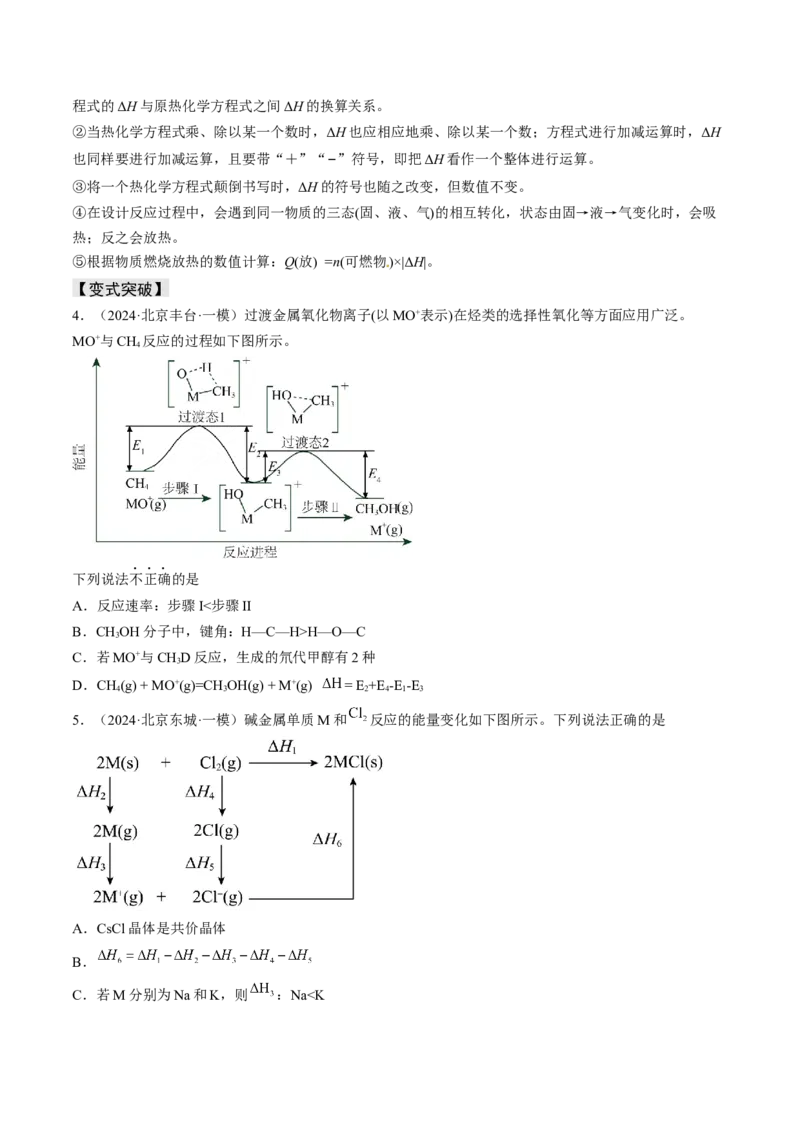
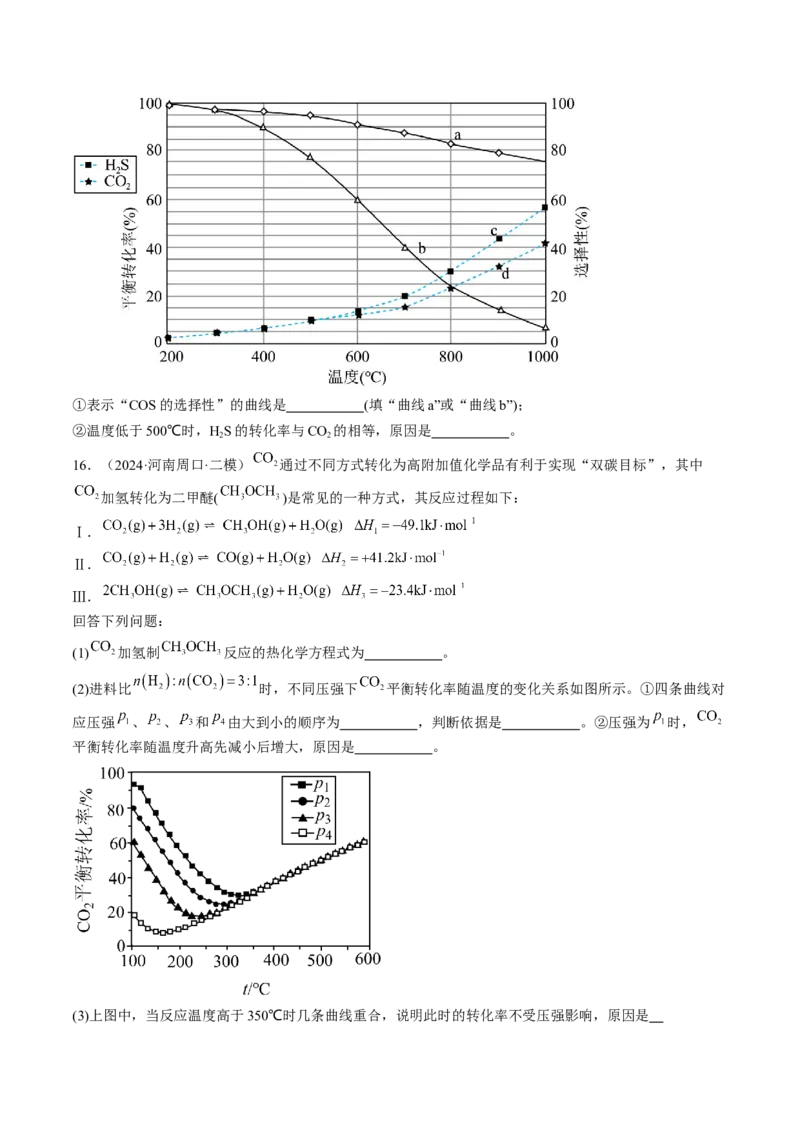
3.(2023·上海虹口·二模)气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷( )的
能量变化如图所示。下列说法错误的是A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应
D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
易错点二 反应热的计算
【易错典例】
例2(2024·天津南开·一模)工业合成尿素以 和 作为原料,其能量转化关系如下图:
已知 。下列有关说法正确的是
A.
B.
C.
D.过程③反应速率慢,使用合适的催化剂可减小 而加快反应
【解题必备】反应热的有关计算
(1)根据热化学方程式计算:反应热与反应物各物质的物质的量成正比。
(2)根据反应物和生成物的总能量计算:ΔH=E生成物−E反应物。
(3)依据反应物化学键断裂与生成物化学键形成过程中的能量变化计算:ΔH=反应物的化学键断裂吸收的
能量−生成物的化学键形成释放的能量。
(4)根据盖斯定律的计算:应用盖斯定律进行简单计算时,关键在于设计反应过程,同时注意:
①参照新的热化学方程式(目标热化学方程式),结合原热化学方程式(一般2~3个)进行合理“变形”,如
热化学方程式颠倒、乘除以某一个数,然后将它们相加、减,得到目标热化学方程式,求出目标热化学方程式的ΔH与原热化学方程式之间ΔH的换算关系。
②当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH
也同样要进行加减运算,且要带“+”“−”符号,即把ΔH看作一个整体进行运算。
③将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
④在设计反应过程中,会遇到同一物质的三态(固、液、气)的相互转化,状态由固→液→气变化时,会吸
热;反之会放热。
⑤根据物质燃烧放热的数值计算:Q(放) =n(可燃物)×|ΔH|。
【变式突破】
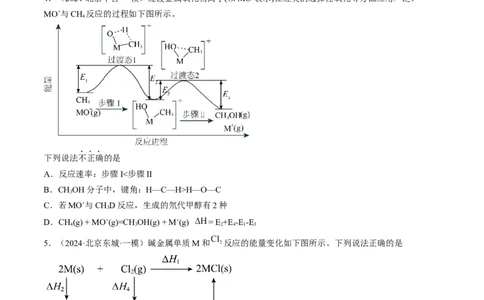
4.(2024·北京丰台·一模)过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。
MO+与CH 反应的过程如下图所示。
4
下列说法不正确的是
A.反应速率:步骤I<步骤II
B.CHOH分子中,键角:H—C—H>H—O—C
3
C.若MO+与CHD反应,生成的氘代甲醇有2种
3
D.CH(g) + MO+(g)=CH OH(g) + M+(g) = E +E-E -E
4 3 2 4 1 3
5.(2024·北京东城·一模)碱金属单质M和 反应的能量变化如下图所示。下列说法正确的是
A.CsCl晶体是共价晶体
B.
C.若M分别为Na和K,则 :Na