文档内容
易错点 5 钠及其化合物易错点
易错题【01】钠与水、乙醇及酸、碱、盐溶液的反应规律
(1)钠与水、酸、盐溶液反应的本质与顺序:本质上均是与H+的反应,反应顺序是:有
酸酸在前,无酸水为先。
(2)钠与乙醇反应的特点——“慢、沉”:钠与乙醇反应时,钠的密度大于水,钠块先沉
在液面下,后上下浮动、能看到表面冒出气泡,并不能熔化成小球。
(3)钠与酸反应的特点——“快,浮”:钠与酸反应时,由于c(H+)较大,反应较迅速,
可能燃烧或爆炸。
(4)钠投入碱溶液中,钠与水反应生成NaOH和H,再考虑反应生成NaOH对碱溶液的
2
影响
易错题【02】Na O 与CO 、HO(g)反应的“四大规律”
2 2 2 2
从反应结果看,NaO 与CO、HO(g)的混合气体反应时,可看作NaO 先
先后规律 2 2 2 2 2 2
与CO 反应,后与HO(g)反应
2 2
当NaO 与CO、HO(g)反应时,物质的量关系为2NaO~O ~2e-,
2 2 2 2 2 2 2
电子转移 1
n(e-)=n(Na O)= n(O )
2 2 2 2
若CO、HO(g)(或二者的混合气体)通过足量NaO,气体体积的减少量是
2 2 2 2
体积变化 1 1
原来气体体积的 ,等于生成氧气的量,ΔV=V(O )= V(混合)
2 2 2
CO、HO(g)分别与足量NaO 反应时,固体相当于吸收了CO 中的“CO”
2 2 2 2 2
质量变化 和HO(g)中的“H”,故固体增加的质量Δm(CO)=28 g/mol×n(CO),
2 2 2 2
Δm(H O)=2 g/mol×n(H O)
2 2
易错题【03】Na CO 和NaHCO 的实验设计
2 3 3
NaCO NaHCO
2 3 3
俗名 纯碱、苏打 小苏打
颜色状态 白色粉末 白色晶体
溶解性 易溶于水 易溶于水(溶解度比NaCO 小)
2 3
与足量盐酸反应 CO + 2H + == =CO ↑ + H O HCO + H + == = H O + CO ↑
2 2 2 2
与NaOH反应 HCO + OH == =CO + H O -
2
与足量Ca(OH) Ca 2 + + OH - + HCO == =
2
Ca2++CO===CaCO ↓
3
溶液反应 CaCO ↓ + H O
3 2
与CO 反应 CO + CO + H O == =2HCO
2 2 2
2NaHCO =====NaCO+CO↑
3 2 3 2
热稳定性 较稳定,不易分解
+HO
2
用途 重要的化工原料 焙制糕点、治疗胃酸过多
相互转化1.Na CO 和NaHCO 的鉴别方法
2 3 3
[易错警示] 不可用Ca(OH) 溶液鉴别NaCO 溶液和NaHCO 溶液,因为Ca(OH) 溶液与
2 2 3 3 2
这两种溶液反应时都产生白色沉淀,现象相同。
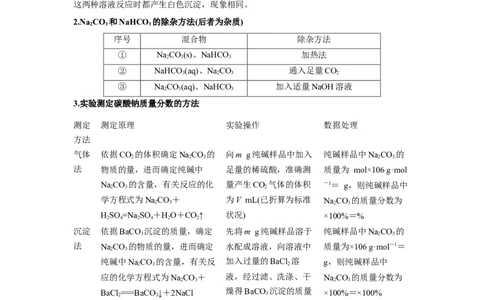
2.Na CO 和NaHCO 的除杂方法(后者为杂质)
2 3 3
序号 混合物 除杂方法
① NaCO(s)、NaHCO 加热法
2 3 3
② NaHCO (aq)、NaCO 通入足量CO
3 2 3 2
③ NaCO(aq)、NaHCO 加入适量NaOH溶液
2 3 3
3.实验测定碳酸钠质量分数的方法
测定 测定原理 实验操作 数据处理
方法
气体 依据CO 的体积确定NaCO 的 向m g纯碱样品中加入 纯碱样品中NaCO 的
2 2 3 2 3
法 物质的量,进而确定纯碱中 足量的稀硫酸,准确测 质量为 mol×106 g·mol
NaCO 的含量,有关反应的化 量产生CO 气体的体积 -1= g,则纯碱样品中
2 3 2
学方程式为NaCO+ 为V mL(已折算为标准 NaCO 的质量分数为
2 3 2 3
HSO =NaSO +HO+CO↑ 状况) ×100%=%
2 4 2 4 2 2
沉淀 依据BaCO 沉淀的质量,确定 先将m g纯碱样品溶于 纯碱样品中NaCO 的
3 2 3
法 NaCO 的物质的量,进而确定 水配成溶液,向溶液中 质量为×106 g·mol-1=
2 3
纯碱中NaCO 的含量,有关反 加入过量的BaCl 溶 g,则纯碱样品中
2 3 2
应的化学方程式为NaCO+ 液,经过滤、洗涤、干 NaCO 的质量分数为
2 3 2 3
BaCl 2 ===BaCO 3 ↓+2NaCl 燥得BaCO 3 沉淀的质量 ×100%=×100%
为n g
利用“双指示剂法”(酚酞-甲 第一步使用酚酞作指示 n(NaHCO )=c(HCl)×(V
3 2
基橙)测定NaCO 和NaHCO 剂,消耗标准盐酸(V
2 3 3 1 -V)×10—3 mol,
混合物中NaCO 的质量分数, mL)用于物质转化: 1
2 3
有关反应的化学方程式为 Na 2 CO 3 →NaHCO 3 ,滴 m(NaHCO 3 )=c(HCl)×(V 2
NaCO+HCl=NaHCO +NaCl、 定终点现象是:溶液由
滴定 2 3 3 -V)×10—3 mol×84
浅红色变为无色;第二 1
法 NaHCO +HCl=NaCl+H O+CO↑ 步使用甲基橙作指示 g/mol
3 2 2
剂,滴定原理:,消耗
标准盐酸(V mL)用
2
于物质转化:
NaHCO →NaCl,滴定
3终点现象是:溶液由黄
色变为橙色
典例分析
例1、某同学想通过下图装置实验,探究SO 与NaO 反应的产物。
2 2 2
Ⅰ、检验反应中是否有O 生成的方法是___________________________________;若有O
2 2
生成,请写出装置C中的化学方程式____________。
Ⅱ、A中盛装HSO 溶液的仪器名称是________;D装置除起了防止空气中的水蒸气和二
2 4
氧化碳进入C装置与NaO 反应作用外,还可以________________________________。
2 2
Ⅲ、(1)C中固体产物可能只有NaSO 、只有________、NaSO 和NaSO 两种都有。
2 3 2 3 2 4
(2)若NaO 反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选试剂
2 2
和仪器帮助他完成该探究过程。
限选试剂和仪器:0.1 mol·L-1 KMnO 酸性溶液、0.01 mol·L-1 KMnO 酸性溶液、0.1
4 4
mol·L-1 Ba(NO ) 溶液、0.1 mol·L-1 BaCl 、1 mol·L-1 HNO 溶液、1 mol·L-1盐酸、试管、
3 2 2 3
胶头滴管。
实验操作 预期现象和结论
步骤一:取少量C中固体产物于试管中, 固体完全溶解,得到无色透明溶液
加入适量的蒸馏水、搅拌溶解,分别取少
量于A、B试管中
步骤二:取试管 A,向溶液中加入 若________;则________
________,振荡,观察溶液颜色变化
步骤三:取试管 B,向其中先加入 产生________再加入另一试剂看到产生白色
________,振荡;再加入________,振荡 沉淀,则固体C中还含有________
【解析】NaO 完全反应后的产物有三种情况,只有 NaSO 、只有 NaSO 、NaSO 与
2 2 2 3 2 4 2 3
NaSO 的混合物,当产物溶解后,溶液中加入几滴KMnO 酸性溶液,溶液紫色若褪去,
2 4 4
说明有NaSO (它有还原性),但检验不出 NaSO ;若溶液紫色不褪去,说明 C中没有
2 3 2 4
NaSO ,只有NaSO 。检验NaSO 可先加入盐酸,再加入BaCl 溶液。
2 3 2 4 2 4 2
【答案】Ⅰ.用带火星的木条靠近干燥管口 a,观察木条是否复燃 2SO +
2
2NaO===2Na SO +OⅡ.分液漏斗 吸收过量(或多余)的SO ,以免污染空气(或保护环
2 2 2 3 2 2
境)Ⅲ.(1)Na SO (2)几滴(少量)0.01 mol·L-1KMnO 酸性溶液、紫红色的KMnO 溶液振荡后
2 4 4 4
褪色、C中含有NaSO 、过量的1 mol·L-1盐酸、适量0.1mol·L-1BaCl 溶液、无色刺激性
2 3 2气味气体、NaSO
2 4
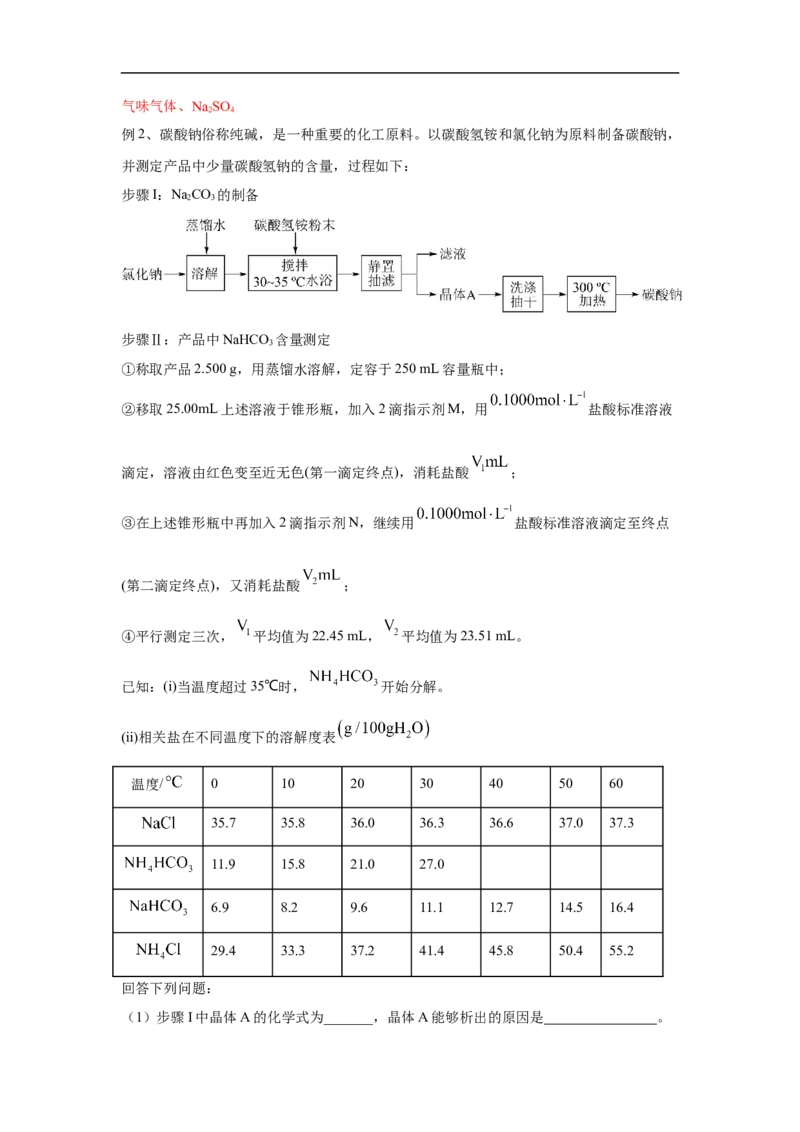
例2、碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,
并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I:NaCO 的制备
2 3
步骤Ⅱ:产品中NaHCO 含量测定
3
①称取产品2.500 g,用蒸馏水溶解,定容于250 mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液
滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点
(第二滴定终点),又消耗盐酸 ;
④平行测定三次, 平均值为22.45 mL, 平均值为23.51 mL。
已知:(i)当温度超过35℃时, 开始分解。
(ii)相关盐在不同温度下的溶解度表
温度/ 0 10 20 30 40 50 60
35.7 35.8 36.0 36.3 36.6 37.0 37.3
11.9 15.8 21.0 27.0
6.9 8.2 9.6 11.1 12.7 14.5 16.4
29.4 33.3 37.2 41.4 45.8 50.4 55.2
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是 。(2)步骤I中“300℃加热”所选用的仪器是 (填标号)。
A. B. C. D.
(3)指示剂N为 ,描述第二滴定终点前后颜色变化 。
(4)产品中NaHCO 的质量分数为 (保留三位有效数字)。
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO 质量分数的计算结
3
果_______(填“偏大”“偏小”或“无影响”)。
【解析】(1)根据题给信息中盐在不同温度下的溶解度看出,控制温度在30~35 C,目的
是为了时NH HCO 不发生分解,同时析出NaHCO 固体,得到晶体A,因为在30~35 C时,
4 3 3
NaHCO 的溶解度最小。
3
(3)第二次滴定时,使用的指示剂N为甲基橙试液,滴定到终点前溶液的溶质为碳酸氢
钠和氯化钠,滴定达到终点后溶液的溶质为氯化钠,故溶液的颜色变化为:由黄色变为橙
色,且半分钟内不褪色。
(4)第一次滴定发生反应:NaCO+HCl=NaHCO +NaCl,则n(Na CO)=n (NaHCO )
2 3 3 2 3 生成 3
=n(HCl)=0.1000mol/L 22.45 10-3L=2.245 10-3mol。第二次滴定消耗的盐酸的体积
V=23.51mL,则根据方程式NaHCO +HCl=NaCl+H O+CO↑可知,消耗的NaHCO 的物质
2 3 2 2 3
的量n (NaHCO )= 0.1000mol/L 23.51 10-3L=2.351 10-3mol,则原溶液中的NaHCO 的物
总 3 3
质的量n(NaHCO )= n (NaHCO )- n (NaHCO )= 2.351 10-3mol-2.245 10-3mol=
3 总 3 生成 3
1.06 10-4mol,则原产品中NaHCO 的物质的量为 =1.06 10-3mol,故
3
产品中NaHCO 的质量分数为 。
3
(5)第一次滴定时,其他操作均正确的情况下,俯视读数,则会使标准液盐酸的体积偏小,
即测得V 偏小,所以原产品中NaHCO 的物质的量会偏大,最终导致其质量分数会偏大。
1 3
【答案】(1) NaHCO 在30~35℃时NaHCO 的溶解度最小(其他合理答案均可)
3 3
(2)D
(3)甲基橙 由黄色变橙色,且半分钟内不褪色
(4)3.56%(5)偏大
例3、某含NaCl、NaCO·10H O和NaHCO 的混合物,某同学设计如图所示的实验装置,
2 3 2 3
通过测量反应产生的CO 和HO的质量,来确定该混合物中各组分的质量分数。
2 2
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_____________________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U
形管D的质量。
③打开活塞K、K,关闭K,缓缓鼓入空气数分钟,其目的是____________________。
1 2 3
④关闭活塞K、K,打开K,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学
1 2 3
方程式为______________________、____________________。
⑤打开活塞K,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质
1
量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是__________________________。
②E处干燥管中盛放的药品是________,其作用是________________________________,
如果实验中没有该装置,则会导致测得的NaHCO 的质量________(填“偏大”“偏小”或
3
“无影响”)。
③若样品质量为 w g,反应后C、D装置增加的质量分别为 m g、m g,则混合物中
1 2
NaCO·10H O的质量分数为______________(用含w、m、m 的代数式表示)。
2 3 2 1 2
【解析】(1)①组装好实验装置后首先应检查装置的气密性。
③由于装置中存在CO 和水蒸气,应先除去装置中的CO 和水蒸气。
2 2
④由物质的性质可知,在加热时该装置中发生的反应为 2NaHCO =====NaCO +HO↑+
3 2 3 2
CO↑、NaCO·10H O=====NaCO+10HO↑。
2 2 3 2 2 3 2
(2)①加热后有部分CO 和水蒸气会残留在装置中,必须鼓入空气使其完全被吸收,若不
2
鼓入空气,则测得的NaHCO 和NaCO·10H O的质量分数会偏小,NaCl的质量分数会偏
3 2 3 2
大。
②装置E是防止空气中的CO 和水蒸气进入装置D,故干燥管中盛放的药品是碱石灰,如
2
果没有该装置,会使测得的NaHCO 的质量偏大。
3
③由题 目信息知 反应 放出的 CO 的质量为 m g ,根据反应的化学方程式
2 2
2NaHCO =====NaCO +HO↑+CO↑,可计算出该反应中产生的水的质量为 g,从而计算
3 2 3 2 2
出 NaCO·10H O 分解产生水的质量为(m -) g,再根据 NaCO·10H O=====NaCO +
2 3 2 1 2 3 2 2 310HO↑,计算出NaCO·10H O的质量,最后计算出混合物中NaCO·10H O的质量分数。
2 2 3 2 2 3 2
【答案】(1)①检查装置的气密性 ③除去装置中的水蒸气和二氧化碳
④2NaHCO =====NaCO+HO↑+CO↑ Na CO·10H O=====NaCO+10HO↑
3 2 3 2 2 2 3 2 2 3 2
(2)①NaCO·10H O和NaHCO 的质量分数测定结果偏小,NaCl的质量分数测定结果偏
2 3 2 3
大
②碱石灰 防止空气中的CO 和水蒸气进入D中影响测定结果 偏大
2
③ ×100%
1.钠和钾是两种常见金属,下列说法正确的是
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
2.下列有关物质的性质与用途具有对应关系的是
A.金属钠熔点较低,可用于冶炼金属钛
B.次氯酸钠具有强氧化性,可用作环境消毒剂
C.碳酸钠受热不易分解,可用于去清洗油污
D.碳酸氢钠溶液显碱性,可用作发酵剂
3.在烧杯中加水和苯(密度:0.88 g/cm3)各50 mL,将一小粒金属钠(密度:0.97 g/cm3)投入
烧杯中。观察到的现象可能是
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并做上下跳动
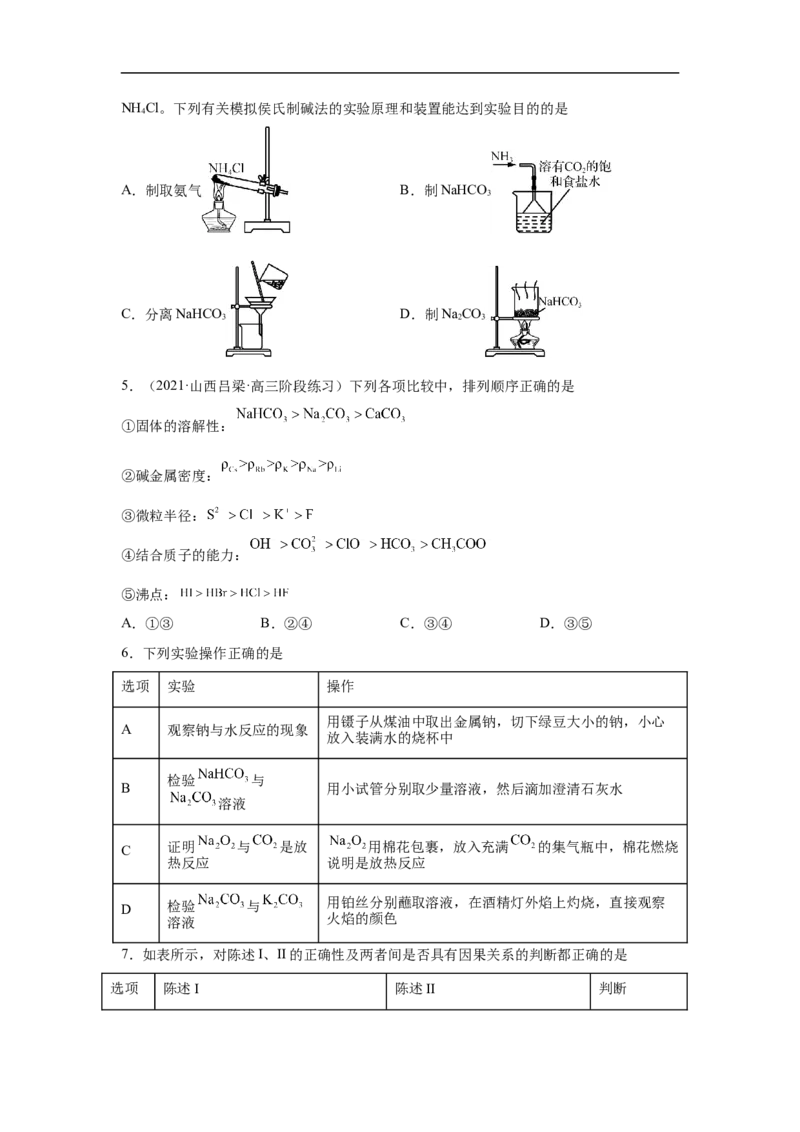
4.(2022·江苏苏州·模拟预测)侯氏制碱法原理为NaCl+NH +CO+HO=NaHCO ↓+
3 2 2 3NH Cl。下列有关模拟侯氏制碱法的实验原理和装置能达到实验目的的是
4
A.制取氨气 B.制NaHCO
3
C.分离NaHCO D.制NaCO
3 2 3
5.(2021·山西吕梁·高三阶段练习)下列各项比较中,排列顺序正确的是
①固体的溶解性:
②碱金属密度:
③微粒半径:
④结合质子的能力:
⑤沸点:
A.①③ B.②④ C.③④ D.③⑤
6.下列实验操作正确的是
选项 实验 操作
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心
A 观察钠与水反应的现象
放入装满水的烧杯中
检验 与
B 用小试管分别取少量溶液,然后滴加澄清石灰水
溶液
证明 与 是放 用棉花包裹,放入充满 的集气瓶中,棉花燃烧
C
热反应 说明是放热反应
检验 与 用铂丝分别蘸取溶液,在酒精灯外焰上灼烧,直接观察
D
溶液 火焰的颜色
7.如表所示,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是
选项 陈述I 陈述II 判断I对,II对,
A 碳酸钠溶液可用于治疗胃病 NaCO 可与盐酸反应
2 3 有
向滴有酚酞的水溶液中加入NaO I对,II错,
B 2 2 NaO 与水反应生成氢氧化钠
变红色 2 2 无
I对,II对,
C 金属钠具有强还原性 高压钠灯发出透雾性强的黄光
有
NaO 能与CO 和HO反应生 I对,II对,
D 过氧化钠可为航天员供氧 2 2 2 2
成O 有
2
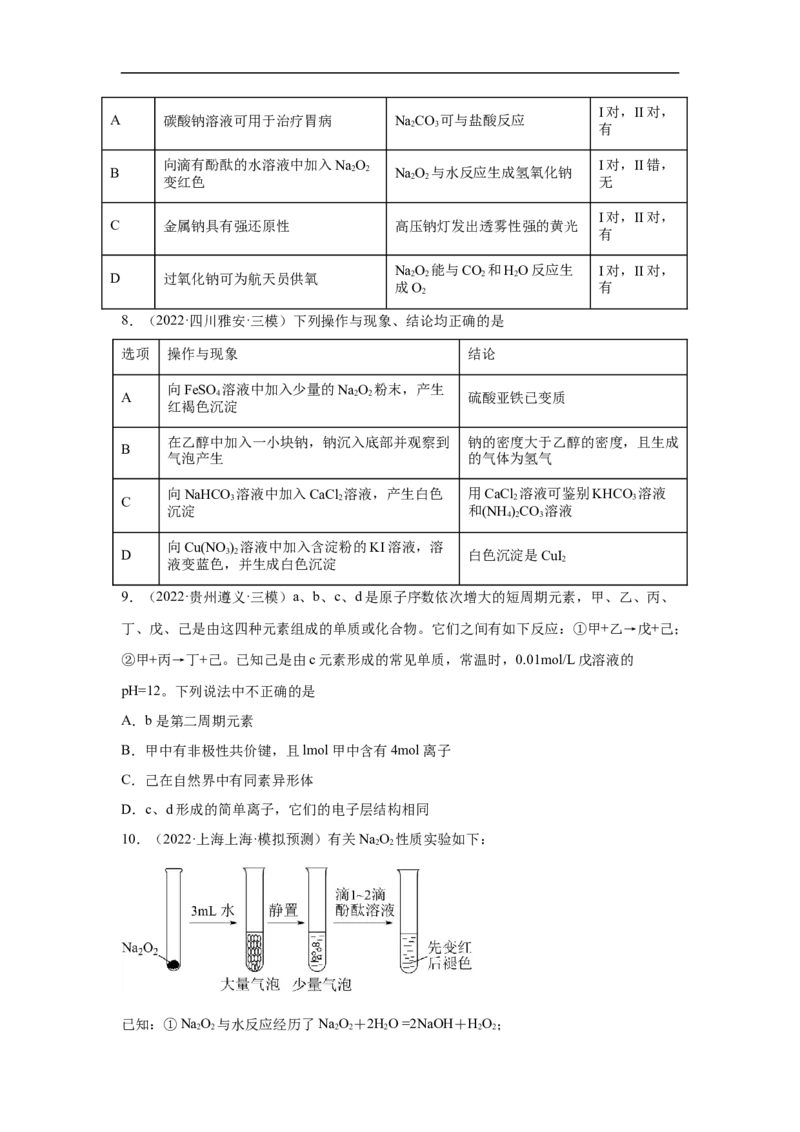
8.(2022·四川雅安·三模)下列操作与现象、结论均正确的是
选项 操作与现象 结论
向FeSO 溶液中加入少量的NaO 粉末,产生
A 4 2 2 硫酸亚铁已变质
红褐色沉淀
在乙醇中加入一小块钠,钠沉入底部并观察到 钠的密度大于乙醇的密度,且生成
B
气泡产生 的气体为氢气
向NaHCO 溶液中加入CaCl 溶液,产生白色 用CaCl 溶液可鉴别KHCO 溶液
C 3 2 2 3
沉淀 和(NH )CO 溶液
4 2 3
向Cu(NO ) 溶液中加入含淀粉的KI溶液,溶
D 3 2 白色沉淀是CuI
液变蓝色,并生成白色沉淀 2
9.(2022·贵州遵义·三模)a、b、c、d是原子序数依次增大的短周期元素,甲、乙、丙、
丁、戊、己是由这四种元素组成的单质或化合物。它们之间有如下反应:①甲+乙→戊+己;
②甲+丙→丁+己。已知己是由c元素形成的常见单质,常温时,0.01mol/L戊溶液的
pH=12。下列说法中不正确的是
A.b是第二周期元素
B.甲中有非极性共价键,且lmol甲中含有4mol离子
C.己在自然界中有同素异形体
D.c、d形成的简单离子,它们的电子层结构相同
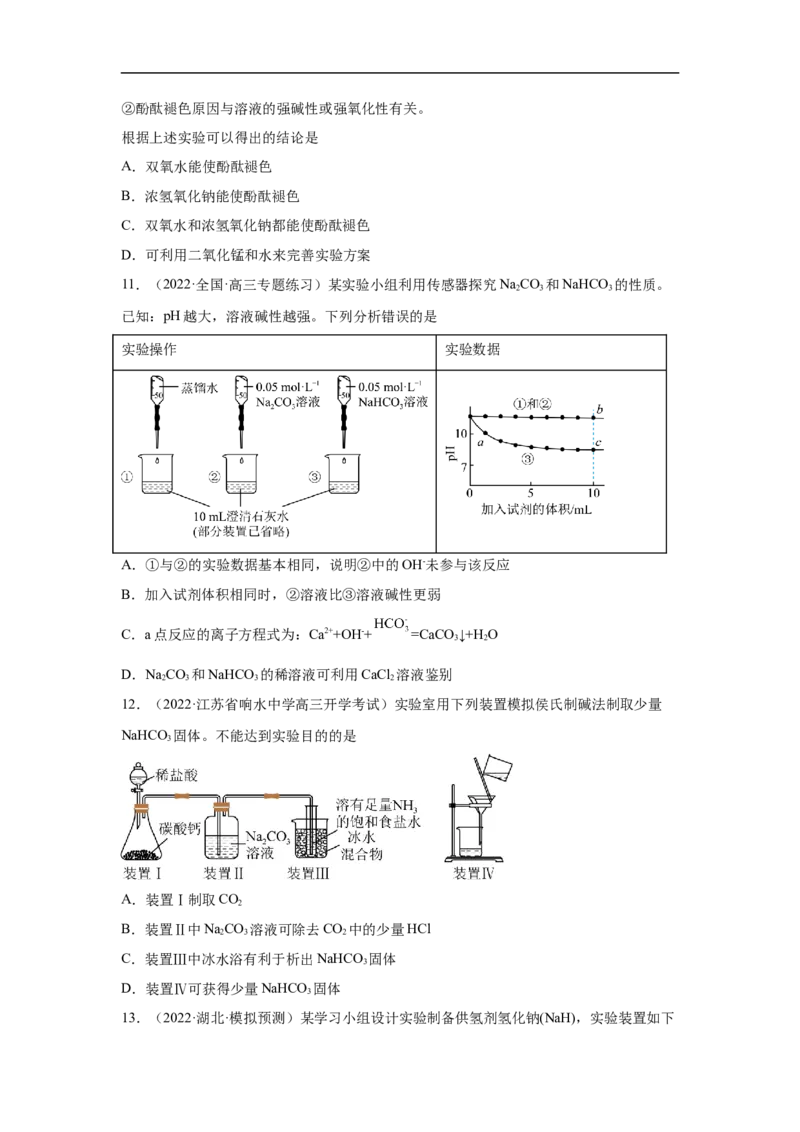
10.(2022·上海上海·模拟预测)有关NaO 性质实验如下:
2 2
已知:①NaO 与水反应经历了NaO+2HO =2NaOH+HO;
2 2 2 2 2 2 2②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
A.双氧水能使酚酞褪色
B.浓氢氧化钠能使酚酞褪色
C.双氧水和浓氢氧化钠都能使酚酞褪色
D.可利用二氧化锰和水来完善实验方案
11.(2022·全国·高三专题练习)某实验小组利用传感器探究NaCO 和NaHCO 的性质。
2 3 3
已知:pH越大,溶液碱性越强。下列分析错误的是
实验操作 实验数据
A.①与②的实验数据基本相同,说明②中的OH-未参与该反应
B.加入试剂体积相同时,②溶液比③溶液碱性更弱
C.a点反应的离子方程式为:Ca2++OH-+ =CaCO ↓+H O
3 2
D.NaCO 和NaHCO 的稀溶液可利用CaCl 溶液鉴别
2 3 3 2
12.(2022·江苏省响水中学高三开学考试)实验室用下列装置模拟侯氏制碱法制取少量
NaHCO 固体。不能达到实验目的的是
3
A.装置Ⅰ制取CO
2
B.装置Ⅱ中NaCO 溶液可除去CO 中的少量HCl
2 3 2
C.装置Ⅲ中冰水浴有利于析出NaHCO 固体
3
D.装置Ⅳ可获得少量NaHCO 固体
3
13.(2022·湖北·模拟预测)某学习小组设计实验制备供氢剂氢化钠(NaH),实验装置如下图所示。
下列说法错误的是
A.相同条件下,粗锌比纯锌反应速率快
B.装置a还能用来制备CO 和HS气体
2 2
C.实验时先打开活塞K,再点燃c处酒精灯
D.判断钠是否剩余,可取c中固体加水检验
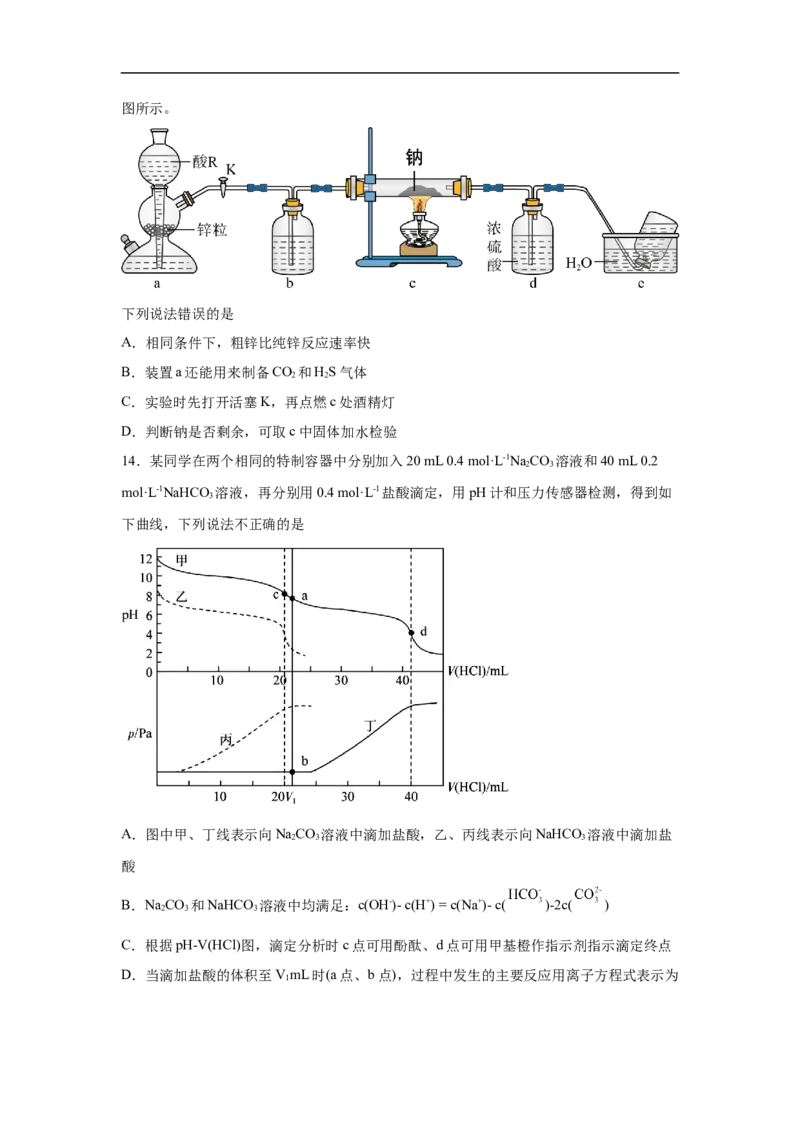
14.某同学在两个相同的特制容器中分别加入20 mL 0.4 mol·L-1NaCO 溶液和40 mL 0.2
2 3
mol·L-1NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,用pH计和压力传感器检测,得到如
3
下曲线,下列说法不正确的是
A.图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶液中滴加盐
2 3 3
酸
B.NaCO 和NaHCO 溶液中均满足:c(OH-)- c(H+) = c(Na+)- c( )-2c( )
2 3 3
C.根据pH-V(HCl)图,滴定分析时c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.当滴加盐酸的体积至VmL时(a点、b点),过程中发生的主要反应用离子方程式表示为
1+ H+ = CO↑+ H O
2 2
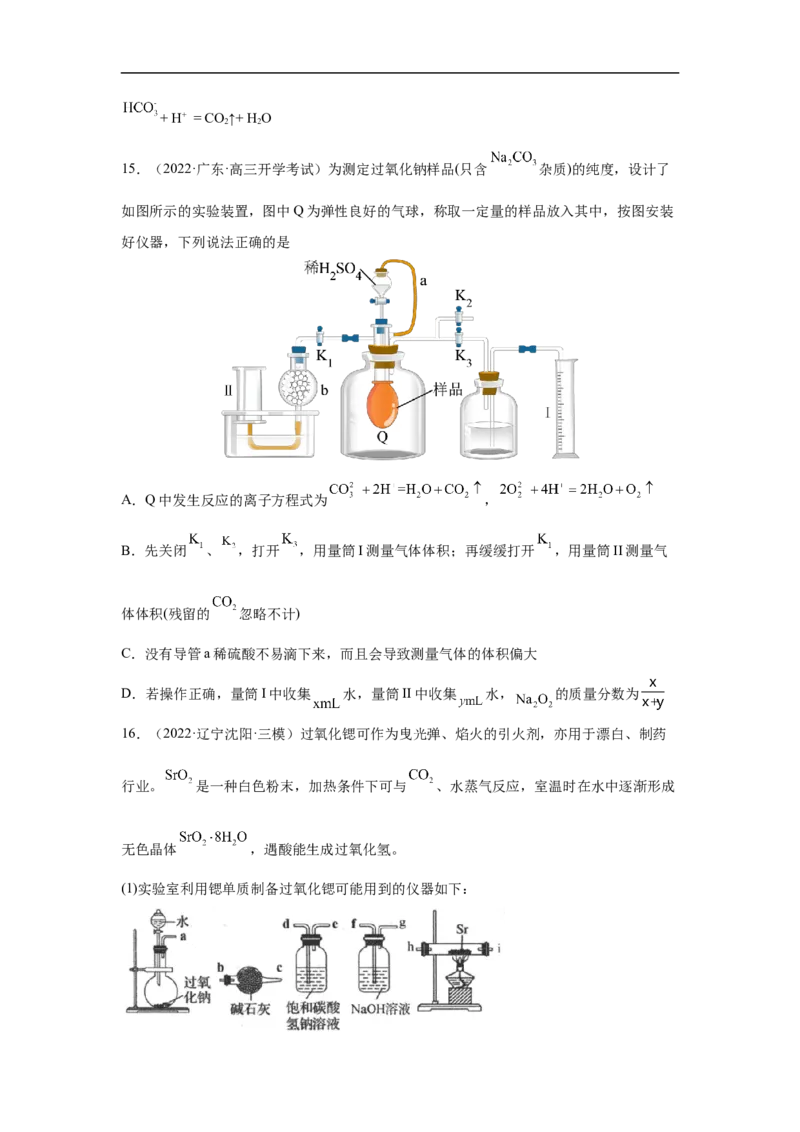
15.(2022·广东·高三开学考试)为测定过氧化钠样品(只含 杂质)的纯度,设计了
如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装
好仪器,下列说法正确的是
A.Q中发生反应的离子方程式为 ,
B.先关闭 、 ,打开 ,用量筒I测量气体体积;再缓缓打开 ,用量筒II测量气
体体积(残留的 忽略不计)
C.没有导管a稀硫酸不易滴下来,而且会导致测量气体的体积偏大
D.若操作正确,量筒I中收集 水,量筒II中收集 水, 的质量分数为
16.(2022·辽宁沈阳·三模)过氧化锶可作为曳光弹、焰火的引火剂,亦用于漂白、制药
行业。 是一种白色粉末,加热条件下可与 、水蒸气反应,室温时在水中逐渐形成
无色晶体 ,遇酸能生成过氧化氢。
(1)实验室利用锶单质制备过氧化锶可能用到的仪器如下:①按气流从左到右的流向,制备过氧化锶的导管接口顺序为a→_______。(选择必要的仪器,
可重复选择)
② 在空气中会变质生成碳酸盐,写出该反应的化学方程式_______。
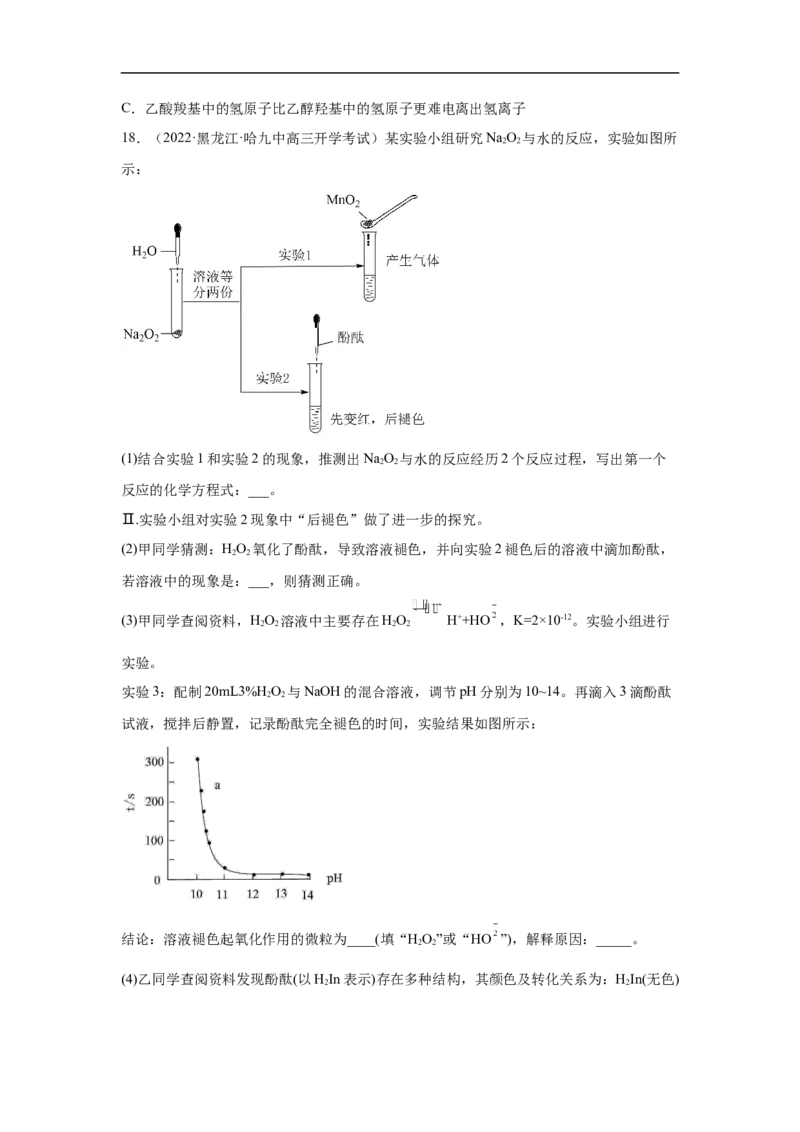
(2)通入氨气的条件下,在水溶液中可制备得到 ,实验装置如下:
仪器a的名称为_______,装置乙的作用为_______。
(3)装置丙中制备 的离子方程式_______, 的作用是_______。
(4)为测定 样品的纯度,可进行下列实验:准确称取2.0g 样品置于锥
形瓶中,加入适量的盐酸充分溶解;加入过量KI溶液,摇匀后置于暗处;充分反应后加入
少量淀粉溶液,用0.8000mol/L 标准溶液滴定至溶液蓝色恰好消失,记下此时消耗
标准溶液的体积,重复实验3~4次,得下表数据:
平行实验 1 2 3 4
消耗标准溶液体积(mL) 14.98 14.50 15.00 15.02
样品的纯度为_______。(已知: )
17.(2022·全国·高三专题练习)某兴趣小组探究钠与水、盐酸、醋酸和乙醇反应的快慢。
I.兴趣小组成员根据已有认知模型提出以下猜测:
猜测1:钠分别与水、盐酸反应,钠与盐酸反应更快。
猜测2:钠分别与乙醇、醋酸反应,钠与醋酸反应更快。
Ⅱ.设计实验进行“证实与证伪”
实验I配制一定浓度的HCl
(1)用12.00mol·L-1HCl配制0.50mol·L-1HCl和5.00mol·L-1HCl时,除用到烧杯、胶头滴管、
玻璃棒外,还必须用到下列仪器中的_______(写对应字母)。实验Ⅱ相同温度下,比较钠与水、0.50mol·L-1HCl、5.00mol·L-1HCl反应的快慢
序号 钠块(形状几乎相同) 反应液体(50mL) 钠块消失时间
Ⅰ 0.15g 水
Ⅱ 0.15g 0.50mol·L-1HCl Ⅱ<Ⅰ<Ⅲ
Ⅲ 0.15g 5.00mol·L-1HCl
该小组查阅资料知,相同温度下,影响钠与盐酸反应速率的主要因素是c(H+)和钠表面的
c(Na+)。
(2)钠与5.00mol·L-1HCl反应,速率最慢的原因可能是_______。
实验Ⅲ相同温度下,比较钠与乙醇、醋酸反应的快慢
(3)根据信息,完成如下表格:
实
钠块(形状 两个相同的烧 钠块完全反
验
大小几乎 杯(反应液体 实验现象 应完所需时 实验结论
序
一样) 50mL) 间
号
钠_______,产
Ⅰ 0.15g 无水乙醇 1285s
生气泡较快
钠与无水乙醇反应的
反应速率比钠与冰醋
钠_______,产 酸反应的速率快得多
Ⅱ 0.15g 冰醋酸 3625s
生气泡较慢
(4)通过上述实验,该小组同学发现实验结果是钠与无水乙醇反应时,钠块完全反应需要的
时间更短。对此,同学们对实验现象进行了分析,发现上述实验设计存在缺陷,该缺陷是
_______。
(5)请你帮助该小组同学设计新的实验方案,对上述实验进行改进_______。
(6)通过实验探究,该小组同学认为钠与醋酸反应比钠与乙醇反应慢,原因可能是_______。
A.冰醋酸是无水乙酸,无水情况下难以电离出氢离子
B.乙醇钠在乙醇中的溶解度大于乙酸钠在乙酸中的溶解度C.乙酸羧基中的氢原子比乙醇羟基中的氢原子更难电离出氢离子
18.(2022·黑龙江·哈九中高三开学考试)某实验小组研究NaO 与水的反应,实验如图所
2 2
示:
(1)结合实验1和实验2的现象,推测出NaO 与水的反应经历2个反应过程,写出第一个
2 2
反应的化学方程式:___。
Ⅱ.实验小组对实验2现象中“后褪色”做了进一步的探究。
(2)甲同学猜测:HO 氧化了酚酞,导致溶液褪色,并向实验2褪色后的溶液中滴加酚酞,
2 2
若溶液中的现象是:___,则猜测正确。
(3)甲同学查阅资料,HO 溶液中主要存在HO H++HO ,K=2×10-12。实验小组进行
2 2 2 2
实验。
实验3:配制20mL3%H O 与NaOH的混合溶液,调节pH分别为10~14。再滴入3滴酚酞
2 2
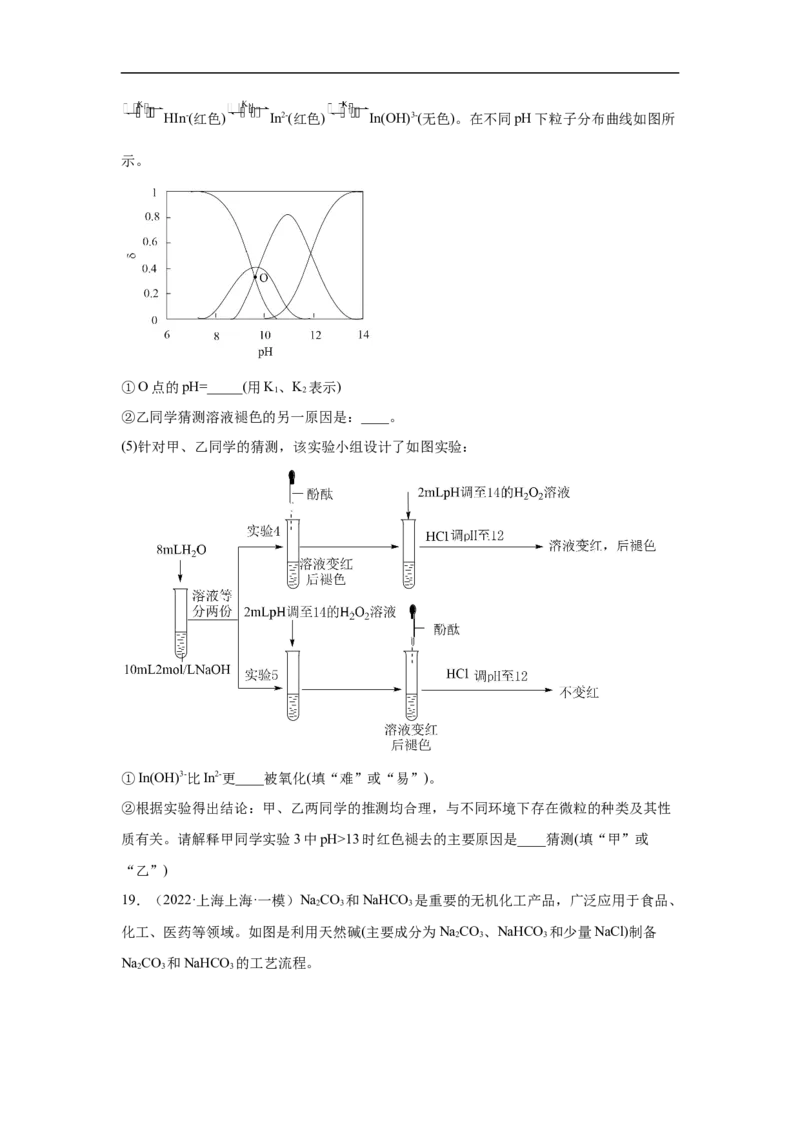
试液,搅拌后静置,记录酚酞完全褪色的时间,实验结果如图所示:
结论:溶液褪色起氧化作用的微粒为____(填“HO”或“HO ”),解释原因:_____。
2 2
(4)乙同学查阅资料发现酚酞(以HIn表示)存在多种结构,其颜色及转化关系为:HIn(无色)
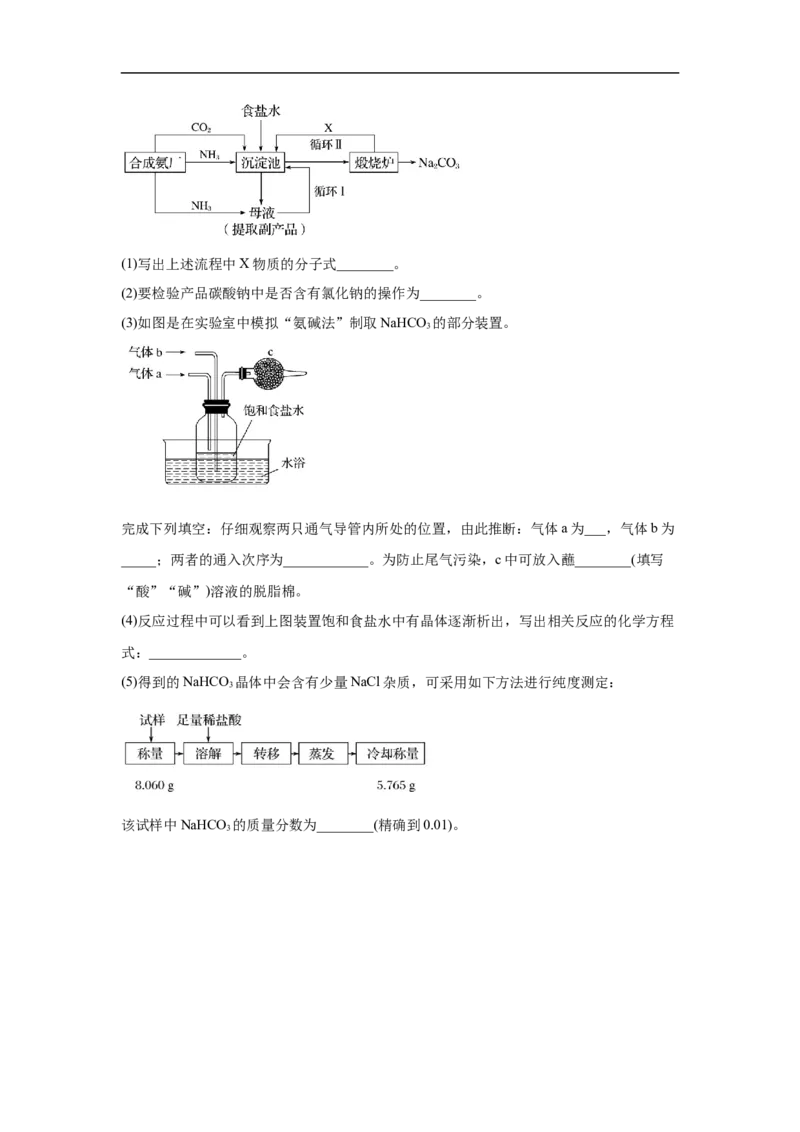
2 2HIn-(红色) In2-(红色) In(OH)3-(无色)。在不同pH下粒子分布曲线如图所
示。
①O点的pH=_____(用K、K 表示)
1 2
②乙同学猜测溶液褪色的另一原因是:____。
(5)针对甲、乙同学的猜测,该实验小组设计了如图实验:
①In(OH)3-比In2-更____被氧化(填“难”或“易”)。
②根据实验得出结论:甲、乙两同学的推测均合理,与不同环境下存在微粒的种类及其性
质有关。请解释甲同学实验3中pH˃13时红色褪去的主要原因是____猜测(填“甲”或
“乙”)
19.(2022·上海上海·一模)NaCO 和NaHCO 是重要的无机化工产品,广泛应用于食品、
2 3 3
化工、医药等领域。如图是利用天然碱(主要成分为NaCO、NaHCO 和少量NaCl)制备
2 3 3
NaCO 和NaHCO 的工艺流程。
2 3 3完成下列填空:
(1)操作①为___。
(2)碳化装置中反应的离子方程式___。
(3)解释选择0.34~0.4MPa干燥的原因___。
(4)对比索尔维制碱法,说明利用天然碱制碱的优势___。
(5)为了测定产品中小苏打中NaHCO 的含量进行以下实验。
3
实验步骤:
步骤一:称2.000g小苏打样品,配制小苏打溶液250mL。
步骤二:取20.00mL小苏打溶液置于锥形瓶中,用0.1000mol·L-1盐酸滴定,溶液pH随盐
酸体积变化如图所示。
完成下列填空:
①取20.00mL小苏打溶液需要使用的定量仪器名称____。
②根据滴定曲线分析,若采用传统滴定法,应选择的指示剂是___,此时滴定终点的现象为
___。
③计算该样品中NaHCO 的质量分数为____。
3
20.(2020·河北·张家口市第一中学高三期中)我国化学家侯德榜改革国外的纯碱生产工
艺,生产流程可简要表示为图所示:(1)写出上述流程中X物质的分子式________。
(2)要检验产品碳酸钠中是否含有氯化钠的操作为________。
(3)如图是在实验室中模拟“氨碱法”制取NaHCO 的部分装置。
3
完成下列填空:仔细观察两只通气导管内所处的位置,由此推断:气体a为___,气体b为
_____;两者的通入次序为____________。为防止尾气污染,c中可放入蘸________(填写
“酸”“碱”)溶液的脱脂棉。
(4)反应过程中可以看到上图装置饱和食盐水中有晶体逐渐析出,写出相关反应的化学方程
式:_____________。
(5)得到的NaHCO 晶体中会含有少量NaCl杂质,可采用如下方法进行纯度测定:
3
该试样中NaHCO 的质量分数为________(精确到0.01)。
3