文档内容
热点 01 陌生化学(离子)方程式的书写
►命题趋势►解题策略►真题回眸►限时检测
考向一 氧化还原反应化学(离子)方程式的书写
陌生化学(离子)方程式的书写
考向二 非氧化还原反应化学(离子)方程式的书写
在高考化学中,经常涉及陌生情景中的化学方程式书写,这部分内容是高中化学的重、难点知识,也
是高考必考的内容。
预计2024年高考化学中,该部分考题将会结合化学工艺流程、综合实验进行考察,伴随陌生度较高的
新信息和新情境,灵活度较高,涉及陌生氧化还原反应方程式的书写,而且以离子反应的形式出现可能性
更大。
信息“新”、内容别致、陌生度高是这部分考题的特点,它要求学生通过有效自学,敏捷地接受试题
给出的新信息,并将题给信息与课本知识有机地结合起来,达到以旧带新、触类旁通的作用,进而产生新
思路,发现新规律,创造性地解决问题。
【策略1】知识储备——明确一些特殊物质中元素的化合价
CuFeS:Cu为+2,Fe为+2,S为-2; C O:C为+3;
2 2
KFeO:Fe为+6; HCN:C为+2;N为-3;
2 4
FePO :Fe为+3; CuH:Cu为+1,H为-1;
4
LiFePO :Fe为+2; BH:B为+3、H为-1;
4
LiNH、LiNH、AlN:N为-3; FeO:Fe为+(8-n);
2 2
NH:N为-2; Si N:Si为+4,N为-3;
2 4 3 4
NaSO:S为+2; MnO(OH):Mn为+3;
2 2 3
SO:S为+6; CrO:Cr为+6;
2
VO:V为+5;
【策略2】书写关键——识记常见氧化剂、还原剂及产物预测
(1)常见的氧化剂及还原产物预测
氧化剂 还原产物
KMnO Mn2+(酸性);MnO (中性);MnO(碱性)
4 2
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
HSO (浓) SO
2 4 2X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO)
2 2 2 3
Cl Cl-
2
HClO、NaClO、Ca(ClO) (或ClO-) Cl-、Cl
2 2
NaClO Cl、ClO 、Cl-
3 2 2
PbO Pb2+
2
Fe3+ Fe2+
(2)常见的还原剂及氧化产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或HSO 、SO、NaHSO) SO
2 2 3 3
S2-(或HS、NaHS) S、SO (或SO)、SO
2 2
HC O、C O CO、CO
2 2 4 2 2
HO O
2 2 2
I-(或HI、NaI) I、IO
2
CO CO
2
金属单质(Zn、Fe、Cu等) Zn2+、Fe2+(与强氧化剂反应生成Fe3+)、Cu2+
H H+(酸性)、HO(碱性)
2 2
【策略3】熟练书写复杂氧化还原反应方程式的步骤及常见误区
(1)“读”取题目中的有效信息,找出发生氧化还原反应的物质或离子。
①常见强氧化性物质或离子:NaO 、Fe3+、NO 、HNO(浓)、HNO(稀)、O 、O 、HO 、HSO (浓)、
2 2 2 3 3 2 3 2 2 2 4
Cl、Br 、HClO、NaClO、Ca(ClO) 、KMnO (H+)。
2 2 2 4
②常见强还原性物质或离子:Fe2+、Fe(OH) 、SO (H SO 、NaSO 、NaHSO 、SO)、HS(Na S、
2 2 2 3 2 3 3 2 2
NaHS、S2-)、HI(NaI、I-)等。
(2)依据掌握的氧化还原反应规律合理地预测产物(这里要重视题目中的信息提示,或给出的生成物),写
出主要反应物和生成物的化学式。
(3)根据氧化还原反应的守恒规律确定氧化剂、还原剂、还原产物、氧化产物的相应计量数。
(4)根据原子守恒和溶液的酸碱性,通过在反应方程式的两端添加H+、OH-或HO的形式使方程式的两
2
端的电荷守恒。
【误区1】误认为酸碱性不同对产物无影响。溶液的酸碱性不同产物也不同,如高锰酸钾的还原产物:【误区2】忽视溶液的酸碱性条件。
①在酸性条件下,离子方程式中不能出现OH-;在碱性条件下,离子方程式中不能出现H+。
②酸性条件下多氧配H+,另一侧补水;碱性条件下多氧配水,另一侧补OH-。
(5)再依据质量守恒,写出规范的方程式。
考向一 氧化还原反应化学(离子)方程式的书写
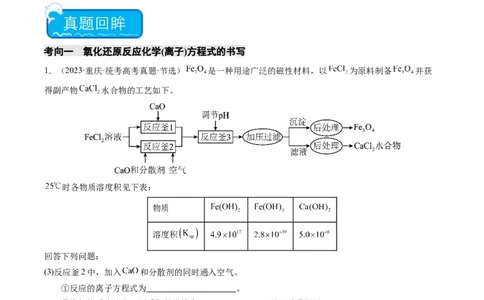
1.(2023·重庆·统考高考真题·节选) 是一种用途广泛的磁性材料,以 为原料制备 并获
得副产物 水合物的工艺如下。
时各物质溶度积见下表:
物质
溶度积
回答下列问题:
(3)反应釜2中,加入 和分散剂的同时通入空气。
①反应的离子方程式为 。
②为加快反应速率,可采取的措施有 。(写出两项即可)。
【答案】(3) 适当升高温度、搅拌
【详解】 溶液加入氧化钙生成氢氧化亚铁, 溶液加入氧化钙和空气生成氢氧化铁,反应釜1、2
中物质混合后调节pH,加压过滤分离出沉淀处理得到四氧化三铁,滤液处理得到氯化钙水合物;,
(3)①反应釜2中,加入 和分散剂的同时通入空气,氧气将二价铁氧化三价铁,三价铁与氧化钙和
水生成的氢氧化钙生成氢氧化铁,反应的离子方程式为 。
②为加快反应速率,可采取的措施有适当升高温度、搅拌等;
2.(2023·辽宁·统考高考真题·节选)某工厂采用如下工艺处理镍钴矿硫酸浸取液(含和 )。实现镍、钴、镁元素的回收。
已知:
物
质
回答下列问题:
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为 (
的电离第一步完全,第二步微弱);滤渣的成分为 、 (填化学式)。
(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为 。
【答案】
(3) CaSO 、Fe(OH)
4 3
(5)
【详解】在“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 ,用石灰
乳调节 , 被 氧化为 ,发生反应 ,Fe3+水解同
时生成氢氧化铁,“沉钻镍”过程中,Co2+变为Co(OH) ,在空气中可被氧化成 。
2
(3)用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为:
;氢氧化铁的Ksp=10-37.4,当铁离子完全沉淀时,溶液中c(Fe3+)=10-
5mol/L, ,c(OH-)=10-10.8mol/L,根据Kw=10-14,pH=3.2,此时溶
液的pH=4,则铁离子完全水解,生成氢氧化铁沉淀;由于CaSO 微溶于水,故滤渣还有CaSO 和氢氧化
4 4
铁;
(5)“沉钻镍”中得到的Co(OH) ,在空气中可被氧化成 ,该反应的化学方程式为:
2
;
3.(2023·海南·统考高考真题·节选)铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要
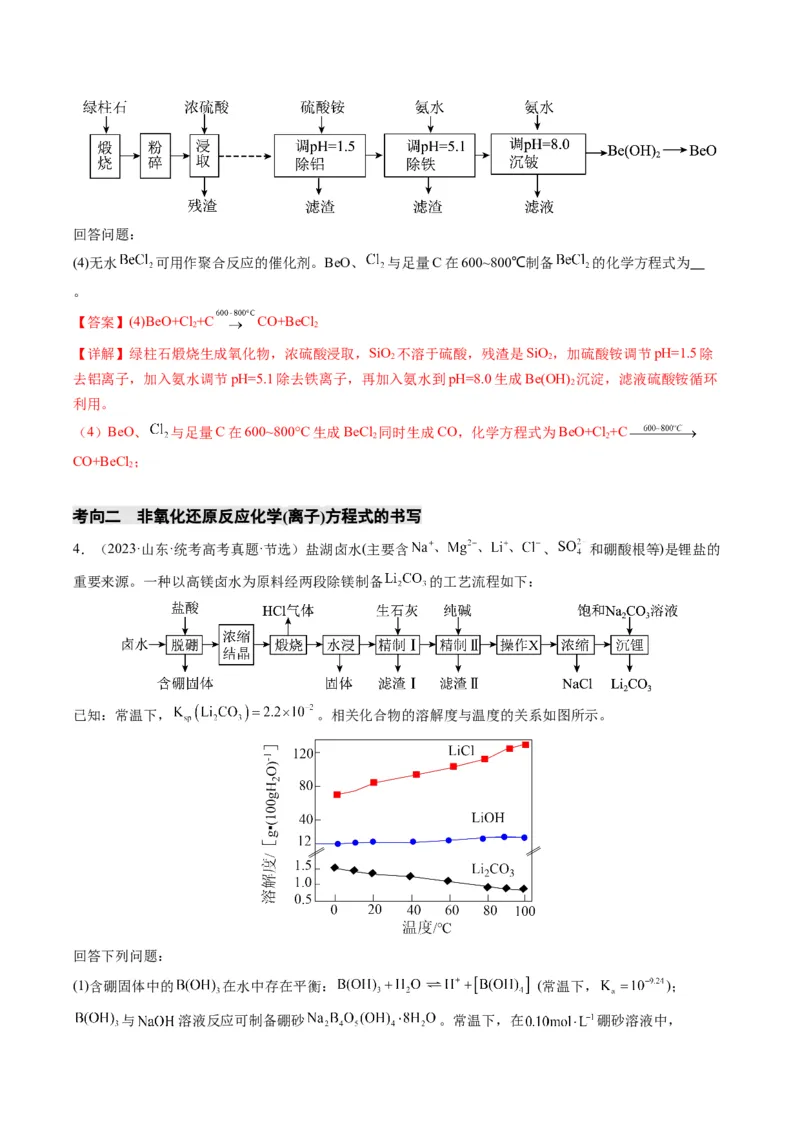
的战略物资。利用绿柱石(主要化学成分为( ,还含有一定量的FeO和 )生产BeO的一种工
艺流程如下。回答问题:
(4)无水 可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备 的化学方程式为
。
【答案】(4)BeO+Cl +C CO+BeCl
2 2
【详解】绿柱石煅烧生成氧化物,浓硫酸浸取,SiO 不溶于硫酸,残渣是SiO,加硫酸铵调节pH=1.5除
2 2
去铝离子,加入氨水调节pH=5.1除去铁离子,再加入氨水到pH=8.0生成Be(OH) 沉淀,滤液硫酸铵循环
2
利用。
(4)BeO、 与足量C在600~800°C生成BeCl 同时生成CO,化学方程式为BeO+Cl +C
2 2
CO+BeCl ;
2
考向二 非氧化还原反应化学(离子)方程式的书写
4.(2023·山东·统考高考真题·节选)盐湖卤水(主要含 、 和硼酸根等)是锂盐的
重要来源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为
,该溶液 。
【答案】(1)
【详解】由流程可知,卤水中加入盐酸脱硼后过滤,所得滤液经浓缩结晶后得到晶体,该晶体中含有
Na+、Li+、Cl-、 等,焙烧后生成HCl气体;烧渣水浸后过滤,滤液中加生石灰后产生沉淀,滤渣Ⅰ的
主要成分为Mg(OH) 、 ;精制Ⅰ所得滤液中再加纯碱又生成沉淀,则滤渣Ⅱ为 、Mg(OH) ;
2 2
精制Ⅱ所得滤液经操作X后,所得溶液经浓缩结晶、过滤得到氯化钠,浓缩后的滤液中加入饱和碳酸钠溶
液沉锂,得到 。
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下.在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为
,由B元素守恒可知, 和 的浓度均为
, ,则该溶液 。
5.(2023·湖北·统考高考真题·节选) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
进行氯化处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量
烟雾,用化学方程式表示其原因 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
。“850℃煅烧”时的化学方程式为 。
【答案】
(2)
(4)【详解】由流程和题中信息可知, 粗品与 在500℃焙烧时生成氧气和烧渣,烧渣是LiCl、
和 的混合物;烧渣经水浸、过滤后得滤液1和滤饼1,滤饼1的主要成分是 和 ;滤
液1用氢氧化钠溶液沉钴,过滤后得滤饼2(主要成分为 )和滤液2(主要溶质为LiCl);滤饼2
置于空气中在850℃煅烧得到 ;滤液2经碳酸钠溶液沉锂,得到滤液3和滤饼3,滤饼3为 。
(2)“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,由此可知,四氯化硅与可水
反应且能生成氯化氢和硅酸,故其原因是: 遇水剧烈水解,生成硅酸和氯化氢,该反应的化学方程
式为 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中
, 浓度为 。“850℃煅烧”时,
与 反应生成 和 ,该反应的化学方程式为 。
6.(2023·浙江·统考高考真题·节选)工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
已知:
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式 。
(3)设计实验验证化合物A中含有S元素 ;写出实验过程中涉及的反
应方程式 。
【答案】
(1)
(3)取化合物A加入足量氢氧化钠,反应完全后加入盐酸酸化,无明显现象,再加入氯化钡生成白色沉淀,
说明A中含有S元素 +2NaOH=CHOH+Na SO +H O、
3 2 4 2
NaSO +BaCl =BaSO ↓+2NaCl
2 4 2 4
【详解】含硫矿物燃烧生成二氧化硫,二氧化硫和氧气、碳酸钙生成硫酸钙和二氧化碳,二氧化硫被氧气氧化为三氧化硫,三氧化硫和等物质量的甲醇发生已知反应生成A: ;
(1)氧气具有氧化性,能被四价硫氧化为六价硫,二氧化硫、空气中氧气、碳酸钙高温生成硫酸钙和二
氧化碳,反应为 ;
(3)由分析可知,A为 ,A碱性水解可以生成硫酸钠、甲醇,硫酸根离子能和氯化钡生
成不溶于酸的硫酸钡沉淀,故实验设计为:取化合物A加入足量氢氧化钠,反应完全后加入盐酸酸化,无
明显现象,再加入氯化钡生成白色沉淀,说明A中含有S元素;涉及反应为:
+2NaOH=CHOH+Na SO +H O、NaSO +BaCl =BaSO ↓+2NaCl。
3 2 4 2 2 4 2 4
(建议用时:35分钟)
1.(2023·江苏南通·统考模拟预测·节选)电催化还原 是当今资源化利用二氧化碳的重点课题,常用
的阴极材料有有机多孔电极材料、铜基复合电极材料等。
(2)一种铜基复合电极材料 的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中
逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得 ,溶液呈蓝色。写出 还原
的离子方程式: 。
【答案】(2)
【详解】(2)将一定量 分散至水与乙醇的混合溶液中,向溶液中逐滴滴加 (一种强酸)溶液,搅
拌一段时间后离心分离,溶液呈蓝色,说明生成铜离子。故 还原 的离子方程式:
。
2.(2023·北京西城·统考二模·节选)制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究。
已知:i.纳米Fe具有很高的活性,易被氧化使表面形成氧化层
ii.纳米Fe将 还原为 的转化关系如下:
(2)酸性条件下,纳米Fe和 反应生成 和 的离子方程式是 。
(4)水体中含有的 与 反应,会降低 的去除率。 与 反应的离子方程式是 。【答案】
(2)
(4)
【详解】(2)根据题意,可知还有H+参与反应,还生成了HO,离子方程式为
2
。
(4) 与 反应生成FeCO 沉淀和CO 气体,离子方程式是 。
3 2
3.(2023·江苏南通·统考三模·节选)单宁酸 -硫酸体系中,低品位软锰矿( 质量分数为
29%)中的Mn(Ⅳ)可被还原为 而浸出。其浸出过程如图所示。
(2)写出葡萄糖还原 生成 的离子反应方程式: 。
【答案】(2)
【详解】(2)葡萄糖还原 生成 ,根据得失电子守恒,离子反应方程式为
;
4.(2023·北京海淀·校考一模)正极材料为LiCoO 的锂离子电池已被广泛用作便携式电源。但钴的资源
2
匮乏限制了其进一步发展。
(1)橄榄石型LiFePO 是一种潜在的锂离子电池正极材料,它可以通过(NH )Fe(SO )、HPO 与LiOH溶液
4 4 2 4 2 3 4
发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应除了得到LiFePO 外,还有另外一种酸式盐产物,请写出共沉淀的化学方程式为 。
4
②高温成型前,常向LiFePO 中加入少量活性炭黑,其作用除了可以改善诚信后的LiFePO 的导电性能外,
4 4
还能 。
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO 及少量Al、Fe等)可通过下列实验方法回收钴、锂。
2①在上述溶解过程中,SO 被氧化成SO ,LiCoO 在溶解过程中反应的化学方程式为 。
2 2
②已知Co的氧化物与Fe的氧化物类似。Co(OH) 在空气中加热时,固体残留率随温度的变化如图所示。
2
已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 (填化学式),在
350~400℃范围内,剩余固体的成分为 (填化学式)。
【答案】
(1)(NH )Fe(SO )+LiOH+H PO =LiFePO ↓+2NHHSO +H O 与空气中O 反应,防止LiFePO 中的
4 2 4 2 3 4 4 4 4 2 2 4
Fe2+被氧化
(2)8LiCoO +Na SO+11H SO =4Li SO +8CoSO+Na SO +11H O CoO Co O、Co O
2 2 2 3 2 4 2 4 4 2 4 2 2 3 3 4
【详解】(1)①题给信息:(NH )、HPO 与LiOH溶液发生共沉淀反应生成LiFePO 、NH HSO 和HO,
4 2 3 4 4 4 4 2
反应的化学方程式为(NH )Fe(SO )+LiOH+H PO =LiFePO +2NHHSO +H O,
4 2 4 2 3 4 4 4 4 2
故答案为:(NH )Fe(SO )+LiOH+H PO =LiFePO ↓+2NHHSO +H O;
4 2 4 2 3 4 4 4 4 2
②高温成型前,常向LiFePO 中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO 的导电性能外,
4 4
还能消耗空气中的氧气,保护Fe2+,防止Fe2+被氧化,
故答案为:与空气中O 反应,防止LiFePO 中的Fe2+被氧化;
2 4
(2)正极材料试样主要含有LiCoO 及少量Al、Fe等,加入稀HSO 、NaSO,SO2-被氧化成SO 2-,具
2 2 4 2 2 3 2 3 4
有还原性,正极材料中只有LiCoO 具有氧化性,与反应NaSO 反应生成CoSO ,反应化学方程式为
2 2 2 3 4
8LiCoO +Na SO+11H SO =4Li SO +8CoSO+Na SO +11H O,
2 2 2 3 2 4 2 4 4 2 4 2
故答案为:8LiCoO +Na SO+11H SO =4Li SO +8CoSO+Na SO +11H O;
2 2 2 3 2 4 2 4 4 2 4 2
②根据质量守恒定律,在变化过程中,Co的质量没有变,假设原始固体质量为100g,则n(Co)= mol,
m(Co)=100× g;在1000℃时,固体质量不再变化,说明Co(OH) 完全分解,n(Co):n(O)= :
2=1:1,剩余固体成分为CoO;在350-400℃时,固体的质量在89.25%-86.38%之间,可以
通过极点进行分析,在290℃,n(Co):n(O)= : =2:3,其化学式为Co O;在
2 3
500℃n(Co):n(O)= : =3:4,其化学式为Co O;所以可以确定在350-400℃时的化学
3 4
式为Co O 和Co O,故答案为:CoO;Co O、Co O。
2 3 3 4 2 3 3 4
5.(2023上·江西校考一模·节选)以重晶石(BaSO)为原料,可按如下工艺生产立德粉(ZnS和BaSO 的混
4 4
合物):
①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为____________________。
回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO 和一种清洁能源气体,该反应
2
的化学方程式为________________________。
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原
料”表面生成了难溶于水的______(填化学式)。
③沉淀器中反应的离子方程式为___________________。
【答案】①BaSO+4C BaS+4CO↑ ②CO+HO CO+H ③BaCO ④S2-+Ba2++
4 2 2 2 3
Zn2++SO =ZnS·BaSO ↓
4
【详解】①由流程图中经浸出槽后得到净化的硫化钡溶液以及回转炉尾气中含有有毒气体可知,回转炉中
硫酸钡与过量的焦炭粉在900—1200℃的高温条件下反应生成可溶性的硫化钡和一氧化碳,反应的化学方
程式为BaSO+4C BaS+4CO↑;由题意可知,生产上可通过一氧化碳与水蒸气在高温下反应生成
4
二氧化碳和氢气,达到除去回转炉中的有毒气体CO,同时得到氢气做清洁能源的目的,反应的化学方程
式为CO+HO CO+H,故答案为:BaSO+4C BaS+4CO↑;CO+HO CO+H;
2 2 2 4 2 2 2
②还原料的主要成分是硫化钡,硫化钡是强碱弱酸盐,在潮湿空气中,硫化钡与空气中的水蒸气发生水解
反应生成具有臭鸡蛋气味的硫化氢气体和氢氧化钡,氢氧化钡与空气中的二氧化碳反应生成难溶的碳酸钡,
导致还原料硫化钡的水溶性变差,故答案为:BaCO ;
3
③由立德粉的成分可知,沉淀器中硫化钡溶液与硫酸锌溶液发生复分解反应反应生成ZnS·BaSO 沉淀,反
4
应的离子方程式为S2-+Ba2++Zn2++SO =ZnS·BaSO ↓,故答案为:S2-+Ba2++Zn2++SO
4
=ZnS·BaSO ↓。
46.(2023·福建厦门·校考一模·节选)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。
回答下列问题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为____________________________,生成的沉淀与硝酸反应,
生成_______后可循环使用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_____________________;若反应物
用量比 时,氧化产物为______________;当 ,单质碘的收率
会降低,原因是______________。
(2)以 为原料制备 的方法是:先向 溶液中加入过量的 ,生成碘化物;再向混合溶
液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_____________________。
(3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为_______ 。
在 溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水
蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是______________。
【答案】
(1)①2AgI+Fe=2Ag+ Fe2++2I- AgNO ②FeI+Cl= I+FeCl I、FeCl I 被过量的 进一步氧化
3 2 2 2 2 2 3 2
(2)
(3) 4 防止单质碘析出
【详解】(1) ①由流程图可知悬浊液中含AgI ,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在离子方
2 2
程式中能拆,故加入 粉进行转化反应的离子方程式为2AgI+Fe=2Ag+ Fe2++2I-,生成的银能与硝酸反应
生成硝酸银参与循环中,故答案为:2AgI+Fe=2Ag+ Fe2++2I-;AgNO;
3
②通入 的过程中,因I-还原性强于Fe2+, 先氧化还原性强的I-,若氧化产物只有一种,则该氧化产
物只能是I,故反应的化学方程式为FeI+Cl= I+FeCl ,若反应物用量比 时即 过
2 2 2 2 2
量,先氧化完全部I-再氧化Fe2+,恰好将全部I-和Fe2+氧化,故氧化产物为I、FeCl ,当
2 3
即 过量特别多,多余的氯气会与生成的单质碘以及水继续发生氧化还原反应,
单质碘的收率会降低,故答案为:FeI+Cl= I+FeCl ;I、FeCl ;I 被过量的 进一步氧化;
2 2 2 2 2 3 2
(2)先向 溶液中加入计量的 ,生成碘化物即含I-的物质;再向混合溶液中(含I-)加入溶液,反应得到 ,上述制备 的两个反应中I-为中间产物,总反应为 与 发生氧化还原
反应,生成 和 ,根据得失电子守恒、电荷守恒]及元素守恒配平离子方程式即可得:
,故答案为: ;
(3) 溶液和 溶液混合可生成 沉淀和 ,化学方程式为4KI+2CuSO =2CuI +I +2K SO ,
4 2 2 4
若生成 ,则消耗的 至少为4mol;反应中加入过量 ,I-浓度增大,可逆反应 平衡
右移,增大 溶解度,防止 升华,有利于蒸馏时防止单质碘析出,故答案为:4;防止单质碘析出。
7.(2023·浙江金华·校考一模·节选)NiSO •6H O是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生
4 2
产电池、医药工业、催化行业以及印染工业等行业中。由一种废料(主要成分是铁镍合金,还含有铜、镁、
硅的氧化物)为原料制取NiSO •6H O的步骤如图:
4 2
已知:镍能溶于稀酸但溶解不完全,通常表现为+2价。
(1)“溶解”时加入HO 溶液的目的是_______________。
2 2
(2)“除铁”时生成黄钠铁矾[Na Fe (SO )(OH) ]沉淀,写出其离子方程式:____________________ 。
2 6 4 4 12
(3)NiSO 在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的化学方程式为
4
____________________________。
【答案】
(1)使Fe2+氧化成Fe3+,使镍元素完全转化成Ni2+
(2)6Fe3++4SO +6H O+2Na++6MgO=6Mg2++Na Fe (SO )(OH) ↓
2 2 6 4 4 12
(3)2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O
4 2 4 2
【解析】由一种废料(主要成分是铁镍合金,还含有铜、镁、硅的氧化物)为原料制取NiSO •6H O步骤如图,
4 2
废料溶解后加入稀硫酸和过氧化氢溶液,反应后过滤,加入硫酸钠和 MgO 除去铁,生成黄钠铁矾
[Na Fe (SO )(OH) ]沉淀,通入HS气体除铜,过滤后的滤液中加入NaF溶液,使Mg2+转化为MgF 沉淀除
2 6 4 4 12 2 2
去,加入氢氧化钠溶液沉镍,再加入稀硫酸得到硫酸镍溶液,蒸发浓缩、冷却结晶、过滤洗涤得到
NiSO •6H O,据此分析回答问题。
4 2
(1)加入的硫酸具有酸性,可以把Fe以及Cu、Mg的氧化物溶解,部分Ni溶解,转化得到的金属离子有
Fe2+、Cu2+、Mg2+、Ni2+,加入的HO 具有氧化性,可以促进Ni的溶解,使其全部转化为Ni2+,同时把
2 2
Fe2+氧化为Fe3+。
(2)“除铁”时加入NaSO 溶液和MgO,根据元素守恒和电荷守恒,离子方程式为6Fe3++4SO
2 4+6H O+2Na++6MgO=6Mg2++Na Fe (SO )(OH) ↓。
2 2 6 4 4 12
(3)NaClO具有强氧化性,Cl元素由+1价降低到-1价,则Ni元素由NiSO 中+2价升高到NiOOH中+3
4
价,根据得失电子守恒和元素守恒,化学方程式为
2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O。
4 2 4 2
8.(2023·陕西渭南·统考模拟预测·节选)某小组同学探究 与新制 悬浊液的反应。
资料: 为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成 ,该物质在空气中会
立即被氧化成 而使溶液显蓝色。
C中实验现象
序号 物质a
通入 前 通入 后
开始时有砖红色沉淀出现,一段时间后,砖红色沉淀
Ⅰ 溶液 产生蓝色絮状沉淀 消失,静置,试管底部有少量紫红色固体,溶液呈绿
色
开始时有黄色沉淀出现,一段时间后,黄色沉淀消
Ⅱ 溶液 产生蓝色絮状沉淀
失,静置,生成大量白色沉淀,溶液呈绿色
(1)装置B的作用是控制 气体的流速,则B中试剂是 。
(2)通入 前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为 。
(3)实验Ⅰ通入 后产生砖红色沉淀 ,该反应的化学方程式为 。分析实
验Ⅰ一段时间后砖红色沉淀消失的可能原因 。
(4)同学们对实验Ⅱ中白色沉淀的成分继续探究。
①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:
、 。
②乙同学用另一种方法证明了该白色沉淀为 ,实验方案如下:填写下表空格:
试剂1 试剂2 蒸馏水
现象1 现象2
(5)实验Ⅰ和实验Ⅱ中 与新制 悬浊液均发生了 反应,反应现象的不同与 有关。
【答案】
(1)饱和NaHSO 溶液
3
(2)Cu2++2OH-=Cu(OH)
2
(3)2Cu(OH) +SO+2NaOH=Na SO +Cu O+3HO 溶液中溶解的SO 增多,溶液的酸性增强,使Cu O溶
2 2 2 4 2 2 2 2
解,砖红色沉淀消失
(4) 浓盐酸 白色沉淀溶解 出
现白色沉淀
(5)氧化还原 配制Cu(OH) 所用铜盐的阴离子种类
2
【详解】(1)B的作用是控制二氧化硫气体的流速,B中试剂不能吸收二氧化硫,所以B中试剂是饱和
NaHSO 溶液。
3
(2)通入SO 前,实验Ⅰ、Ⅱ中铜离子和氢氧根离子反应生成氢氧化铜蓝色絮状沉淀,反应的离子方程式
2
为:Cu2++2OH-=Cu(OH) 。
2
(3)实验Ⅰ通入SO 后产生砖红色氧化亚铜沉淀,铜元素化合价由+2价降低为+1价,S元素化合价由+4
2
价升高为+6价,该反应的化学方程式2Cu(OH) +SO+2NaOH=Na SO +Cu O+3HO;Cu O在酸性溶液中溶
2 2 2 4 2 2 2
解转化为Cu和Cu2+,实验Ⅰ一段时间后, 溶液中溶解的SO 增多,溶液的酸性增强,使Cu O溶解,砖红
2 2
色沉淀消失。
(4)①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液, 在空气中会立即被氧化成
而使溶液显蓝色,此过程中反应的离子方程式为:
、
;
②CuCl为白色固体,难溶于水,能溶于浓盐酸;取白色固体加浓盐酸,白色固体溶解,在加蒸馏水,又
出现白色沉淀,则说明白色固体是CuCl。(5)实验Ⅰ和实验Ⅱ中SO 与新制Cu(OH) 悬浊液均发生了氧化还原反应,反应现象的不同与配制
2 2
Cu(OH) 所用铜盐的阴离子种类有关。
2
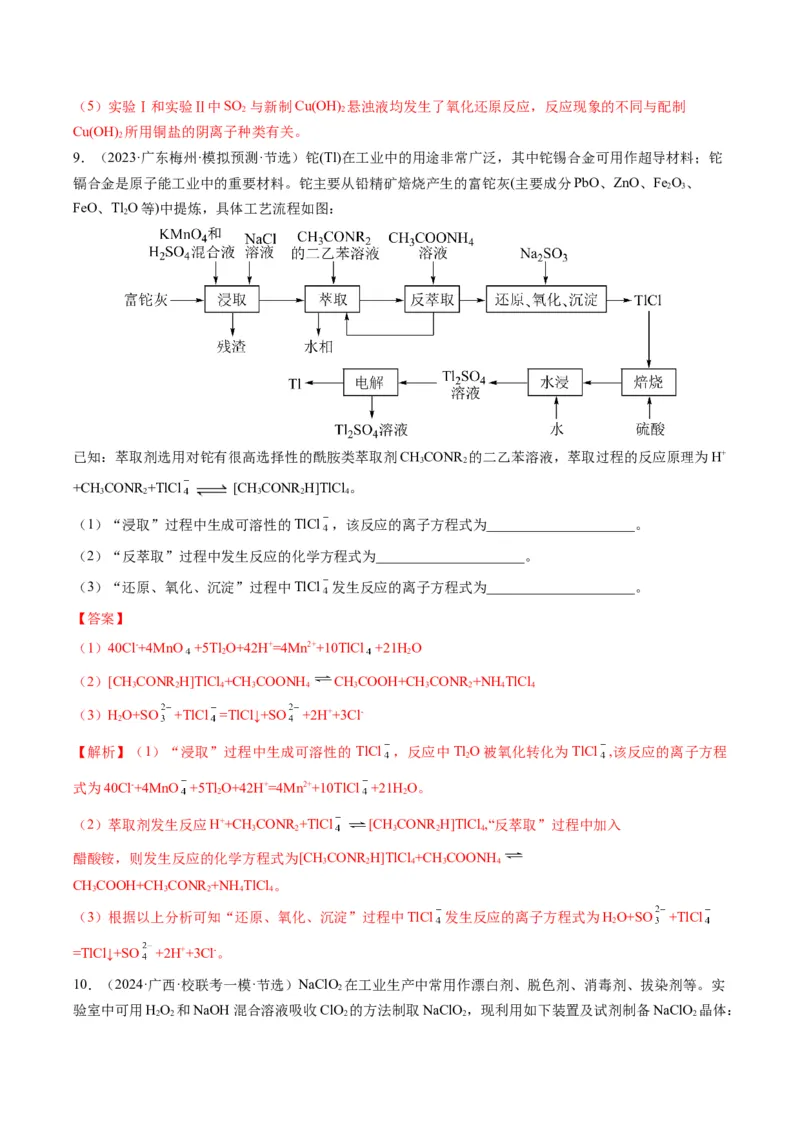
9.(2023·广东梅州·模拟预测·节选)铊(Tl)在工业中的用途非常广泛,其中铊锡合金可用作超导材料;铊
镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe O、
2 3
FeO、TlO等)中提炼,具体工艺流程如图:
2
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CHCONR 的二乙苯溶液,萃取过程的反应原理为H+
3 2
+CH CONR +TlCl [CHCONR H]TlCl 。
3 2 3 2 4
(1)“浸取”过程中生成可溶性的TlCl ,该反应的离子方程式为_____________________。
(2)“反萃取”过程中发生反应的化学方程式为_____________________。
(3)“还原、氧化、沉淀”过程中TlCl 发生反应的离子方程式为_____________________。
【答案】
(1)40Cl-+4MnO +5Tl O+42H+=4Mn2++10TlCl +21H O
2 2
(2)[CHCONR H]TlCl +CH COONH CHCOOH+CH CONR +NHTlCl
3 2 4 3 4 3 3 2 4 4
(3)HO+SO +TlCl =TlCl↓+SO +2H++3Cl-
2
【解析】(1)“浸取”过程中生成可溶性的TlCl ,反应中TlO被氧化转化为TlCl ,该反应的离子方程
2
式为40Cl-+4MnO +5Tl O+42H+=4Mn2++10TlCl +21H O。
2 2
(2)萃取剂发生反应H++CH CONR +TlCl [CHCONR H]TlCl ,“反萃取”过程中加入
3 2 3 2 4
醋酸铵,则发生反应的化学方程式为[CHCONR H]TlCl +CH COONH
3 2 4 3 4
CHCOOH+CH CONR +NHTlCl 。
3 3 2 4 4
(3)根据以上分析可知“还原、氧化、沉淀”过程中TlCl 发生反应的离子方程式为HO+SO +TlCl
2
=TlCl↓+SO +2H++3Cl-。
10.(2024·广西·校联考一模·节选)NaClO 在工业生产中常用作漂白剂、脱色剂、消毒剂、拔染剂等。实
2
验室中可用HO 和NaOH混合溶液吸收ClO 的方法制取NaClO,现利用如下装置及试剂制备NaClO 晶体:
2 2 2 2 2已知:①NaClO 饱和溶液在温度低于38℃时析出的晶体是NaClO•3H O,高于38℃时析出的晶体是
2 2 2
NaClO,高于60℃时NaClO 分解成NaClO 和NaCl。
2 2 3
②ClO 气体浓度较大时易发生爆炸。
2
(2)装置A中生成ClO 的化学方程式为 。
2
【答案】
(2)
【详解】(2)利用浓硫酸、NaClO 和NaSO 制备ClO ,反应中氯元素化合价由+5变为+4被还原,则硫
3 2 3 2
元素被氧化,故亚硫酸钠被氧化为硫酸钠,反应为 ;
11.(2023·四川绵阳·统考一模·节选)电解锌的生产过程中产生大量富钴渣,主要含金属Zn、Cd及
CoO、MnO和FeO。采用以下工艺可利用富钴渣生产高纯锌:
回答下列问题:
(1)在“溶浸”中,需搅拌并控制温度85℃,其目的是 。
(2)加入HO 后生成FeOOH的化学方程式为 。
2 2
(3)“滤液①”中含有的金属离子有Cd2+、Co2+、 。
(4)“除锰钴”中,生成MnO 的离子方程式为 。
2
【答案】
(1)加快反应速率,提高溶浸率
(2)2FeSO +H O+2H O=2FeOOH↓+2H SO
4 2 2 2 2 4
(3)Zn2+、Mn2+
(4)3Mn2++2MnO +2H O=5MnO ↓+4H+
2 2
【详解】富钴渣主要含金属Zn、Cd及CoO、MnO和FeO,加入硫酸酸浸,溶解,加入过氧化氢把Fe2+氧
化成Fe3+,pH调整到5生成FeOOH沉淀,过滤后加入高锰酸钾生成MnO 和CoOOH沉淀过滤,加入Zn
2
除去溶液中的Cd2+,过滤,加入氢氧化钠,把锌溶解生成NaZnO,电解生成单质Zn,反应方程式为
2 22NaZnO+2H O=4NaOH+2Zn+O 。
2 2 2 2
(1)在“溶浸”中,温度低于85℃,温度越高反应越快,温度高于85℃有爆炸的危险,故温度控制85℃
是增加反应速率,提高溶浸率;
故答案为:加快反应速率,提高溶浸率。
(2)加入HO 后,Fe2+被氧化生成FeOOH的化学方程式为2FeSO +H O+2H O=2FeOOH↓+2H SO ;
2 2 4 2 2 2 2 4
故答案为:2FeSO +H O+2H O=2FeOOH↓+2H SO 。
4 2 2 2 2 4
(3)“滤液①”中含有富钴渣中的除铁外的其它金属离子,有Cd2+、Co2+、Zn2+、Mn2+;
故答案为:Zn2+、Mn2+。
(4)“除锰钴”中,高锰酸钾和Mn2+反应生成MnO ,离子方程式为3Mn2++2MnO
2
+2H O=5MnO ↓+4H+;
2 2
故答案为:3Mn2++2MnO +2H O=5MnO ↓+4H+。
2 2
12.(2023·河南·校联考模拟预测·节选)以某废锌渣(主要成分为 及一定量的 、 、 、
、 )为原料制备碳酸锌的工艺流程如图:
已知:相关金属离子形成氢氧化物沉淀的 如表所示:
金属离子
开始沉淀 5.5 1.3 6.5 7.0 3.3
刚好完全沉淀 8.0 3.2 9.2 8.8 4.7
回答下列问题:
(3)“浸出”时 除直接溶于硫酸外,有部分 在酸性条件下与 发生了氧化还原反应。
①“浸出”步骤中,滤渣I的主要成分除硫单质外还有 (填化学式)。
②写出在酸性条件下 与 反应的化学方程式: 。
(4)“转化”步骤中,发生的主要反应的离子方程式为 ; 的加入量高于理论值的主要原因
为 。
【答案】
(3) 、
(4) 可以催化 分解
【详解】由题给流程可知,向废锌渣中加入稀硫酸浸出时,ZnFe O 与FeS、ZnS在酸性条件下反应得到
2 4
FeSO 、ZnSO 和S沉淀,PbO溶于稀硫酸生成难溶PbSO ,Al O 溶于稀硫酸生成Al (SO ),SiO 不与稀
4 4 4 2 3 2 4 3 2
硫酸反应,过滤得到含有S、PbSO 、SiO 的滤渣Ⅰ和含有可溶性硫酸盐的滤液;向滤液中加入HO 溶液,
4 2 2 2将溶液中的Fe2+氧化为Fe3+,加入NaOH溶液调节溶液pH在4.7 pH<5.5的范围内,将溶液中的Fe3+、
Al3+转化为Fe(OH) 沉淀、Al(OH) 沉淀,过滤得到含有Fe(OH) 、Al(OH) 的滤渣Ⅱ和ZnSO 溶液;向
3 3 3⩽ 3 4
ZnSO 溶液中加入NaHCO 溶液,将溶液中Zn2+转化为ZnCO ,过滤得到ZnCO 。
4 3 3 3
(3)①由分析可知,滤渣Ⅰ的主要成分为S、PbSO 、SiO;
4 2
②由分析可知,ZnFe O 与ZnS在酸性条件下反应得到FeSO 、ZnSO、S沉淀和水,反应的化学方程式为
2 4 4 4
;
(4)由分析可知,转化步骤中向滤液中加入HO 溶液,将溶液中的Fe2+氧化为Fe3+,反应的离子方程式
2 2
为 ;HO 在反应生成的Fe3+催化作用下会分解,所以反应中过氧化氢的
2 2
加入量大于理论值;
13.(2023·四川雅安·统考模拟预测·节选)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其
氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5mol·L-1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的作用除了去除催化剂表面的油脂外,还具有作用是 (用化学方程式表示)。
为回收金属,通常用稀硫酸将“滤液①”调为中性,生成沉淀,该沉淀的化学式为
。
(2)“滤液②”中含有的金属离子除了“Ni2+”,还有 。
(3)“转化”中加入HO 的主要作用是 (用离子方程式表示)。
2 2
【答案】
(1) 、 Al(OH)
3
(2)Fe2+、Fe3+
(3)
【详解】废镍催化剂[某油脂厂废弃的油脂加氢镍催化剂(主要含金属Ni、Al、Fe及其氧化物,还有少量其
他不溶性物质)]先与氢氧化钠反应,除掉油污和铝及铝的化合物,过滤,向滤渣中加入硫酸溶解,过滤出
不溶性杂质,再向滤液中价双氧水氧化亚铁离子,再加入氢氧化钠溶液调节溶液pH值沉淀铁离子,过滤,
将滤液控制pH值浓缩结晶得到硫酸镍晶体。
(1)根据油脂厂废弃的油脂加氢镍催化剂(主要含金属Ni、Al、Fe及其氧化物),则“碱浸”中NaOH的作用是除去油脂,溶解铝及其氧化物,发生反应: 、
。为回收金属,滤液①中主要含有偏铝酸钠,用稀硫酸将“滤液①”调为中
性,发生反应::AlO +H++H O=Al(OH) ↓,生成沉淀Al(OH) ;
2 3 3
(2)滤渣①和稀硫酸反应生成硫酸铁、硫酸亚铁、硫酸镍等,因此“滤液②”中含有的金属离子是Fe3+和
Ni2+、 Fe2+;
(3)HO 作用是氧化亚铁离子,反应离子方程式为 ;
2 2
14.(2024·广西·校联考一模·节选)工业上常用炼钢残渣(主要含FeO•VO,还有少量铁粉、SiO、Al O
2 3 2 2 3
等杂质)为原料提取金属钒,其工艺流程如图所示:
已知:焙烧后铁全部转化为+3价氧化物。
(1)“研磨”的目的是 ,“磁选”后分离出的X为 。
(2)“焙烧”过程中,若转移电子数为2.5N ,则被氧化的FeO•VO 为 mol。
A 2 3
(3)“酸浸”时,生成VO 的离子方程式为 。
2 5
【答案】
(1)增大接触面,加快反应速率 铁粉
(2)0.5
(3)2VO +2H+=V O+H O
2 5 2
【详解】用炼钢残渣(主要含FeO•VO,还有少量铁粉、SiO、Al O 等杂质)为原料提取金属钒,首先残渣
2 3 2 2 3
研磨、磁选,除去铁粉,得到钒渣,钒渣加入NaCO、空气焙烧,得到氧化铁、氧化铝和NaVO ,然后
2 3 3
加入硫酸,NaVO 转化为VO,氧化铁转化为硫酸铁、氧化铝转化为硫酸铝,过滤得到VO,VO 碱溶、
3 2 5 2 5 2 5
除杂,滤液加入硫酸铵、硫酸沉钒,过滤得到偏钒酸铵,加热得到VO,进一步还原得到V,据此解答。
2 5
(1)“研磨”的目的是增大接触面,加快反应速率,“磁选”后分离出的X为铁粉。
(2)“焙烧”过程中,FeO转化为Fe O,铁由+2价转化为+3价;VO 转化为NaVO ,V由+3价升高为
2 3 2 3 3
+5价,若转移电子数为2.5N ,则被氧化的FeO•VO 为 。
A 2 3
(3)“酸浸”时,生成VO 的离子方程式为2VO +2H+=V O+H O。
2 5 2 5 215.(2023·内蒙古赤峰·统考一模)叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安
全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利
用其进一步反应制取 的流程如下:
已知:① 易溶于水,具有强还原性,易被氧化成N;
2
②一定条件下,碱性NaClO溶液与尿素溶液反应生成
(1)写出反应器1中生成水合肼的化学方程式: 。
(2)反应器2中加入无水乙醚的作用是 。
(3)已知亚硝酸乙酯的结构简式为 。写出反应器2中生成NaN 和 的化学方程式:
3
。若生成39gNaN ,则该反应中转移电子的物质的量为 。
3
(4)反应器1要控制 NaClO溶液的用量,其主要目的是 。
(5)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的 解离成OH-和H+并可
分别通过阴、阳膜定向移动。
①双极膜中产生的 (填“H⁺”或“OH-”)移向多孔铂电极。
②石墨电极反应式为 。
(6)对于反应中生成的碳酸钠,可以通过以下过程转化为亚硫酸钠。
常用作还原性漂白剂。在测定某液体葡萄糖中 残留量时,取50.0mL样品,先通入足量
Cl,再加入足量盐酸酸化的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质量为0.11g。通入足
2
量Cl 发生反应的离子方程式为 ,该样品中 残留量为 g·L−1。(以
2
SO 计,结果保留1位小数)
2
【答案】
(1)(2)降低叠氮化钠的溶解度,便于叠氮化钠结晶析出
(3) 2mol
(4)防止过量的NaClO将生成的 氧化
(5)OH-
(6) 0.6
【详解】由题给流程可知,氯气与氢氧化钠溶液在吸收塔中反应得到次氯酸钠溶液,次氯酸钠溶液与尿素
在反应器1中硫酸锰做催化剂作用下、碱性条件下反应得到含有碳酸钠、氯化钠的水合肼溶液,溶液经蒸
馏、脱盐、精制得到碳酸钠和水合肼,水合肼溶于无水乙醚后,与亚硝酸乙酯和氢氧化钠混合液在反应器
2中发生反应生成叠氮化钠和乙醇,所得反应液经过结晶、抽滤、洗涤,重结晶,制得叠氮化钠。
(1)已知,一定条件下,碱性NaClO溶液与尿素溶液反应生成 ;结合分析可知,反应器1中
反应器1中生成水合肼的反应为次氯酸钠溶液与尿素在硫酸锰做催化剂作用下,碱性条件下反应得到含有
碳酸钠、氯化钠和水合肼,反应的化学方程式为
;
(2)由题中信息可知,叠氮化钠是离子化合物,不溶于乙醚,微溶于乙醇,易溶于水,所以在反应器2中
加入无水乙醚的作用是降低叠氮化钠的溶解度,便于叠氮化钠结晶析出;
(3)由题意可知反应器2中发生的反应为水合肼与亚硝酸乙酯和氢氧化钠混合液在反应器2中发生反应生
成叠氮化钠和乙醇, ,反应则肼中氮元素化合
价由-2变为叠氮化钠中的 ,电子转移关系为 ,若反应生成39g叠氮化钠,反应中转移电
子的物质的量为 2mol;
(4)由题给信息可知,水合肼具有强还原性,易被氧化成氮气,若次氯酸钠溶液过量,会将水合肼氧化,
导致产率降低,故答案为:防止过量的NaClO将生成的 氧化;
(5)由图可知,多孔铂电极为负极,氨分子在负极失去电子发生氧化反应生成肼,石墨为正极,在水分
子作用下,次氯酸根离子在正极得到电子发生还原反应生成氯离子和氢氧根离子;
①由分析可知,多孔铂电极为负极,石墨为正极,原电池中的溶液中阴离子氢氧根离子向负极多孔铂电
极移动,故答案为:OH-;
②由分析可知,石墨为正极,氯酸根离子在正极得到电子发生还原反应生成氯离子和氢氧根离子,电极反
应式为 ;
(6)氯气具有强氧化性,通入足量Cl 将亚硫酸钠氧化为硫酸钠,同时生成氯离子,
2
;硫酸根离子和钡离子生成硫酸钡沉淀0.11g,根据硫元素守恒可知,该样品中 残留量(以SO 计)为 。
2