文档内容
热点 05 反应机理图和能量历程图
(建议用时:35分钟)
【真题再现】
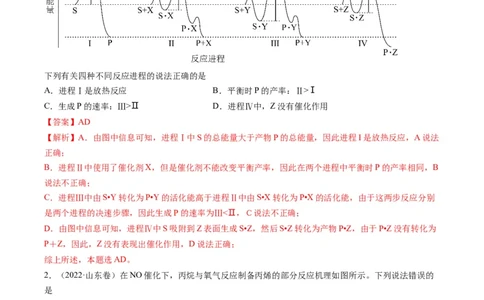
1.(2022·湖南卷)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法
正确;
B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,B
说法不正确;
C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应分别
是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;
D.由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为
P+Z,因此,Z没有表现出催化作用,D说法正确;
综上所述,本题选AD。
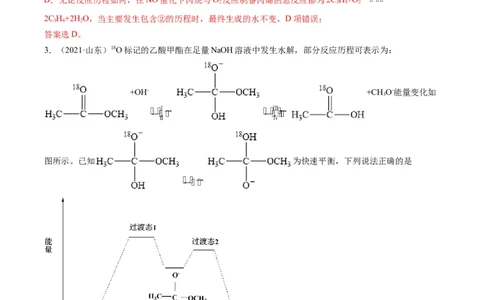
2.(2022·山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元
2 2 2 3 7 3 6 2
素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有
电子转移,A项正确;
B.根据图示,由NO生成HONO的反应历程有2种,B项正确;
C.NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;
3 8
D.无论反应历程如何,在NO催化下丙烷与O 2 反应制备丙烯的总反应都为2C 3 H 8 +O 2 NO
2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;
3 6 2
答案选D。
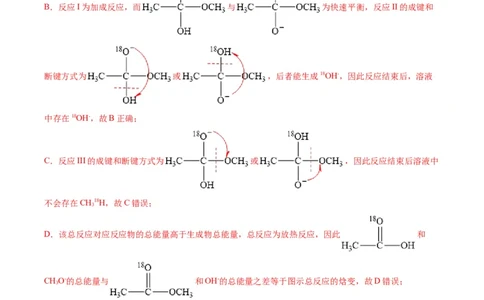
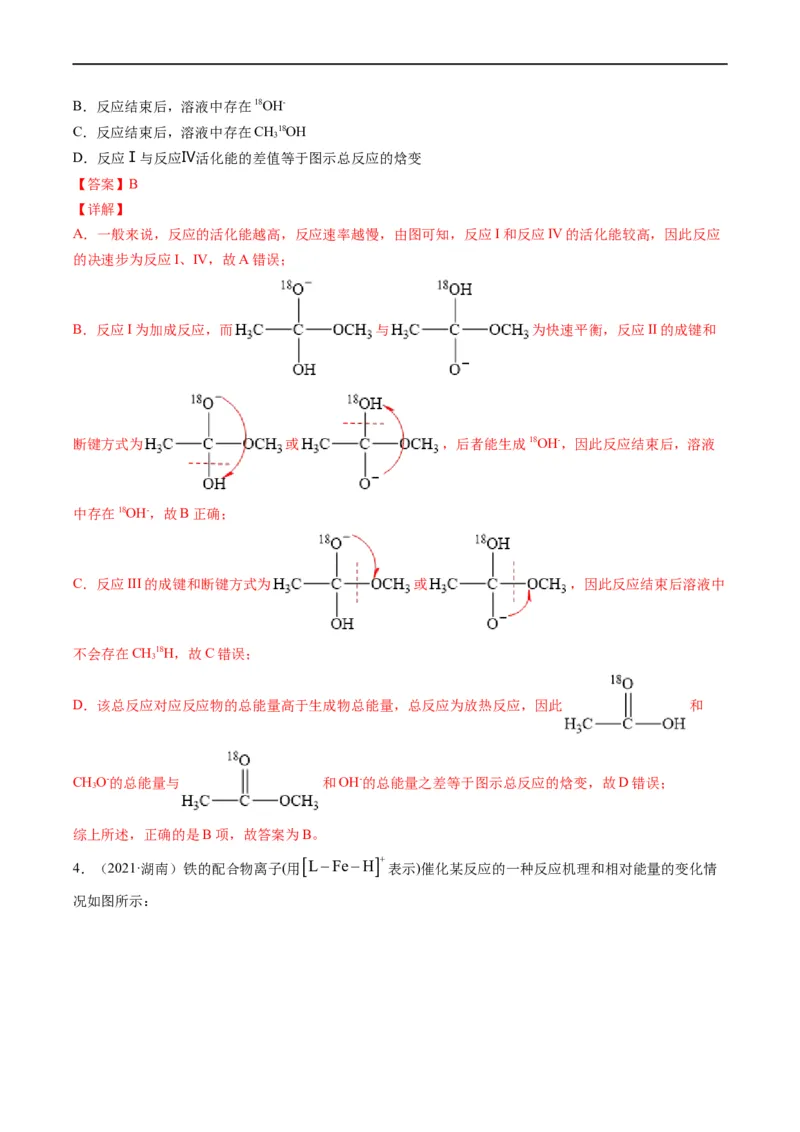
3.(2021·山东)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如
3
Ⅰ Ⅲ
Ⅱ Ⅳ
图所示。已知 为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【详解】
A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较高,因此反应
的决速步为反应I、IV,故A错误;
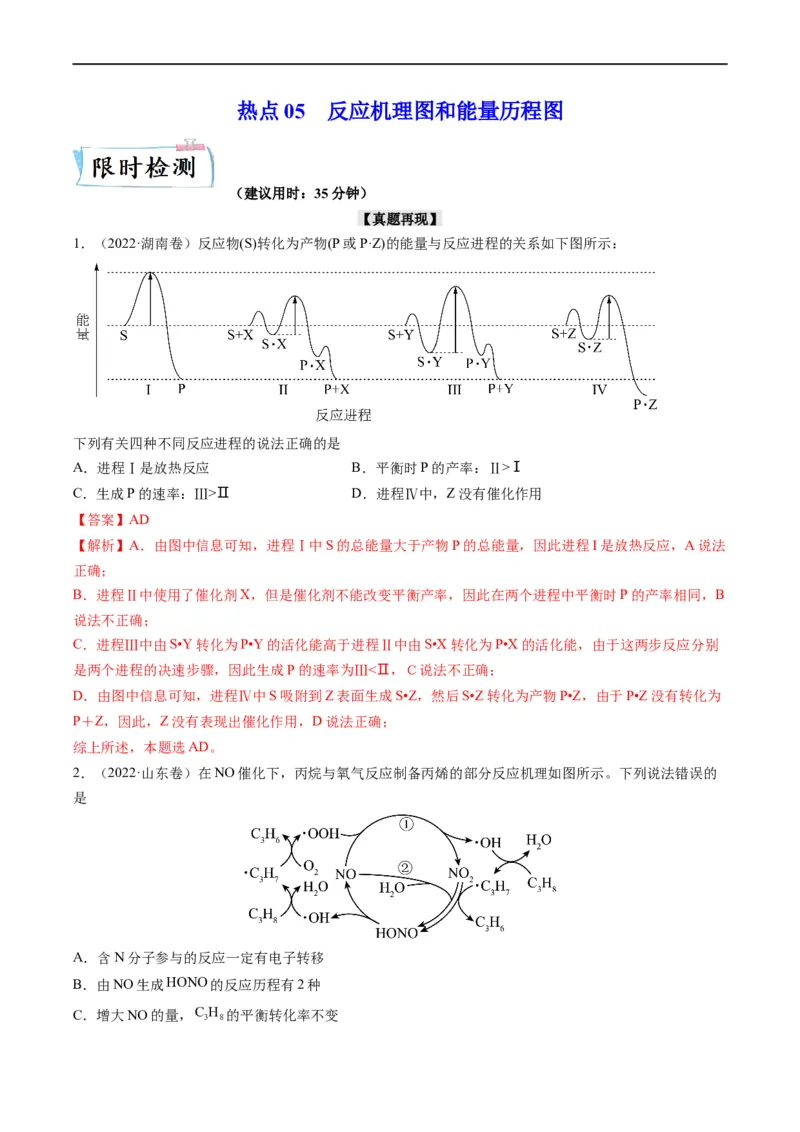
B.反应I为加成反应,而 与 为快速平衡,反应II的成键和
断键方式为 或 ,后者能生成18OH-,因此反应结束后,溶液
中存在18OH-,故B正确;
C.反应III的成键和断键方式为 或 ,因此反应结束后溶液中
不会存在CH18H,故C错误;
3
D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此 和
CHO-的总能量与 和OH-的总能量之差等于图示总反应的焓变,故D错误;
3
综上所述,正确的是B项,故答案为B。
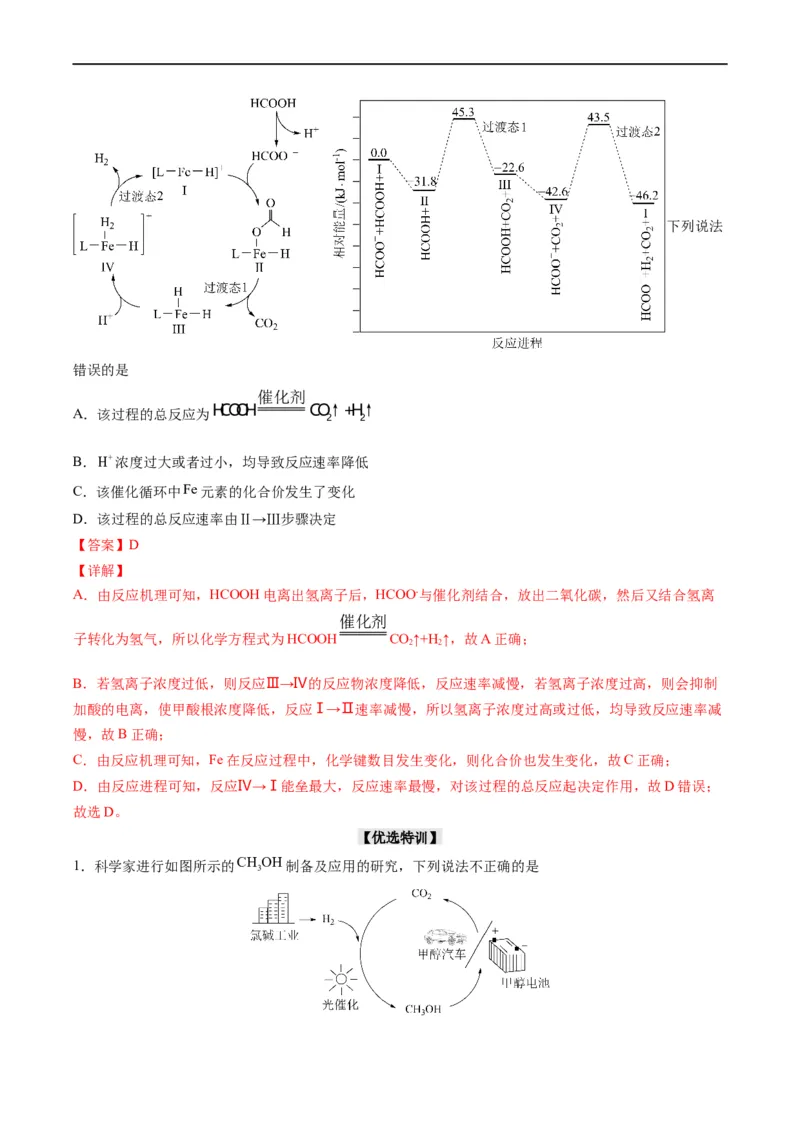
4.(2021·湖南)铁的配合物离子(用
LFeH
表示)催化某反应的一种反应机理和相对能量的变化情
况如图所示:下列说法
错误的是
催化剂
A.该过程的总反应为HCOOH CO↑+H↑
2 2
B.H浓度过大或者过小,均导致反应速率降低
C.该催化循环中Fe元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】D
【详解】
A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后又结合氢离
催化剂
子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,故A正确;
2 2
B.若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制
加酸的电离,使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减
慢,故B正确;
C.由反应机理可知,Fe在反应过程中,化学键数目发生变化,则化合价也发生变化,故C正确;
D.由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错误;
故选D。
【优选特训】
1.科学家进行如图所示的CH OH制备及应用的研究,下列说法不正确的是
3A.CH OH中C原子的杂化类型为sp3
3
B.1molCO 含有约2.26.021024个电子
2
C.CO 和H 合成甲醇符合原子利用率100%
2 2
D.图中涉及反应包含非极性键的断裂和生成
【答案】C
【详解】A.CH OH中C原子形成4个共价键,杂化类型为sp3,A正确;
3
B.1分子二氧化碳含有22个电子,则1molCO 含有电子22mol,数目约2.26.021024个电子,B正确;
2
C.CO 中碳氧原子个数为1:2,甲醇中碳氧原子个数为1:1,故CO 和H 合成甲醇原子利用率不会是
2 2 2
100%,C错误;
D.图中H 参与反应,涉及非极性键的断裂,氯碱工业生成H 和Cl 涉及非极性键的形成,D正确;
2 2 2
故选C。
2.CO 光催化反应机理如图所示,当催化剂受到能量大于禁带宽度的光照时,价带上的电子被激发,跃
2
迁到导带,同时形成空穴。导带上的光生电子( )作还原剂,价带上的光生空穴(⊕)作氧化剂,下列说法
不正确的是
A.在价带上H O被氧化 B.推测TiO 起催化作用
2 2
C.反应过程中光能转化为化学能 D.1mol CO 生成1mol CH 得到4mol电子
2 4
【答案】D
【分析】如图,在催化剂TiO 作用下,H O在价带上生成O ,其中氧元素化合价升高,H O被氧化;
2 2 2 2
CO 和H O在导带上生成CH 和CO;
2 2 4
【详解】A.如图,H O在价带上生成O ,其中氧元素化合价升高,H O被氧化,故A正确;
2 2 2
B.如图,TiO 在反应前后性质不变,可推测整个过程中可推测TiO 起催化作用,故B正确;
2 2
C.如图,该反应是在TiO 和光共同作用下进行,反应过程中光能转化为化学能,故C正确;
2
D.CO 生成CH ,C元素化合价降低8,即1mol CO 生成1mol CH 得到8mol电子,故D错误;
2 4 2 4故选D。
3.光催化剂的催化原理为:催化剂在光照下产生电子
e-
和空穴
h+
,催化剂表面的物种分别与电子和
空穴发生还原反应和氧化反应。CdS光催化甲醇 CH
3
OH 分别转化为乙二醇 CH
2
OHCH
2
OH 和甲醛
(HCHO)的原理如图所示,两种途径均有H 产生。下列说法不正确的是
2
A.CH OH 和OCH 均为反应的中间体
2 3
B.HCHO从催化剂表面脱附需吸收能量
C.途径1中产生H 的原理为2H++2e-=H
2 2
D.途径1和途径2中CH OH断裂的化学键相同
3
【答案】D
【解析】根据图像信息进行判断,物质的能量变化根据能量纵坐标进行判断,物质的断键也可通过图像进
行判断,根据图像中的转化过程判断,中间产物首先是生成后又转化,而催化剂是在第一步就参于反应。
A.根据图像中反应过程中第1步反应是生成物,第二步反应是反应物,判断是中间产物,故A说法正确;
B.根据图像判断甲醛在从催化剂表面脱附时能量由低到高,故需吸收能量;故B说法正确;
C.根据图像:途径1中甲醇分离出氢离子,故氢离子转化为氢气的电极的反应为:2H++2e-=H ;故C
2
说法正确;
D.途径1中甲醇断裂的键是碳氢键,而途径2根据图像判断断裂的键是氧氢键,故D不正确;
故选答案D。
4.(2022·河北保定·一模)苯亲电取代反应中卤代反应的反应进程与能量变化曲线如图所示,下列说法正
确的是A.反应分三步进行,且各步均为吸热反应
B.决速步的能垒是ΔE
2
C.总反应的ΔH=ΔE +ΔE +ΔE
1 2 3
D.升温既能加快反应速率,又能提高该卤代反应的平衡转化率
【答案】B
【解析】A.根据图中信息得出前两步是吸热反应,第三步是放热反应,故A错误;
B.第二步能垒最大,是整个反应的决速步,其能垒是E ,故B正确;
2
C.总反应的焓变是生成物总能量减去反应物总能量或反应物的活化能减去生成物活化能,因此
H E+E+E ,故C错误;
1 2 3
D.由于总反应是放热反应,故升温可以加快反应速率,平衡逆向移动,因此不能提高该卤代反应的平衡
转化率,故D错误。
5.(2022·北京·模拟预测)某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO、HO
2 2 2
的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列叙述错误的是( )
A.该历程中HCHO中所有的C-H键均断裂
B.该过程的总反应为HCHO+O HAPCO+H O
2 2 2
C.该反应中反应物的总能量低于生成物的总能量
D.生成物CO 中的氧原子由HCHO和O 共同提供
2 2
【答案】C
【解析】A.反应HCHO→CO ,HCHO中所有的C-H键均断裂,A项正确;
2
B.根据题干所示,反应物为HCHO和O,生成物为CO 和HO,HAP做催化剂,反应方程式为:
2 2 2
HCHO+O HAPCO+H O,B项正确;
2 2 2
点燃
C.该反应与甲醛和氧气燃烧:HCHO+O 2==CO
2
+H
2
O能量变化大致相同,甲醛燃烧为放热反应,故题中
反应也为放热反应,反应物的总能量高于生成物的总能量,C项错误;
D.根据图示反应时HCHO中C-H键均断裂,连接O 提供的一个O原子形成CO,则生成物CO 中的氧原
2 2 2
子由HCHO和O 共同提供,D项正确;
2
答案选C。
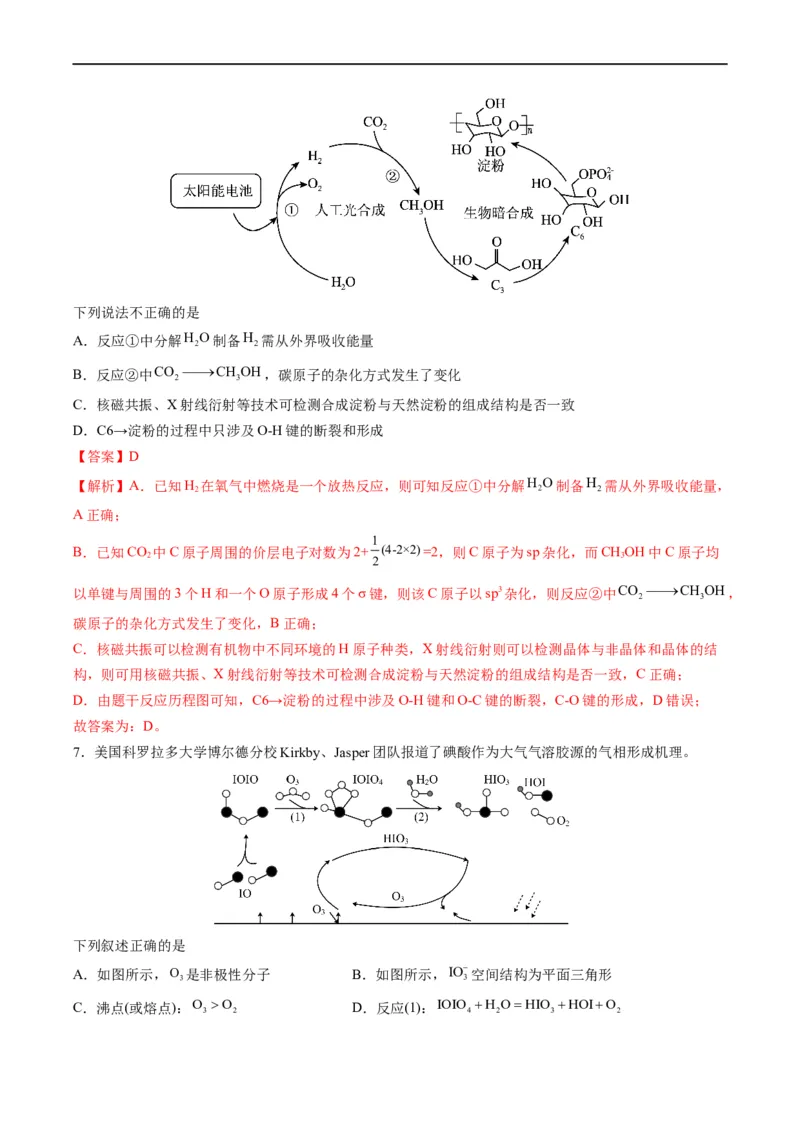
6.(2022·北京朝阳·一模)2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示
意如下:下列说法不正确的是
A.反应①中分解H O制备H 需从外界吸收能量
2 2
B.反应②中CO CH OH,碳原子的杂化方式发生了变化
2 3
C.核磁共振、X射线衍射等技术可检测合成淀粉与天然淀粉的组成结构是否一致
D.C6→淀粉的过程中只涉及O-H键的断裂和形成
【答案】D
【解析】A.已知H 在氧气中燃烧是一个放热反应,则可知反应①中分解H O制备H 需从外界吸收能量,
2 2 2
A正确;
1
B.已知CO 中C原子周围的价层电子对数为2+ (4-2×2)=2,则C原子为sp杂化,而CHOH中C原子均
2 2 3
以单键与周围的3个H和一个O原子形成4个σ键,则该C原子以sp3杂化,则反应②中CO CH OH,
2 3
碳原子的杂化方式发生了变化,B正确;
C.核磁共振可以检测有机物中不同环境的H原子种类,X射线衍射则可以检测晶体与非晶体和晶体的结
构,则可用核磁共振、X射线衍射等技术可检测合成淀粉与天然淀粉的组成结构是否一致,C正确;
D.由题干反应历程图可知,C6→淀粉的过程中涉及O-H键和O-C键的断裂,C-O键的形成,D错误;
故答案为:D。
7.美国科罗拉多大学博尔德分校Kirkby、Jasper团队报道了碘酸作为大气气溶胶源的气相形成机理。
下列叙述正确的是
A.如图所示,O 是非极性分子 B.如图所示,IO 空间结构为平面三角形
3 3
C.沸点(或熔点):O O D.反应(1):IOIO H OHIO HOIO
3 2 4 2 3 2【答案】C
【详解】A.O 是V形分子,属于极性分子,选项A错误;
3
B.IO 中Ⅰ采用sp3杂化,呈三角锥形,选项B错误:
3
C.O 、O 都是分子晶体,O 的相对分子质量大于O ,O 分子间范德华力大于O ,选项C正确;
3 2 3 2 3 2
D.根据图示,反应(1)为IOIO+O =IOIO ,选项D错误;
3 4
答案选C。
8.(2022·陕西·宝鸡市渭滨区教研室模拟预测)铁的配合物离子(用
L-Fe-H+
表示)催化某反应的一种反应
机理和相对能量的变化情况如图所示:
下列说法正确的是
催化剂
A.该过程的总反应为HCOOH CO↑+H↑且为放热反应
2 2
B.增大H+浓度一定加快反应速率
C.反应Ⅲ→Ⅳ的活化能为20.0KJ/mol
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】A
【解析】A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂Ⅰ结合生成Ⅱ,Ⅱ生成二氧化
催化剂
碳与Ⅲ,Ⅲ然后又结合氢离子转化为Ⅳ,Ⅳ生成氢气与催化剂Ⅰ,所以化学方程式为HCOOH
CO↑+H ↑,故A正确;
2 2
B.若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制
甲酸的电离,使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减
慢,故B错误;
C.由反应进程图可知,反应Ⅲ→Ⅳ的ΔH=-20.0KJ/mol,故C错误;
D.活化能越高,反应越慢。由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应
起决定作用,故D错误;故选A。
9.科研工作者通过计算机模拟和数学计算,设计出三条在含[Pt-O]结构的化合物中插入CO的反应路径,
其相对能量变化如图所示,下列说法正确的是
A.反应II中,活化能最大的能垒为39.7kJ/mol
B.根据图像分析,该历程应按照路径Ⅲ进行
C.在该反应中,CO是反应的催化剂
D.该反应为吸热反应
【答案】A
【解析】A.由图可知,反应II中,活化能最大的能垒为37.8kJ/mol-(-1.9kJ/mol)= 39.7kJ/mol,故A正确;
B.由图可知,相对与路径II和Ⅲ,路径Ⅰ的中间反应少,决速步骤的活化能最小,反应速率最快,因此
该历程应按照路径Ⅰ进行,故B错误;
C.由图可知,CO是该反应的反应物,Pt是该反应的催化剂,故C错误;
D.由图可知,反应物的总能量高于生成物的总能量,该反应为放热反应,故D错误;
答案选A。
10.(2022·陕西宝鸡·三模)我国科学家研究了不同含金化合物催化乙烯加氢[C H(g)+H(g)=C H(g)
2 4 2 2 6
H=akJ·mol-1]的反应历程如下图所示,下列说法正确的是
△
A.1molC H(g)与1molH (g)具有的能量之和小于1molC H(g)的能量
2 4 2 2 6
B.过渡态物质的稳定性:过渡态1>过渡态2
C.该反应的焓变:ΔH=—129.6kJ·mol-1D.相应的活化能:催化剂AuF<催化剂AuPF+
3
【答案】C
【解析】A.由图可知,该反应为反应物总能量高于生成物的总能量的放热反应,故A错误;
B.由图可知,过渡态1的相对能量高于过渡态2,物质的能量越高,越不稳定,所以过渡态1的稳定性小
于过渡态2,故B错误;
C.由图可知,反应的焓变ΔH=—[0—(—129.6kJ·mol-1)]=—129.6kJ·mol-1,故C正确;
D.由图可知,催化剂AuF、催化剂AuPF+的活化能分别为109.34 kJ·mol-1、26.3 kJ·mol-1,则催化剂AuF
3
的活化能大于催化剂AuPF+,故D错误;
3
故选C。
11.(2022·浙江金华·二模)如图表示氯自由基与甲烷反应生成氯甲烷的两步链反应的势能变化,下列说
法正确的是
A.第二步链反应的ΔH =105.4kJmol1
2
B.第二步链反应决定了总反应的反应速率
C.第一步链反应还存在一种可能的反应,产物为CH ClH,该反应之所以未发生可能是因为其活化能
3
相对过高
D.由图可知,两步链反应均为放热反应反应进程
【答案】C
【解析】A.根据图示可知第二步链反应的ΔH =112.9kJmol1,A错误;
2
B.多步反应的总反应速率由活化能大的慢反应决定。根据图示可知第一步反应的活化能大于第二步,因
此第一步链反应决定了总反应的反应速率,B错误;
C.反应的活化能越大,反应就越不容易发生,根据物质反应方式可知第一步链反应还存在一种可能的反
应,产物为CH ClH,该反应之所以未发生可能是因为其活化能相对过高,C正确;
3
D.第一步反应中生成物能量高于反应物,反应属于吸热反应;第二步反应中反应物的能量比生成物的高,
反应为放热反应,可见两步反应中第一步为吸热反应,第二步为放热反应,D错误;故合理选项是C。
12.联氨(N H)可用于处理水中的溶解氧,其反应机理如下图所示:
2 4
下列说法不正确的是
A.N H 分子的共价键只有sp键
2 4
B.N H 具有还原性,在一定条件下可被O 氧化
2 4 2
C.②中反应产物是CuNH 而不是CuNH ,说明CuNH 相对较稳定
3 2 3 4 3 2
D.③中发生反应:4CuNH O 8NH H O4CuNH 2 4OH6H O
3 2 2 3 2 3 4 2
【答案】A
sp pp
【详解】A.NH 分子的共价键有N-H之间的 键和N-N之间的 ,A错误;
2 4
B.由题干信息可知,NH 能够被CuO氧化生成N,即NH 具有还原性,而O 的氧化性强于CuO,故
2 4 2 2 4 2
NH 具有还原性,在一定条件下可被O 氧化,B正确;
2 4 2
C.由题干信息可知,②中反应物NH
3
‧H
2
O是足量的,但是反应产物是
CuNH
3
2
而不是
CuNH
3
4
,
说明CuNH 相对较稳定,C正确;
3 2
D.根据氧化还原反应配平可知,③中发生反应:
4CuNH O 8NH H O4CuNH 2 4OH6H O,D正确;
3 2 2 3 2 3 4 2
故答案为:A。
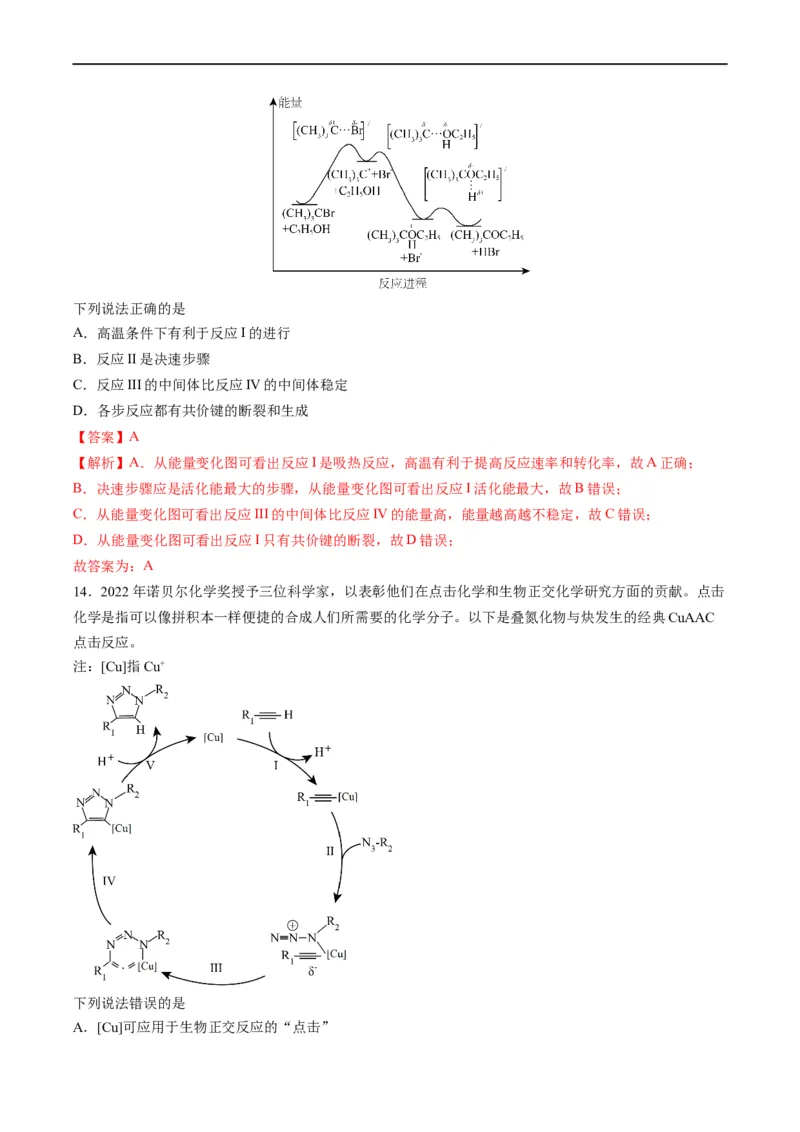
13.卤代烃可以和乙醇反应生成醚,反应历程可表示如图:
能量变化如图所示,下列说法正确的是
A.高温条件下有利于反应I的进行
B.反应II是决速步骤
C.反应III的中间体比反应IV的中间体稳定
D.各步反应都有共价键的断裂和生成
【答案】A
【解析】A.从能量变化图可看出反应I是吸热反应,高温有利于提高反应速率和转化率,故A正确;
B.决速步骤应是活化能最大的步骤,从能量变化图可看出反应I活化能最大,故B错误;
C.从能量变化图可看出反应III的中间体比反应IV的能量高,能量越高越不稳定,故C错误;
D.从能量变化图可看出反应I只有共价键的断裂,故D错误;
故答案为:A
14.2022年诺贝尔化学奖授予三位科学家,以表彰他们在点击化学和生物正交化学研究方面的贡献。点击
化学是指可以像拼积本一样便捷的合成人们所需要的化学分子。以下是叠氮化物与炔发生的经典CuAAC
点击反应。
注:[Cu]指Cu+
下列说法错误的是
A.[Cu]可应用于生物正交反应的“点击”B.反应中要保护[Cu],防止其氧化或歧化
C.分别在两个待拼接分子中引入叠氨基与炔基,在[Cu]的“点击”下,可完成分子的拼接
D.在反应历程中,存在共价键的断裂与离子键的生成
【答案】D
【详解】A.根据题意,[Cu]可应用于生物正交反应的“点击”,A正确;
B.Cu+易被氧化和发生歧化反应,反应中要保护[Cu],防止其氧化或歧化,B正确;
C.根据经典CuAAC点击反应历程,在[Cu]的“点击”下,完成了叠氮化物与炔分子的拼接,C正确;
D.根据反应历程图,Cu+与炔分子反应使≡C-H中的C-H键断裂以及后续反应中旧的共价键断裂和新的共
价键生成,整个历程中无阴阳离子构成的离子化合物,[Cu]与有机物以短线即共价键结合,则没有离子键
的生成,D错误;
答案选D。
15.某科研团队利用缺陷工程(贫氧环境焙烧)制备了含有大量氧缺陷和表面羟基的α-Fe O ,该α-Fe O 参
2 3 2 3
与如图所示的NO还原。下列说法正确的是
x
A.α-Fe O 为该过程的氧化剂
2 3
B.图中总反应可能为4NH 4NOO 4N 6H O
3 2 2 2
C.整个流程中含铁元素的物质中铁的化合价均相同
D.该催化合成时,溶液的pH越小越好
【答案】B
【详解】A.由图可知,先加入了Fe O 后又生成了Fe O ,Fe O 为该过程的催化剂,A项错误;
2 3 2 3 2 3
B.由图可知,该反应过程是NH 和NO、O 反应生成N 和HO,方程式为:
3 2 2 2
4NH 4NOO 4N 6H O,故B正确;
3 2 2 2C.整个流程中发生了氧化还原反应,铁的化合价发生了变化,C项错误;
D.Fe O 会与H发生反应,溶液的pH越小, D项错误;
2 3
故选B。
16.我们要给子孙后代留下绿水青山等最美好的生态环境,就必须对污水进行处理。用电解法(图Ⅰ)可以
对同时含有NH和PO3的生活污水进行处理,除去NH的原理如图Ⅱ所示,除PO3是将其转化为
4 4 4 4
Fe PO 沉淀。实验在NH和PO3联合脱除过程中,测得溶液pH变化如图Ⅲ所示。
3 4 2 4 4
下列说法正确的是
A.在0~20min时,a为电源的正极
B.除NH时,阴极附近的pH减小
4
C.除NH时,阳极反应为:2NH 6e=N 8H
4 4 2
D.除PO3过程中的总离子反应式为:3Fe6H2PO3=Fe PO 3H
4 4 3 4 2 2
【答案】D
【详解】A.0-20min,若a为正极,铁就作阳极,失电子变为了Fe2,与磷酸根产生沉淀。阴极为石墨,
属于惰性电极,水放电,产生OH,溶液pH升高,与图像不符,故A错误;
B.除NH
4
时,阳极氯离子放电生成氯气,阴极是H
2
O放电,局部产生大量 OH,阴极附近的pH增大,
故B错误;
C.除NH时,阳极氯离子放电生成氯气,阳极反应为2Cl2e=Cl ,故C错误;
4 2
D.除PO3 时,铁就作阳极,失电子变为了Fe2,与磷酸根产生沉淀,阴极为石墨,氢离子得电子生成氢
4
气,总离子反应式为:3Fe6H2PO3=Fe PO 3H ,故D正确;
4 3 4 2 2
选D。