文档内容
热点强化练 14 速率常数与化学平衡常数综合分析
1.(2020·重庆月考)丙酮的碘代反应CH COCH +I ―→CH COCH I+HI的速
3 3 2 3 2
率方程为v=kcm(CH COCH )cn(I ),其半衰期(当剩余反应物恰好是起始的一半时
3 3 2
所需的时间)为0.7/k改变反应物浓度时,反应的瞬时速率如表所示。
c(CH COCH )/mol·L-1 c(I )/mol·L-1 v/10-3 mol·L-1·min-1
3 3 2
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是( )
A.速率方程中的m=1、n=1
B.该反应的速率常数k=2.8×10-3 min-1
C.增大I 的浓度,反应的瞬时速率加快
2
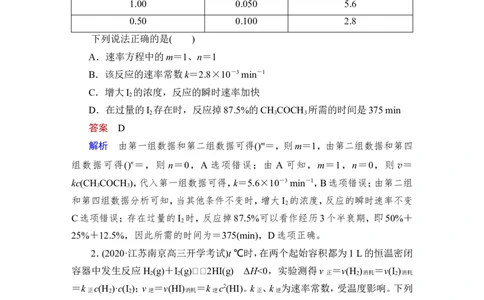
D.在过量的I 存在时,反应掉87.5%的CH COCH 所需的时间是375 min
2 3 3
答案 D
解析 由第一组数据和第二组数据可得()m=,则m=1,由第二组数据和第四
组数据可得()n=,则 n=0,A 选项错误;由 A 可知,m=1,n=0,则 v=
kc(CH COCH ),代入第一组数据可得,k=5.6×10-3 min-1,B选项错误;由第二组
3 3
和第四组数据分析可知,当其他条件不变时,增大I 的浓度,反应的瞬时速率不变
2
C选项错误;存在过量的I 时,反应掉87.5%可以看作经历3个半衰期,即50%+
2
25%+12.5%,因此所需的时间为=375(min),D选项正确。
2.(2020·江苏南京高三开学考试)t ℃时,在两个起始容积都为1 L的恒温密闭
容器中发生反应H (g)+I (g)2HI(g) ΔH<0,实验测得v =v(H ) =v(I )
2 2 正 2 消耗 2 消耗
=k c(H )·c(I );v =v(HI) =k c2(HI)。k 、k 为速率常数,受温度影响。下列
正 2 2 逆 消耗 逆 正 逆
说法正确的是( )
物质的起始浓度/(mol/L) 物质的平衡浓度/(mol/L)
容器
c(H ) c(I ) c(HI) c(I )
2 2 2
Ⅰ(恒容) 0.1 0.1 0 0.07
Ⅱ(恒压) 0 0 0.8
A.平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为4∶1
B.平衡时,容器Ⅱ中c(I )>0.28 mol/L
2
C.t ℃吋,反应H (g)+I (g)2HI(g)的平衡常数为K=
2 2D.平衡时,向容器Ⅰ中再通入0.1 mol H 、0.1 mol I 和0.2 mol HI,此时v >v
2 2 正
逆
答案 C
解析 H (g)+I (g)2HI(g),反应前后气体分子总数不变,容器Ⅰ、Ⅱ等温等
2 2
体积,则气体压强之比为物质的量之比,从投料看,容器Ⅱ的量为容器Ⅰ的4倍,
故平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1∶4,A错误;结合反应特点和投料
看,容器Ⅰ、Ⅱ的平衡为等效平衡,则平衡时容器Ⅰ中c(I )=0.07 mol/L,Ⅱ中c(I )
2 2
=0.28 mol/L,B 错误;平衡时,v =v ,已知 v =v(H ) =v(I ) =k
正 逆 正 2 消耗 2 消耗 正
c(H )·c(I );v =v(HI) =k c2(HI),则平衡时, k c(H )·c(I )=k c2(HI),则t ℃
2 2 逆 消耗 逆 正 2 2 逆
吋,反应H (g)+I (g)2HI(g)的平衡常数为:K=, K=,则C正确;平衡时,向容
2 2
器Ⅰ中再通入0.1 mol H 、0.1 mol I 和0.2 mol HI,等效于增压,则平衡不移动,此
2 2
时v =v ,D错误。
正 逆
3.(2020·山东中区济南外国语学校高三月考)某温度下,在起始压强为80 kPa
的刚性容器中,发生NO的氧化反应:2NO(g)+O (g)2NO (g) ΔH,该反应的
2 2
反应历程分两步进行,其速率方程和反应过程中能量变化如下:
①2NO(g)N O (g) v =k c2(NO)
2 2 1正 1正
v =k c(N O )
1逆 1逆 2 2
②N O (g)+O (g)2NO (g)
2 2 2 2
v =k c(N O )·c(O ) v =k c2(NO )
2正 2正 2 2 2 2逆 2逆 2
下列说法正确的是( )
A.NO氧化反应速率快慢的决定步骤的活化能是E —E
5 3
B.一定温度下,2NO(g)+O (g)2NO (g)平衡常数表达式K=
2 2
C.升高温度,NO氧化反应的化学平衡向正反应方向移动
D.该温度下,将等物质的量的NO和O 混合反应(忽略2NO N O ),NO的
2 2 2 4
平衡转化率为40%时,该反应的平衡常数K = kPa-1
p
答案 B
解析 整体的反应速率取决于慢反应,活化能越大,反应速率越慢,据图可知活化能大的步骤为第二步反应,活化能为 E —E ,故 A 错误;2NO(g)+
4 2
O (g)2NO (g)平衡常数表达式K==·,而对于反应①平衡时正逆反应速率相
2 2
等,即k c2(NO)=k c(N O ),所以K ==,同理可得反应②的平衡常数K ==,
1正 1逆 2 2 1 2
所以K=K ·K =,故B正确;据图可知该反应的反应物总能量高于生成物总能量,
1 2
所以为放热反应,升高温度,平衡逆向移动,故C错误;设等物质的量的NO和O
2
分别为40 mol,NO的平衡转化率为40%,列三段式有
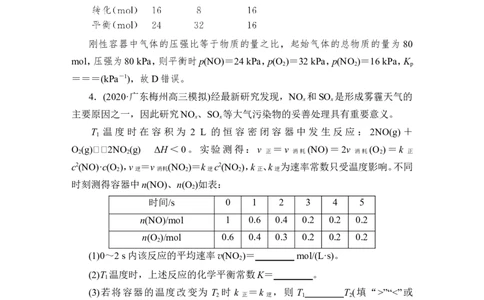
刚性容器中气体的压强比等于物质的量之比,起始气体的总物质的量为 80
mol,压强为80 kPa,则平衡时p(NO)=24 kPa,p(O )=32 kPa,p(NO )=16 kPa,K
2 2 p
===(kPa-1),故D错误。
4.(2020·广东梅州高三模拟)经最新研究发现,NO 和SO 是形成雾霾天气的
x x
主要原因之一,因此研究NO 、SO 等大气污染物的妥善处理具有重要意义。
x x
T 温 度 时 在 容 积 为 2 L 的 恒 容 密 闭 容 器 中 发 生 反 应 : 2NO(g) +
1
O (g)2NO (g) ΔH<0。实验测得:v =v (NO)=2v (O )=k
2 2 正 消耗 消耗 2 正
c2(NO)·c(O ),v =v (NO )=k c2(NO ),k 、k 为速率常数只受温度影响。不同
2 逆 消耗 2 逆 2 正 逆
时刻测得容器中n(NO)、n(O )如表:
2
时间/s 0 1 2 3 4 5
n(NO)/mol 1 0.6 0.4 0.2 0.2 0.2
n(O )/mol 0.6 0.4 0.3 0.2 0.2 0.2
2
(1)0~2 s内该反应的平均速率v(NO )=________ mol/(L·s)。
2
(2)T 温度时,上述反应的化学平衡常数K=________。
1
(3)若将容器的温度改变为 T 时 k =k ,则 T ________T (填“>”“<”或
2 正 逆 1 2
“=”)。
答案 (1)0.15 mol·L-1·s-1 (2)160 (3)<
解析 (1)由表中数据可知,0~2 s内反应的平均速率v(NO)==0.15 mol·L-
1·s-1,根据同一反应中各物质的速率之比等于化学计量数之比,则v(NO )=v(NO)
2
=0.15 mol·L-1·s-1。
(2)由表中数据,可知c(NO) ==0.5 mol·L-1,c(O ) ==0.3 mol·L-1,平衡
起始 2 起始
时,c(NO)=c(O )==0.1 mol·L-1,c(NO )==0.4 mol·L-1,利用三段式计算平衡常
2 2数:
K===160 (mol·L-1)-1
(3)若将容器的温度改变为T 时其k =k ,则K=1<160,因反应2NO(g)+
2 正 逆
O (g)2NO (g) ΔH<0,K值减小,则对应的温度增大,即T >T 。
2 2 2 1
5.(2020·山东泰安高三三模)雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮
氧化物(NO )、CO、SO 等。化学在解决雾霾污染问题中有着重要的作用。
x 2
若反应2NO(g)+2CO(g)N (g)+2CO (g)的正、逆反应速率分别可表示为v
2 2
=k c2(NO)·c2(CO);v =k c(N )·c2(CO ),k 、k 分别为正、逆反应速率常数,c
正 正 逆 逆 2 2 正 逆
为物质的量浓度。一定温度下,在体积为1 L的恒容密闭容器中加入4 mol NO和
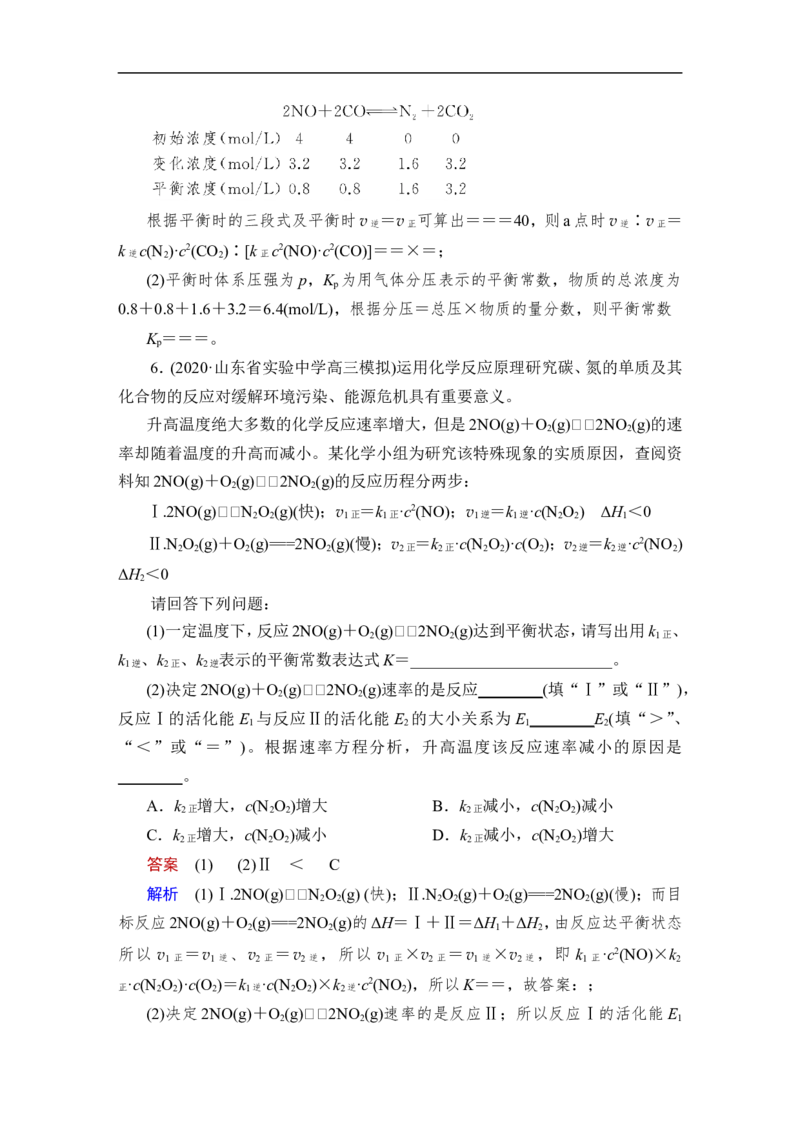
4 mol CO发生上述反应,测得CO和CO 的物质的量浓度随时间的变化如图所示。
2
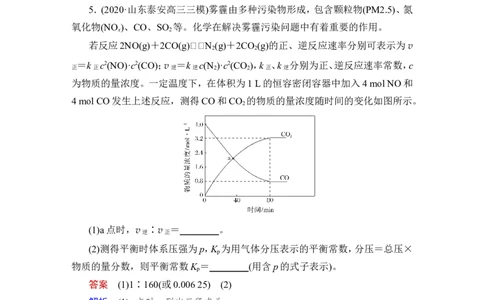
(1)a点时,v ∶v =________。
逆 正
(2)测得平衡时体系压强为p,K 为用气体分压表示的平衡常数,分压=总压×
p
物质的量分数,则平衡常数K =________(用含p的式子表示)。
p
答案 (1)1∶160(或0.006 25) (2)
解析 (1)a点时,列出三段式为:
因为CO和CO 的物质的量浓度相等,即4-x=x,解得x=2;
2
平衡时有:根据平衡时的三段式及平衡时v =v 可算出===40,则a点时v ∶v =
逆 正 逆 正
k c(N )·c2(CO )∶[k c2(NO)·c2(CO)]==×=;
逆 2 2 正
(2)平衡时体系压强为p,K 为用气体分压表示的平衡常数,物质的总浓度为
p
0.8+0.8+1.6+3.2=6.4(mol/L),根据分压=总压×物质的量分数,则平衡常数
K ===。
p
6.(2020·山东省实验中学高三模拟)运用化学反应原理研究碳、氮的单质及其
化合物的反应对缓解环境污染、能源危机具有重要意义。
升高温度绝大多数的化学反应速率增大,但是2NO(g)+O (g)2NO (g)的速
2 2
率却随着温度的升高而减小。某化学小组为研究该特殊现象的实质原因,查阅资
料知2NO(g)+O (g)2NO (g)的反应历程分两步:
2 2
Ⅰ.2NO(g)N O (g)(快);v =k ·c2(NO);v =k ·c(N O ) ΔH <0
2 2 1正 1正 1逆 1逆 2 2 1
Ⅱ.N O (g)+O (g)===2NO (g)(慢);v =k ·c(N O )·c(O );v =k ·c2(NO )
2 2 2 2 2正 2正 2 2 2 2逆 2逆 2
ΔH <0
2
请回答下列问题:
(1)一定温度下,反应2NO(g)+O (g)2NO (g)达到平衡状态,请写出用k 、
2 2 1正
k 、k 、k 表示的平衡常数表达式K=_________________________。
1逆 2正 2逆
(2)决定2NO(g)+O (g)2NO (g)速率的是反应________(填“Ⅰ”或“Ⅱ”),
2 2
反应Ⅰ的活化能 E 与反应Ⅱ的活化能 E 的大小关系为 E ________E (填“>”、
1 2 1 2
“<”或“=”)。根据速率方程分析,升高温度该反应速率减小的原因是
________。
A.k 增大,c(N O )增大 B.k 减小,c(N O )减小
2正 2 2 2正 2 2
C.k 增大,c(N O )减小 D.k 减小,c(N O )增大
2正 2 2 2正 2 2
答案 (1) (2)Ⅱ < C
解析 (1)Ⅰ.2NO(g)N O (g) (快);Ⅱ.N O (g)+O (g)===2NO (g)(慢);而目
2 2 2 2 2 2
标反应2NO(g)+O (g)===2NO (g)的ΔH=Ⅰ+Ⅱ=ΔH +ΔH ,由反应达平衡状态
2 2 1 2
所以 v =v 、v =v ,所以 v ×v =v ×v ,即 k ·c2(NO)×k
1正 1逆 2正 2逆 1正 2正 1逆 2逆 1正 2
·c(N O )·c(O )=k ·c(N O )×k ·c2(NO ),所以K==,故答案:;
正 2 2 2 1逆 2 2 2逆 2
(2)决定2NO(g)+O (g)2NO (g)速率的是反应Ⅱ;所以反应Ⅰ的活化能E
2 2 1远小于反应Ⅱ的活化能E ;决定反应速率的是慢反应Ⅱ,而温度越高k 增大,反
2 2正
应速率加快,N O 的浓度减少,故C符合题意。
2 2
7.(2020·福建厦门市高三模拟)乙烯、环氧乙烷是重要的化工原料,用途广泛。
实验测得2CH ===CH (g)+O (g)2 (g) ΔH<0中,v =k c2( ),v =k
2 2 2 逆 逆 正
·c2(CH ===CH )·c(O )(k 、k 为速率常数,只与温度有关)。
正 2 2 2 正 逆
(1)反应达到平衡后,仅降低温度,下列说法正确的是( )
A.k 、k 均增大,且k 增大的倍数更多
正 逆 正
B.k 、k 均减小,且k 减小的倍数更少
正 逆 正
C.k 增大、k 减小,平衡正向移动
正 逆
D.k 、k 均减小,且k 减小的倍数更少
正 逆 逆
(2)若在1 L的密闭容器中充入1 mol CH ===CH (g)和1 mol O (g),在一定温
2 2 2
度下只发生上述反应,经过 10 min反应达到平衡,体系的压强变为原来的 0.875
倍,则0~10 min内v(O )=________,=________。
2
答案 ①B ②0.025 mol·L-1·min-1 0.75
解析 ①该反应是放热反应,反应达到平衡后,仅降低温度,速率降低,k 、k
正
均减小,平衡向放热方向即正向进行,正反应速率大于逆反应速率,因此k 减小
逆 正
的倍数更少。
=0.875,x=0.25 mol,则0~10 min内v===0.025 mol·L-1·min-1,k c2( )
逆
=k ·c2(CH ===CH )·c(O ),==0.75。
正 2 2 2
8.(2020·河南安阳市高三二模)碳、氮能形成多种氧化物、氢化物。
化学动力学上将一步完成的反应称为基元反应。对于基元反应:aA+bB→cC
+dD,其速率方程式为v=k·ca(A)·cb(B)(k为只与温度有关的速率常数),复杂反应
(由几个基元反应构成)的速率取决于慢的基元反应。
①已知反应NO (g)+CO(g)NO(g)+CO (g) ΔH<0,在温度低于250 ℃时
2 2
是由两个基元反应构成的复杂反应,该反应的速率方程式为v=k·c2(NO ),则其两
2
个基元反应分别为:Ⅰ.________===NO +________;Ⅱ.略,这两个反应中活化能
3
较小的是________。②某科研小组测得380 ℃时该反应的c(NO )、c(CO)生成CO 的速率[v(CO )]
2 2 2
的关系如下:
c(CO)/(mol·L-1) 0.025 0.05 0.025
c(NO )/(mol·L-1) 0.04 0.04 0.12
2
v(CO )/(mol·L-1·s-1) 2.2×10-4 4.4×10-4 6.6×10-4
2
则该温度下的反应速率常数k=________ L·mol-1·s-1。
答案 ①2NO NO Ⅱ ②0.22
2
解析 ①温度低于250 ℃时,该反应的速率方程式为v=k·c2(NO ),说明NO
2 2
和CO不参与同一个基元反应,且NO 参与的基元反应为慢反应,决定了该反应的
2
反应速率,基元反应Ⅰ中产物有NO ,根据元素守恒可知该基元反应反应物应为
3
NO ,则该基元反应Ⅰ为:2NO ===NO +NO;活化能越大,反应速率越慢,基元反
2 2 3
应Ⅰ决定整个反应速率,说明反应Ⅰ活化能较大,即反应Ⅱ活化能较小;②根据表
格分析可知CO和NO 的浓度均会影响反应速率,由于该反应不是基元反应,可设
2
该反应的正反应速率v=k·cx(NO )·cy(CO),将表格中相应数据代入有
2
联立可解得x=1,y=1,k=0.22 L·mol-1·s-1。