文档内容
热点强化练 15 弱电解质的图像分析与电离常数计算
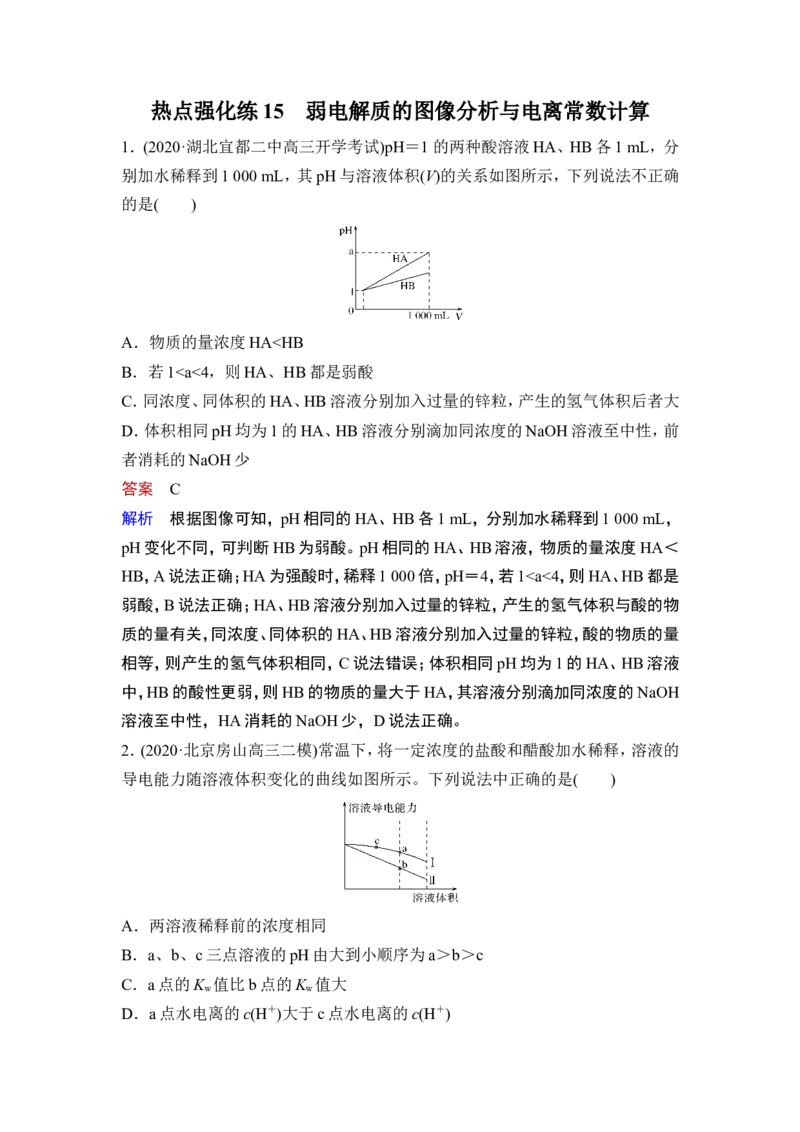
1.(2020·湖北宜都二中高三开学考试)pH=1 的两种酸溶液HA、HB各1 mL,分
别加水稀释到1 000 mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确
的是( )
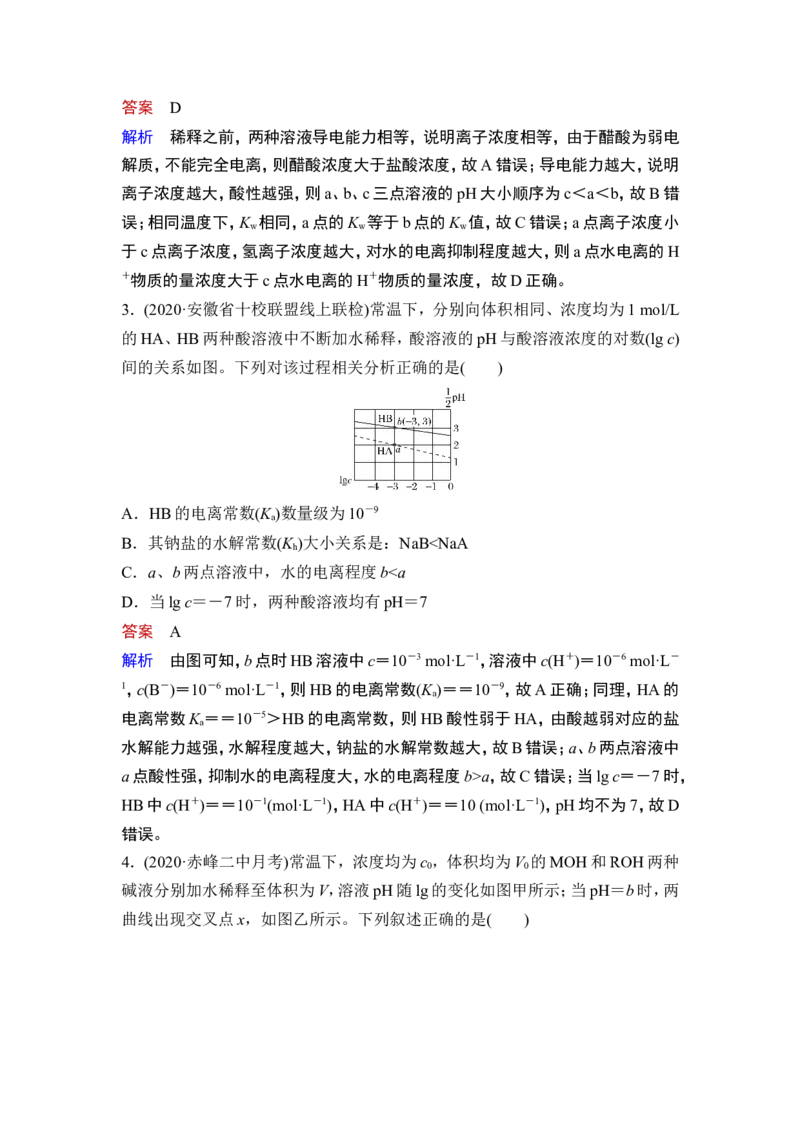
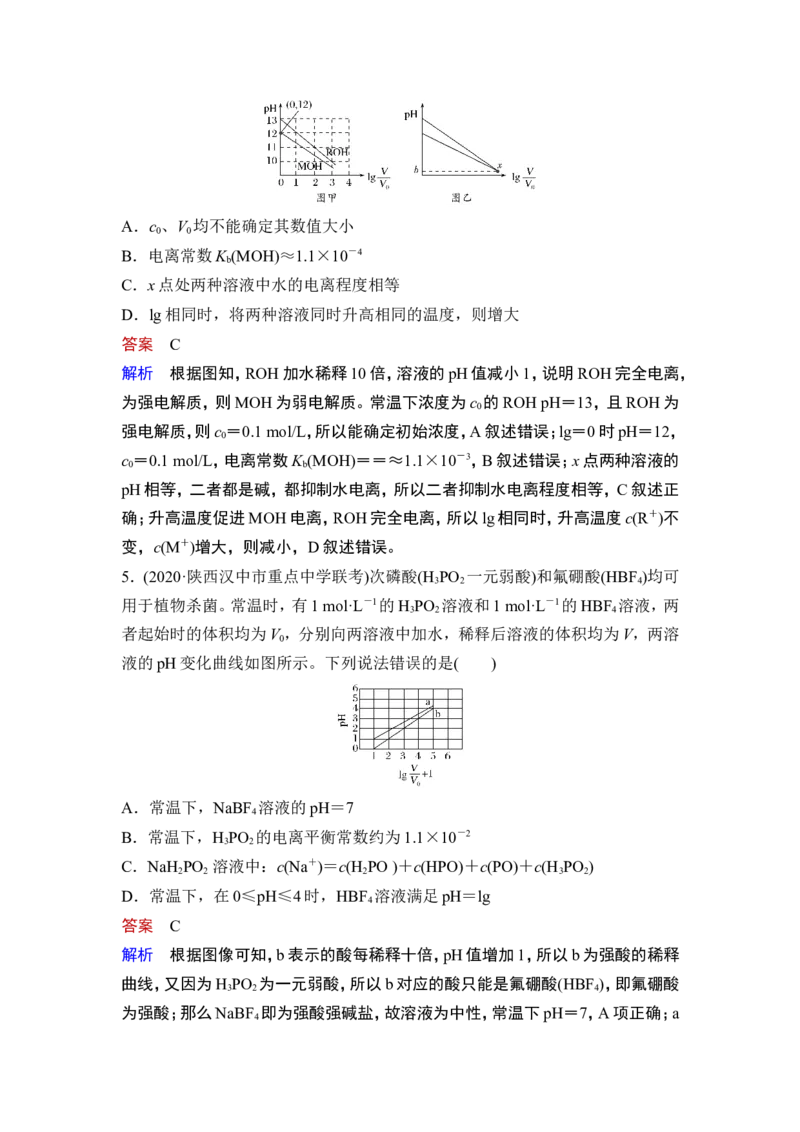
A.物质的量浓度HAa,故C错误;当lg c=-7时,
HB中c(H+)==10-1(mol·L-1),HA中c(H+)==10 (mol·L-1),pH均不为7,故D
错误。
4.(2020·赤峰二中月考)常温下,浓度均为c ,体积均为V 的MOH和ROH两种
0 0
碱液分别加水稀释至体积为V,溶液pH随lg的变化如图甲所示;当pH=b时,两
曲线出现交叉点x,如图乙所示。下列叙述正确的是( )A.c 、V 均不能确定其数值大小
0 0
B.电离常数K (MOH)≈1.1×10-4
b
C.x点处两种溶液中水的电离程度相等
D.lg相同时,将两种溶液同时升高相同的温度,则增大
答案 C
解析 根据图知,ROH加水稀释10倍,溶液的pH值减小1,说明ROH完全电离,
为强电解质,则MOH为弱电解质。常温下浓度为c 的ROH pH=13,且ROH为
0
强电解质,则c =0.1 mol/L,所以能确定初始浓度,A叙述错误;lg=0时pH=12,
0
c =0.1 mol/L,电离常数K (MOH)==≈1.1×10-3,B叙述错误;x点两种溶液的
0 b
pH相等,二者都是碱,都抑制水电离,所以二者抑制水电离程度相等,C叙述正
确;升高温度促进MOH电离,ROH完全电离,所以lg相同时,升高温度c(R+)不
变,c(M+)增大,则减小,D叙述错误。
5.(2020·陕西汉中市重点中学联考)次磷酸(H PO 一元弱酸)和氟硼酸(HBF )均可
3 2 4
用于植物杀菌。常温时,有1 mol·L-1的H PO 溶液和1 mol·L-1的HBF 溶液,两
3 2 4
者起始时的体积均为V ,分别向两溶液中加水,稀释后溶液的体积均为V,两溶
0
液的pH变化曲线如图所示。下列说法错误的是( )
A.常温下,NaBF 溶液的pH=7
4
B.常温下,H PO 的电离平衡常数约为1.1×10-2
3 2
C.NaH PO 溶液中:c(Na+)=c(H PO )+c(HPO)+c(PO)+c(H PO )
2 2 2 3 2
D.常温下,在0≤pH≤4时,HBF 溶液满足pH=lg
4
答案 C
解析 根据图像可知,b表示的酸每稀释十倍,pH值增加1,所以b为强酸的稀释
曲线,又因为H PO 为一元弱酸,所以b对应的酸只能是氟硼酸(HBF ),即氟硼酸
3 2 4
为强酸;那么NaBF 即为强酸强碱盐,故溶液为中性,常温下pH=7,A项正确;a
4曲线表示的是次磷酸的稀释曲线,由曲线上的点的坐标可知,1 mol/L的次磷酸溶
液的pH=1,即c(H+)=0.1 mol/L;次磷酸电离方程式为:H PO H++H PO,所
3 2 2
以1 mol/L的次磷酸溶液中c(H PO )=0.9 mol/L,c(H PO)=0.1 mol/L,那么次磷
3 2 2
酸的电离平衡常数即为:K ==≈1.1×10-2,B项正确;次磷酸为一元弱酸,H PO
a 2
无法继续电离,溶液中并不含有HPO和PO两类离子;此外,H PO还会发生水解
2
产生次磷酸分子,所以上述等式错误,C项错误;令y=pH,x=lg+1,由图可知,
在0≤pH≤4区间内,y=x-1,代入可得pH=lg,D项正确。
6.(2021·1月重庆市学业水平选择考适应性测试,13)草酸H C O 是二元弱酸。向
2 2 4
100 mL 0.40 mol/L H C O 溶液中加入1.0 mol/L NaOH溶液调节pH,加水控制溶
2 2 4
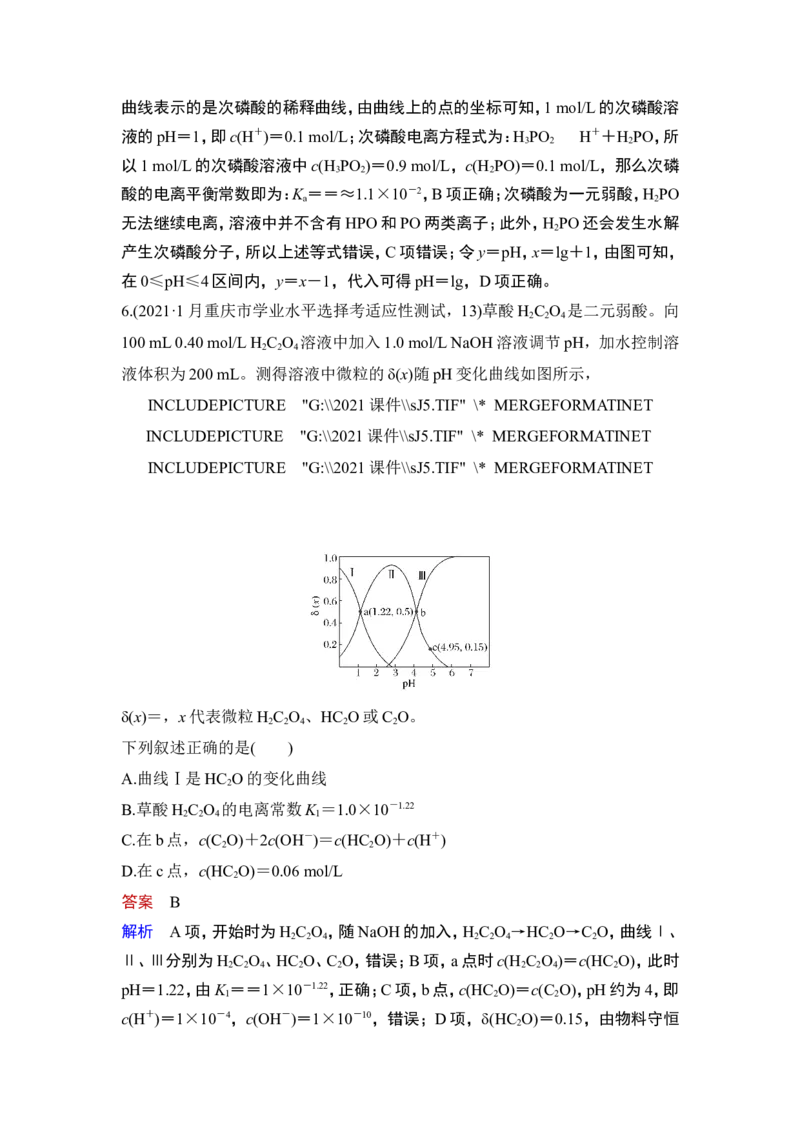
液体积为200 mL。测得溶液中微粒的δ(x)随pH变化曲线如图所示,
INCLUDEPICTURE "G:\\2021课件\\sJ5.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\sJ5.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\sJ5.TIF" \* MERGEFORMATINET
δ(x)=,x代表微粒H C O 、HC O或C O。
2 2 4 2 2
下列叙述正确的是( )
A.曲线Ⅰ是HC O的变化曲线
2
B.草酸H C O 的电离常数K =1.0×10-1.22
2 2 4 1
C.在b点,c(C O)+2c(OH-)=c(HC O)+c(H+)
2 2
D.在c点,c(HC O)=0.06 mol/L
2
答案 B
解析 A项,开始时为H C O ,随NaOH的加入,H C O →HC O→C O,曲线Ⅰ、
2 2 4 2 2 4 2 2
Ⅱ、Ⅲ分别为H C O 、HC O、C O,错误;B项,a点时c(H C O )=c(HC O),此时
2 2 4 2 2 2 2 4 2
pH=1.22,由K ==1×10-1.22,正确;C项,b点,c(HC O)=c(C O),pH约为4,即
1 2 2
c(H+)=1×10-4,c(OH-)=1×10-10,错误;D项,δ(HC O)=0.15,由物料守恒
2c(H C O )+c(HC O)+c(C O)=0.2 mol/L,c(HC O)=0.3 mol/L(注意溶液的体积
2 2 4 2 2 2
为200 mL),错误。
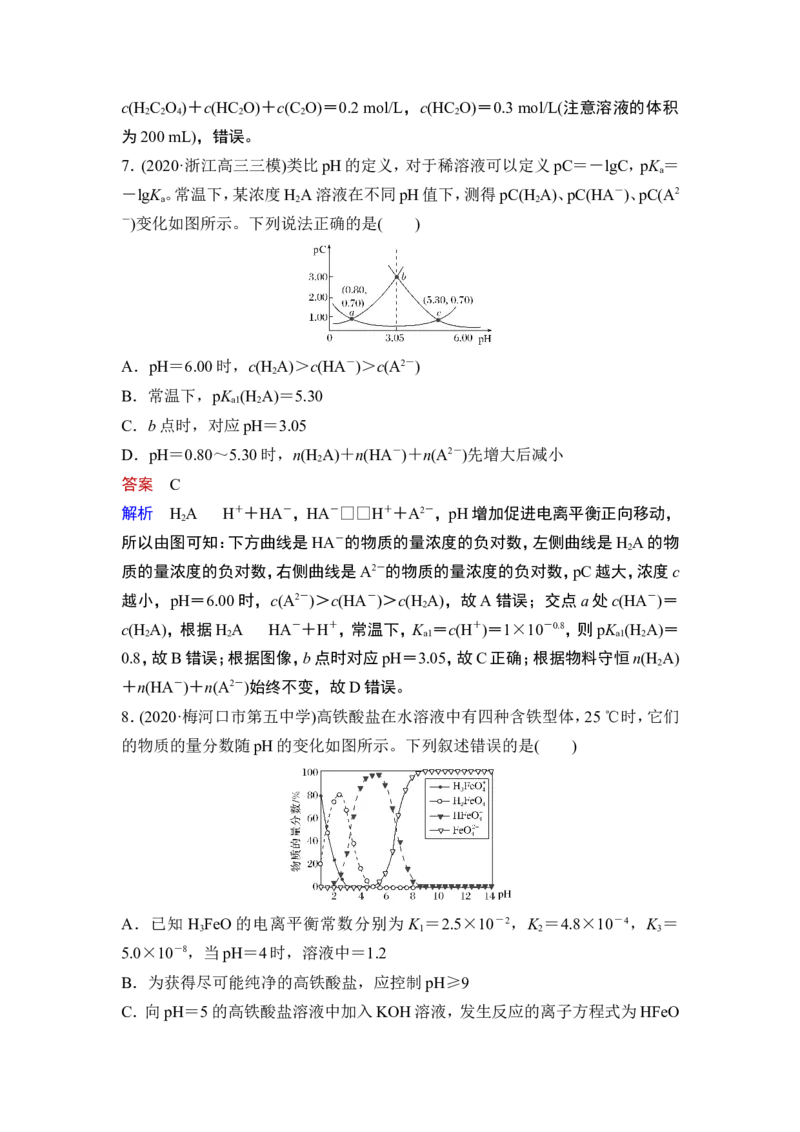
7.(2020·浙江高三三模)类比pH的定义,对于稀溶液可以定义pC=-lgC,pK =
a
-lgK 。常温下,某浓度H A溶液在不同pH值下,测得pC(H A)、pC(HA-)、pC(A2
a 2 2
-)变化如图所示。下列说法正确的是( )
A.pH=6.00时,c(H A)>c(HA-)>c(A2-)
2
B.常温下,pK (H A)=5.30
a1 2
C.b点时,对应pH=3.05
D.pH=0.80~5.30时,n(H A)+n(HA-)+n(A2-)先增大后减小
2
答案 C
解析 H AH++HA-,HA-H++A2-,pH增加促进电离平衡正向移动,
2
所以由图可知:下方曲线是HA-的物质的量浓度的负对数,左侧曲线是H A的物
2
质的量浓度的负对数,右侧曲线是A2-的物质的量浓度的负对数,pC越大,浓度c
越小,pH=6.00时,c(A2-)>c(HA-)>c(H A),故A错误;交点a处c(HA-)=
2
c(H A),根据H AHA-+H+,常温下,K =c(H+)=1×10-0.8,则pK (H A)=
2 2 a1 a1 2
0.8,故B错误;根据图像,b点时对应pH=3.05,故C正确;根据物料守恒n(H A)
2
+n(HA-)+n(A2-)始终不变,故D错误。
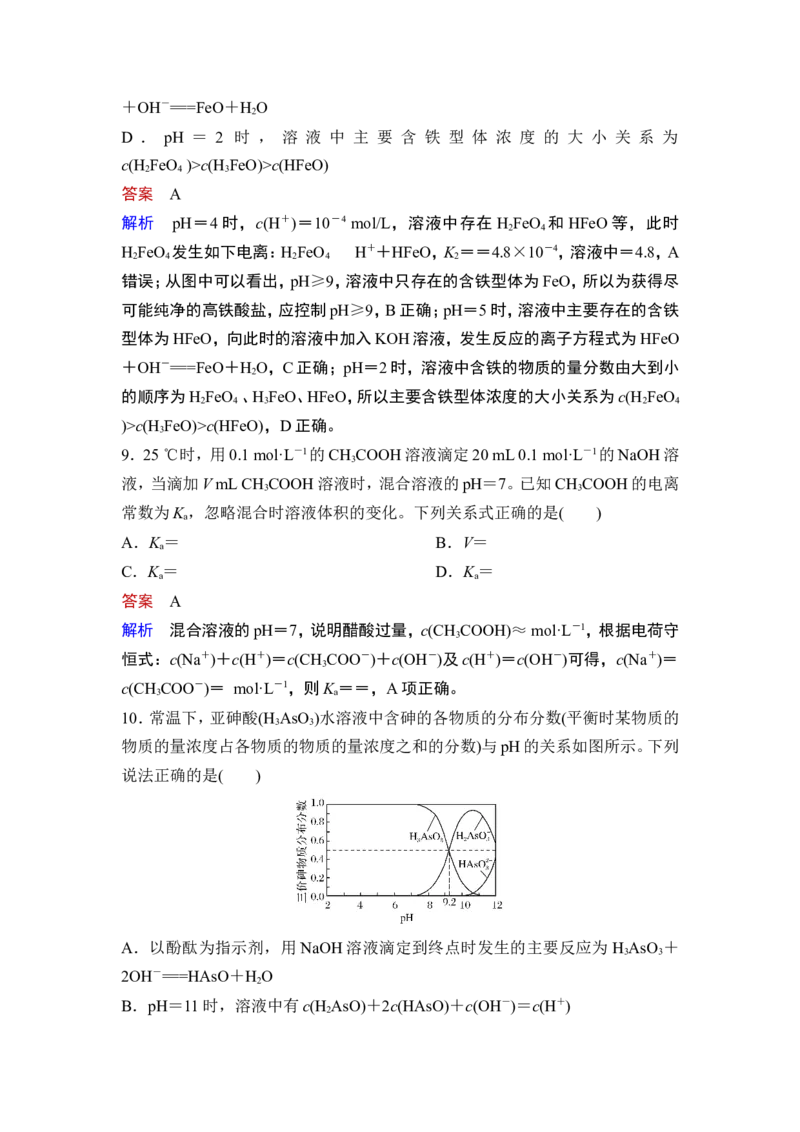
8.(2020·梅河口市第五中学)高铁酸盐在水溶液中有四种含铁型体,25 ℃时,它们
的物质的量分数随pH的变化如图所示。下列叙述错误的是( )
A.已知 H FeO的电离平衡常数分别为 K =2.5×10-2,K =4.8×10-4,K =
3 1 2 3
5.0×10-8,当pH=4时,溶液中=1.2
B.为获得尽可能纯净的高铁酸盐,应控制pH≥9
C.向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO+OH-===FeO+H O
2
D . pH = 2 时 , 溶 液 中 主 要 含 铁 型 体 浓 度 的 大 小 关 系 为
c(H FeO )>c(H FeO)>c(HFeO)
2 4 3
答案 A
解析 pH=4 时,c(H+)=10-4 mol/L,溶液中存在 H FeO 和 HFeO 等,此时
2 4
H FeO 发生如下电离:H FeO H++HFeO,K ==4.8×10-4,溶液中=4.8,A
2 4 2 4 2
错误;从图中可以看出,pH≥9,溶液中只存在的含铁型体为FeO,所以为获得尽
可能纯净的高铁酸盐,应控制pH≥9,B正确;pH=5时,溶液中主要存在的含铁
型体为HFeO,向此时的溶液中加入KOH溶液,发生反应的离子方程式为HFeO
+OH-===FeO+H O,C正确;pH=2时,溶液中含铁的物质的量分数由大到小
2
的顺序为H FeO 、H FeO、HFeO,所以主要含铁型体浓度的大小关系为c(H FeO
2 4 3 2 4
)>c(H FeO)>c(HFeO),D正确。
3
9.25 ℃时,用0.1 mol·L-1的CH COOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶
3
液,当滴加V mL CH COOH溶液时,混合溶液的pH=7。已知CH COOH的电离
3 3
常数为K ,忽略混合时溶液体积的变化。下列关系式正确的是( )
a
A.K = B.V=
a
C.K = D.K =
a a
答案 A
解析 混合溶液的pH=7,说明醋酸过量,c(CH COOH)≈ mol·L-1,根据电荷守
3
恒式:c(Na+)+c(H+)=c(CH COO-)+c(OH-)及c(H+)=c(OH-)可得,c(Na+)=
3
c(CH COO-)= mol·L-1,则K ==,A项正确。
3 a
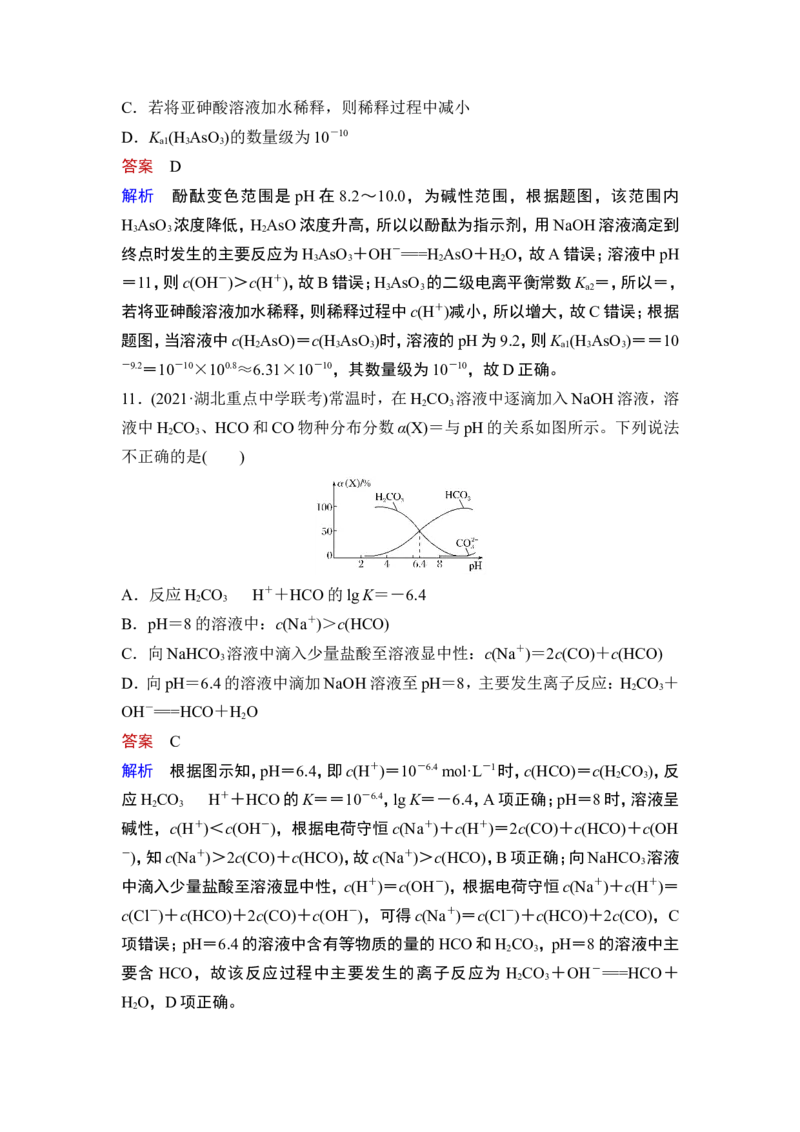
10.常温下,亚砷酸(H AsO )水溶液中含砷的各物质的分布分数(平衡时某物质的
3 3
物质的量浓度占各物质的物质的量浓度之和的分数)与pH的关系如图所示。下列
说法正确的是( )
A.以酚酞为指示剂,用NaOH溶液滴定到终点时发生的主要反应为 H AsO +
3 3
2OH-===HAsO+H O
2
B.pH=11时,溶液中有c(H AsO)+2c(HAsO)+c(OH-)=c(H+)
2C.若将亚砷酸溶液加水稀释,则稀释过程中减小
D.K (H AsO )的数量级为10-10
a1 3 3
答案 D
解析 酚酞变色范围是 pH 在 8.2~10.0,为碱性范围,根据题图,该范围内
H AsO 浓度降低,H AsO浓度升高,所以以酚酞为指示剂,用NaOH溶液滴定到
3 3 2
终点时发生的主要反应为H AsO +OH-===H AsO+H O,故A错误;溶液中pH
3 3 2 2
=11,则c(OH-)>c(H+),故B错误;H AsO 的二级电离平衡常数K =,所以=,
3 3 a2
若将亚砷酸溶液加水稀释,则稀释过程中c(H+)减小,所以增大,故C错误;根据
题图,当溶液中c(H AsO)=c(H AsO )时,溶液的pH为9.2,则K (H AsO )==10
2 3 3 a1 3 3
-9.2=10-10×100.8≈6.31×10-10,其数量级为10-10,故D正确。
11.(2021·湖北重点中学联考)常温时,在H CO 溶液中逐滴加入NaOH溶液,溶
2 3
液中H CO 、HCO和CO物种分布分数α(X)=与pH的关系如图所示。下列说法
2 3
不正确的是( )
A.反应H CO H++HCO的lg K=-6.4
2 3
B.pH=8的溶液中:c(Na+)>c(HCO)
C.向NaHCO 溶液中滴入少量盐酸至溶液显中性:c(Na+)=2c(CO)+c(HCO)
3
D.向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生离子反应:H CO +
2 3
OH-===HCO+H O
2
答案 C
解析 根据图示知,pH=6.4,即c(H+)=10-6.4 mol·L-1时,c(HCO)=c(H CO ),反
2 3
应H CO H++HCO的K==10-6.4,lg K=-6.4,A项正确;pH=8时,溶液呈
2 3
碱性,c(H+)<c(OH-),根据电荷守恒c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH
-),知c(Na+)>2c(CO)+c(HCO),故c(Na+)>c(HCO),B项正确;向NaHCO 溶液
3
中滴入少量盐酸至溶液显中性,c(H+)=c(OH-),根据电荷守恒c(Na+)+c(H+)=
c(Cl-)+c(HCO)+2c(CO)+c(OH-),可得c(Na+)=c(Cl-)+c(HCO)+2c(CO),C
项错误;pH=6.4的溶液中含有等物质的量的HCO和H CO ,pH=8的溶液中主
2 3
要含 HCO,故该反应过程中主要发生的离子反应为 H CO +OH-===HCO+
2 3
H O,D项正确。
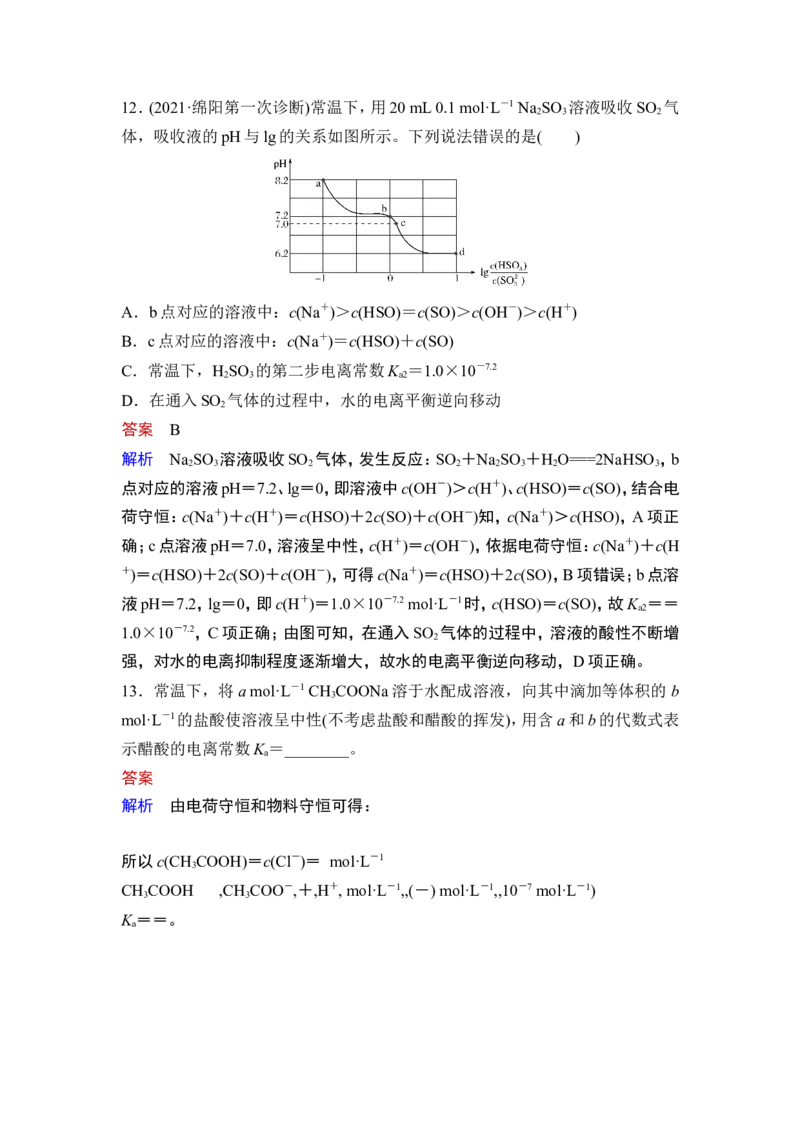
212.(2021·绵阳第一次诊断)常温下,用20 mL 0.1 mol·L-1 Na SO 溶液吸收SO 气
2 3 2
体,吸收液的pH与lg的关系如图所示。下列说法错误的是( )
A.b点对应的溶液中:c(Na+)>c(HSO)=c(SO)>c(OH-)>c(H+)
B.c点对应的溶液中:c(Na+)=c(HSO)+c(SO)
C.常温下,H SO 的第二步电离常数K =1.0×10-7.2
2 3 a2
D.在通入SO 气体的过程中,水的电离平衡逆向移动
2
答案 B
解析 Na SO 溶液吸收SO 气体,发生反应:SO +Na SO +H O===2NaHSO ,b
2 3 2 2 2 3 2 3
点对应的溶液pH=7.2、lg=0,即溶液中c(OH-)>c(H+)、c(HSO)=c(SO),结合电
荷守恒:c(Na+)+c(H+)=c(HSO)+2c(SO)+c(OH-)知,c(Na+)>c(HSO),A项正
确;c点溶液pH=7.0,溶液呈中性,c(H+)=c(OH-),依据电荷守恒:c(Na+)+c(H
+)=c(HSO)+2c(SO)+c(OH-),可得c(Na+)=c(HSO)+2c(SO),B项错误;b点溶
液pH=7.2,lg=0,即c(H+)=1.0×10-7.2 mol·L-1时,c(HSO)=c(SO),故K ==
a2
1.0×10-7.2,C项正确;由图可知,在通入SO 气体的过程中,溶液的酸性不断增
2
强,对水的电离抑制程度逐渐增大,故水的电离平衡逆向移动,D项正确。
13.常温下,将a mol·L-1 CH COONa溶于水配成溶液,向其中滴加等体积的 b
3
mol·L-1的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表
示醋酸的电离常数K =________。
a
答案
解析 由电荷守恒和物料守恒可得:
所以c(CH COOH)=c(Cl-)= mol·L-1
3
CH COOH,CH COO-,+,H+, mol·L-1,,(-) mol·L-1,,10-7 mol·L-1)
3 3
K ==。
a