文档内容
玉溪一中高 2023 届高三上学期开学检测卷
化学学科试卷
命题人:孟丽红 余思贤
总分:100分,考试时间:90分钟 审题人:孟丽红 余思贤
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 S—32 Cl—35.5
第I卷选择题(共42分)
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意)
1. 2022年4月17日神舟十三号载人飞船与天和核心舱实现对接后顺利返航。下列说法正确的是
A. 航天器的操纵杆采用的碳纤维属于有机高分子材料
B. 火箭推进剂的燃烧可将化学能完全转化为机械能
C. 空间站使用的太阳能电池板主要材料是二氧化硅
D. 核心舱内氧气来源于水的电解,此过程中氧气为氧化产物
2. 化学与生产、生活密切相关。下列说法错误的是
A. 一定条件下,秸秆、杂草、人畜粪便等经隔绝空气发酵可产生沼气
B. 饱和食盐水中先通入二氧化碳至饱和,再通入氨气后可析出碳酸氢钠晶体
C. 绿色植物的光合作用、食物的腐败、钢铁的锈蚀等都发生了氧化还原反应
D. 药物在促进人类健康的同时,可能对机体产生与用药目的无关的有害作用
3. 设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A. 12.0 g 熔融的NaHSO 中含有的阳离子数为0.1 N
4 A
的
B. 17.0 g -OH和OH- 混合体所含电子数为10N
A
C. 标准状况下,2.24 L 甲醇中含有的C-H数为0.3N
A
D. 将足量MnO 与含4molHCl的浓盐酸混合,转移电子数为2N
2 A
4. 下列说法正确的是
A. H O+的空间结构:平面三角形 B. 冰中的氢键示意图:
3C. 基态氧原子价电子排布图: D. 基态Cr原子电子排布式[Ar]3d44s2
5. 下列反应的离子方程式书写正确的是
A. 铜与稀硝酸反应:Cu+2NO +4H+ = Cu2++2NO↑+2H O
2 2
B. 氯化铝溶液与过量氨水反应:Al3++4NH•H O = AlO +4NH +2H O
3 2 2
C. 铬酸钾溶液中滴加稀硫酸:2CrO +2H+ Cr O +H O
2 2
D. 硫代硫酸钠溶液与稀硫酸反应:SO +6H++2SO = 4SO ↑+3H O
2 2 2
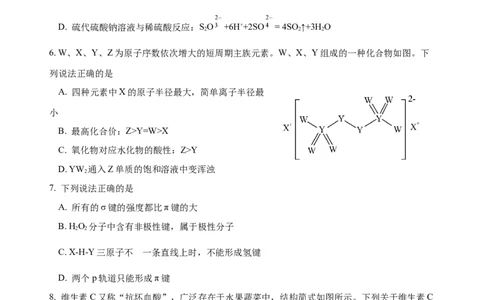
6. W、X、Y、Z为原子序数依次增大的短周期主族元素。W、X、Y组成的一种化合物如图。下
列说法正确的是
A. 四种元素中X的原子半径最大,简单离子半径最
小
B. 最高化合价:Z>Y=W>X
C. 氧化物对应水化物的酸性:Z>Y
D. YW 通入Z单质的饱和溶液中变浑浊
2
7. 下列说法正确的是
A. 所有的σ键的强度都比π键的大
B. HO 分子中含有非极性键,属于极性分子
2 2
在
C. X-H-Y三原子不 一条直线上时,不能形成氢键
D. 两个p轨道只能形成π键
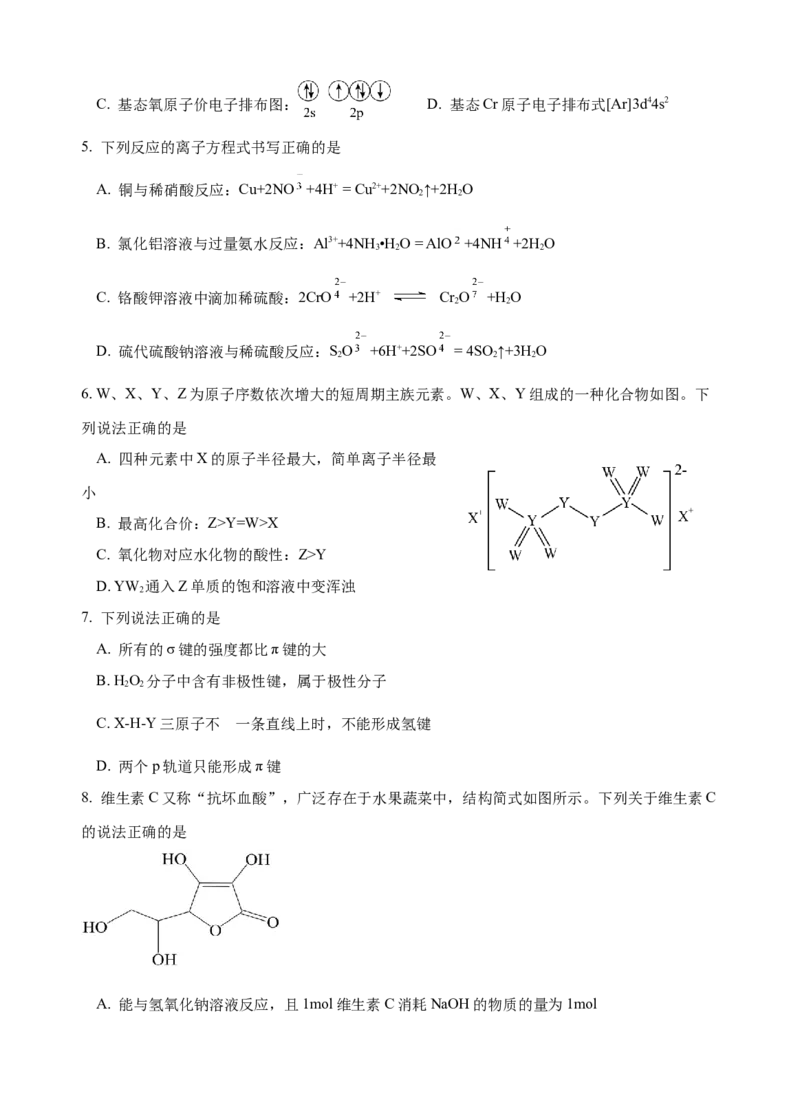
8. 维生素C又称“抗坏血酸”,广泛存在于水果蔬菜中,结构简式如图所示。下列关于维生素C
的说法正确的是
A. 能与氢氧化钠溶液反应,且1mol维生素C消耗NaOH的物质的量为1molB. 可用酸性高锰酸钾溶液检验其中的碳碳双键
C. 存在含有苯环的同分异构体
D. 分子中所有原子共面
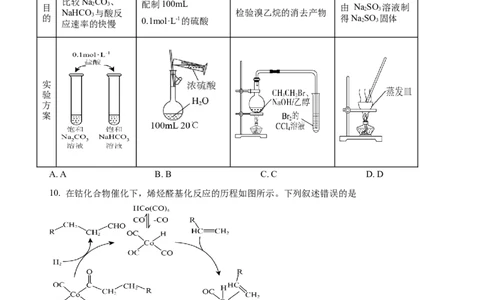
9. 下列实验方案能达到实验目的的是
选
A B C D
项
目 比较Na 2 CO 3 、 配制100mL 由 NaSO 溶液制
NaHCO 与酸反 检验溴乙烷的消去产物 2 3
的 应速率的 3 快慢 0.1mol·L-1的硫酸 得Na 2 SO 3 固体
实
验
方
案
A. A B. B C. C D. D
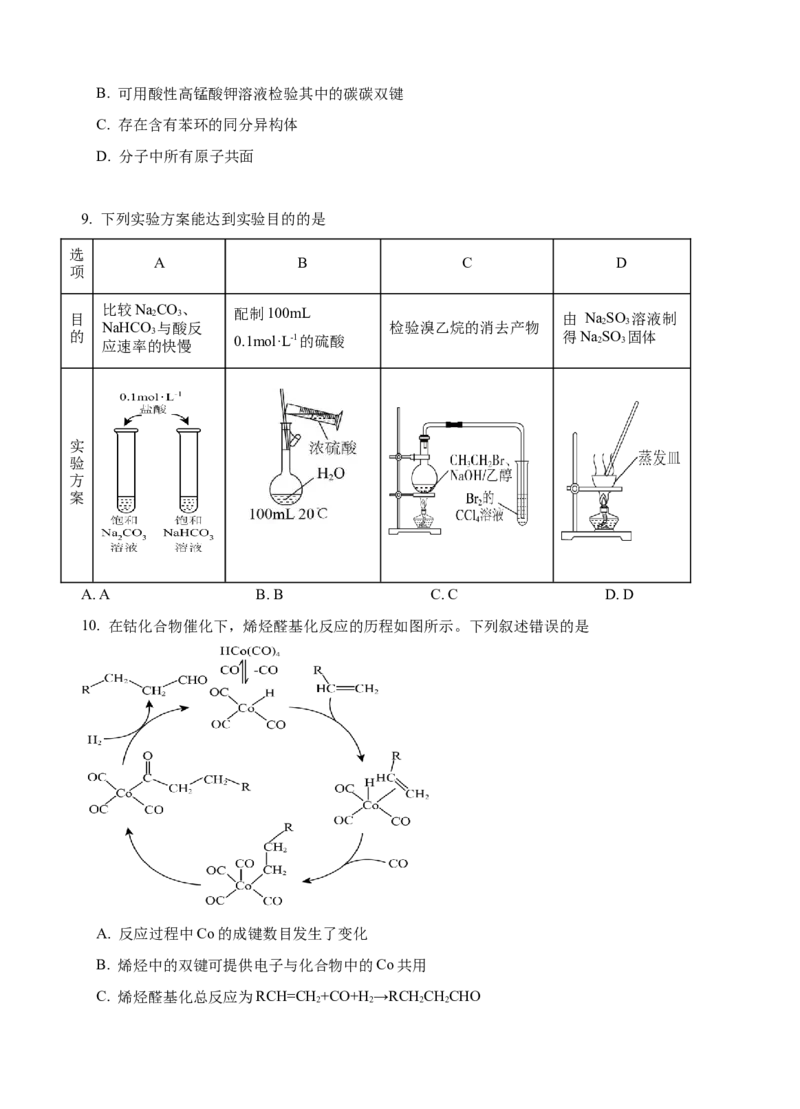
10. 在钴化合物催化下,烯烃醛基化反应的历程如图所示。下列叙述错误的是
A. 反应过程中Co的成键数目发生了变化
B. 烯烃中的双键可提供电子与化合物中的Co共用
C. 烯烃醛基化总反应为RCH=CH+CO+H →RCHCHCHO
2 2 2 2D. 该含钴化合物可降低烯烃醛基化反应的活化能,提高平衡转化率
的
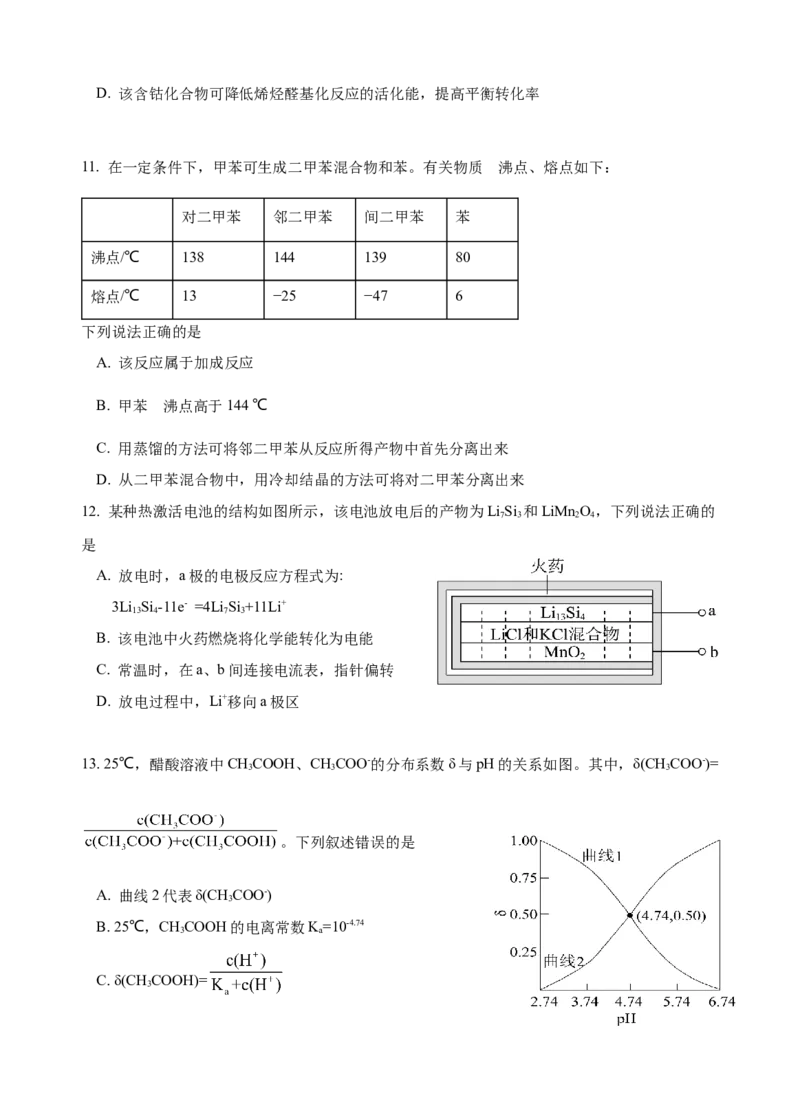
11. 在一定条件下,甲苯可生成二甲苯混合物和苯。有关物质 沸点、熔点如下:
对二甲苯 邻二甲苯 间二甲苯 苯
沸点/℃ 138 144 139 80
熔点/℃ 13 −25 −47 6
下列说法正确的是
A. 该反应属于加成反应
的
B. 甲苯 沸点高于144 ℃
C. 用蒸馏的方法可将邻二甲苯从反应所得产物中首先分离出来
D. 从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来
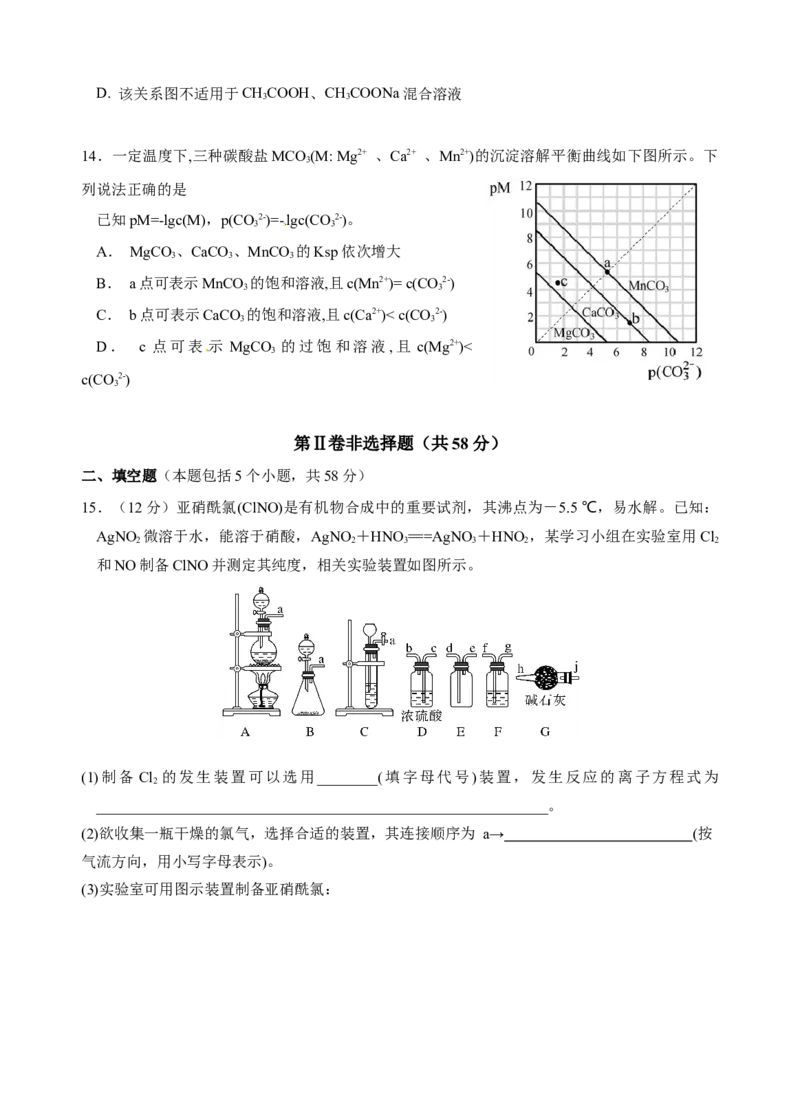
12. 某种热激活电池的结构如图所示,该电池放电后的产物为LiSi 和LiMn O,下列说法正确的
7 3 2 4
是
A. 放电时,a极的电极反应方程式为:
3Li Si -11e- =4Li Si +11Li+
13 4 7 3
B. 该电池中火药燃烧将化学能转化为电能
C. 常温时,在a、b间连接电流表,指针偏转
D. 放电过程中,Li+移向a极区
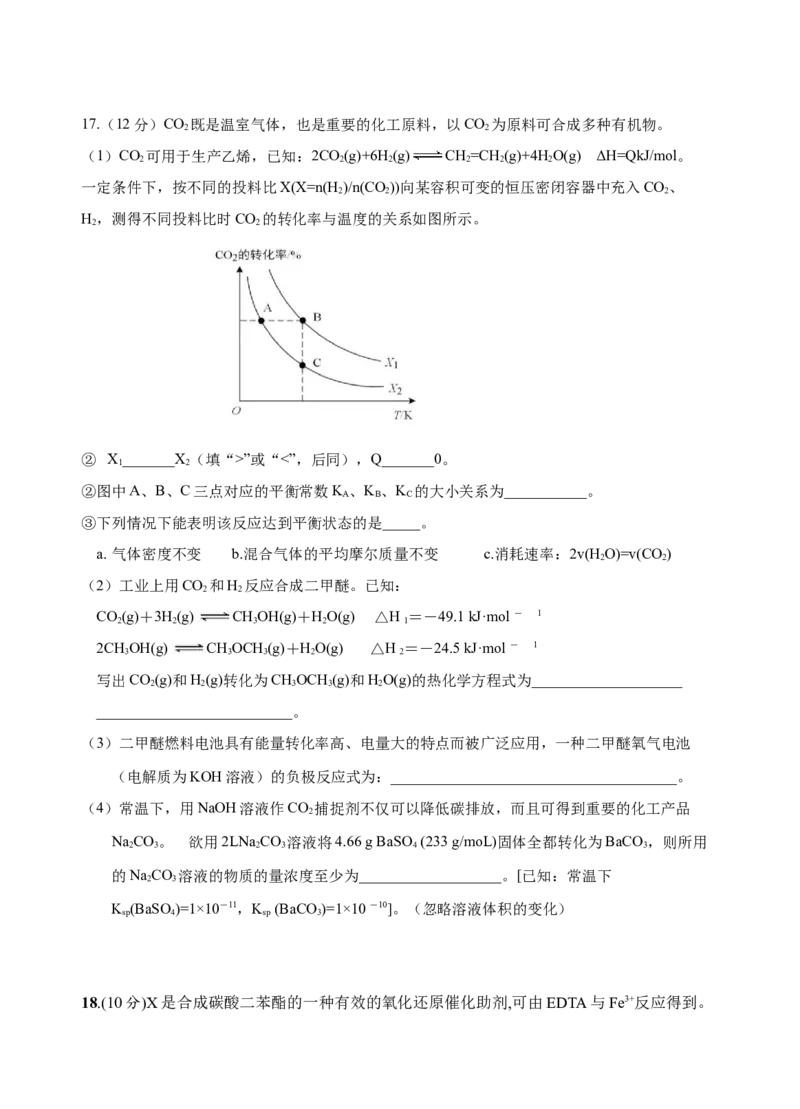
13. 25℃,醋酸溶液中CHCOOH、CHCOO-的分布系数δ与pH的关系如图。其中,δ(CH COO-)=
3 3 3
。下列叙述错误的是
A. 曲线2代表δ(CH COO-)
3
B. 25℃,CHCOOH的电离常数K=10-4.74
3 a
C. δ(CH COOH)=
3D. 该关系图不适用于CHCOOH、CHCOONa混合溶液
3 3
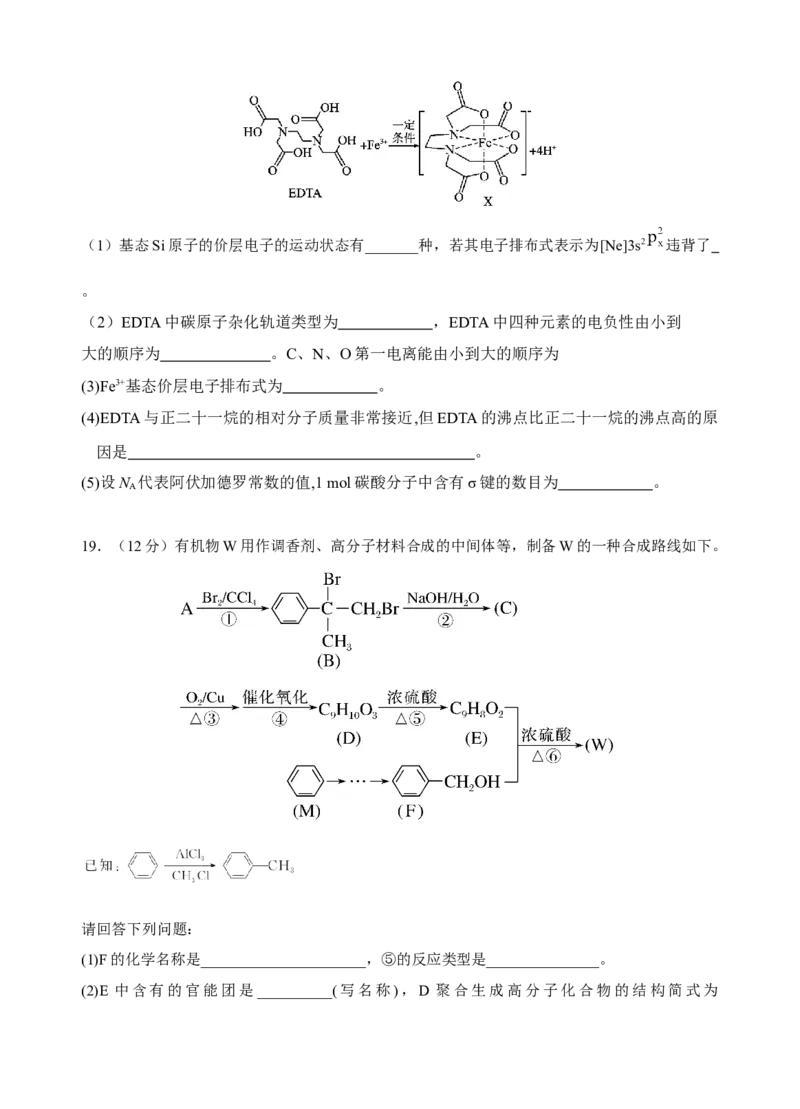
14.一定温度下,三种碳酸盐MCO (M: Mg2+ 、Ca2+ 、Mn2+)的沉淀溶解平衡曲线如下图所示。下
3
列说法正确的是
已知pM=-lgc(M),p(CO2-)=-lgc(CO 2-)。
3 3
A. MgCO 、CaCO 、MnCO 的Ksp依次增大
3 3 3
B. a点可表示MnCO 的饱和溶液,且c(Mn2+)= c(CO2-)
3 3
C. b点可表示CaCO 的饱和溶液,且c(Ca2+)< c(CO2-)
3 3
D. c 点可表 示 MgCO 的过饱和溶液,且 c(Mg2+)<
3
c(CO2-)
3
第Ⅱ卷非选择题(共58分)
二、填空题(本题包括5个小题,共58分)
15.(12分)亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为-5.5 ℃,易水解。已知:
AgNO 微溶于水,能溶于硝酸,AgNO +HNO===AgNO +HNO ,某学习小组在实验室用Cl
2 2 3 3 2 2
和NO制备ClNO并测定其纯度,相关实验装置如图所示。
(1)制备 Cl 的发生装置可以选用________(填字母代号)装置,发生反应的离子方程式为
2
____________________________________________________________。
(2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→ (按
气流方向,用小写字母表示)。
(3)实验室可用图示装置制备亚硝酰氯:①实验室也可用该装置制备NO气体,X装置的优点为_________________________________。
②检验装置气密性并装入药品,打开 K ,然后再打开 K ,通入一段时间气体,其目的是
2 3
____________________________,然后进行其他操作,当Z中有一定量液体生成时,停止实验。
③通过以下实验测定ClNO样品的纯度。取Z中所得液体m g 溶于水,配制成250 mL 溶液;取
出25.00 mL样品溶于锥形瓶中,以KCrO 溶液为指示剂,用c mol·L-1 AgNO 标准溶液滴定
2 4 3
至终点,消耗标准溶液的体积为20.00 mL。滴定终点的现象__________________________
__________________________,亚硝酰氯(ClNO)的质量分数为____________。[已知Ag CrO 为
2 4
砖红色固体;K (AgCl)=1.56×10-10,K (Ag CrO)=1×10-12]
sp sp 2 4
16.(12分)三氧化二钴(Co O )是重要的化工原料。用含钴废料(主要成分为Co O ,含少量
2 3 2 3
SiO、NiO、Fe O 等)制备Co O 的流程如下图:
2 2 3 2 3
已知:“滤液1”中含有的阳离子有H+、Co2+、Fe3+、Ni2+。
(1)“滤渣1”的主要成分是_________(写化学式)。
(2)“酸浸”时,HO 可将Co O 还原为Co2+,离子方程式为 。
2 2 2 3
(3)“调pH”时,常温下,为保证“滤液1”中Fe3+完全沉淀,需调节“滤液1”的pH的最小值为
________。(已知:溶液中离子浓度小于1×10-5mol·L-1,则认为离子完全沉淀;Fe(OH) 的
3
K 为1×10-38)
sp
(4)加入有机萃取剂的目的是 。
(5)由“滤液2”可得到的主要副产品是 (写化学式)。
(6)“沉钴”过程中,生成Co (OH) CO 的离子方程式为 。
2 2 317.(12分)CO 既是温室气体,也是重要的化工原料,以CO 为原料可合成多种有机物。
2 2
(1)CO 可用于生产乙烯,已知:2CO(g)+6H(g) CH=CH (g)+4HO(g) ΔH=QkJ/mol。
2 2 2 2 2 2
一定条件下,按不同的投料比X(X=n(H )/n(CO))向某容积可变的恒压密闭容器中充入CO、
2 2 2
H,测得不同投料比时CO 的转化率与温度的关系如图所示。
2 2
② X_______X(填“>”或“<”,后同),Q_______0。
1 2
②图中A、B、C三点对应的平衡常数K 、K 、K 的大小关系为___________。
A B C
③下列情况下能表明该反应达到平衡状态的是_____。
a. 气体密度不变 b.混合气体的平均摩尔质量不变 c.消耗速率:2v(H O)=v(CO)
2 2
(2)工业上用CO 和H 反应合成二甲醚。已知:
2 2
CO(g)+3H(g) CHOH(g)+HO(g) △H =-49.1 kJ·mol - 1
2 2 3 2 1
2CHOH(g) CHOCH (g)+HO(g) △H =-24.5 kJ·mol - 1
3 3 3 2 2
写出CO(g)和H(g)转化为CHOCH (g)和HO(g)的热化学方程式为____________________
2 2 3 3 2
__________________________。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池
(电解质为KOH溶液)的负极反应式为:______________________________________。
(4)常温下,用NaOH溶液作CO 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
2
NaCO。 欲用2LNa CO 溶液将4.66 g BaSO (233 g/moL)固体全都转化为BaCO ,则所用
2 3 2 3 4 3
的NaCO 溶液的物质的量浓度至少为___________________。[已知:常温下
2 3
K (BaSO)=1×10-11,K (BaCO)=1×10 -10]。(忽略溶液体积的变化)
sp 4 sp 3
18.(10分)X是合成碳酸二苯酯的一种有效的氧化还原催化助剂,可由EDTA与Fe3+反应得到。(1)基态Si原子的价层电子的运动状态有_______种,若其电子排布式表示为[Ne]3s2 违背了
。
(2)EDTA中碳原子杂化轨道类型为 ,EDTA中四种元素的电负性由小到
大的顺序为 。C、N、O第一电离能由小到大的顺序为
(3)Fe3+基态价层电子排布式为 。
(4)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点比正二十一烷的沸点高的原
因是 。
(5)设N 代表阿伏加德罗常数的值,1 mol碳酸分子中含有σ键的数目为 。
A
19.(12分)有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
请回答下列问题:
(1)F的化学名称是______________________,⑤的反应类型是_______________。
(2)E 中含有的官能团是__________(写名称),D 聚合生成高分子化合物的结构简式为_______________。
(3)与A含有相同官能团的芳香化合物的同分异构体还有________种(不含立体异构),其中核磁共
振氢谱为六组峰,且峰面积之比为1∶1∶2∶2∶2∶2的结构简式为______________________。
(4) 参照有机物W的上述合成路线,以M和CHCl为原料制备F的合成路线(无机试剂任选)。
3