文档内容
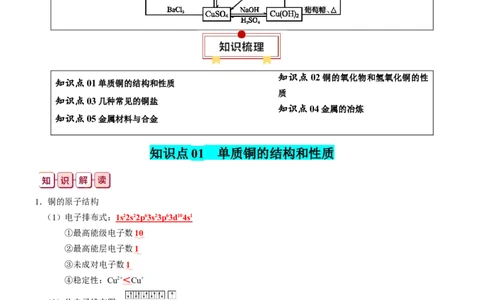
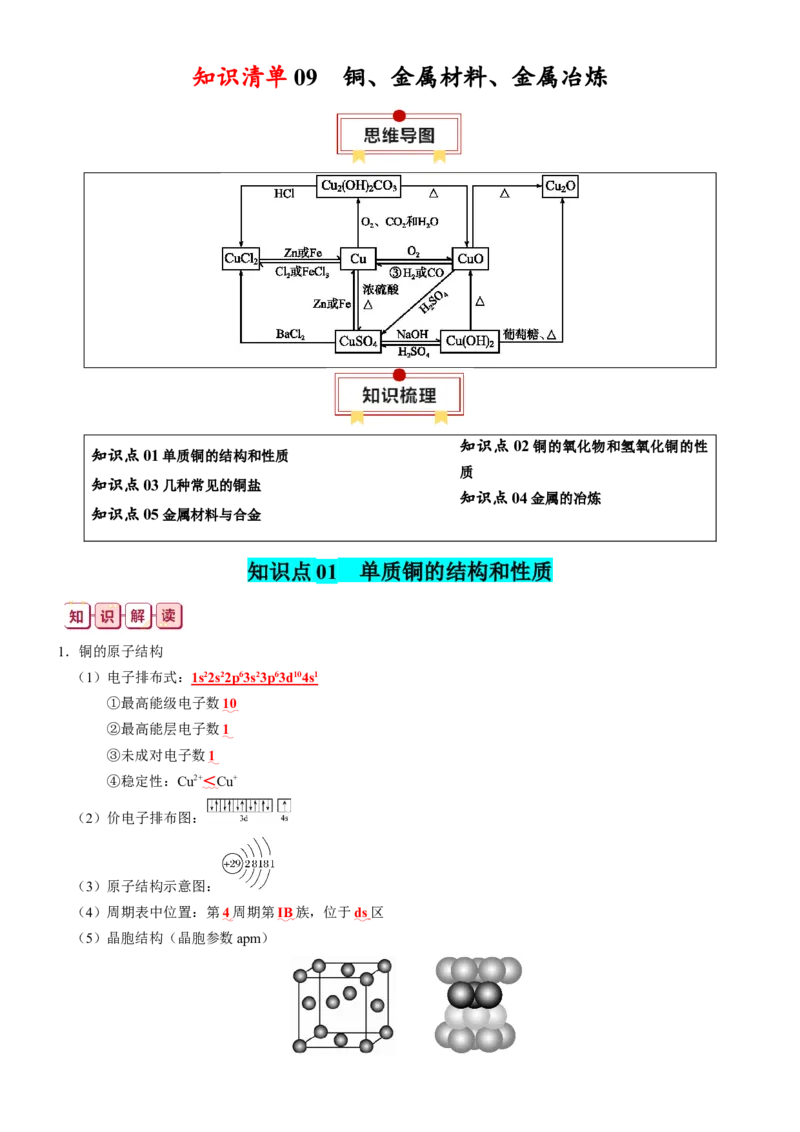
知识清单 09 铜、金属材料、金属冶炼
知识点02铜的氧化物和氢氧化铜的性
知识点01单质铜的结构和性质
质
知识点03几种常见的铜盐
知识点04金属的冶炼
知识点05金属材料与合金
知识点 01 单质铜的结构和性质
1.铜的原子结构
(1)电子排布式: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1
①最高能级电子数10
②最高能层电子数1
③未成对电子数1
④稳定性:Cu2+<Cu+
(2)价电子排布图:
(3)原子结构示意图:
(4)周期表中位置:第4 周期第IB 族,位于ds 区
(5)晶胞结构(晶胞参数apm)①堆积名称:面心立方最密堆积,堆积类型:A 型或铜型
1
②堆积方式:…ABCABC…
③配位数12
④晶胞中含Cu的个数:4
4M
256×1030
⑤晶胞密度:ρ= (a×10-10 )3 ×N A= a3N A g · cm - 3
4× 4 πr3 4× 4 π( √2 a)3
3 3 4 √2
⑥空间利用率:φ=
a3
×100%=
a3
×100%=
6
π×100%≈74%
2.铜的物理性质
(1)颜色:呈红色或紫红色
(2)三性:导电性、导热性和延展性良好
3.与非金属单质反应
(1)与氧气反应:条件不同,产物不同
①加热:2Cu+O 2CuO
2
②常温:2Cu+O + CO + H O Cu ( OH ) CO
2 2 2 2 2 3
(2)与其他非金属反应
①Cu-----→Cu S ②Cu------→CuCl
2 2
4.与酸反应
(1)稀硫酸
①普通条件:Cu不能置换出H
2
②电解条件:Cu+H SO ( 稀 ) Cu SO +H ↑
2 4 4 2
(2)浓硫酸:Cu+2H SO ( 浓 ) CuSO +SO ↑ +2H O
2 4 4 2 2
(3)浓硝酸:Cu+4HNO ( 浓 ) Cu ( NO )+2NO ↑ +2H O
3 3 2 2 2
(4)稀硝酸:3Cu+8HNO ( 稀 ) 3Cu ( NO ) +2NO ↑ +4H O
3 3 2 2
5.与盐溶液反应
(1)硝酸银:2AgNO +Cu 2Ag+Cu ( NO )
3 3 2
(2)氯化铁:2FeCl+Cu 2FeCl+CuCl
3 2 2
6.单质铜在化学实验中的应用
(1)除去某种气体中的氧气
(2)乙醇催化氧化的催化剂
①催化原理:Cu CuO Cu
②催化反应:2CH CH OH+O 2CH CHO+2H O
3 2 2 3 2
(3)防止可燃性气体燃烧回火的安全装置易错点:铜的易错知识点
(1)铜和氧气在常温下反应生成Cu ( OH ) CO ,在加热条件下生成CuO。
2 2 3
(2)单质铜可以除去某种气体中的氧气,也可以作乙醇催化氧化的催化剂。
(3)在普通条件下Cu不能从稀硫酸中置换出H,但在通电条件下Cu能从稀硫酸中置换出H。
2 2
【典例01】(2022·大连一模)下列实验的前后,铜的质量一定发生变化的是( )。
A.铜丝在空气中灼烧后立即插入乙醇
B.铜片放入酸化的硝酸钠溶液
C.铜和铁的混合物放入稀硝酸
D.铜、锌、稀硫酸构成的原电池放电
【解析】选B。由于氧化铜能够和乙醇反应生成乙醛和铜,铜变成氧化铜,氧化铜又被还原成铜,最终铜质量
没有变化,故A错误;铜和稀硝酸反应生成了硝酸铜,质量一定减少,故B正确;由于铁还原性大于铜的,铁
先参加反应,若是铁足量,铜变化消耗,故C错误;铜、锌构成的原电池,锌是负极,铜是正极不消耗,故D
错误。
知识点 02 铜的氧化物和氢氧化铜的性质
1.氧化铜
(1)物性:黑色粉末状固体
(2)弱氧化性:CuO-------------------→Cu
①Al:2Al+3CuO 3Cu+Al O
2 3
②C:2CuO+C 2Cu+CO ↑
2
③NH :2NH +3CuO N+3Cu+3H O
3 3 2 2
④乙醇:CH CH OH+CuO CH CHO+H O+Cu
3 2 3 2
(3)热不稳定性
①反应:4CuO 2 Cu O +O ↑
2 2
②原因: Cu + 的价电子构型为 3d 10 的稳定结构
2.氧化亚铜
(1)物性:砖红色固体
(2)Cu O的晶胞(小黑点实心代表Cu原子)
2
①含Cu O数:2
2
②配位数:Cu的配位数为2;O的配位数为4(3)用途:作为红色玻璃和搪瓷的着色剂
3.氢氧化铜
(1)物理性质:蓝色不溶于水的固体
(2)化学性质
①弱碱性: Cu ( O H ) +2 H + Cu 2+ + 2H O
2 2
②不稳定性: Cu ( OH ) CuO+H O
2 2
③弱氧化性: 2Cu ( O H ) + RCHO +NaOH R COO Na + Cu O ↓ + 3 H O
2 2 2
④络合性: Cu ( OH ) +4NH · H O [ Cu ( NH ) ] 2 + + 2OH - +4H O
2 3 2 3 4 2
易错点:氢氧化铜的易错知识点
(1)氢氧化铜既能溶于酸又能溶于碱(氨水),但它不是两性氢氧化物。
(2)向硫酸铜溶液中滴加氨水的现象是:先产生蓝色沉淀,后沉淀溶解生成深蓝色溶液
(3)新制的氢氧化铜悬浊液具有弱氧化性,可以用来检验醛基。
【典例02】已知酸性条件下有如下反应:2Cu+ Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能
产生Cu或Cu O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物做了验证,实
2
验操作和实验现象记录如下:
加入试剂 实验现象
稀硫酸 红色固体和蓝色溶液
浓硫酸、加热 无色气体
稀硝酸 无色气体和蓝色溶液
浓硝酸 红棕色气体和绿色溶液
由此推出本次氢气还原氧化铜实验的产物是( )。
A.Cu
B.Cu O
2
C.一定有Cu,可能有Cu O
2
D.一定有Cu O,可能有Cu
2
【解析】选D。H 还原CuO生成红色固体,可能是Cu和Cu O中的一种或两种,产物中加入稀HSO 溶液变蓝
2 2 2 4
并得到红色固体,证明产物中含Cu O,在酸性条件下2Cu+=Cu2++Cu,故不能证明产物中是否含有Cu。A项,
2
产物中不一定含有铜,错误;B项,产物中一定有Cu O,也可能有铜,错误;C项,产物中不一定有铜,一定
2
有Cu O,错误;D项,产物中一定有Cu O,可能有铜,正确。
2 2
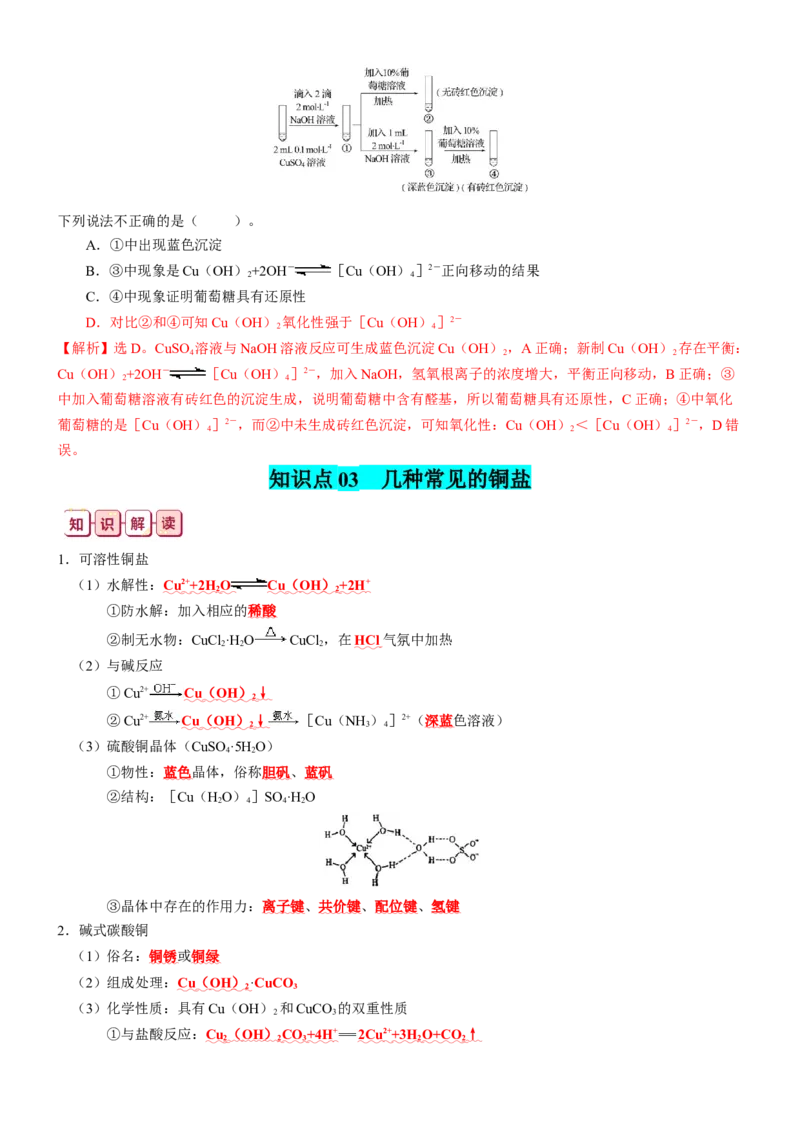
【典例03】(2023·张家口模拟)新制氢氧化铜存在平衡:Cu(OH)+2OH- [Cu(OH)]2-(深蓝
2 4
色)。某同学进行下列实验:下列说法不正确的是( )。
A.①中出现蓝色沉淀
B.③中现象是Cu(OH)+2OH- [Cu(OH)]2-正向移动的结果
2 4
C.④中现象证明葡萄糖具有还原性
D.对比②和④可知Cu(OH) 氧化性强于[Cu(OH)]2-
2 4
【解析】选D。CuSO 溶液与NaOH溶液反应可生成蓝色沉淀Cu(OH),A正确;新制Cu(OH) 存在平衡:
4 2 2
Cu(OH)+2OH- [Cu(OH)]2-,加入NaOH,氢氧根离子的浓度增大,平衡正向移动,B正确;③
2 4
中加入葡萄糖溶液有砖红色的沉淀生成,说明葡萄糖中含有醛基,所以葡萄糖具有还原性,C正确;④中氧化
葡萄糖的是[Cu(OH)]2-,而②中未生成砖红色沉淀,可知氧化性:Cu(OH)<[Cu(OH)]2-,D错
4 2 4
误。
知识点 03 几种常见的铜盐
1.可溶性铜盐
(1)水解性: Cu 2+ +2H O Cu ( OH ) +2H +
2 2
①防水解:加入相应的稀酸
②制无水物:CuCl·HO CuCl,在HCl 气氛中加热
2 2 2
(2)与碱反应
①Cu2+ Cu ( OH ) ↓
2
②Cu2+ Cu ( OH ) ↓ [Cu(NH )]2+(深蓝色溶液)
2 3 4
(3)硫酸铜晶体(CuSO ·5HO)
4 2
①物性:蓝色晶体,俗称胆矾、蓝矾
②结构:[Cu(HO)]SO ·HO
2 4 4 2
③晶体中存在的作用力:离子键、共价键、配位键、氢键
2.碱式碳酸铜
(1)俗名:铜锈或铜绿
(2)组成处理: Cu ( OH ) ·CuCO
2 3
(3)化学性质:具有Cu(OH) 和CuCO 的双重性质
2 3
①与盐酸反应:Cu ( OH ) CO +4H + 2Cu 2+ +3H O+CO ↑
2 2 3 2 2②热分解反应:Cu ( OH ) CO 2CuO+CO ↑ +H O
2 2 3 2 2
③与氢气反应:Cu ( OH ) CO + 2 H 2Cu+CO ↑ +2H O
2 2 3 2 2 2
④与铝反应:3Cu ( OH ) CO + 4 Al 6Cu+CO ↑ + 2 A l O+3H O
2 2 3 2 2 3 2
易错点:铜盐的易错知识点
(1)CuSO 常用来检验某些气体或液态有机物中微量水的存在,而不是用于除水。
4
(2)CuSO 溶液与过量氨水反应的过程:Cu2+ Cu ( OH ) ↓ [Cu(NH )]2+(深蓝色溶液)
4 2 3 4
(3)碱式碳酸铜可以认为是 Cu ( OH ) 和CuCO 组成的混合型化合物
2 3
(4)硫酸铜溶液和消石灰配制波尔多液,其杀菌原理是重金属盐使细菌蛋白质变性
【典例04】某兴趣小组的同学发现,将CuSO 溶液与KCO 溶液混合会产生蓝绿色沉淀。他们对沉淀的组成很
4 2 3
感兴趣,决定采用实验的方法进行探究。
(1)【提出假设】
假设1:所得沉淀为Cu(OH);
2
假设2:所得沉淀为_________;(填化学式)
假设3:所得沉淀为碱式碳酸铜[化学式可表示为[mCu(OH)•nCuCO]。
2 3
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)
【定性探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
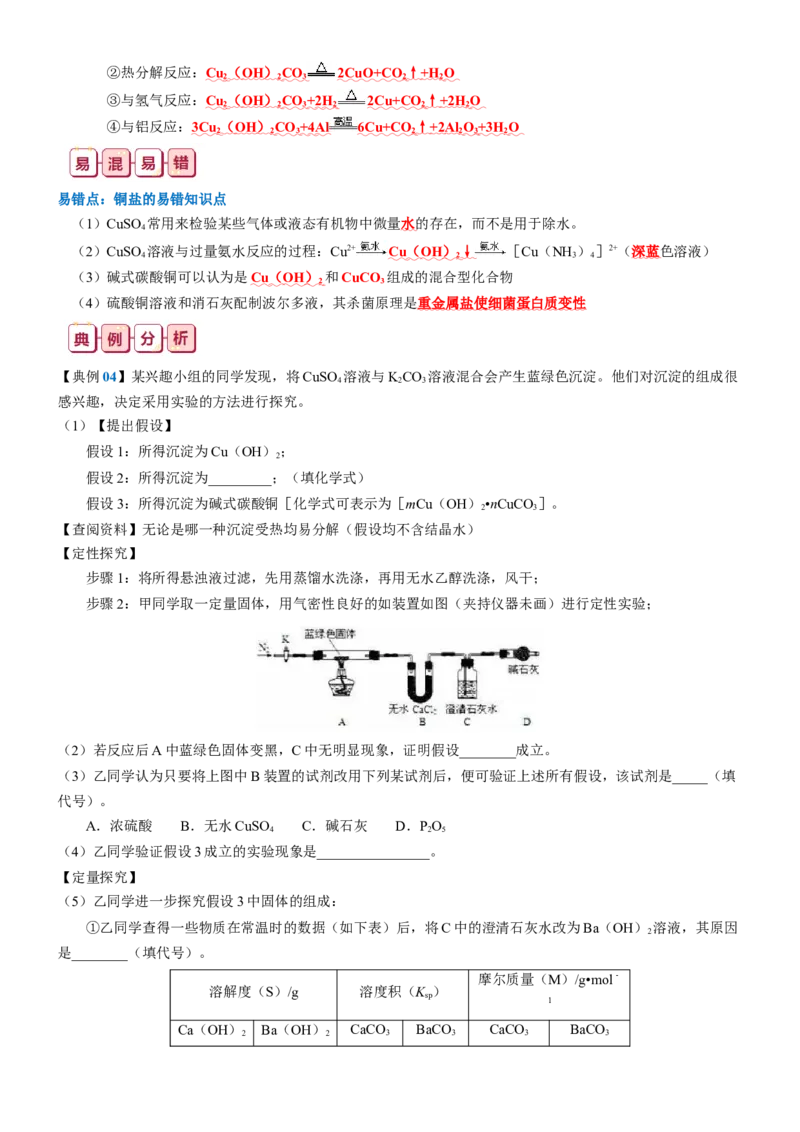
步骤2:甲同学取一定量固体,用气密性良好的如装置如图(夹持仪器未画)进行定性实验;
(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设________成立。
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是_____(填
代号)。
A.浓硫酸 B.无水CuSO C.碱石灰 D.PO
4 2 5
(4)乙同学验证假设3成立的实验现象是________________。
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH) 溶液,其原因
2
是________(填代号)。
摩尔质量(M)/g•mol﹣
溶解度(S)/g 溶度积(K )
sp
1
Ca(OH) Ba(OH) CaCO BaCO CaCO BaCO
2 2 3 3 3 32.9×10﹣ 2.6×10﹣
0.16 3.89 100 197
9 9
A.Ba(OH) 溶解度大于Ca(OH),能充分吸收CO
2 2 2
B.Ba(OH) 为强碱,Ca(OH) 为弱碱
2 2
C.吸收等量CO 生成的BaCO 的质量大于CaCO ,测量误差小
2 3 3
D.相同条件下,CaCO 的溶解度明显大于BaCO
3 3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g。
则该蓝绿色固体的化学式为________;A中发生反应的化学方程式为_______________。
【解析】(1)CuSO 溶液与NaCO 溶液混合产生蓝绿色沉淀,氢氧化铜和碳酸铜都是蓝色沉淀,可能是反应
4 2 3
复分解反应生成了碳酸铜沉淀,或双水解生成了氢氧化铜沉淀,或碱式碳酸铜,假设1中沉淀为Cu(OH),
2
假设2为CuCO;(2)加热氢氧化铜生成水蒸气和黑色氧化铜,加热碳酸铜分解生成二氧化碳和黑色氧化铜,
3
二氧化碳能使澄清的石灰水变浑浊,若反应后A中蓝绿色固体变黑,C中澄清石灰水不变浑,证明一定不含有
碳酸铜,现象的产生为氢氧化铜,假设1正确。(3)加热氢氧化铜生成水蒸气和黑色氧化铜,加热碳酸铜分解
生成二氧化碳和黑色氧化铜,二氧化碳能使澄清的石灰水变浑浊,所以需要验证水的存在和二氧化碳的存在就
可以证明产生的物质成分,装置A中加热是否变化为黑色固体,装置B选择无水硫酸铜验证是否生成水,澄清
石灰水是否变浑浊证明是否生成二氧化碳。(4)假设3:所得沉淀为碱式碳酸铜[化学式可表示为mCu
(OH)•nCuCO],氢氧化铜、碳酸铜分解,装置A中加热都会变化为黑色固体,装置B选择无水硫酸铜,
2 3
根据是否变蓝色验证是否生成水,根据装置C中澄清石灰水是否变浑浊证明是否生成二氧化碳,所以证明假设
是否正确的现象为:A中蓝绿色固体变黑色说明氢氧化铜、碳酸铜分解,B中无水CuSO 固体变蓝说明存在Cu
4
(OH),C中有白色沉淀产生说明存在CuCO,即能验证假设3成立,即A中蓝绿色固体变黑色,B中无水
2 3
CuSO 固体变蓝,C中有白色沉淀产生。(5)①Ba(OH) 溶解度大于Ca(OH),能充分吸收CO,故A正
4 2 2 2
确;氢氧化钙也为强碱,故B错误;BaCO 的摩尔质量大于CaCO ,测量误差小,故C正确;CaCO 的溶解度
3 3 3
和BaCO 溶解度相差不大,故D错误。②B中吸收水的物质的量n(HO)= =0.15mol,C中吸收二
3 2
氧化碳生成碳酸钡白色沉淀,根据碳原子守恒二氧化碳的物质的量:n(CO)=n(BaCO )= =
2 3
0.1mol,m(CO)=0.1mol×44g·mol-1=4.4g,氧化铜的质量为:m(CuO)=27.1g-2.7g-4.4g=20g,其物质
2
的量为:n(CuO)= =0.25mol,则铜离子、氢氧根离子和碳酸根离子的物质的量之比=
0.25mol∶0.3mol∶0.1mol=5∶6∶2,所以其化学式为:2CuCO•3Cu(OH) 或3Cu(OH)•2CuCO 或Cu
3 2 2 3 5
(OH)(CO),2CuCO•3Cu(OH) 受热分解生成CuO、二氧化碳和水,其反应的方程为:2CuCO•3Cu
6 3 2 3 2 3
(OH) 5CuO+3HO↑+2CO↑。
2 2 2
【答案】(1)CuCO(2)1(3)B
3
(4)A中蓝绿色固体变黑色,B中无水CuSO 固体变蓝,C中有白色沉淀产生
4
(5)①AC ②2CuCO•3Cu(OH) 或3Cu(OH)•2CuCO 或Cu (OH)(CO)
3 2 2 3 5 6 3 2
2CuCO•3Cu(OH) 5CuO+3HO↑+2CO ↑
3 2 2 2
知识点 04 金属的冶炼1.金属在自然界中的存在
(1)化合态:大多数金属
(2)游离态:金、铂等极少数金属
2.冶炼实质:金属离子 金属原子(Mn++ne-=M)
3.冶炼依据:金属离子的氧化性强弱不同
4.冶炼方法
(1)电解法:冶炼金属活泼性很强的金属(如K、Ca、Na、Mg、Al等)
①2NaCl(熔融) 2Na+Cl ↑
2
②MgCl (熔融) Mg+Cl ↑
2 2
③2Al O(熔融) 4Al+3O ↑
2 3 2
(2)热还原法:用还原剂(C、CO、H、Al、Na等)还原金属活泼性介于Zn~Cu之间的金属化合物。
2
①Fe O+3CO 2Fe+3CO
2 3 2
②2CuO+C 2Cu+CO ↑
2
③WO+3H W+3H O
3 2 2
④TiCl +4Na Ti+4NaCl
4
⑤Cr O+2Al 2Cr+Al O
2 3 2 3
(3)热分解法:用于冶炼不活泼金属Hg、Ag。
①2HgO 2Hg+O↑ ②2Ag O 4Ag+O↑
2 2 2
5.铜的冶炼“两方法”
(1)湿法炼铜:Fe+CuSO=FeSO +Cu。
4 4
(2)高温炼铜
①工业上用高温冶炼黄铜矿的方法获得粗铜
2CuFeS +4O Cu S+3SO+2FeO(炉渣)
2 2 2 2
2Cu S+3O 2Cu O+2SO
2 2 2 2
2Cu O+Cu S 6Cu+SO↑
2 2 2
②电解精炼铜:用粗铜做阳极,失电子变为Cu2+,用纯铜棒做阴极即可得精铜
易错点1:金属冶炼的易错知识点
(1)在化合物中金属元素都显正价,表现氧化性,但是处于中间价态的金属还表现还原性。
(2)金属冶炼的实质是金属阳离子得电子被还原为金属单质。
(3)金属越不活泼,其相应的金属阳离子的氧化性越强,越容易被冶炼。
易错点2:用还原法来冶炼某些很活泼的金属原理
Na+KCl=====K↑+NaCl
2RbCl+Mg========MgCl +2Rb↑
2主要运用了化学平衡移动原理,利用K、Rb沸点低,汽化离开反应体系,使化学反应得以向正反应方向进行。
【典例05】工业上,金属的制取有多种方法,选择何种方法与金属的性质密切相关。
(1)金属Na、Mg、Al等的制取常采用电解法。写出以铂为电极电解熔融氯化镁制镁的电极反应式。
阳极_______________________;阴极________________________________。
(2)金属钾因为易溶于盐而不易分离,且电解时有副反应发生,工业上通常用钠与氯化钾在高温下反应制取,
该反应为:Na(l)+KCl(l) NaCl(l)+K(g);ΔH>0,根据下表有关数据回答下列问题:
熔点 沸点
物质 密度(g/cm3)
(℃) (℃)
Na 0.97 97.81 890
K 0.86 63.65 770
NaCl 801 1465
KCl 776 1437
①制取钾的适宜温度范围为________________。
②制取钾的条件为________________。
A.适当高温高压 B.适当低温低压
C.适当高温低压 D.适当低温高压
③工业上采用此法制得的钾往往不纯,最可能含有的杂质是________________,检验方法为
_______________________________________。
(3)用铝热反应方法将Fe O 中的铁还原出来,写出该反应的化学方程式:
3 4
________________________________________________________
若用此法制得0.84t Fe,则转移电子________mol。
【解析】(1)电解熔融氯化镁制镁时,阳极是Cl―失去电子被氧化成Cl ,电极反应式为2Cl――2e―=Cl↑;
2 2
阴极是Mg2+得到电子被还原成Mg,电极反应式为Mg2++2e―=Mg。
(2)①K、Na的活泼性相近,要从上述可逆的置换反应中制取 K,主要是利用K的沸点比Na的低,而控制温
度使K气化,其余三种物质均为液体,便于生成的K蒸气不断逸出,使反应向生成K的方向进行而制得K。所
以温度应该高于K的沸点(774℃),高于其余三种物质中熔点最高的NaCl的熔点(801℃),而低于其余三
种物质中沸点最低的Na的沸点(890℃),综上分析,合适的温度范围应大于801℃,小于890℃。②从上分析
可知,制备钾必须采用适当的高温,保证钾以蒸汽形式存在,而减小压强,平衡 Na(l)+KCl(l) NaCl
(l)+K(g)正向移动,所以制取钾的条件为适当高温低压。③因为制备反应为可逆反应,而且钾蒸汽和钠蒸
汽的沸点差别不是特别大,所以制备的钾蒸汽中一定含有少量的钠蒸汽。检验金属钠可以用焰色试验,钠的焰
色为黄色。
(2)铝热反应是热还原法的一种,利用铝的还原性比铁的强将铁置换出来,反应的化学方程式为8Al+3Fe O
3 4
9Fe+4Al O ,该反应转移电子数为 24,即 9Fe~24e―,所以 n(e―)= n(Fe)= × =
2 3
4×104mol。
【答案】(1)阳极:2Cl――2e―=Cl↑ 阴极:Mg2++2e―=Mg
2
(2)①801℃~890℃ ②C ③钠 焰色试验(3)8Al+3Fe O 9Fe+4Al O 4×104mol
3 4 2 3
知识点 05 金属材料与合金
一、金属材料与合金的性质
1.金属材料:包括纯金属及其合金
2.合金的组成和性能
(1)形成:所有成分在一定温度范围内都是液体
(2)合金具有金属特性,如导电、传热等。
(3)合金硬度变大的原因:改变了金属原子有规则的层状排列,使原子层间的相对滑动变得困难。
二、铁合金
1.合金元素:主要是铁和碳
2.铁合金分类:根据含碳的不同分类
(1)生铁:含碳量2%~4.3%,硬度大,抗压、性脆、韧性差
(2)钢:含碳量0.03%~2%,硬度小,延展性好、韧性好、机械性能好
3.钢的分类
(1)碳素钢
①低碳钢:韧性、焊接性好,但硬度低,用于制造钢板、钢丝和钢管等
②中碳钢:硬度高,韧性及加工性好,用于制造钢轨、车轮和建材等
③高碳钢:硬而脆,热处理后弹性好,用于制造器械、弹簧和刀具等
(2)合金钢(特种钢)
①形成:在碳素钢中适量加入合金元素,使钢的组织机构发生变化
②性能:强度、硬度大,可塑性、韧性好,耐磨,耐腐蚀等
③不锈钢:合金元素主要是 铬( C r ) 和 镍( N i )
三、其他合金
1.铝合金
(1)硬铝
①合金元素:Cu、Mg、Si、Mn
②性能:密度小、强度高,具有较强的抗腐蚀能力
(2)镁铝合金:制造飞机和宇宙飞船的理想材料
2.青铜:铜和锡合金,最早使用的合金3.储氢合金
(1)概念:能够大量吸收氢气,并与氢气结合成金属氢化物的材料
(2)实用性要求
①储氢量大
②金属氢化物容易形成,稍微加热容易分解
③室温下吸、放氢速率快
(3)代表物:Ti-Fe合金,La-Ni合金
4.其他新型合金:钛合金、耐热合金、形状记忆合金等
易错点:合金的易错知识点
(1)合金中一定含有金属元素,可能含有非金属元素。
(2)合金是混合物,不是化合物。
(3)在合金中各组成成分元素的化合价都为 0 价 。
(4)合金在空气中容易形成原电池,所以一般合金比纯金属易被腐蚀。但是不锈钢不易被腐蚀。
(5)具有特定组成的合金,具有固定的熔沸点。
【典例06】JerryWoodall教授经研究发现,含有95%的铝和5%的镓、铟及锡组成的新型合金与水能快速反应制
得氢气,由于整个反应中,只消耗铝,而反应生成的Al O 可回收再利用,这样不仅降低了制氢气的成本,而
2 3
且方便快捷,这一发现将燃氢汽车的研发推向新的里程碑。据此,下列说法不正确的是( )。
A.铝作为燃料,有资源丰富的优势
B.组成合金的几种金属元素都位于周期表第ⅢA族
C.合金与水反应的总反应式为:2Al+3H O=Al O+3H ↑
2 2 3 2
D.合金中的镓、铟及锡对铝与水的反应起到催化作用
【解析】选B。铝是地壳中含有最多的金属,所以铝作为燃料,有资源丰富的优势,故A正确;铝、镓、铟是
周期表第ⅢA族元素,锡是周期表第ⅣA族元素,故B错误;整个反应中,只消耗铝,而反应生成的Al O,
2 3
则反应的方程式为2Al+3H O=Al O+3H ↑,故C正确;由镓、铟及锡组成的新型合金与水能快速反应制得氢
2 2 3 2
气,且只有铝反应进行,则合金中的镓、铟及锡对铝与水的反应起到催化作用,故D正确。