文档内容
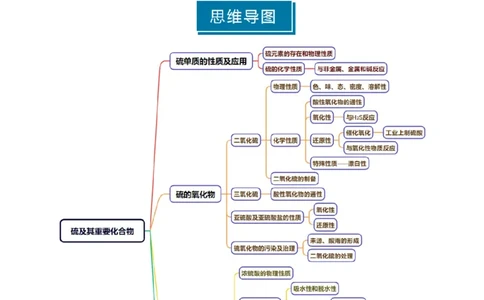
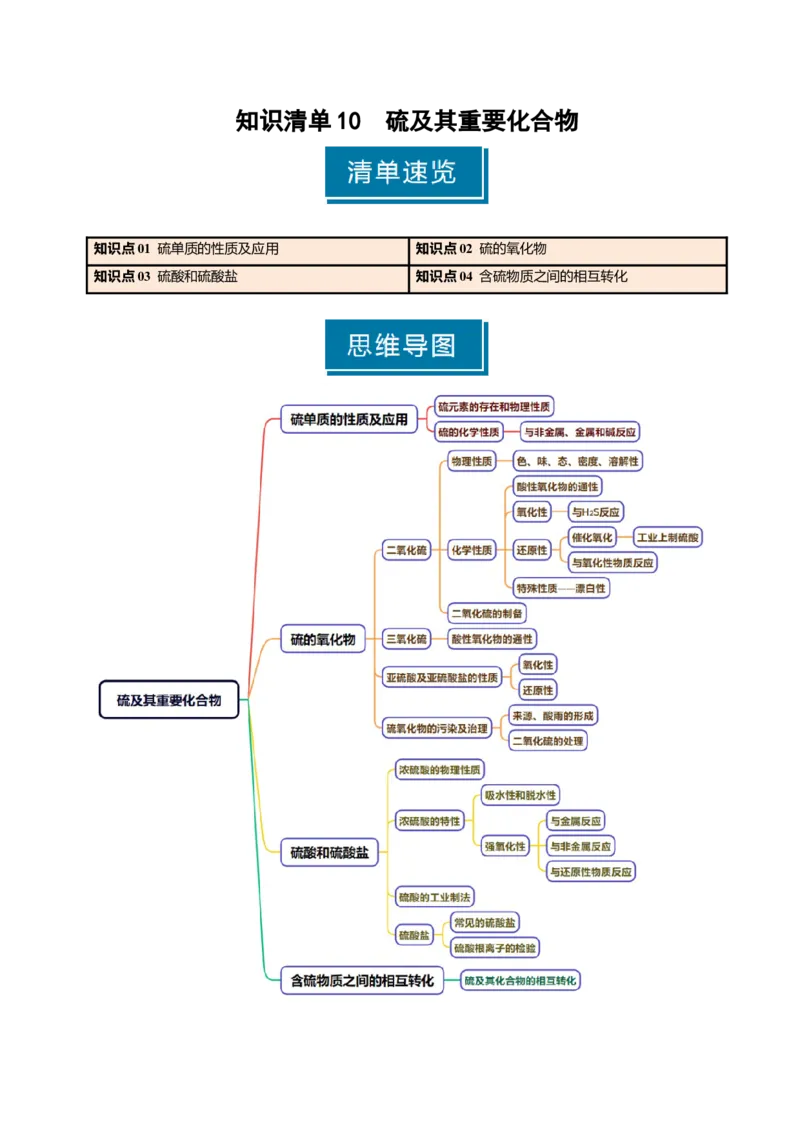
知识清单 10 硫及其重要化合物
知识点01 硫单质的性质及应用 知识点02 硫的氧化物
知识点03 硫酸和硫酸盐 知识点04 含硫物质之间的相互转化知识点 01 硫单质的性质及应用
1.硫元素的存在形态
游离态:_________附近或地壳的_________;
化合态:主要以_________和_________的性质存在。
2.硫的物理性质
______色或______色固体;俗称_______,质脆,易研成粉末,密度比水大,_____溶于水,______
溶于酒精,易溶于________。
3.硫的化学性质
S←――――――→S
(1)与非金属单质反应
与氧气反应:___________________________
与氢气反应:___________________________
(2)与金属反应
与钠反应:___________________________
与铁反应:___________________________
与铜反应:___________________________
与汞反应:___________________________ 应用:去除洒落的汞
硫与变价金属反应生成______价态化合物
(3)与NaOH溶液反应:____________________________________ 应用:清洗试管壁残留的硫
(1)硫与Fe反应生成FeS,与Cu反应生成CuS( )
(2)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理( )
(3)硫与少量的O 反应生成SO ,与过量的O 反应生成SO ( )
2 2 2 3
(4)硫与少量的O 反应生成SO ,与过量的O 反应生成SO ( )
2 2 2 3
(5)实验室洗涤附着在试管内壁上的硫,可用酒精清洗( )
1.硫和氯气的氧化性强弱比较方法
(1)与变价金属反应,Cl 与变价金属反应生成_______价态化合物,S与变价金属反应生成______价态化
2
合物;(2)氢化物的稳定性:HCl____HS;
2
(3)置换反应:____________________________________;
(4)最高价含氧酸的酸性:HClO_____HSO ;
4 2 4
(5)还原性:S2-_______Cl-。
2.S与NaOH溶液反应的方程式为:3S+6NaOH=====2NaS+Na SO +3H O,氧化剂与还原剂的物质的
2 2 3 2
量之比为_________,每1 mol S参加反应,转移的电子数为_________。
知识点 02 硫的氧化物
一、二氧化硫(SO )
2
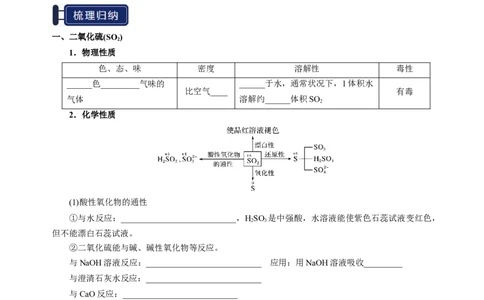
1.物理性质
色、态、味 密度 溶解性 毒性
______色_________气味的 ______于水,通常状况下,1体积水
比空气____ 有毒
气体 溶解约______体积SO
2
2.化学性质
(1)酸性氧化物的通性
①与水反应:___________________________,HSO 是中强酸,水溶液能使紫色石蕊试液变红色,
2 3
但不能漂白石蕊试液。
②二氧化硫能与碱、碱性氧化物等反应。
与NaOH溶液反应:___________________________ 应用:用NaOH溶液吸收_________
与澄清石灰水反应:___________________________
与CaO反应:___________________________
③NaSO 溶液中通入SO 气体:___________________________
2 3 2
(2)氧化性(如与HS反应):___________________________
2
(3)还原性
①催化氧化:___________________________ (_________反应) 应用:工业上制取_________
②在溶液中,SO 、HSO 、SO与氧化性物质(如Cl 、Br 、I 、O 、HO 、Fe3+、酸性KMnO 、硝
2 2 3 2 2 2 2 2 2 4
酸等)反应,产物是SO。
SO 与氯水反应:____________________________________
2
SO 与HO 反应:____________________________________
2 2 2
HSO 被氧气氧化:____________________________________
2 3NaSO 被氧气氧化:____________________________________
2 3
SO 与Fe3+反应:____________________________________
2
SO与酸性高锰酸钾溶液反应:____________________________________
(4)漂白性
使某些有色物质(如品红溶液)生成_________的无色物质,若加热,__________________的颜色。
应用:实验室常用___________检验SO 气体。
2
3.亚硫酸的性质
(1)弱酸性: ____________________________________(电离方程式)
(2)不稳定性:____________________________________
(3)强还原性(与O、HO 反应):
2 2 2
____________________________________;____________________________________
(4)弱氧化性(与HS反应):____________________________________
2
二、三氧化硫(SO )
3
1.物理性质
标准状况下,SO 是一种_________固体,熔点、沸点_________。
3
2.化学性质
SO 是_________氧化物,具有_________氧化物的通性。
3
①SO 与水反应:___________________________,反应放出大量的热。
3
②SO 与碱性氧化物反应:
3
与CaO反应的方程式为:___________________________
③SO 与碱反应:
3
与Ca(OH) 反应的方程式为:____________________________________
2
三、硫的氧化物的污染与治理
1.硫的氧化物来源、危害及治理
(1)来源:____________的燃烧及____________的冶炼等。
(2)危害:危害人体健康,形成酸雨(pH小于_______)
(3)治理:燃煤脱硫、改进燃烧技术、废气中的二氧化硫回收处理等。
2.硫酸型酸雨的形成过程(两条路径):
有关化学方程式:
路径一:___________________________,___________________________
路径二:___________________________,___________________________
3.常见的SO 处理方法
2
方法一:钙基固硫法
用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共同反应生成硫酸钙,从而使硫转移到煤
2
渣中,反应原理为:___________________________ , ___________________________ ,
___________________________。
方法二:氨水脱硫法
雾化的氨水与烟气中的SO 直接接触吸收SO ,其反应的化学方程式为:
2 2
____________________________________,____________________________________。
方法三:钠碱脱硫法
钠碱脱硫法是用NaOH/Na CO 吸收烟气中的SO ,得到NaSO 和NaHSO ,发生反应的化学方程式
2 3 2 2 3 3
为:
___________________________ , ___________________________ ,
___________________________。
方法四:双碱脱硫法
先利用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的 NaOH碱液可循环使用,化学反应原
2
理为:
①吸收反应:___________________________,___________________________。
②再生反应:____________________________________,____________________________________。
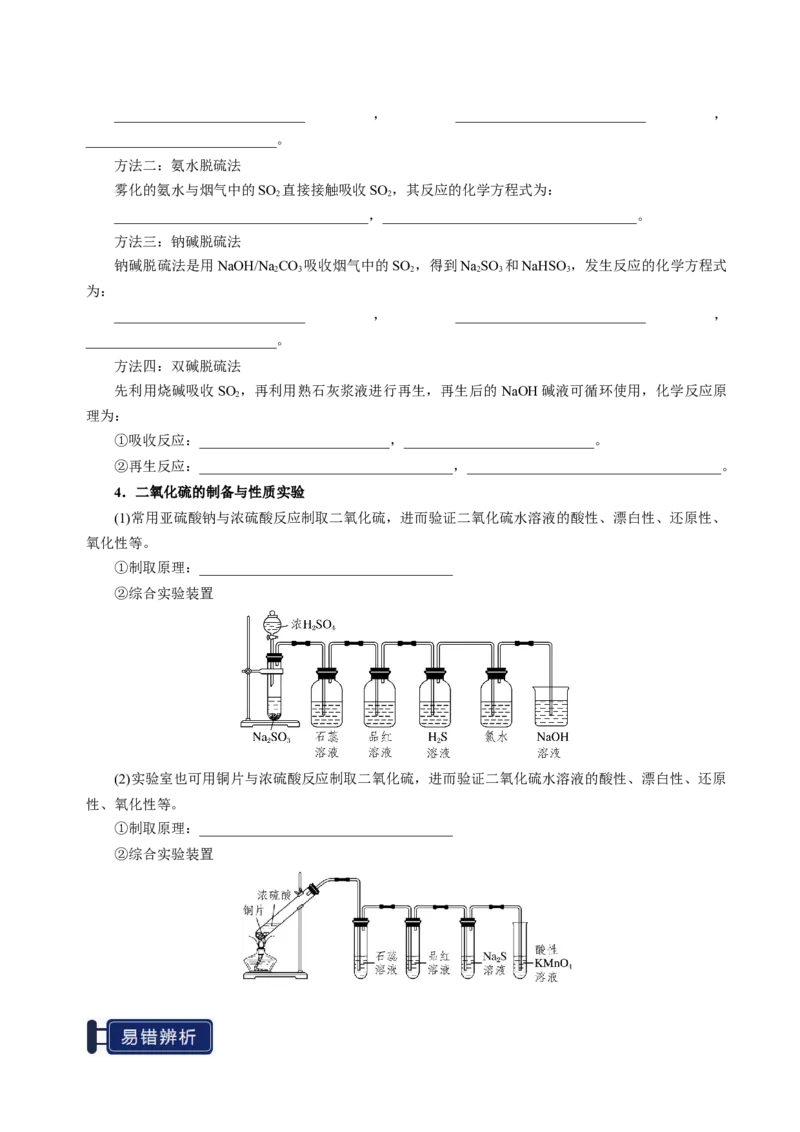
4.二氧化硫的制备与性质实验
(1)常用亚硫酸钠与浓硫酸反应制取二氧化硫,进而验证二氧化硫水溶液的酸性、漂白性、还原性、
氧化性等。
①制取原理:____________________________________
②综合实验装置
(2)实验室也可用铜片与浓硫酸反应制取二氧化硫,进而验证二氧化硫水溶液的酸性、漂白性、还原
性、氧化性等。
①制取原理:____________________________________
②综合实验装置(1)标准状况下,2.24 L SO 中含有硫原子数为N ( )
3 A
(2)将SO 通入紫色石蕊溶液中先变红后褪色( )
2
(3)SO 具有氧化性,可用于漂白纸浆( )
2
(4)SO 使溴水、酸性高锰酸钾溶液褪色, SO 体现漂白性( )
2 2
(5)SO 与NaClO溶液混合使用,漂白效果更好( )
2
(6)在空气中加热蒸干NaSO 溶液,最终得到NaSO 固体( )
2 3 2 4
(7)SO 2-和S2-在碱性条件下能够大量共存,在酸性条件下不能大量共存( )
3
(8)将SO 通入漂白液中涉及的反应为SO +ClO−+H O HSO−+HClO( )
2 2 2 3
一、二氧化硫性质的多重性
1.二氧化硫和某些盐溶液反应的产物
(1)把SO 气体通入BaCl 溶液中,没有__________沉淀生成;
2 2
(2)把SO 气体通入BaCl 溶液中,再通入NH 或加入NaOH溶液,有_________沉淀生成;
2 2 3
(3)把SO 气体通入BaCl 和HO 的混合溶液中,有_________沉淀生成;
2 2 2 2
(3)把SO 气体通入Ba(NO ) 溶液中,产生_________沉淀;
2 3 2
(4)把 CO 气体通入 Ca(ClO) 溶液中,产生_________沉淀;把 SO 气体通入 Ca(ClO) 溶液中,产生
2 2 2 2
_________沉淀。
2.将SO 分别通入下列五种溶液中:
2
(1)试管①中的实验现象:KMnO 酸性溶液______________,证明SO 具有____________性。
4 2
(2)试管②中的实验现象:品红溶液________________,证明SO 具有____________性。
2
(3)试管③中能否观察到沉淀______________(填“能”或“否”)。
(4)试管④中能产生白色沉淀,该沉淀是____________。
(5)试管⑤中能产生白色沉淀,该沉淀是____________,用离子方程式表示产生沉淀的过程:
________________________________________________。
二、几种漂白性物质的比较
下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、酸性高锰酸钾溶液、石蕊溶液褪色
2
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同
2 2 2
D.将SO 气体通入滴有酚酞的NaOH溶液中,溶液褪色,说明SO 具有漂白性
2 2
【归纳小结】三类漂白剂的区别
类型 原理 举例 特点 备注HClO、NaClO、
将有机色质内部“生色
氧化型 Ca(ClO) 、NaO、HO、 不可逆、持久 无选择性
2 2 2 2 2
团”破坏掉
O 等
3
与有机色质内部“生色
加合型 团”“化合”成无色物 SO 可逆、不持久 有选择性
2
质
吸附型 将有色物质吸附而褪色 活性炭 物理变化 吸附色素
三、二氧化硫的检验
1.为确定某纯净的气体是否为SO ,进行了如下几种实验,其中不正确的是( )
2
选项 操作及现象(现象在括号内) 结论
A 闻气味(有刺激性)――→酸性KMnO 溶液(褪色) 一定是SO
4 2
B 闻气味(有刺激性)――→澄清石灰水(变浑浊) 可能是SO
2
C ――→品红溶液(褪色)――→变红色 一定是SO
2
D ――→紫色石蕊溶液(先变红色后褪色) 一定不是SO
2
2.下图是检验某无色气体A是SO 和CO 的混合气体的装置图,按要求回答下列问题:
2 2
(1)B中加入的试剂是________,作用是_____________________________________________。
(2)C中加入的试剂是__________,作用是__________________________________________。
(3)D中加入的试剂是______________,作用是______________________________________。
(4)实验时,C中应观察到的现象是________________________________________________。
【归纳小结】检验SO 和CO 同时存在的一般流程
2 2
SO 和CO 都能使澄清的石灰水变浑浊,检验二者同时存在的一般流程如下:
2 2
流程设计 检验SO 除去SO 检验SO 是否除尽⇒检验CO
2 2 2 2
选用试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清的石灰水
⇒ 4 ⇒
预期现象 褪色 褪色 不褪色 变浑浊
注意:有时为简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,用较浓的酸性KMnO
2 2 4
溶液,现象是酸性KMnO 溶液颜色变浅,但不褪成无色。
4
知识点 03 硫酸和硫酸盐
1.硫酸的物理性质
(1)实验室常用的浓硫酸质量分数为_______,密度大(1.84 g·cm-3),沸点_____,______挥发,常
温下比较稳定。(2)硫酸与水以任意比互溶,浓硫酸溶解时可放出大量的热;浓硫酸的稀释方法是______________
________________________________________________________。
2.浓硫酸的特性
(1)吸水性和脱水性
①吸水性是物质本身具有HO水分子被浓硫酸吸走(包括_______和_______); 脱水性是被脱水物
2
质本身_______HO水分子,但含有_______,被浓硫酸按______________脱去(如蔗糖炭化实验)。
2
②浓硫酸作干燥剂的注意点
可干燥酸性气体(如CO、SO 、Cl 等)和中性气体(如O、N、CO等)。
2 2 2 2 2
不可干燥的气体:碱性气体(如NH )和某些还原性气体(如HBr、HI、HS等)。
3 2
(2)强氧化性
①常温下,铁、铝表面被浓硫酸氧化为______________而钝化,从而阻止了酸与内层金属的进一步
反应,所以常温下可以用______________容器来盛装浓硫酸。
②与Zn反应:开始产生_______,后来产生_______:
___________________________________;___________________________________
③与铜反应:___________________________________
④与非金属的反应
浓硫酸与木炭反应的化学方程式:___________________________________。
⑤与还原性化合物反应:
浓硫酸能将还原性化合物(如FeO、HBr、HI、HS等)氧化。
2
浓硫酸与FeO反应:___________________________________。
浓硫酸与HBr反应:___________________________________。
浓硫酸与HS反应:___________________________________。
2
3.SO的检验
(1)检验SO的操作过程
待测液――――→取清液――――→_______沉淀,即可确定是否存在SO。
(2)理论解释
①先加稀盐酸的目的是________________________________________。
②再加BaCl 溶液,有白色沉淀产生,发生反应的离子方程式:_____________________。
2
4.几种常见的硫酸盐
硫酸盐 主要性质 主要应用
CaSO·2H O======2CaSO·H O 制作_______和医用___________,调节
硫酸钙 4 2 4 2
生石膏 熟石膏 水泥的______________
CuSO ======CuSO ·5H O(胆矾) 检验_____的存在,与___________混合
硫酸铜 4 4 2
白色 蓝色 制备波尔多液
又称重晶石,不溶于水和酸,且不易被X射 用作消化系统X射线检查的
硫酸钡
线透过 ___________,即“钡餐”
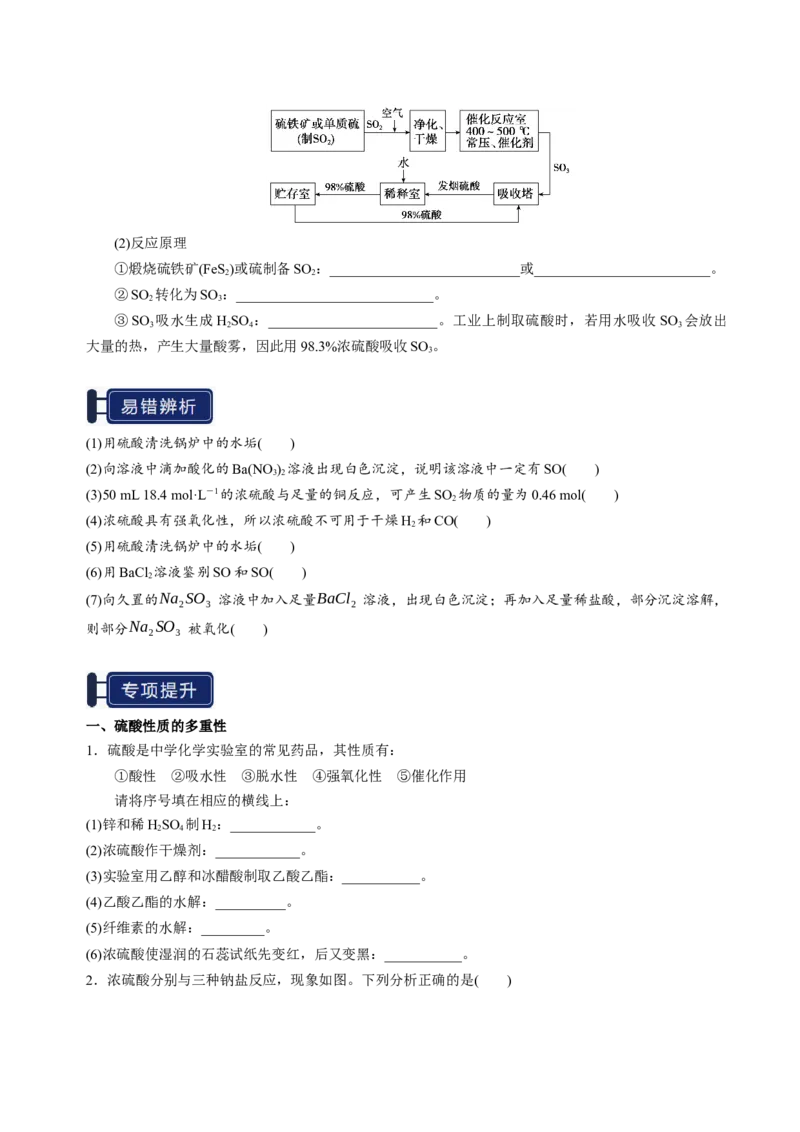
5.工业制备硫酸的反应原理
(1)工艺流程(2)反应原理
①煅烧硫铁矿(FeS )或硫制备SO :___________________________或_________________________。
2 2
②SO 转化为SO :____________________________。
2 3
③SO 吸水生成HSO :________________________。工业上制取硫酸时,若用水吸收 SO 会放出
3 2 4 3
大量的热,产生大量酸雾,因此用98.3%浓硫酸吸收SO 。
3
(1)用硫酸清洗锅炉中的水垢( )
(2)向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有SO( )
3 2
(3)50 mL 18.4 mol·L-1的浓硫酸与足量的铜反应,可产生SO 物质的量为0.46 mol( )
2
(4)浓硫酸具有强氧化性,所以浓硫酸不可用于干燥H 和CO( )
2
(5)用硫酸清洗锅炉中的水垢( )
(6)用BaCl 溶液鉴别SO和SO( )
2
(7)向久置的Na SO 溶液中加入足量BaCl 溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解,
2 3 2
则部分Na SO 被氧化( )
2 3
一、硫酸性质的多重性
1.硫酸是中学化学实验室的常见药品,其性质有:
①酸性 ②吸水性 ③脱水性 ④强氧化性 ⑤催化作用
请将序号填在相应的横线上:
(1)锌和稀HSO 制H:____________。
2 4 2
(2)浓硫酸作干燥剂:____________。
(3)实验室用乙醇和冰醋酸制取乙酸乙酯:___________。
(4)乙酸乙酯的水解:__________。
(5)纤维素的水解:_________。
(6)浓硫酸使湿润的石蕊试纸先变红,后又变黑:___________。
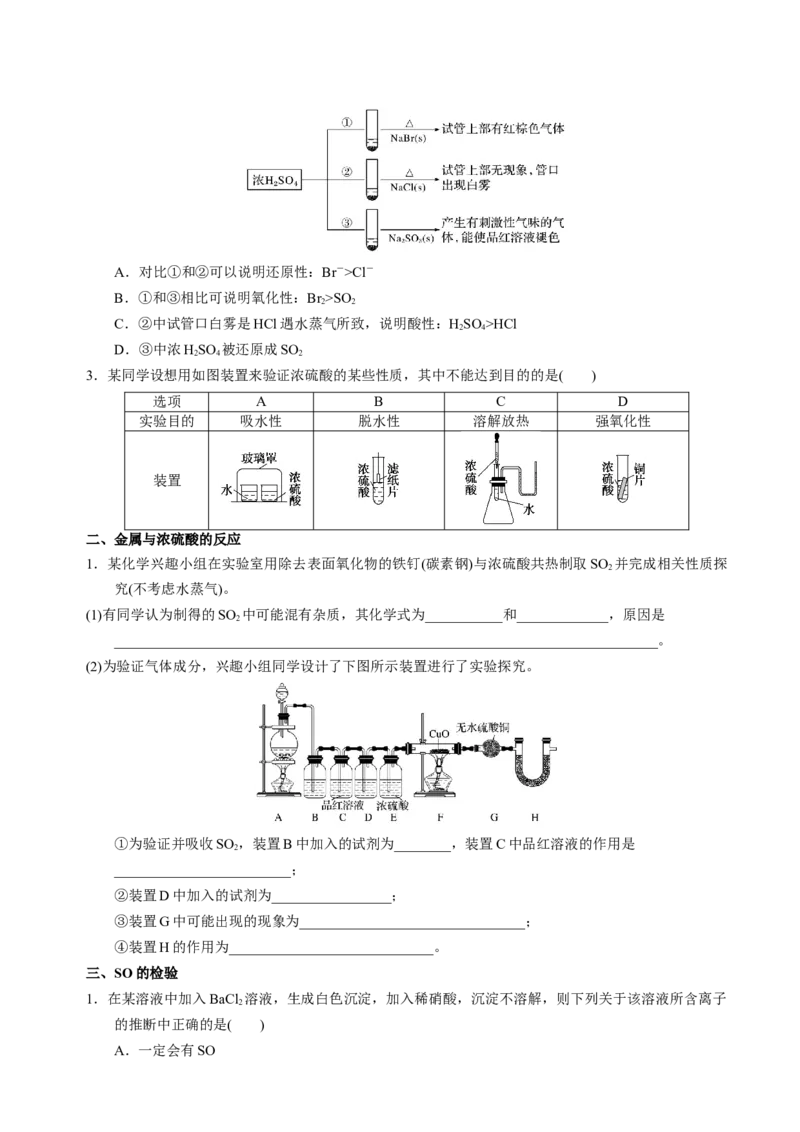
2.浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )A.对比①和②可以说明还原性:Br->Cl-
B.①和③相比可说明氧化性:Br >SO
2 2
C.②中试管口白雾是HCl遇水蒸气所致,说明酸性:HSO >HCl
2 4
D.③中浓HSO 被还原成SO
2 4 2
3.某同学设想用如图装置来验证浓硫酸的某些性质,其中不能达到目的的是( )
选项 A B C D
实验目的 吸水性 脱水性 溶解放热 强氧化性
装置
二、金属与浓硫酸的反应
1.某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO 并完成相关性质探
2
究(不考虑水蒸气)。
(1)有同学认为制得的SO 中可能混有杂质,其化学式为___________和_____________,原因是
2
_____________________________________________________________________________。
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究。
①为验证并吸收SO ,装置B中加入的试剂为________,装置C中品红溶液的作用是
2
_________________________;
②装置D中加入的试剂为_________________;
③装置G中可能出现的现象为________________________________;
④装置H的作用为_____________________________。
三、SO的检验
1.在某溶液中加入BaCl 溶液,生成白色沉淀,加入稀硝酸,沉淀不溶解,则下列关于该溶液所含离子
2
的推断中正确的是( )
A.一定会有SOB.含有SO和Ag+
C.可能含有SO、Ag+、SO中的一种或同时含有SO、SO
D.可能含有SO或CO
2.有一瓶NaSO 溶液,可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO ) 溶液,产
2 3 3 2
生白色沉淀,再加入足量稀硝酸,充分振荡后,白色沉淀不溶解。对此实验的下列叙述正确的是(
)
A.实验证实NaSO 已部分氧化
2 3
B.实验中加入Ba(NO ) 溶液后的沉淀一定是BaSO
3 2 4
C.实验中加入足量硝酸后的沉淀是BaSO 和BaSO 的混合物
4 3
D.此次实验不能确定NaSO 是否部分被氧化
2 3
知识点 04 含硫物质之间的相互转化
1.硫元素的价态—类别二维图
2.含硫化合物之间的相互转化
含硫物质多种多样,在一定条件下可相互转化。通过____________反应可实现含有不同价态硫元素
的物质之间的转化;通过____________反应可实现含有相同价态硫元素的不同物质间的转化。
(1)相同价态硫的转化是通过酸、碱反应实现的
如:
写出②③④反应的化学方程式:
②__________________________________________;
③__________________________________________;
④__________________________________________。
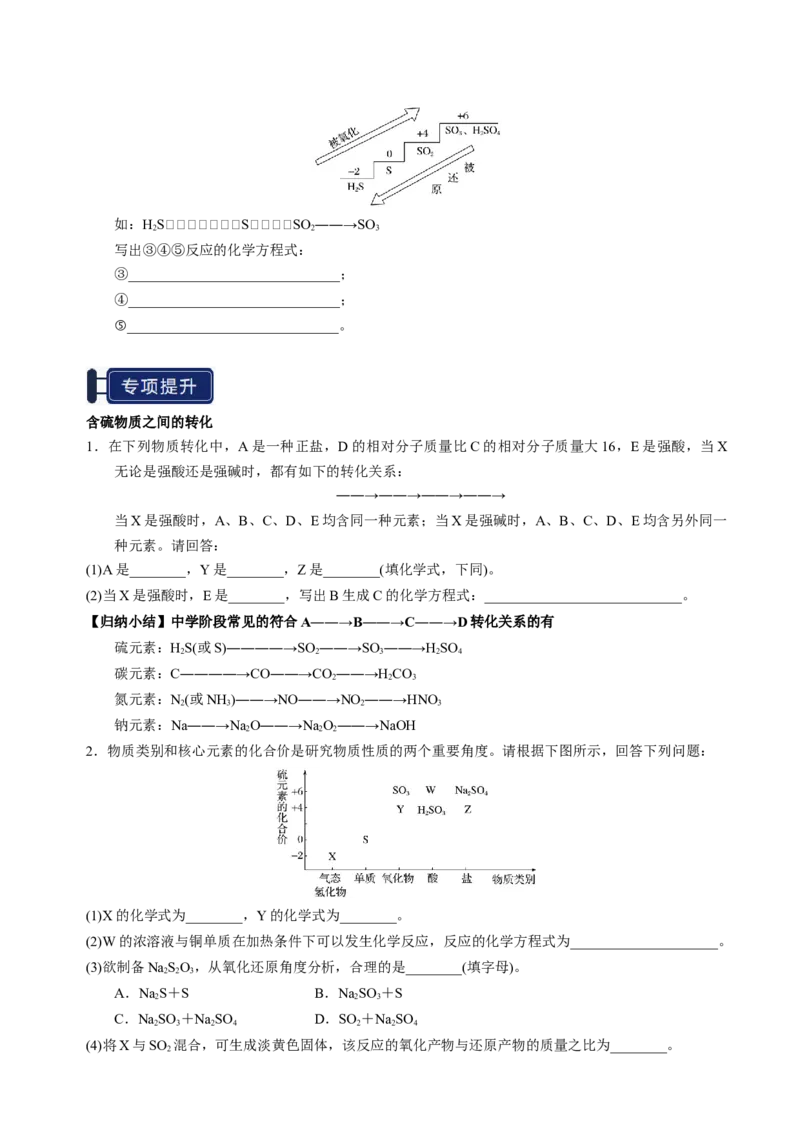
(2)不同价态硫的转化是通过氧化还原反应实现的
当硫元素的化合价升高或降低时,一般升高或降低到其
相邻的价态,即台阶式升降,可用下图表示如:HSSSO ――→SO
2 2 3
写出③④⑤反应的化学方程式:
③______________________________;
④______________________________;
⑤______________________________。
含硫物质之间的转化
1.在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是强酸,当X
无论是强酸还是强碱时,都有如下的转化关系:
――→――→――→――→
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一
种元素。请回答:
(1)A是________,Y是________,Z是________(填化学式,下同)。
(2)当X是强酸时,E是________,写出B生成C的化学方程式:____________________________。
【归纳小结】中学阶段常见的符合A――→B――→C――→D转化关系的有
硫元素:HS(或S)――――→SO ――→SO ――→HSO
2 2 3 2 4
碳元素:C――――→CO――→CO――→HCO
2 2 3
氮元素:N(或NH )――→NO――→NO ――→HNO
2 3 2 3
钠元素:Na――→NaO――→NaO――→NaOH
2 2 2
2.物质类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:
(1)X的化学式为________,Y的化学式为________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_____________________。
(3)欲制备NaSO,从氧化还原角度分析,合理的是________(填字母)。
2 2 3
A.NaS+S B.NaSO +S
2 2 3
C.NaSO +NaSO D.SO +NaSO
2 3 2 4 2 2 4
(4)将X与SO 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为________。
2