文档内容
专项训练 离子的检验和推断(解析版)
1.(2023春·四川成都·高一树德中学校考阶段练习)X溶液中含有下表所示离子中的
某5种,且其离子浓度均为 (不考虑水的电离和离子水解)。向X溶液中加入
足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是
阳离
、 、 、 、 、
子
阴离
、 、 、 、
子
A.原溶液中一定含有
B.X溶液中一定没有
C.X溶液中含有3种阳离子、2种阴离子
D.生成气体的离子方程式为
【答案】C
【分析】各种离子的物质的量浓度均为0.1mol/L,向X溶液中加入足量稀盐酸,有气
体生成,反应前后阴离子种类不变,产生气体不可能是碳酸根离子;根据表中的离子,
可以推知是Fe2+、 在酸性环境下生成的一氧化氮,加入盐酸,溶液中阴离子种类
不变,所以原来溶液中含有Cl-,若只含有氯离子和硝酸根离子,二者的浓度为
0.1mol/L,根据电荷守恒是不可能的,所以还含有阴离子 ,由于总共含有5种离子,
再根据电荷守恒可知还含有一种带有两个正电荷Mg2+,所以原溶液中含有的五种离子
为: Cl-、 、 、Fe2+、Mg2+,据此进行解答。
【详解】A.原溶液中一定含有Mg2+,故A选项正确;
B.根据分析可知,溶液中一定不存在 ,故B选项正确;
C.根据分析可知,原溶液中含有的五种离子为:C1-、 、 、 Fe2+、 Mg2+,3
种阴离子、2种阳离子,故C选项错误;
D.根据分析可知,生成气体为NO,反应的离子方程式为:
1
学科网(北京)股份有限公司,故D选项正确;
故选C。
2.(2023秋·陕西西安·高一西安市第七十五中学校考期末)混合物的水溶液中只可能
含有以下离子中的若干种: 、 、Mg2+、Ba2+、K+、 、 ,现取三份体
积均为100mL的该溶液进行如下实验:第一份加入AgNO;溶液有沉淀产生;第二份
3
加入足量NaOH溶液并加热,收集到气体0.04mol;第三份加入足量BaCl 溶液后,经
2
过滤、洗涤、干燥,得到沉淀6.27g,再用足量盐酸洗涤、干燥,沉淀质量减少为
2.33g。根据上述实验,下列有关该溶液组成的推断正确的是
A.一定不存在K+ B.可能存在Cl-
C.含有 ,其浓度为0.1mol/L D.可能存在Mg2+、Ba2+
【答案】B
【分析】第一份加入 ,溶液有沉淀产生,溶液中可能含有 和 ;第二份
加入足量 溶液并加热,收集到气体0.04mol,溶液中一定含有 ,物质的量
为0.04mol;第三份加入足量BaCl 溶液后,经过滤、洗涤、干燥,得到沉淀6.27g,再
2
用足量盐酸洗涤、干燥,沉淀质量减少为2.33g,得到的沉淀为 和 ,其中
为2.33g,物质的量为 , 为 ,所以溶
液中一定含有 , ,溶液中一定不存在 和 ,正电荷
的离子为 ,带负电荷的离子为 , ,根据电荷守
恒,溶液中一定含有 ,可能存在 。
【详解】A.根据以上分析,溶液中一定含有 ,A错误;
B.根据以上分析,溶液中可能存在 ,B正确;
C.根据计算,溶液中含有 ,浓度为 ,C错误;
D.根据以上分析,溶液中含有 ,一定不存在 和 ,D错误;
试卷第2页,共30页故选B。
3.(2023·安徽黄山·统考三模)某工业废水中可能含有K+、Ag+、Mg2+、Cu2+、Al3+、
NH 、Cl-、CO 、NO 、SO 、I-中的几种,且各离子物质的量浓度均为0.2mol/
L(忽略水的电离及离子的水解),欲探究废水的组成,进行了如下实验:
I.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV.向III中所得溶液中加入BaCl 溶液,有白色沉淀生成。
2
下列推断不正确的是
A.溶液中一定不含的阳离子是K+、NH 、Cu2+、Ag+
B.III中加入盐酸生成无色气体的离子方程式为:8H++6I-+2NO =3I +2NO↑+4HO
2 2
C.原溶液除H+和OH-外只含有Mg2+、Al3+、NO 、SO 、I-
D.另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤、洗涤、灼烧沉淀
至恒重,得到固体质量0.8g
【答案】C
【分析】I.取该无色溶液5 mL,说明一定不含有Cu2+,滴加一滴氨水有沉淀生成,且
离子种类增加,说明增加的是NH ,所以原溶液中一定不含NH ,可能含有Mg2+、
Al3+,不含NH 、CO ;
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰,说明没有
K+;
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时
溶液依然澄清,说明有还原性离子I-与NO 和H+反应生成NO,即溶液中有I-、NO
,一定不含有Ag+。
IV.向III中所得的溶液中加入BaCl 溶液,有白色沉淀生成,说明有SO ;
2
综上所述,一定含有的阴离子为NO 、SO 、I-,各离子物质的量浓度均为
3
学科网(北京)股份有限公司0.2mol/L,结合电荷守恒可知,溶液中一定有Mg2+和Al3+,且还含有一种-1价的阴离
子为Cl-,以此解答。
【详解】A.由分析可知,溶液中一定不含的阳离子是K+、NH 、Cu2+、Ag+,故A正
确;
B.III中加入盐酸,I-与NO 和H+反应生成NO,根据得失电子守恒和电荷守恒配平离
子方程式为:8H++6I-+2NO =3I +2NO↑+4HO,故B正确;
2 2
C.由分析可知,原溶液除H+和OH-外只含有Mg2+、Al3+、NO 、SO 、I-、Cl-,故C
错误;
D.另取100 mL原溶液,加入足量的NaOH溶液,Mg2+、Al3+反应生成Mg(OH) 、
2
NaAlO ,充分反应后过滤,洗涤,灼烧沉淀至恒重,根据元素守恒:
2
n(MgO)=n(Mg2+)=cV=0.2 mol/L×0.1 L=0.02 mol,m(MgO)=0.02 mol×40 g/mol=0.8 g,故
D正确;
故选C。
4.(2023·安徽马鞍山·统考一模)某溶液仅由 、Cl-、 、 、 、
Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀:
2
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁
C.原溶液中一定不存在 、Al3+,可能含有K+
D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
【答案】C
【分析】加入过量的碱产生气体为NH ,溶液有 。信息②知加入过量的碱产生了
3
沉淀Fe(OH) ,溶液中有Fe3+, 与Fe3+会发生双水解不能共存,则溶液中不存在
3
试卷第4页,共30页。信息③知加溶液中有 。
【详解】A.由上分析溶液中一定有 ,A项正确;
B.Fe(OH) 受热分解为氧化铁Fe O,B项正确;
3 2 3
C.由上分析溶液中一定有 和Fe3+而阴离子有 ,又溶液中各离子浓度相同,
溶液中电荷不守恒,所以一定还有Cl-和 。溶液中这五种离子刚好电荷守恒,所以
一定不存在 和Al3+、K+,C项错误;
D.由C项分析溶液中一定存在 、Fe3+、 、Cl-和 ,D项正确;
故选C。
5.(2023·辽宁·校联考二模)某溶液中可能存在K+、Na+、Fe2+、Al3+、SO 、SO 中
的若干种(除水电离出的H+、OH-之外),并且每种离子的浓度均为0.2mol/L。为确定溶
液的组成进行了如下实验:
i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色。
ii.往i的溶液中加BaCl 溶液,产生难溶于水的白色沉淀。
2
下列有关判断正确的是
A.SO ,Fe2+可能同时存在于溶液中
B.若溶液中有SO ,则蘸取该溶液做焰色试验,可能观察到黄色火焰
C.溶液中可能有Al3+,一定没有SO
D.产生红棕色气体的离子方程式一定是3Fe2++4H++NO=3Fe3++NO↑
【答案】B
【分析】i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色,
则含有还原性的离子 或 ;ii.往i的溶液中加BaCl 溶液,产生难溶于水的白色
2
沉淀,则为硫酸钡沉淀。由电荷守恒分析出该溶液可能有两种组成,一种是 ,
。一种是 , , 。
5
学科网(北京)股份有限公司【详解】A. , 因双水解而不可能同时存在,只能二选一,A选项错误。
B.若溶液中有 ,则含有 , ,做焰色试验,可能观察到黄色火焰,B选项
正确。
C.据分析,溶液中不可能有 ,故C选项错误。
D.产生红棕色气体的离子方程式可能是 ,也可能
是 和 反应,故D选项错误。
故选B。
6.(2023·上海·高三专题练习)某溶液由Na+、Al3+、Fe3+、NH 、Cl-、NO 、CO 、
SO 中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适
量溶液进行如下实验。
步骤一 加入过量NaOH溶液,加热,出现气泡和沉淀;
步骤二 过滤,得滤液、滤渣;
步骤三 取滤渣,洗涤、灼烧,得固体a;
步骤四 取少量滤液,加入足量BaCl 溶液,出现白色沉淀;
2
根据实验,下列推断错误的是
A.根据步骤一,肯定存在NH 、Fe3+
B.步骤三所得固体a为氧化铁
C.原溶液一定不存在Al3+、CO
D.原溶液可能存在Na+
【答案】D
【分析】取该溶液加入过量NaOH溶液,加热,出现气泡和沉淀,说明含有NH 、
Fe3+,Fe3+与CO 会发生完全双水解而不能共存,则一定不含CO ,步骤四中取少量
滤液,加入足量BaCl 溶液,出现白色沉淀,说明含有SO ,根据以上分析可知,原
2
试卷第6页,共30页溶液中含有NH 、Fe3+、SO ,由于各离子的物质的量浓度相同,根据溶液呈电中性
规则可知,原溶液中一定含有Cl-、NO ,一定不含Na+、Al3+;
【详解】A.据分析可知,根据步骤一,肯定存在NH 、Fe3+,A正确;
B.Fe3+与NaOH反应生成Fe(OH) 沉淀,Fe(OH) 沉淀灼烧得到Fe O,则步骤三所得
3 3 2 3
固体a为氧化铁,B正确;
C.据分析可知,原溶液一定不存在Al3+、CO ,C正确;
D.据分析可知,原溶液一定不存在Na+,D错误;
故选D。
7.(2023·广东肇庆·高要一中校考二模)某无色溶液中可能含有Na+、K+、Fe3+、
Cu2+、SO 、SO 、CO 、Cl-、Br-中的若干种,依次进行下列实验,观察到的现象
记录如下。
①pH试纸检验,溶液的pH>7
②取少量原溶液,向溶液中加入过量的BaCl 和盐酸的混合溶液,无白色沉淀生成
2
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,再加入CCl 振荡,静置后
4
CCl 层呈橙色,用分液漏斗分液
4
④向分液后的水溶液中加入Ba(NO ) 溶液和HNO 溶液,有白色沉淀产生,过滤
3 2 3
⑤在滤液中加入AgNO 和HNO 的混合溶液,有白色沉淀产生
3 3
则关于原溶液的判断中不正确的是
A.肯定存在的离子是Na+、K+、SO 、Br-
B.肯定不存在的离子是Fe3+、Cu2+、SO 、CO
C.无法确定原溶液中是否存在Cl-
D.若步骤④改用BaCl 溶液和盐酸的混合溶液,对溶液中离子的判断也无影响
2
【答案】A
【分析】因为溶液无色,所以溶液中一定不存在:Fe3+、Cu2+,
①pH试纸检验,溶液的pH>7,证明溶液显示碱性,根据电荷守恒可知,溶液中一定
含有钠离子或是钾离子中的至少一种;
②取少量原溶液,向溶液中加入过量的BaCl 和盐酸的混合溶液,无白色沉淀生成,则
2
7
学科网(北京)股份有限公司一定不存在SO ;
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,则一定不含CO ,可能含
有SO ,亚硫酸根能被氯水氧化为硫酸根离子,再加入CCl 振荡,静置后CCl 层呈
4 4
橙色,则为溴水的颜色,一定含有Br-;
④向分液后的水溶液中加入Ba(NO ) 溶液和HNO 溶液,有白色沉淀产生,可以证明
3 2 3
硫酸根离子的存在,即亚硫酸根被氧化生成的硫酸根离子,溶液中一定存在SO ;
⑤在滤液中加入AgNO 和HNO 的混合溶液有白色沉淀产生,即为氯化银沉淀,但是
3 3
在③中加入的氯水中含有氯离子,不能确定是否存在待测离子中的氯离子。
【详解】A.由分析可知,液中一定含有钠离子或是钾离子中的至少一种,一定存在
SO 、Br-,故A错误;
B.由分析可知,溶液中肯定不存在的离子是Fe3+、Cu2+、SO 、CO ,故B正确;
C.由分析可知,无法确定原溶液中是否存在Cl-,故C正确;
D.若步骤④用BaCl 溶液和盐酸的混合溶液,则硫酸根离子会和BaCl 溶液反应生成
2 2
难溶物质硫酸钡,但是硫酸根一定是步骤③中亚硫酸根离子被氧化来的,此时对溶液
中离子的判断无影响,故D正确;
故选A。
8.(2023春·上海·高三上海市南洋模范中学校联考阶段练习)某无色溶液中可能含以
下离子中的几种:Na+、Ag+、 、Al3+、 、 、 、 。为确定该溶
液中的离子,现取该溶液进行有关实验,现象如下:
下列说法正确的是
A.气体甲中一定有
B.淡黄色沉淀甲是AgBr
试卷第8页,共30页C.原溶液可能存在的离子有 、
D.溶液甲→气体乙的反应仅有
【答案】A
【分析】无色溶液中加入过量HBr,有淡黄色沉淀生成,若此淡黄色沉淀为AgBr,则
溶液中含有Ag+,不存在 、 、 、 ,溶液中不含有阴离子,此种情
况不可能,所以溶液中不含有Ag+,一定含有 ;溶液甲中加入过量NH HCO ,产
4 3
生白色沉淀和气体乙,则溶液甲中含有 ,原溶液中不含有Ag+、 、Al3+,一定
含有Na+;溶液乙中加入过量的Ba(OH) ,产生的白色沉淀中通入过量CO 后全部溶解,
2 2
则白色沉淀为BaCO ,原溶液中一定不含有 。综合以上分析,原溶液中一定含有
3
Na+、 、 ,一定不含有Ag+、 、Al3+、 ,不能确定 是否存在。
【详解】A.由分析可知,原溶液中一定含有 ,加入过量HBr,生成S沉淀和
SO 气体,所以气体甲中一定有SO ,A正确;
2 2
B.由分析可知,淡黄色沉淀甲是S,不可能是AgBr,B不正确;
C.原溶液中一定存在 ,可能存在 ,C不正确;
D.溶液甲→气体乙,除去发生反应 ,还发生过量
HBr与NH HCO 的反应,D不正确;
4 3
故选A。
9.(2022秋·浙江·高一期中)某100mL溶液可能含有H+、K+、 、Ba2+、 、
、Cl-中的若干种,取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部
逸出)。已知: +OH- NH + H O。下列说法中不正确的是
3 2
9
学科网(北京)股份有限公司A.原溶液一定存在Cl-,c(Cl-)>0.1 mol/L
B.原溶液一定不存在H+、Ba2+
C.可以通过焰色试验确定原溶液中是否存在K+
D.沉淀1转化为沉淀2时,放出的气体可使石灰水变浑浊
【答案】A
【分析】原溶液中加入BaCl 溶液生成沉淀,原溶液中一定含有CO 和SO 中的至少
2
一种,则沉淀1为BaSO、BaCO 中的至少一种,由沉淀1部分溶解于盐酸可知其一定
4 3
是BaSO、BaCO 的混合物,原溶液中一定存在CO 和SO ,沉淀2是BaSO,物质
4 3 4
的量为 =0.01mol ,则BaCO 的物质的量为 =0.01mol,CO 、
3
SO 与Ba2+均不能共存,原溶液中一定不存在Ba2+,碳酸根离子会和氢离子反应,则
一定不含H+;滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有
NH ,由氮元素守恒可知NH 的物质的量为 =0.05mol,阳离子所带正电荷
的物质的量为0.05mol,CO 和SO 所带负电荷的物质的量之和为
0.02+0.02=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,K+不能确定,故
n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1,根据以上分析进行解答。
【详解】A.由分析可知,原溶液中一定存在Cl-,c(Cl-)≥0.1 mol·L-1,故A错误;
B.由分析可知,原溶液中一定存在CO 和SO ,一定不存在H+、Ba2+,可能存在
K+,故B正确;
C.钾离子焰色实验为紫色,可以通过焰色试验确定原溶液中是否存在K+,故C正确;
D.由分析可知,沉淀1转化为沉淀2时,BaCO 与盐酸反应生成二氧化碳气体,可使
3
石灰水变浑浊,故D正确;
试卷第10页,共30页故选A。
10.(2023春·山东·高一校联考阶段练习)某溶液中可能含有如下离子: 、 、
、 、 、 (不考虑水的电离)。当向该溶液中逐滴加入NaOH溶液
时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正
确的是
A.原溶液中一定含有的阳离子是 、 、 、
B.原溶液中含有的阴离子是 、
C.原溶液中
D.反应最后形成的溶液中的溶质只含NaCl和
【答案】C
【分析】根据图像,所加入的NaOH的量为0-2mL时候没有沉淀生成说明溶液中含有
氢离子,接下来生成沉淀,并且沉淀最终完全溶解,说明生成的沉淀为氢氧化铝,则
溶液中一定有铝离子,一定没有镁离子和偏铝酸根,NaOH的体积为5-8mL的时候加
入碱没有沉淀生成,则溶液中含有铵根,根据电荷守恒,溶液中需要有阴离子氯离子,
综合可知溶液中肯定含有 、 、 和 ,肯定不存在 和 ,以此分析;
【详解】A.根据分析,溶液中肯定含有的阳离子为, 、 、 ,A错误;
B.根据分析,溶液中肯定含有的阴离子为 ,B错误;
C.结合图像中的数量关系可得 ,C正确;
D.反应到最后溶液中的溶质为 、 和 ,D错误;
故答案为:C。
11
学科网(北京)股份有限公司11.(2023秋·黑龙江大庆·高一大庆实验中学校考期末)某100mL溶液可能含有H+、
K+、NH 、Ba2+、CO 、SO 、Cl-中的若干种。取该溶液进行连续实验,过程如图
(所加试剂均过量,气体全部逸出)。下列说法中不正确的是
A.不能确定原溶液是否存在Cl- B.原溶液一定不存在H+、Ba2+
C.原溶液c(SO )=0.1mol/L D.原浴液可能存在K+
【答案】A
【分析】原溶液中加入BaCl 溶液生成沉淀,原溶液中一定含有CO 和SO 中的至少
2
一种,则沉淀1为BaSO、BaCO 中的至少一种,由沉淀1部分溶解于盐酸可知其一定
4 3
是BaSO、BaCO 的混合物,原溶液中一定存在CO 和SO ,沉淀2是BaSO,物质
4 3 4
的量为 =0.01mol ,则BaCO 的物质的量为 =0.01mol,CO 、
3
SO 与Ba2+均不能共存,原溶液中一定不存在Ba2+,碳酸根离子会和氢离子反应,则
一定不含H+;滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有
NH ,由氮元素守恒可知NH 的物质的量为 =0.05mol,阳离子所带正电荷
的物质的量为0.05mol,CO 和SO 所带负电荷的物质的量之和为
0.02+0.02=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,K+不能确定,故
n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1,根据以上分析进行解答。
【详解】A.由分析可知,原溶液中一定存在有Cl-,故A错误;
B.由分析可知,原溶液中一定存在CO 和SO ,一定不存在H+、Ba2+,故B正确;
试卷第12页,共30页C.由分析可知,沉淀2是BaSO,物质的量为 =0.01mol ,原溶液c(SO
4
)= =0.1mol/L,故C正确;
D.由分析可知,K+不能确定,原浴液可能存在K+,故D正确;
故选A。
12.(2023春·江西上饶·高一校联考阶段练习)现有一混合物的水溶液,可能含有以
下离子中的几种: 、 、 、 、 、 、 。现取三份各
溶液进行如下实验:第一份加入 溶液有沉淀产生;第二份加足量 溶液加
热后,收集到 气体;第三份加足量 溶液后,得到干燥沉淀 ,经足
量盐酸充分浸泡后,过滤、洗涤、干燥后,沉淀质量为 。下列说法正确的是
A.该混合液中一定含有 、 ,可能含 、 、
B.该混合液中一定含有 、 、 ,可能含 、
C.该混合液中一定含有 、 、 、 ,可能含 ,且n(K+)≥0.04mol
D.该混合液中一定含有 、 、 、 ,可能含 、
【答案】C
【分析】第一份加入硝酸银溶液有沉淀产生,Cl-、CO 、SO 与Ag+均能生成沉淀,
无法判断;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体,该气体为NH ,说明原溶液
3
中含有NH ,根据原子守恒,n(NH )=0.08mol;
第三份加入足量氯化钡溶液后,得到干燥沉淀12.54g,经足量盐酸充分浸泡后,过滤、
洗涤、干燥后,沉淀质量为4.66g,该沉淀为BaSO,n(SO )= =0.02mol,加
4
入盐酸后沉淀质量减少,说明12.54g沉淀中除硫酸钡沉淀外,还含有BaCO ,
3
13
学科网(北京)股份有限公司n(BaCO)= =0.04mol,原溶液中含有CO ,因为Ba2+与CO 、SO 反
3
应生成沉淀,Mg2+与CO 反应生成沉淀,因此原溶液中不含有Ba2+、Mg2+;
综上所述,原溶液中含有n(NH )=0.08mol,n(SO )= =0.02mol,n(CO
)=0.04mol,根据溶液呈电中性,因此还含有K+,Cl-可能存在,据此分析;
【详解】根据上述分析,原溶液中一定含有NH 、SO 、CO 、K+,可能含有Cl-,
根据溶液呈电中性,K+物质的量至少0.04mol,若含有Cl-,则n(K+)≥0.04mol,选项C
正确;
答案为C。
13.(2023·全国·高三专题练习) 的溶液X中可能存在 、 、 、
、 、 、 、 、 中的若干种,现取适量该溶液进行如图所示实
验,下列说法正确的是
A.溶液X中一定不存在 、 、
B.溶液X中一定存在 、 、 、 、 、
C.步骤③中一定发生反应
D.沉淀A是 ,沉淀B是 ,沉淀C是
【答案】A
【分析】 说明溶液X是强酸性溶液,则 不能大量存在;由于酸性条件下
和 会发生反应,则二者不能同时存在。向溶液X中加入足量 溶液,
试卷第14页,共30页生成气体,证明溶液X中一定存在 ,一定不存在 ,则气体A为 ;沉淀A
为 ,则溶液X中一定不存在 ,一定存在 。溶液A中加入足量 溶
液生成的气体B应为 ,则溶液X中存在 ;沉淀B为 ,但不能确定溶
液X中是否存在 ;由于溶液B中存在 、 ,加入少量二氧化碳会发生反应
生成 ,则沉淀C中一定存在 ,可能存在 ,则溶液X中可能存在
,据此分析解答。
【详解】A.根据分析,溶液X中一定不存在 、 、 ,A正确;
B.根据分析,溶液X中一定存在 、 、 、 ,可能存在 、 ,B
错误;
C.步骤③中一定发生反应 ,可能发生反应
,C错误;
D.根据分析,沉淀A是 ,沉淀B是 ,沉淀C中一定存在 ,可
能存在 ,D错误;
故选A。
14.(2023春·辽宁·高一凤城市第一中学校联考期中)某固体样品可能含有NaNO 、
3
NaHCO 、NaSO 和NaSO 。取少量样品进行如下实验:步骤①:将样品溶于水,得
3 2 3 2 4
到澄清溶液;步骤②:向①的溶液中滴加过量稀盐酸,有气泡产生;步骤③:取②的
上层清液,向其中滴加BaCl 溶液,有沉淀生成。下列说法中正确的是
2
A.该固体样品中一定含有NaSO
2 4
B.该固体样品中一定含有NaHCO
3
C.该固体样品不可能只含有NaSO
2 3
D.步骤②的试管口产生的气体一定是无色的
【答案】C
15
学科网(北京)股份有限公司【分析】步骤①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能
大量共存;
步骤②向①的溶液中滴加过量稀盐酸,有气泡产生,说明可能含有NaHCO 或NaSO
3 2 3
或两者都有;若气泡是NO,说明是NaNO 和NaSO 均有;
3 2 3
步骤③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为BaSO,说明
2 4
固体中存在NaSO 和NaSO 至少一种。
2 3 2 4
【详解】A.结合分析可知不一定含有NaSO ,白色沉淀可能是NaNO 和NaSO 在加
2 4 3 2 3
盐酸后发生氧化还原反应生成硫酸根离子,硫酸根离子和钡离子生成白色的硫酸钡沉
淀,A错误;
B.若气泡是NO,说明是NaNO 和NaSO 均有,不一定有NaHCO ,B错误;
3 2 3 3
C.该固体样品若只含有NaSO ,则步骤③不会产生沉淀,故该固体样品不可能只含
2 3
有NaSO ,C正确;
2 3
D.由分析可知步骤②产生的气体可能是NaNO 和NaSO 在加盐酸后发生氧化还原反
3 2 3
应生成的NO,NO易与试管内氧气反应生成红棕色二氧化氮,试管口产生的气体可能
是红棕色的,D错误;
答案选C。
15.(2022秋·湖南长沙·高三长沙一中校考阶段练习)某学习兴趣小组拟对溶液A的
成分进行分析,溶液A中可能含有如下离子: 、 、 、 、 、
、 、 ,设计并完成了如下的试验,下列说法不正确的是
A.气体E的体积是224mL(标准状况)
B.气体F能使湿润的红色石蕊试纸变蓝
C.溶液A中一定存在 、 、 、
D.溶液A中
【答案】D
试卷第16页,共30页【分析】溶液A加入过量 溶液生成沉淀B的质量为4.50g,且沉淀部分溶解于稀
盐酸,说明原来有 ,则原溶液中没有 ,沉淀没有完全溶解,说明原溶液中有
,且 的质量为2.33g,则说明原溶液中 的物质的量为0.01mol,
的质量为 ,则 的物质的量为0.01mol,溶液加入NaOH溶液加
热生成448mL气体和溶液G, ,说明含有0.02mol
,也说明无 ,阴离子的电荷总数为
,阳离子的电荷总数为 , ,根据电荷守
恒溶液中肯定存在其他阳离子,故存在 ,可能有 , 。
【详解】A. 的物质的量为0.01mol,气体SO 的体积是224mL(标准状况),故A
2
正确;
B. 气体F为氨气溶于水呈碱性,能使湿润的红色石蕊试纸变蓝,故B正确;
C. 溶液A中一定存在 、 、 、 ,可能有 ,故C正确;
D.由分析可知,溶液A中存在 ,可能有 , ,故D错误;
故选D。
16.(2023秋·上海杨浦·高一复旦附中校考期末)向500ml 2mol·L-1的NaOH溶液中通
入一定体积的CO 充分反应,再向所得溶液中逐滴滴加1mol·L-1的稀盐酸。测得产生
2
CO 的物质的量随加入盐酸的体积变化如图所示。则下列说法正确的是
2
17
学科网(北京)股份有限公司A.整个过程中Na+没有参与化学反应,故c(Na+)保持不变
B.图中的a=0.4,b=1.2
C.稀盐酸滴加在0→0.2L过程中,发生的离子反应是:CO +H+=HCO
D.在A、B、C、D四处的溶液中,能与大量K+、Ba2+、NO 、OH-共存的只有1处
【答案】D
【分析】向NaOH溶液中通入一定量CO 气体,先发生反应:
2
2NaOH+CO =Na CO+H O,当该反应完成后,向所得溶液中滴入稀盐酸,发生反应:
2 2 3 2
NaCO+HCl=NaCl+NaHCO ,然后生成的碳酸氢钠继续和盐酸发生反应:
2 3 3
NaHCO +HCl=NaCl+H O+CO↑。两步反应消耗HCl的物质的量及体积相同。在500
3 2 2
mL2 mol/LNaOH溶液中含有溶质的物质的量n(NaOH)=2 mol/L×0.5 L=1.0 mol,从B点
到C点发生反应:NaHCO +HCl=NaCl+H O+CO↑,在C点CO 气体达到最大量,此时
3 2 2 2
反应完全,溶液为NaCl溶液,根据元素守恒可知n(HCl)=n(NaCl)= n(NaOH)=1.0
mol,由于稀盐酸浓度是1 mol/L,故此时盐酸的体积是1 L,b=1.0;发生该反应消耗
HCl溶液体积是V=1.0 L-0.6 L=0.4 L<0.6 L,说明NaOH溶液与CO 气体反应时NaOH
2
未完全反应,所得溶液为NaOH与NaCO 混合溶液。在OA段发生反应:
2 3
NaOH+HCl=NaCl+H O,AB段发生反应:NaCO+HCl=NaCl+NaHCO ,BC段发生反
2 2 3 3
应:NaHCO +HCl=NaCl+H O+CO↑,C点溶液恰好为NaCl溶液,后加入稀盐酸,不
3 2 2
发生反应,溶液为NaCl、HCl混合溶液。
【详解】A.在所有过程中,Na+没有参与化学反应,故n(Na+)一直保持不变,但由于
滴入盐酸,溶液的体积逐渐增大,故根据c(Na+)逐渐减小,A错误;
B.根据上述分析可知:b=1.0。B→C过程中发生的反应为
NaHCO +HCl=NaCl+H O+CO↑,根据物质反应转化关系可知n(CO)=n(HCl)=0.4 L×1
3 2 2 2
mol/L=0.4 mol,所以a=0.4,B错误;
C.根据上述分析可知,二氧化碳和NaOH溶液反应后的溶液中含有NaOH和碳酸钠,
稀盐酸滴加在0→0.2L过程中,发生的离子反应:OH-+H+=H O,C错误;
2
D.向NaOH溶液中通入一定量CO 气体后,所得溶液为NaOH、NaCO 混合溶液,
2 2 3
在OA段发生反应:NaOH+HCl=NaCl+H O,A点为NaCO、NaCl混合溶液, 与
2 2 3
Ba2+会反应产生BaCO 沉淀而不能大量共存;在AB段发生反应:
3
NaCO+HCl=NaCl+NaHCO ,B点溶液为NaCl、NaHCO 混合溶液,OH-与 会
2 3 3 3
试卷第18页,共30页发生反应而不能大量共存;在BC段发生反应:NaHCO +HCl=NaCl+H O+CO↑,C点
3 2 2
溶液为NaCl溶液,Na+、Cl-与K+、Ba2+、 、OH-不能发生任何反应而能够大量共
存;C点后的D点为NaCl、HCl混合溶液,H+与OH-反应产生HO而不能大量共存。
2
故在A、B、C、D四处的溶液中,只有C点离子可以大量共存,D正确;
故答案为:D。
17.(2023·全国·高三专题练习)常温下, 的溶液A中含有 、 、 、
、 、 、 、 、 、 、 中的四种,且溶液中各离子的浓度
均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确
的是
A.溶液A中一定含有 、 、 、
B.若实验消耗 14.4g,则生成气体丁的体积为3.36L
C.沉淀乙中一定有 ,可能有
D.溶液A中一定没有 ,但是无法确定是否含有
【答案】A
【分析】肯定性原则:由 可知溶液A呈酸性,存在大量 ;向溶液A中加过量
溶液,产生的白色沉淀甲为氢氧化铝或 形成的物质或二者的混合物,
可以排除 ,则溶液A中一定含有 和 中的一种或两种;向溶液乙中加 和
稀硫酸能产生气体丙,且气体丙在空气中能生成红棕色的气体丁,则丙为 ,说明
19
学科网(北京)股份有限公司溶液A中有 。
互斥性原则:溶液A中存在大量 ,则不存在 ;强酸性溶液中含有 时一定
不存在具有还原性的 和 。
电中性原则:根据以上分析可知,溶液A中存在0.1 、0.1 、0.1
,根据溶液呈电中性可知,溶液A中还应该含有 和 。
【详解】A.溶液A中一定有 、 、 、 ,A正确;
B.由得失电子守恒可得关系式 ,由原子守恒可得关系式 ,若实
验消耗14.4g(0.225 ) ,则生成0.15 ,气体若处于标准状况下,其体积
为 ,但未说明气体所处状况,无法确定其体积,B错误;
C.溶液A中含有 ,向溶液A中加过量 、 ,所得沉淀乙中一
定含有 、 ,C错误;
D.一定不存在 ,D错误;
答案选A。
18.(2023·全国·高三专题练习)常温下,20 X溶液中可能含有 、 、
、 、 、 中的若干种。现对X溶液进行如图所示实验:
试卷第20页,共30页下列说法正确的是
A.X溶液的
B.X溶液中一定含有 、 、 ,不能确定是否含有
C.X溶液中一定含有 ,且
D.向滤液中通入足量 ,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,可得
到固体0.51g
【答案】D
【分析】10mL X溶液中加入NaOH的物质的量为0.025L×4mol/L=0.1mol,并得到
224mL(0.01mol) ,则溶液中含有0.01mol ;生成1.16g白色沉淀,反应后
的滤液稀释至100mL, 为13,则 ,说明反应后剩余的
,该1.16g白色沉淀为0.02mol ,溶液中含有0.02mol
Mg2+,Mg2+消耗0.04mol OH-,由于加入的 的物质的量为0.1 ,则还有
0.04mol OH-与Al3+反应生成 ,则Al3+的物质的量为0.01mol;10mL X溶液中加入
足量 酸化的 溶液得到2.33g(0.01mol) ,则 的物质的量为
0.01mol,根据阴、阳离子所带电荷数相等,则还含有0.06 mol Cl-,
。
【详解】A.X溶液中含有 、Mg2+、 ,这些离子均会发生水解,溶液显酸性,
A错误;
B.由分析可知,X溶液中一定含有 ,且 ,B错误;
C.由分析可知,X溶液中一定含有 ,且 ,C错误;
D.滤液中含有 ,向滤液中通入足量 ,可得到 白色沉淀,将沉淀
21
学科网(北京)股份有限公司过滤、洗涤、灼烧至恒重,得到 ,根据原子守恒可得 的物质的量为0.005
,即0.51g,D正确;
故选D。
19.(2023·江西抚州·江西省乐安县第二中学校考一模)在某强酸性溶液X中仅含有
、 、 、 、 、 、 、 、 、 中的一种或几种
(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图,下列有关推断
正确的是
A.生成气体A的离子反应:
B.溶液X中一定含有 、 、 、
C.加热灼烧沉淀F,其产物一定是磁性氧化铁
D.沉淀H中一定含有 和 沉淀
【答案】A
【分析】在强酸性溶液中一定不会存在 、 离子;加入过量硝酸钡生成沉淀,
则该沉淀C为BaSO,说明溶液中含有SO ,不含Ba2+,生成气体A,则A只能是
4
NO,说明溶液中含有还原性离子,则一定为Fe2+,且溶液中不含 ;溶液B中加入
过量NaOH溶液,沉淀F为Fe(OH) ,无气体产生,说明溶液中没有NH 离子;溶液
3
E中通入CO 气体,生成沉淀H,则H为Al(OH) ,E为NaOH和NaAlO ,说明原溶液
2 3 2
中含有Al3+离子;不能确定是否含有的离子Fe3+和Cl-,以此进行解答。
【详解】A.由分析可知,气体A为NO,生成NO的离子反应为:
试卷第22页,共30页,故A正确;
B.由分析可知,溶液中一定存在:H+、Al3+、Fe2+、 ,不能确定Cl-是否存在,故
B错误;
C.由分析可知,F为Fe(OH) ,Fe(OH) 在加热条件下分解产生Fe O,故C错误;
3 3 2 3
D.由分析可知,溶液E中含有过量的Ba2+和OH-,若通入的CO 过量则没有BaCO 沉
2 3
淀,故D错误;
故选A。
20.(2023秋·重庆·高一校联考期末)某红色粉末样品可能含有 和 中的一种
或两种,为探究其组成,研究组同学取少量样品加入过量稀硫酸进行实验。(已知:
)下列有关说法正确的是
A.若固体部分溶解,则样品中一定含有 ,一定不含有
B.若固体全部溶解,则发生的离子反应只有:
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红,则样品中
为2∶1
D.另取ag样品在空气中充分加热至质量不再变化,称其质量为bg(b>a),则混合物中
的质量分数为
【答案】D
【详解】A.固体若是 和 的混合物,放入足量稀硫酸中会有Cu生成,Cu能
将Fe3+还原为Fe2+剩余铜,A错误;
B.固体全部溶解,若固体是 和 的混合物,放入足量稀硫酸中会有Cu生成,
Cu恰好能将Fe3+还原为Fe2+, 、 、
,B错误;
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,因为 溶于硫酸生成Cu
23
学科网(北京)股份有限公司和CuSO ,而硫酸不能溶解Cu,所以混合物中必须有 存在,使其生成的Fe3+溶解
4
产生的Cu,反应的有关离子方程式为 、
、 ,说明样品中
为1∶1,C错误;
D. , ,故混合物中Cu O的质量分数为:
2
,D正确;
故选D。
21.(2023·全国·高三专题练习)溶液X可能含有如下离子中的若干种: 、 、
、 、 、 、 ,为确定其成分,某同学设计并进行了如下实验(假
设气体全部逸出):
下列说法错误的是
A.溶液X中一定不存在 、 和
B.沉淀1的成分是等物质的量的 和
C.溶液X中一定存在 ,且
D.实验③发生反应的离子方程式为
【答案】A
试卷第24页,共30页【分析】溶液X加氯化钡溶液有沉淀1,说明有 或 ,沉淀1加盐酸有气体和
沉淀2,沉淀2为BaSO,沉淀1为BaSO 和BaSO,说明一定有 、 两种离子,
4 4 3
n( )=0.01mol,n( )=0.01mol,一定没有Ba2+;溶液1加氢氧化钠有气体,说明
气体为NH ,说明一定有 ,n( )=0.02mol,一定没有Mg2+;溶液呈电中性,则
3
一定有Na+,Cl-无法确定。
【详解】A. 溶液X无法确定 Cl−,A错误;
B.沉淀2BaSO 为2.33g,物质的量为0.01mol,则沉淀1中BaSO 的质量为2.17g,物
4 3
质的量为0.01mol,B正确;
C.溶液X中n( )=0.01mol,n( )=0.01mol,n( )=0.02mol,溶液呈电中性,
则一定存在Na+,当没有Cl-时,c(Na+)=0.2molL−1,当有Cl-时c(Na+)>0.2molL−1,C
正确; ⋅ ⋅
D.实验③发生反应的离子方程式为 +OH− NH ↑+H O,D正确;
3 2
故答案为:A。
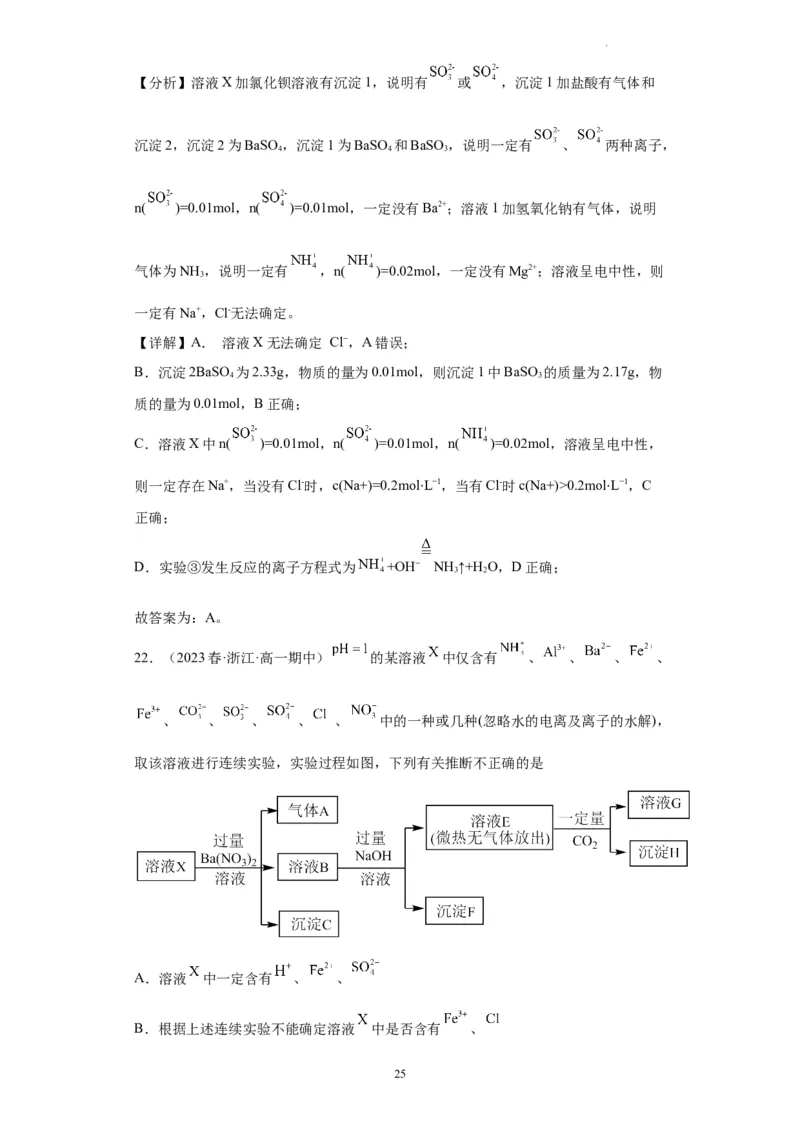
22.(2023春·浙江·高一期中) 的某溶液 中仅含有 、 、 、 、
、 、 、 、 、 中的一种或几种(忽略水的电离及离子的水解),
取该溶液进行连续实验,实验过程如图,下列有关推断不正确的是
A.溶液 中一定含有 、 、
B.根据上述连续实验不能确定溶液 中是否含有 、
25
学科网(北京)股份有限公司C.沉淀F可能为混合物
D.若沉淀 中含有 ,则溶液 中一定没有
【答案】D
【分析】溶液X的 ,说明溶液中存在大量H+,因H+与 、 能发生复分
解反应,因此溶液X中一定不存在 、 ;向溶液X中加入过量Ba(NO ) 溶液后,
3 2
溶液中存在反应,因此溶液X中一定不存在 、 ,酸性溶液中 具有氧化
性,能氧化 , 被还原为NO,因此气体A为NO, 与 能发生复分解
反应生成BaSO 沉淀,因此溶液X中一定存在 、 ;向溶液B中加入过量
4
NaOH溶液生成Fe(OH) 沉淀,溶液E微热无气体放出,说明溶液X中一定不存在
3
,溶液E中含有大量Ba(NO )、NaOH,可能含有NaAlO ,向溶液E中通入一定
3 2 2
量CO,可能产生BaCO 沉淀(CO 少量),也可能产生Al(OH) ,因此溶液X中可能含
2 3 2 3
有 ,实验过程中未涉及 、 检验实验,因此溶液X中可能含有 、 ,
综上所述,溶液X中一定含有H+、 、 ;一定不含 、 、 、 、
;可能含有 、 、 。
【详解】A.由上述分析可知,溶液X中一定含有H+、 、 ,故A项正确;
B.由上述分析可知,溶液X中可能含有 、 、 ,故B项正确;
C.第一步操作中,若溶液X中 未完全氧化,且溶液X中含有 时,沉淀F为
Fe(OH) 和Fe(OH) 的混合物,故C项正确;
2 3
D.通入CO 时,溶液中一定存在OH-与CO 的反应,当CO 不足时能生成 ,生
2 2 2
试卷第26页,共30页成的 能与Ba2+反应,当Ba2+不足时,溶液G中存在 ,故D项错误;
综上所述,不正确的是D项。
23.(2023·全国·高三专题练习)某固体混合物可能含有Al、 、 、
、 、NaCl中的一种或几种,现对该混合物做如图实验,所得现象和有关数
据如图(气体体积已换算成标准状况下体积)。下列说法不正确的是
A.步骤①中发生了氧化还原反应
B.步骤②和步骤③中反应消耗的 的物质的量之比为3∶1
C.混合物中一定不存在 ,可能含有NaCl、AlCl
3
D.混合物中一定含有 ,且物质的量为0.2mol
【答案】B
【分析】由题干可知,加过量氢氧化钠溶液产生的白色沉淀久置无明显变化,则固体
不含FeCl ,11.60g是氢氧化镁沉淀, ,
2
;Al与氢氧化钠溶液产生的氢气为
,根据电子得失守恒 ,
; 浓硫酸吸收氨气,
, ,
27
学科网(北京)股份有限公司则固体含Al、(NH )SO 、MgCl 的质量为 ,则余下
4 2 4 2
是AlCl 和NaCl中的一种或两种。
3
【详解】A.根据分析,固体含Al,步骤①中Al与氢氧化钠溶液产生氢气为氧化还原
反应,A正确;
B.步骤②为H++OH-=H O和 ,步骤③为
2
,二者反应消耗的H+的物质的量之比因过量氢氧根离子未知
而不能计算,B错误;
C.根据分析,混合物中一定不存在FeCl ,可能含有NaCl、AlCl 中的一种或两种,C
2 3
正确;
D.根据分析,混合物中一定含有MgCl 0.2mol,D正确;
2
故选B。
24.(2023·全国·模拟预测)盐X由三种常见元素组成,某科学兴小组称取 盐X
进行实验,数据和现象如下:
已知:①气体B为两种气体的混合物,能被水完全吸收。
②取D溶液 ,用 的 溶液滴定,消耗 溶液 。
下列说法错误的是
A.试剂Y可能为 溶液
B.盐X的化学式为
C.用 的 溶液滴定溶液D时可用酚酞作指示剂
D.若在X的稀溶液中通入足量 气体,发生反应的离子方程式为:
试卷第28页,共30页【答案】D
【分析】A溶于盐酸后得到黄色溶液C,C加入Y得到血红色溶液E,则Y为
溶液,C中含有铁离子,A为1.6g氧化铁(为0.01mol);红棕色气体B和得到强酸
D,则B为二氧化氮和氧气混合气,二氧化氮和氧气、水生成硝酸,HNO 为
3
× ÷ ×1L=0.06mol;则X中含有铁、氮元素分别
为0.2mol(1.12g)、0.6mol(0.84g),则含有氧4.84g-1.12g-0.84g=2.88g,为
0.18mol;三者物质的量之比为1:3:9,X为 ;
【详解】A.由分析可知,Y可能为 溶液, A正确;
B.盐X的化学式为 ,B正确;
C.D为硝酸溶液,用 的 溶液滴定溶液D时可用酚酞作指示剂,
当最后一滴氢氧化钠溶液加入后,溶液变红色且半分钟不褪色说明达到滴定终点,C
正确;
D.若在X的稀溶液中通入足量 气体,硝酸根离子具有强氧化性,也会把二氧化硫
氧化为硫酸根离子同时生成一氧化氮气体,
,D错误;
故选D。
25.(2022秋·安徽·高一校联考期末)某溶液中可能含有如下离子: 、 、 、
、 、 (不考虑水的电离)。当向该溶液中逐滴加入 溶液时,产生沉淀
的物质的量(n)与加入 溶液的体积(V)的关系如图所示,下列说法正确的是
29
学科网(北京)股份有限公司A.原溶液中一定含有的阳离子是 、 、 、
B.反应最后形成的溶液中的溶质只含 和
C.原溶液中 与 的物质的量之比为1:1
D.原溶液中含有的阴离子是
【答案】D
【分析】根据图像可推断出溶液中肯定含有 、 、 和 ,肯定不存在
和 ,以此分析;
【详解】A.根据分析,溶液中肯定含有的阳离子为, 、 、 ,A错误;
B.反应到最后溶液中的溶质为 、 和 ,B错误;
C.结合图像中的数量关系可得 ,C错误;
D.根据分析,溶液中肯定含有的阴离子为 ,D正确;
故答案为:D。
26.(2023春·湖南长沙·高一长沙一中校考开学考试)某水溶液中可能含有以下离子
中的若干种: 、 、 、 、 、 、 、 、 、 ,
现分别取100mL的两份溶液进行如下实验。
①第一份加过量NaOH溶液后加热,收集气体448mL(标准状况)气体,无沉淀生成,
同时得到溶液甲。
②向甲溶液中通入过量 ,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g
固体。
③第二份加足量 溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥
后,得到11.65g固体,向滤液中加入 溶液又有白色沉淀产生。
下列有关叙述正确的是
试卷第30页,共30页A.由①可知源溶液存在离子为 ,其浓度为
B.原溶液一定存在
C.原溶液肯定没有 、 ,一定含有 且
D.
【答案】C
【分析】①第一份加过量NaOH溶液后加热,收集到0.02mol气体,该气体为氨气,
溶液中一定含有 ,物质的量为0.02mol,其浓度为:c( )= ;
无沉淀生成,则一定不含有Fe3+、Mg2+;
②向甲溶液中通入过量CO,生成白色沉淀,该白色沉淀即为Al(OH) ,则原溶液中一
2 3
定有Al3+,由于Al3+与 不能大量共存,所以一定不含有 ,Al3+和过量的NaOH
反应生成NaAlO 溶液,向溶液中通入过量CO,生成白色沉淀,即为氢氧化铝,氢氧
2 2
化铝沉淀经过滤、洗涤、灼烧后,得到1.02g固体即为氧化铝,根据铝元素守恒,得到
铝离子的物质的量是n(Al3+)=2× =0.02mol;c(Al3+)= ;
③第二份溶液中加足量BaCl 溶液后,生成白色沉淀,则一定含有 离子,无
2
Ba2+。沉淀经足量盐酸洗涤、干燥后,得到11.65g固体即BaSO 的质量是11.65g,物
4
质的量为:n(BaSO)=11.65g÷233g/mol=0.05mol,根据S元素守恒,可知 的物质的
4
量是0.05mol,c( )=0.05mol÷0.1L=0.5mol/L;综上可知,一定含有的离子是: 、
Al3+、 ,其浓度分别是:0.2mol/L、0.2mol/L、0.5mol/L,根据电荷守恒可知一定
还含有钠离子,一定不含Fe3+、Mg2+、Ba2+,不能确定是否存在氯离子
【详解】A.由①可知原溶液存在离子为 ,其浓度为 ,A错误;
B.由分析可知不能确定原溶液是否存在 ,B错误;
31
学科网(北京)股份有限公司C.原溶液肯定没有 、 ,任何溶液中都存在电荷守恒, 、Al3+、 ,
其浓度分别是:0.2mol/L、0.2mol/L、0.5mol/L,可知 、Al3+的正电荷总量小于
负电荷总量,依据溶液中阳离子带的正电荷总数等于阴离子带的负电荷总数,则
一定有Na+存在,若无氯离子存在,则0.2 mol/L×1+0.2 mol/L×3+c(Na+)×1=0.5
mol/L×2,解得c(Na+)=0.2mol/L,若含有氯离子,则c(Na+)>0.2mol/L,一定含有
且 ,C正确;
D.由分析可知一定含有的离子是: 、Al3+、 ,其浓度分别是:0.2mol/L、
0.2mol/L、0.5mol/L , ,D错误;
故选C。
27.(2022秋·山东日照·高一校考阶段练习)某工厂用 FeCl 溶液腐蚀镀有铜的绝缘
3
板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:①取
10mL废液加入足量的AgNO 溶液,生成沉淀17.22g;②另取10mL废液放入铜片充分
3
反应,溶液质量增加了0.64g。下列关于原废液组成的判断错误的是
A.一定含有Fe2+、Cu2+、Cl-,不含 Fe3+
B.c(Fe2+):c(Cu2+)=2:1
C.c(Fe2+):c(Fe3+)=1:1
D.c(Fe2+)=2mol/L c(Cl-)=12mol/L
【答案】A
【分析】 向反应后的废液中,加入足量的AgNO 溶液,
3
生成沉淀17.22g,发生反应 ,
,另一份溶液因为发生反应
,溶液质量增加了0.64g,说明固体质量减少0.64g,
试卷第32页,共30页,可知FeCl 的物质的量为0.02mol;
3
【详解】A.因为废液中加入铜导致溶液质量增加,说明溶液中含有Fe3+、Fe2+、Cl-、
Cu2+,A错误;
B.根据 , , ,
B正确;
C.根据分析原废液中n(Fe3+)=0.02mol,n(Cl-)=0.12mol,根据电荷守恒
,原废液中
n(Fe2+)=0.02mol,n(Cu2+)=0.01mol,则 ,C正
确;
D.根据上述分析, , ,D
正确;
故答案为:A。
28.(2023春·河南·高一校联考阶段练习)某化学研究小组对某无色水样的成分进行
检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Ag+、Ca2+、CO 、SO 、Cl-
中的若干种离子。该小组同学取部分水样进行实验。①向水样中先滴加足量硝酸钡溶
液,产生白色沉淀;②再滴加足量稀盐酸,沉淀部分溶解;③最后滴加硝酸银溶液,
又产生白色沉淀。下列说法正确的是
A.经过实验可以确定一定不存在的离子有5种
B.经过实验可以确定一定存在的离子是K+、CO 、SO 、Cl-
C.步骤②中发生反应的化学方程式为CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
D.步骤③中发生反应的离子方程式为Ag++Cl-=AgCl↓
【答案】AD
【分析】某无色水样,则不含有 、 ,向水样中先滴加足量硝酸钡溶液,产生
白色沉淀,则含有 、 中的一种或两种;再滴加足量稀盐酸,沉淀部分溶解,
33
学科网(北京)股份有限公司则 、 均存在;故不存在 、 、 ,根据溶液电中性,则一定含有
一种阳离子 ,最后滴加硝酸银溶液,又产生白色沉淀,该白色沉淀为氯化银,则氯
离子可能来自于前面所加盐酸而不一定是原溶液的,故不能确定原溶液中是否含有 。
【详解】A.根据分析可知,无色水样中一定不存在的离子有 、 、 、
、 ,共5种离子,选项A正确;
B.经过实验可以确定一定存在的离子是 、 、 ,不能确定是否有 ,选
项B错误;
C.步骤②中滴加足量稀盐酸,沉淀部分溶解,发生反应的化学方程式为
BaCO +2HCl=BaCl +CO ↑+H O,选项C错误;
3 2 2 2
D.步骤③中滴加硝酸银溶液,又产生白色沉淀,该白色沉淀为氯化银,发生反应的
离子方程式为Ag++Cl-=AgCl↓,选项D正确。
故答案选AD。
29.(2023秋·河北邢台·高一邢台一中校考期末)固体化合物X由三种元素组成。某
学习小组进行了如下实验:
下列推断不正确的是
A.由现象1得出化合物X含有O元素
B.X的化学式
C.固体混合物Y的成分是Cu和NaOH
D.若X与浓盐酸反应产生黄绿色气体,则反应中浓盐酸只作还原剂
【答案】BD
【分析】固体X经H 还原后得到的混合气体能使白色CuSO 变为蓝色,则说明产物中
2 4
有水蒸气,即化合物X中含有O元素;最终所得固体单质呈紫红色,则该单质为Cu,
说明化合物X含有Cu元素,且m(Cu)=1.28g,则2.38g X中含有Cu 0.02mol;最终所
得碱性溶液的焰色反应为黄色,则说明化合物X中含有Na,该碱性溶液为NaOH,且
试卷第34页,共30页n(NaOH)=n(HCl)=0.02mol;经H 还原后,所得固体混合物Y的成分是Cu和NaOH;
2
综上所述,2.38g化合物X含1.28g Cu、0.02mol Na和O元素,则
m(O)=2.38g-1.28g-0.02mol×23g/mol=0.64g,则n(O)=0.04mol,即2.38g化合物X含
0.02mol Cu、0.02mol Na、0.04mol O,故化合物X的化学式为NaCuO 。
2
【详解】A、现象1为混合气体能使白色CuSO 变为蓝色,说明经H 还原的产物中有
4 2
水蒸气,从而得出化合物X含有O元素,A正确;
B、经分析,2.38g化合物X含0.02mol Cu、0.02mol Na、0.04mol O,故化合物X的化
学式为NaCuO ,B错误;
2
C、固体Y加水得紫红色的该单质为Cu,碱性溶液为NaOH溶液,故固体混合物Y的
成分是Cu和NaOH,C正确;
D、若NaCuO 与浓盐酸反应产生黄绿色气体Cl,同时会生成NaCl、CuCl ,则浓盐酸
2 2 2
除了做还原剂,还起到酸的作用,D错误;
故选BD。
30.(2022秋·河北衡水·高一河北衡水中学校考阶段练习)已知:
,现有一混合物的水溶液,可能含有以下离子中的若干种:
、 、 、 、 、 。现取两份各200 mL溶液进行如下实验:
①第一份加足量NaOH溶液,加热,收集到气体1.36 g;
②第二份加足量 溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀
质量4.66 g。
根据上述实验,以下推测正确的是
A.一定存在 、 、 ,一定不存在 、
B.一定存在 、 、 、 ,可能存在
C. 0.1mol·L ,
D.若溶液中存在 、 、 、 、 五种离子,则 mol·L
【答案】CD
【分析】第一份加足量NaOH溶液,加热,收集到气体1.36g,说明其中含有NH ,
35
学科网(北京)股份有限公司n(NH )= =0.08mol,故n(NH )=0.08mol,由实验②可知沉淀为BaSO、BaCO
3 4 3
的混合物,n(BaCO)= =0.04mol,n(BaSO)= =0.02mol,溶液中
3 4
含有CO 、SO 的物质的量分别为0.04mol和0.02mol,由于Ba2+与CO 、SO 不
共存,溶液中不存在Ba2+,根据溶液中的电荷守恒可得n(K+)+n(NH )=2n(CO )
+2n(SO )+n(Cl-), n(K+)+0.08mol=2×0.04mol+2×0.02mol+ n(Cl-),故一定存在K+,Cl-
可能存在于溶液中。
【详解】A.根据分析,溶液中一定存在NH 、CO 、SO 、K+,一定不存在Ba2+,
可能存在Cl-,A错误;
B.根据分析,溶液中一定存在K+,可能存在Cl-,B错误;
C.c(SO )= =0.1mol/L,c(NH )= =0.4mol/L, ,C正
确;
D.根据分析可知,n(K+)+n(NH )=2n(CO )+2n(SO )+n(Cl-),若没有Cl-,
n(K+)=0.04mol,若存在Cl-,n(K+)>0.04mol,c(K+)> =0.2mol/L,D正确;
故选:CD。
试卷第36页,共30页