文档内容
第 01 讲 化学反应速率及其影响因素
01 模拟基础练
【题型一】化学反应速率的概念及计算
【题型二】影响化学反应速率的因素
02 重难创新练
03 真题实战练
题型一 化学反应速率的概念及计算
1.(23-24高三下·辽宁·开学考试)下列关于化学反应速率的说法正确的是
A.决定化学反应速率的主要因素有温度、浓度、压强和催化剂
B.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率
C.对于放热的可逆反应,升高温度,逆反应速率加快,正反应速率减慢
D.从酯化反应体系中分离出水,反应速率减慢,但有利于提高酯的产率
【答案】D
【解析】A.决定化学反应速率的主要因素是反应物自身的性质,温度、浓度、压强和催化剂等均是外
因,A错误;B.增大反应物浓度,可以提高单位体积内活化分子百分数,从而提高反应速率,活化分子
百分数不变,B错误;C.对于可逆反应,升高温度,正逆反应速率均加快,C错误;D.从酯化反应体系
中分离出水,相当于降低生成物浓度,反应速率减慢,平衡正向移动,有利于提高酯的产率,D正确;答
案选D。
2.(23-24高三上·全国·开学考试)下列关于化学反应速率的说法中,正确的是
①铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②增加反应物的用量,一定会增大化学反应速率
③决定化学反应速率的主要因素是反应物的浓度
④光是影响某些化学反应速率的外界条件之一
⑤使用催化剂,使反应的活化能降低,反应速率加快
A.①⑤ B.④⑤ C.②④ D.③
【答案】B
【解析】①常温下铁在浓硫酸中钝化,得不到氢气,故①错误;②增加反应物的用量,不一定会增大化学
反应速率,例如改变固体的质量,故②错误;③决定化学反应速率的主要因素是反应物自身的性质,如钠
和冷水剧烈反应,但铁需要高温下才能与水蒸气反应,故③错误;④有些物质在光照条件下反应,如次氯
酸的分解等,因此光是影响某些化学反应速率的外界条件之一,故④正确;⑤使用催化剂,使反应的活化
能降低,反应速率加快,故⑤正确;故正确的是④⑤,答案为B。3.(23-24高三上·河南·期中)可逆反应2SO (g)+O(g) 2SO (g)正在逆向进行时,正反应速率和逆反
2 2 3
应速率的大小是
A.v正>v逆 B.v正< v逆 C.v正=v逆 D.不能确定
【答案】B
【解析】可逆反应,正反应和逆反应同时进行,正速率大就正向进行,逆速率大就逆向进行,两者相等处
于平衡状态,但仍在进行,没有停止。现逆向进行,说明逆反应速率大于正反应速率,答案选B。
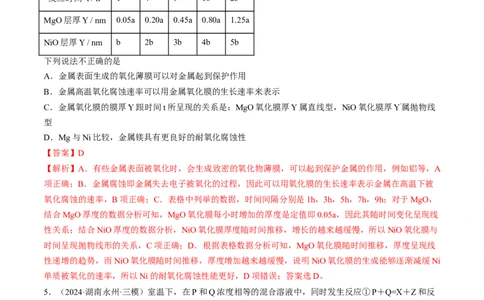
4.(2024·浙江·一模)下表数据是在某高温下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成
氧化薄膜的实验记录如下(a和b均为与温度有关的常数):
反应时间 t / h 1 4 9 16 25
MgO层厚Y / nm 0.05a 0.20a 0.45a 0.80a 1.25a
NiO层厚Y / nm b 2b 3b 4b 5b
下列说法不正确的是
A.金属表面生成的氧化薄膜可以对金属起到保护作用
B.金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示
C.金属氧化膜的膜厚Y跟时间t所呈现的关系是:MgO氧化膜厚Y属直线型,NiO氧化膜厚Y′属抛物线
型
D.Mg与Ni比较,金属镁具有更良好的耐氧化腐蚀性
【答案】D
【解析】A.有些金属表面被氧化时,会生成致密的氧化物薄膜,可以起到保护金属的作用,例如铝等,A
项正确;B.金属腐蚀即金属失去电子被氧化的过程,因此可以用氧化膜的生长速率表示金属在高温下被
氧化腐蚀的速率,B项正确;C.表格中列举的数据,时间间隔分别是1h,3h,5h,7h,9h;对于MgO,
结合MgO厚度的数据分析可知,MgO氧化膜每小时增加的厚度是定值即0.05a,因此其随时间变化呈现线
性关系;结合NiO厚度的数据分析,NiO氧化膜厚度随时间推移,增长的越来越缓慢,所以NiO氧化膜与
时间呈现抛物线形的关系,C项正确;D.根据表格数据分析可知,MgO氧化膜随时间推移,厚度呈现线
性递增的趋势,而NiO氧化膜随时间推移,厚度增加越来越缓慢,说明NiO氧化膜的生成能够逐渐减缓Ni
单质被氧化的速率,所以Ni的耐氧化腐蚀性能更好,D项错误;答案选D。
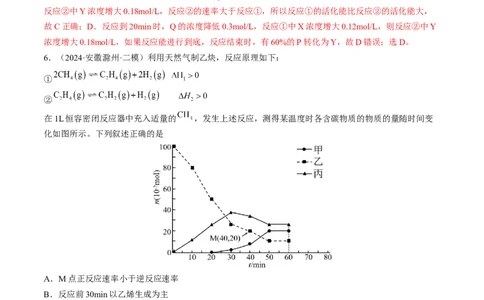
5.(2024·湖南永州·三模)室温下,在P和Q浓度相等的混合溶液中,同时发生反应①P+Q=X+Z和反
应②P+Q=Y+Z,反应①和②的速率方程分别是v=kc2(P)、v=kc2(P)(k 、k 为速率常数)。反应过程中,
1 1 2 2 1 2
Q、X的浓度随时间变化情况如图所示。下列说法错误的是
A.反应开始后,体系中X和Y的浓度之比保持不变B.45min时Z的浓度为0.4mol·L-1
C.反应①的活化能比反应②的活化能大
D.如果反应能进行到底,反应结束时,有40%的P转化为Y
【答案】D
【解析】A.根据①和②的速率方程分别是v=kc2(P)、v=kc2(P)(k 、k 为速率常数),反应开始后,体系中
1 1 2 2 1 2
X和Y的浓度之比为 ,保持不变,故A正确;B.根据反应①P+Q=X+Z和反应②P+Q=Y+Z方程
式,可知每消耗1molQ同时生成1molZ,反应到45min时,Q的浓度降低0.4mol/L, 则Z的浓度为
0.4mol·L-1,故B正确;C.反应到20min时,Q的浓度降低0.3mol/L,反应①中X浓度增大0.12mol/L,则
反应②中Y浓度增大0.18mol/L,反应②的速率大于反应①,所以反应①的活化能比反应②的活化能大,
故C正确;D.反应到20min时,Q的浓度降低0.3mol/L,反应①中X浓度增大0.12mol/L,则反应②中Y
浓度增大0.18mol/L,如果反应能进行到底,反应结束时,有60%的P转化为Y,故D错误;选D。
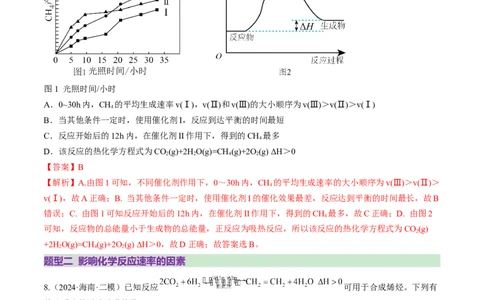
6.(2024·安徽滁州·二模)利用天然气制乙炔,反应原理如下:
①
②
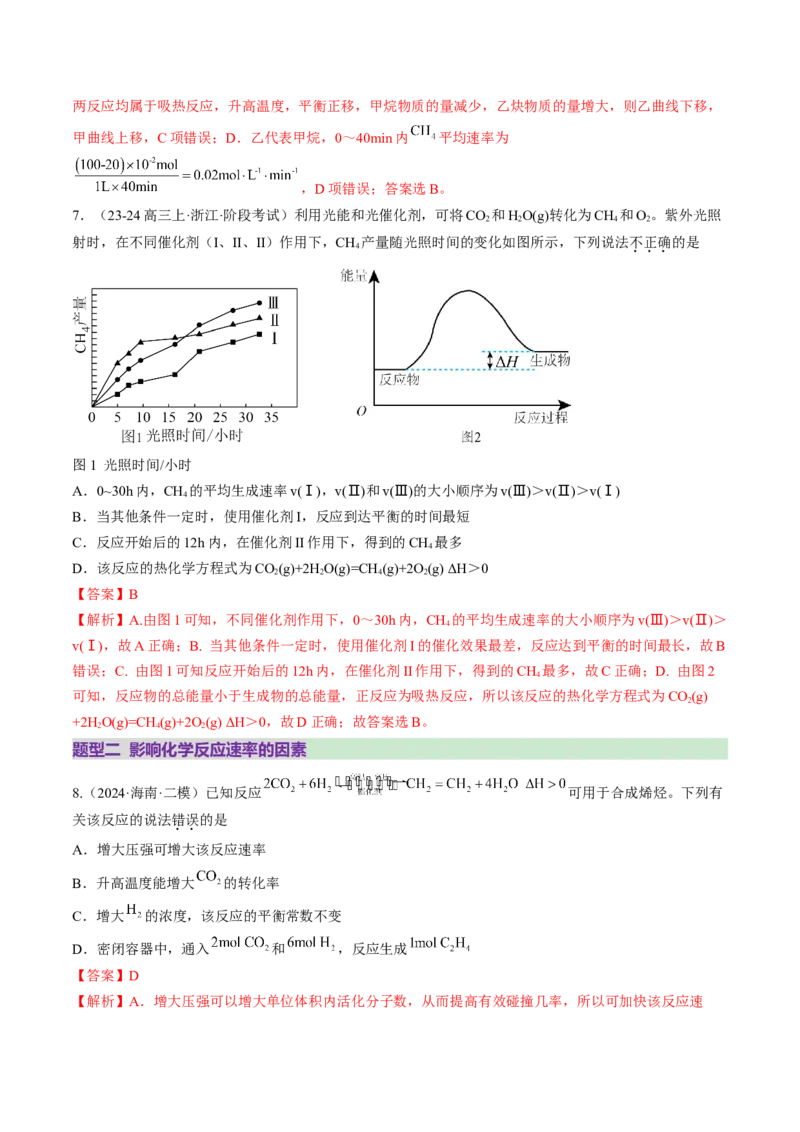
在1L恒容密闭反应器中充入适量的 ,发生上述反应,测得某温度时各含碳物质的物质的量随时间变
化如图所示。下列叙述正确的是
A.M点正反应速率小于逆反应速率
B.反应前30min以乙烯生成为主
C.若60min后升温,乙曲线上移,甲曲线下移
D.0~40min内 平均速率为2.
【答案】B
【分析】根据题干方程式特点,随反应进行,甲烷含量逐渐减小,乙烯物质的量先增大后减小,产物乙炔
物质的量只增大,因此曲线甲代表乙炔、乙代表甲烷、丙代表乙烯;根据曲线变化,30 min前以乙烯生成
为主,30 min后,以乙炔生成反应为主。
【解析】A.由分析可知,乙代表甲烷,M点时,甲烷的物质的量减小,说明反应向正向进行,则正反应
速率大于逆反应速率,A项错误;B.由分析可知,30 min前以乙烯生成为主,B项正确;C.根据题干,两反应均属于吸热反应,升高温度,平衡正移,甲烷物质的量减少,乙炔物质的量增大,则乙曲线下移,
甲曲线上移,C项错误;D.乙代表甲烷,0~40min内 平均速率为
,D项错误;答案选B。
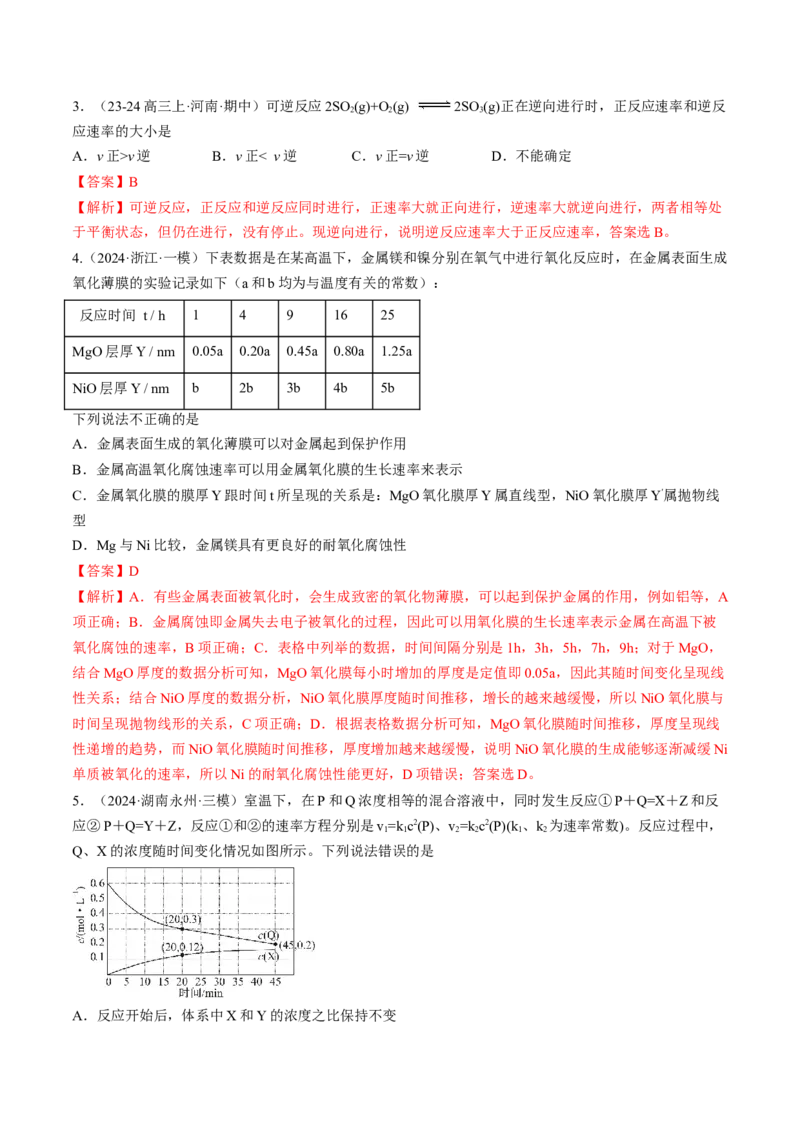
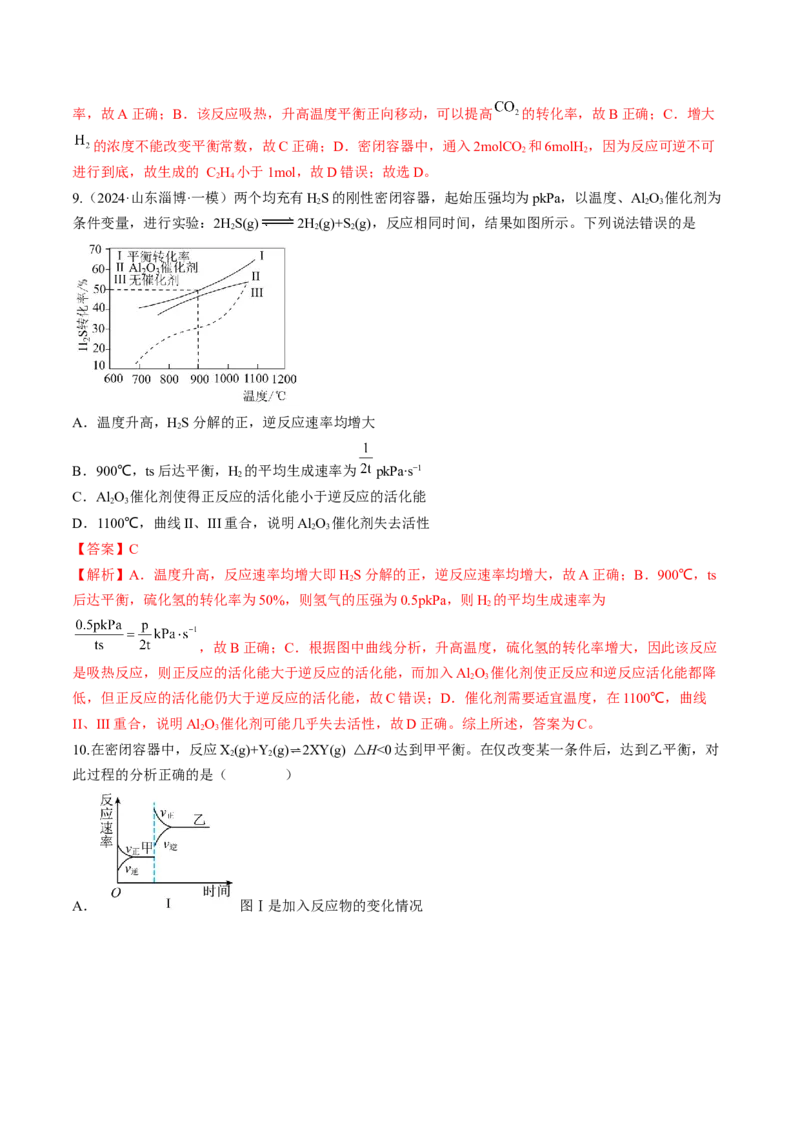
7.(23-24高三上·浙江·阶段考试)利用光能和光催化剂,可将CO 和HO(g)转化为CH 和O。紫外光照
2 2 4 2
射时,在不同催化剂(I、II、II)作用下,CH 产量随光照时间的变化如图所示,下列说法不正确的是
4
图1 光照时间/小时
A.0~30h内,CH 的平均生成速率v(Ⅰ),v(Ⅱ)和v(Ⅲ)的大小顺序为v(Ⅲ)>v(Ⅱ)>v(Ⅰ)
4
B.当其他条件一定时,使用催化剂I,反应到达平衡的时间最短
C.反应开始后的12h内,在催化剂II作用下,得到的CH 最多
4
D.该反应的热化学方程式为CO(g)+2HO(g)=CH(g)+2O(g) ΔH>0
2 2 4 2
【答案】B
【解析】A.由图1可知,不同催化剂作用下,0~30h内,CH 的平均生成速率的大小顺序为v(Ⅲ)>v(Ⅱ)>
4
v(Ⅰ),故A正确;B. 当其他条件一定时,使用催化剂I的催化效果最差,反应达到平衡的时间最长,故B
错误;C. 由图1可知反应开始后的12h内,在催化剂II作用下,得到的CH 最多,故C正确;D. 由图2
4
可知,反应物的总能量小于生成物的总能量,正反应为吸热反应,所以该反应的热化学方程式为CO(g)
2
+2H O(g)=CH(g)+2O(g) ΔH>0,故D正确;故答案选B。
2 4 2
题型二 影响化学反应速率的因素
8.(2024·海南·二模)已知反应 可用于合成烯烃。下列有
关该反应的说法错误的是
A.增大压强可增大该反应速率
B.升高温度能增大 的转化率
C.增大 的浓度,该反应的平衡常数不变
D.密闭容器中,通入 和 ,反应生成
【答案】D
【解析】A.增大压强可以增大单位体积内活化分子数,从而提高有效碰撞几率,所以可加快该反应速率,故A正确;B.该反应吸热,升高温度平衡正向移动,可以提高 的转化率,故B正确;C.增大
的浓度不能改变平衡常数,故C正确;D.密闭容器中,通入2molCO 和6molH ,因为反应可逆不可
2 2
进行到底,故生成的 C H 小于1mol,故D错误;故选D。
2 4
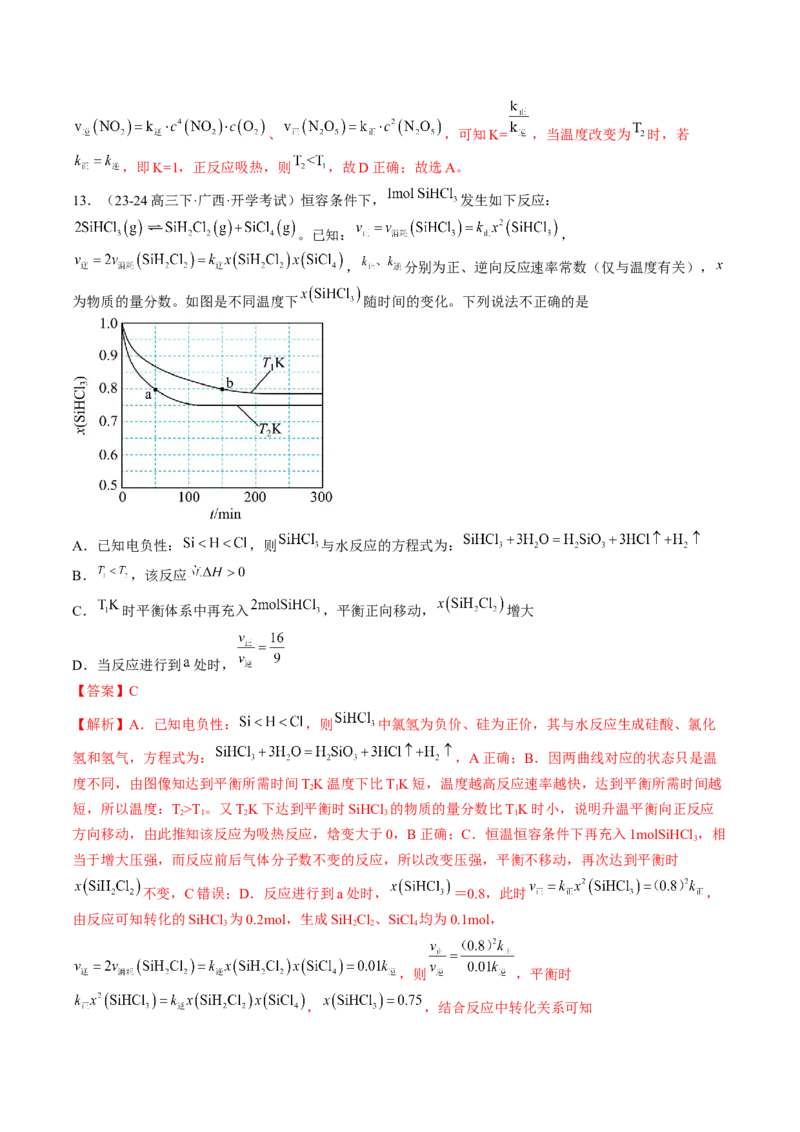
9.(2024·山东淄博·一模)两个均充有HS的刚性密闭容器,起始压强均为pkPa,以温度、Al O 催化剂为
2 2 3
条件变量,进行实验:2HS(g) 2H(g)+S (g),反应相同时间,结果如图所示。下列说法错误的是
2 2 2
A.温度升高,HS分解的正,逆反应速率均增大
2
B.900℃,ts后达平衡,H 的平均生成速率为 pkPa∙s−1
2
C.Al O 催化剂使得正反应的活化能小于逆反应的活化能
2 3
D.1100℃,曲线II、III重合,说明Al O 催化剂失去活性
2 3
【答案】C
【解析】A.温度升高,反应速率均增大即HS分解的正,逆反应速率均增大,故A正确;B.900℃,ts
2
后达平衡,硫化氢的转化率为50%,则氢气的压强为0.5pkPa,则H 的平均生成速率为
2
,故B正确;C.根据图中曲线分析,升高温度,硫化氢的转化率增大,因此该反应
是吸热反应,则正反应的活化能大于逆反应的活化能,而加入Al O 催化剂使正反应和逆反应活化能都降
2 3
低,但正反应的活化能仍大于逆反应的活化能,故C错误;D.催化剂需要适宜温度,在1100℃,曲线
II、III重合,说明Al O 催化剂可能几乎失去活性,故D正确。综上所述,答案为C。
2 3
10.在密闭容器中,反应X
2
(g)+Y
2
(g)⇌2XY(g) △H<0达到甲平衡。在仅改变某一条件后,达到乙平衡,对
此过程的分析正确的是( )
A. 图Ⅰ是加入反应物的变化情况B. 图Ⅱ是扩大容器体积的变化情况
C. 图Ⅲ是增大压强的变化情况
D. 图Ⅲ是升高温度的变化情况
【答案】D
【解析】 加入反应物的瞬间,反应物浓度增大、生成物浓度不变,则正反应速率增大、逆反应速率不
变,I中改变条件瞬间正逆反应速率都增大,图象不符合,故A错误;B.该反应前后气体物质的量之和不
变,则压强不影响平衡移动,增大容器体积,反应物和生成物浓度都减小,所以正逆反应速率都减小,图
象不符合,故B错误;C.增大压强化学反应速率增大,达到平衡状态的时间减小,但是压强不影响该反应
平衡移动,所以达到平衡状态时应该甲、乙中 的含量相同,图象不符合,故C错误;D.该反应的正
反应是放热反应,升高温度化学反应速率增大,缩短反应到达平衡状态时间,且平衡逆向移动, 的
含量减小,图象符合,故D正确;故选:D。
11.(2024·山东·二模)某同学为探究浓度对化学反应速率的影响,设计以下实验。
① ② ③ ④
试剂 1mL0.01mol/L酸性 1mL0.01mol/L酸性高 1mL0.01mol/L酸性高 1mL0.01mol/L酸性高
a 高锰酸钾水溶液 锰酸钾水溶液 锰酸钾水溶液 锰酸钾水溶液
1mL以浓盐酸为溶剂
试剂 2mL0.1mol/LH C O 2mL0.2mol/LH C O 水 1mL0.2mol/LH C O 水
2 2 4 2 2 4 2 2 4
配制的0.2mol/LH C O
2 2 4
b 水溶液 溶液 溶液
水溶液
褪色
690s 677s 600s
时间
下列说法错误的是
A.对比实验①、②可知,HC O 水溶液浓度增大,反应速率加快
2 2 4B.对比实验②、③可知,酸性高锰酸钾水溶液浓度增大,反应速率加快
C.为验证H+浓度对反应速率的影响,设计实验④并与③对照
D.实验③的离子方程式为2 +6H++5H C O=2Mn2++10CO ↑+8H O
2 2 4 2 2
【答案】C
【解析】A. 对比实验①、②可知,两实验中只有HC O 水溶液浓度不同,且浓度大的褪色时间较短,故
2 2 4
HC O 水溶液浓度增大,反应速率加快,选项A正确;B.对比实验②、③可知,两实验中只有HC O 水
2 2 4 2 2 4
溶液的体积不同,且前者大,则相当于高锰酸钾水溶液的浓度小,褪色时间长,则酸性高锰酸钾水溶液浓
度增大,反应速率加快,选项B正确;C.若为验证H+浓度对反应速率的影响,设计实验④并与③对照,
则氯离子也可能对反应速率有影响,从而引起干扰,无法得到验证,选项C错误;D.实验③高锰酸钾氧
化草酸生成二氧化碳,反应的离子方程式为2 +6H++5H C O=2Mn2++10CO ↑+8H O,选项D正确;答
2 2 4 2 2
案选C。
12.(2024·黑龙江大庆·三模)在两个相同恒温( )恒容密闭容器中仅发生反应:
。实验测得: ;
; 、 为速率常数,受温度影响。下列说法错误的是
物质的起始浓度( ) 物质的平衡浓度( )
容器编
号
Ⅰ 4 0 0 1
Ⅱ 1 2 0.5
A.平衡时容器1中再充入一定量的 , 体积分数增大
B.若将容器1改为恒容绝热条件,平衡时
C.反应刚开始时容器Ⅱ中的
D.当温度改变为 时,若 ,则
【答案】A
【解析】A.平衡时容器1中再充入一定量的 ,相当于增大压强,平衡
逆向移动, 体积分数减小,A错误;B.该反应为吸热反应,若将容器
1改为恒容绝热条件,反应过程中容器的温度降低,平衡逆向移动,平衡时 ,B正确;
C.容器Ⅰ平衡时, =1mol/L, =4mol/L, =2mol/L,平衡常数K= =64,容器Ⅱ
开始时Q= =8T。又TK下达到平衡时SiHCl 的物质的量分数比TK时小,说明升温平衡向正反应
2 1 2 3 1
方向移动,由此推知该反应为吸热反应,焓变大于0,B正确;C.恒温恒容条件下再充入1molSiHCl ,相
3
当于增大压强,而反应前后气体分子数不变的反应,所以改变压强,平衡不移动,再次达到平衡时
不变,C错误;D.反应进行到a处时, =0.8,此时 ,
由反应可知转化的SiHCl 为0.2mol,生成SiHCl、SiCl 均为0.1mol,
3 2 2 4
,则 ,平衡时
, ,结合反应中转化关系可知,则 ,则 ,D正确;故选C。
14.在容积不变的密闭容器中进行反应:2SO (g)+O (g) 2SO (g) △H<0。下列各图表示当其他条
2 2 3
件不变时,改变某一条件对上述反应的影响,其中正确的是
A.图I表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t 时刻使用催化剂对反应速率的影响
0
C.图Ⅲ表示t 时刻增大O 的浓度对反应速率的影响
0 2
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
【答案】B
【解析】A.图Ⅰ中乙到达平衡时间较短,乙的温度较高,正反应放热,升高温度,平衡向逆反应方向移
动,SO 的转化率减小,乙的温度较高,故A错误;B.图Ⅱ在t 时刻,正逆反应速率都增大,但仍相等,
3 0
平衡不发生移动,应是加入催化剂的原因,故B正确;C.增大反应物的浓度瞬间,正反速率增大,逆反
应速率不变,之后逐渐增大,图Ⅲ改变条件瞬间,正、逆速率都增大,正反应速率增大较大,平衡向正反
应移动,应是增大压强的原因,故C错误;D.曲线表示平衡常数与温度的关系,曲线上各点都是平衡
点,故D错误;故选B。
15.(2024·湖南·模拟预测)研究 之间的转化对控制大气污染具有重要意义,已知:
。如图所示,在恒容密闭容器中,反应温度为 时, 和 随t
变化曲线分别为Ⅰ、Ⅱ,改变温度到 , 随t变化为曲线Ⅲ。下列判断正确的是
A.反应速率
B.温度C.升高温度,正向反应速率增加,逆向反应速率减小
D.温度 和 下,反应分别达到平衡时, 前者小
【答案】B
【解析】A.升高温度,反应速率增大,达到平衡所需时间变短,根据图像,温度T>T,故反应速率
2 1
,A错误;B.升高温度,反应速率增大,达到平衡所需时间变短,根据图像,温度T>T,B
2 1
正确;C.升高温度,正、逆反应速率均增大,C错误;D.该反应为吸热反应,温度升高,平衡正向移
动,所以温度 和 下,反应分别达到平衡时, 前者大,D错误;本题选B。
16.(2024·河北·一模)某密闭容器中含有X和Y,同时发生以下两个反应:① ;②
。反应①的正反应速率 ,反应②的正反应速率 ,其
中 为速率常数。某温度下,体系中生成物浓度 随时间 变化的曲线如图所示。下列说法正确的
是
A. 时,正反应速率
B. 内,X的平均反应速率
C.若升高温度, 时容器中 的比值减小
D.反应①的活化能大于反应②
【答案】A
【解析】A.由图可知,初始生成M的速率大于N,则 , 时两个反应均达到平衡状态,由于
、 ,则正反应速率 ,A正确;B.①②反应中XQ的系数
均为1,则 内,X的平均反应速率 ,B错误;C. 后M浓度
减小,可能为Q浓度增大导致①逆向移动所致,不确定2个反应的吸热放热情况,不能确定升高温度,
时容器中 的比值变化情况,C错误;D.由图可知,初始生成M的速率大于N,则反应①的话
化能小于反应②,D错误;故选A。
17.(2024·河南·一模)控制变量法在化学实验探究中运用较多,它是指在研究和解决问题的过程中,对
影响事物变化规律的因素或条件加以人为控制,使其中的一些条件按照特定的要求发生或不发生变化,以
便在研究过程中,找到事物变化发展的规律。根据因素和条件的性质,可分为实验变量(自变量)、反应
变量(因变量)和无关变量。某研究小组用酸性KMnO 溶液与HC O 溶液反应中溶液紫色消失的方法,来研
4 2 2 4究浓度对化学反应速率的影响。下列实验有关变量控制的操作错误的是
A.为控制无关变量的影响,将实验温度均确定为25°C、酸性KMnO 溶液与HC O 溶液的体积均确定为
4 2 2 4
4mL,不使用催化剂
B.可选择浓度分别为0.05mol/L、0. 01mol/L、0. 001mol/L的KMnO 酸性溶液和浓度均为0.001mol/L的
4
HC O 溶液反应,来操纵实验变量,进行对照实验
2 2 4
C.可将单位时间内反应所生成的CO 体积作为实验变量(自变量)进行本实验研究
2
D.该实验研究中的反应变量(因变量)是溶液紫色褪去所消耗的时间
【答案】C
【解析】A.相同的反应物及体积和温度,一个使用催化剂,一个不使用催化剂,催化剂为无关变量,所
以该过程为控制无关变量的影响,A正确;B.HC O 溶液的浓度0.001mol/L,KMnO 酸性溶液的浓度分
2 2 4 4
别为0.05mol/L、0. 01mol/L、0.001mol/L,通过控制不同浓度的高锰酸钾溶液来进行对照试验,即控制自
变量的影响,B正确;C.观察单位时间内反应所生成的CO 体积为反应变量,即为因变量,该实验的目
2
的是通过对照观察单位时间内反应所生成的CO 体积,探究化学反应速率的快慢,即控制因变量,C错
2
误;D.反应变量是溶液紫色褪去所消耗的时间,该实验研究中的反应变量为因变量,即控制因变量的影
响, D正确;综上所述,本题正确选项C。
18.(2024·北京·一模)实验小组探究双氧水与KI的反应,实验方案如下表。
序号 ① ② ③
实验装
置及操
作
溶液立即变为黄色,产生大量 溶液立即变为棕黄色,产生少量无色
实验现
溶液无明显变化 无色气体;溶液温度升高;最 气体;溶液颜色逐渐加深,温度无明
象
终溶液仍为黄色 显变化;最终有紫黑色沉淀析出
下列说法不正确的是
A. 对 分解有催化作用
B.对比②和③,酸性条件下 氧化 的速率更大
C.对比②和③,②中的现象可能是因为 分解的速率大于HO 氧化 的速率
2 2
D.实验②③中的温度差异说明, 氧化 的反应放热
【答案】D
【解析】A.比较实验①②的现象可知, 对 分解有催化作用,A正确;B.对比②和③,由实验③
的现象溶液立即交为棕黄色,产生少量无色气体;溶液颜色逐渐加深,温度无明显变化;最终有紫黑色沉
淀析出溶液无明显变化,可知酸性条件下 氧化 的速率更大,B正确;C.对比②和③,②中的现象为溶液立即变为黄色,产生大量无色气体;溶液温度升高;最终溶液仍为黄色,实验③现象为:溶液立即
交为棕黄色,产生少量无色气体;溶液颜色逐渐加深,温度无明显变化;最终有紫黑色沉淀析出溶液无明
显变化,故可能是因为 分解的速率大于HO 氧化 的速率,C正确;D.实验②中主要发生HO 分
2 2 2 2
解,温度明显升高,而实验③中主要发生HO 氧化KI的反应,温度无明显变化,说明HO 催化分解是一
2 2 2 2
个放热反应,不能说明 氧化 的反应放热,D错误;故答案为:D。
19.(2024·上海闵行·三模)T℃时,向2.0L的恒容密闭容器中充入1.0mol 和0.6mol ,发生如下反
应: 。20s时反应达到平衡, 和 相等。
(1)0~20s内, 。
(2)平衡后向容器中再充入0.4mol 和0.3mol ,此时, _______ 。
A.大于 B.小于 C.等于 D.无法判断
(3)相同温度下,起始投料变为0.5mol 和0.3mol , 的平衡转化率_______。
A.增大 B.不变 C.减小 D.无法判断
【答案】(1)0.02(2)A(3)C
【解析】(1)根据三段式可知
,20s后反应达到平衡, 和 相等,则0.5-2x
=0.3-x,解得x=0.2,所以 0.4mol/L÷20s=0.02 ,平衡常数为 ;
(2)平衡后向容器中再充入 和 ,此时浓度熵为 ,平衡正
向进行,则v(正)>v(逆);
(3)相同温度下,起始投料变为 和 ,相当于是减小压强,平衡逆向进行,则 的
平衡转化率减小。
20.(2024·上海虹口·一模)研究反应Ⅰ的逆反应对提高尿素产率有重要意义。某研究学习小组把一定量
的氨基甲酸铵固体放入容积为2L的密闭容器中,在T℃下分解:NH COONH(s) 2NH (g)+CO (g),t 时
2 4 3 2 1
达到化学平衡。c(CO)随时间t变化曲线如图所示。
2(1)可以判断该分解反应已经达到平衡的是___________。
A.混合气体的平均摩尔质量不变 B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
(2)T 时,该反应的化学平衡常数K的值为 。
(3)在0~t 时间内该化学反应速率v(NH )= 。
1 3
(4)若其他条件不变,t 时将容器体积压缩到1L,t 时达到新的平衡。请在图中画出t~t 时间内c(CO)
2 3 2 4 2
随时间t变化的曲线。
【答案】(1)BC
(2)0.0005
(3)0.10/t mol·L-1·s-1
1
(4)
【解析】(1)A.该反应的反应物为固体,混合气体的平均摩尔质量由生成物决定,而两种生成物的物质
的量之比为定值,故混合气体的平均摩尔质量始终保持不变,故A不能说明平衡;B.密闭容器中总压强
取决于气体的物质的量,只要此反应未达到平衡,则气体的物质的量始终发生变化,则压强始终变化,故
压强不变可以说明平衡,故B正确;C.气体的密度等于气体的质量除以容器的体积,容器的体积不变,
只要此反应未达到平衡,则气体的质量始终发生变化,则密度始终变化,故密度不变可以说明平衡,故C
正确;D.密闭容器中氨气和二氧化碳的比例始终为2:1,则氨气的体积分数始终为定值,故密闭容器中
氨气的体积分数不变不能说明平衡,故D错误; 故选BC。
(2)该反应的化学平衡常数 ,平衡时c(CO)=0.05mol/L,而氨气和二氧化碳的比例始终
2
为2:1,故c(NH )=0.1mol/L,故
3
(3)在0~t 时间内,氨气的浓度变化值为0.1mol/L,故该化学反应速率v(NH )= 0.10/t mol·L-1·s-1;
1 3 1
(4)若其他条件不变,t 时将容器体积压缩到1L,则在那一刻二氧化碳的浓度达到0.1mol/L,t 时达到新
2 3的平衡时,根据 且温度不变可知二氧化碳的浓度应该回到0.05mol/L才能保证平衡常数
不变。
1.(2024·北京·高考真题)苯在浓 和浓 作用下,反应过程中能量变化示意图如下。下列说法
不正确的是
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大 键没有变化
D.对于生成Y的反应,浓 作催化剂
【答案】C
【解析】A.生成产物Ⅱ的反应的活化能更低,反应速率更快,且产物Ⅱ的能量更低即产物Ⅱ更稳定,以
上2个角度均有利于产物Ⅱ,故A正确;B.根据前后结构对照,X为苯的加成产物,Y为苯的取代产
物,故B正确;C.M的六元环中与 相连的C为 杂化,苯中大 键发生改变,故C错误;D.苯
的硝化反应中浓 作催化剂,故D正确;故选C。
2.(2024·安徽·高考真题)室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下 浓
度随时间变化关系如下图。
实验序号 水样体积/ 纳米铁质量/ 水样初始① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.实验①中,0~2小时内平均反应速率
B.实验③中,反应的离子方程式为:
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始 越小, 的去除效果越好
【答案】C
【解析】A. 实验①中,0~2小时内平均反应速率
,A不正确;B. 实验③中水样初始 =8,溶
液显弱碱性,发生反应的离子方程式中不能用 配电荷守恒,B不正确;C. 综合分析实验①和②可知,
在相同时间内,实验①中 浓度的变化量大,因此,其他条件相同时,适当增加纳米铁质量可加快反
应速率,C正确;D. 综合分析实验③和②可知,在相同时间内,实验②中 浓度的变化量大,因此,
其他条件相同时,适当减小初始 , 的去除效果越好,但是当初始 太小时, 浓度太大,纳米
铁与 反应速率加快,会导致与 反应的纳米铁减少,因此,当初始 越小时 的去除效果不一
定越好,D不正确;综上所述,本题选C。
3.(2023·河北·高考真题)在恒温恒容密闭容器中充入一定量W(g),发生如下反应:
反应②和③的速率方程分别为 和 ,其中 、 分别为反应②和③的速率常数、反应
③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:
t/min 0 1 2 3 4 5
0.160 0.113 0.080 0.056 0.040 0.028
下列说法正确的是
A. 内,W的平均反应速率为
B.若升高温度,平衡时 减小
C.若 ,平衡时D.若增大容器容积,平衡时Y的产率增大
【答案】B
【解析】A.由表格数据可知,2min时W的浓度为0.080mol/L,则0∼2min内,W的反应速率为
=0.040 mol/(L·min),故A错误;B.反应③的活化能大于反应②说明X转化为Z的反
应为放热反应,升高温度,反应②平衡向逆反应方向移动,Z的浓度减小,故B正确;C.由反应达到平
衡时,正逆反应速率相等可得: = ,若 ,则X和Z的浓度关系为 ,故C
错误;D.由转化关系可知,反应①为W完全分解生成X和Y,Y只参与反应①,所以增大容器容积,平
衡时Y的物质的量不变、产率不变,故D错误;故选B。
4.(2022·广东·高考真题)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时
间t的部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
【答案】D
【解析】A.由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错
误;B.由图可知,催化剂I比催化剂Ⅱ催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错
误;C.由图可知,使用催化剂Ⅱ时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变
化了2.0mol/L,二者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂Ⅱ时X浓度随时间t
的变化,故C错误;D.使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 (Y) = =
=2.0 , (X) = (Y) = 2.0 =1.0 ,故D正确;答案
选D。
5.(2022·浙江·高考真题)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化如图
中曲线甲所示。下列说法不正确的是A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
【答案】C
【解析】A.图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,
从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率,选项A正确;B.b点处的切线的斜
率是此时刻物质浓度除以此时刻时间,为反应物B的瞬时速率,选项B正确;C.化学反应速率之比等于
化学方程式计量数之比分析,3v(B)=2v(X),选项C不正确;D.维持温度、容积不变,向反应体系中加入
催化剂,平衡不移动,反应速率增大,达到新的平衡状态,平衡状态与原来的平衡状态相同,选项D正
确;答案选C。