文档内容
第 03 讲 分子结构与性质、化学键
01 模拟基础练
【题型一】化学键
【题型二】分子的空间结构
【题型三】分子的性质及应用
【题型四】配位键、配合物、超分子
02 重难创新练
03 真题实战练
题型一 化学键
1.(2024·浙江·模拟预测)下列物质中含有共价键的盐是
A.CHCONH B.NH NO C.MgCl D.NaOH
3 2 4 3 2
2.(2024·山东济南·三模)下列物质熔化时,不破坏化学键的是
A.氯化钠 B.十七烷 C.金刚石 D.铜
3.(2024·湖北·三模)十九世纪初,科学家用氰酸银 与 在一定条件下反应制得尿素
,实现了由无机物到有机物的合成。下列有关说法错误的是
A.电负性:
B.氰酸铵与尿素互为同分异构体
C.键角
D. 晶体中含有离子键、极性共价键和配位键
4.(2024·河南·模拟预测)有机玻璃(聚甲基丙烯酸甲酯)透光性好,可制成飞机和车辆的风挡、光学仪
器等,可由甲基丙烯酸甲酯发生如下反应制得。下列说法正确的是
A.甲基丙烯酸甲酯可由酸和醇发生加成反应得到
B.聚甲基丙烯酸甲酯分子中有1个手性碳原子
C.甲基丙烯酸甲酯中 键和 键的个数比为7:1
D.聚甲基丙烯酸甲酯中元素的电负性为
题型二 分子的空间结构5.(2024·安徽安庆·模拟预测)已知反应:NH NO +NHHSO +SO+2H O=[NH OH]+ +(NH)SO 。下
4 3 4 3 2 2 3 4 2 4
列有关说法错误的是
A.HO很稳定是因为分子间含有氢键
2
B.SO 的空间结构为V形
2
C.NH OH的H-N-H键角小于 中H-N-H键角
2
D.HO、 与 的VSEPR模型相同
2
6.(2024·河北唐山·二模)含氮化合物应用广泛,下列说法正确的是
A. 的价层电子对互斥模型为三角锥形
B. 的空间构型为平面三角形
C.每个 中有6个 键
D. 中 的杂化方式不同
7.(2024·湖北·三模)分析微粒结构,下列说法正确的是
A.CH 和P 的空间构型都是正四面体形,键角也相同
4 4
B.OF 与HO的价层电子对情况和空间构型相同,但OF 的极性较小
2 2 2
C.Al Cl( )中Al为sp3杂化,与AlCl 中Al的杂化方式相同
2 6 3
D.PCl 和BCl 中心原子的杂化方式不同,但所有原子都满足8电子结构
3 3
8.(23-24高三下·黑龙江·期末)下列分子或离子中键角由大到小排列顺序是
①BF ②NH ③HO ④NH + ⑤BeCl
3 3 2 4 2
A.⑤④①②③ B.⑤①④②③
C.④①②⑤③ D.③②④①⑤
题型三 分子的性质及应用
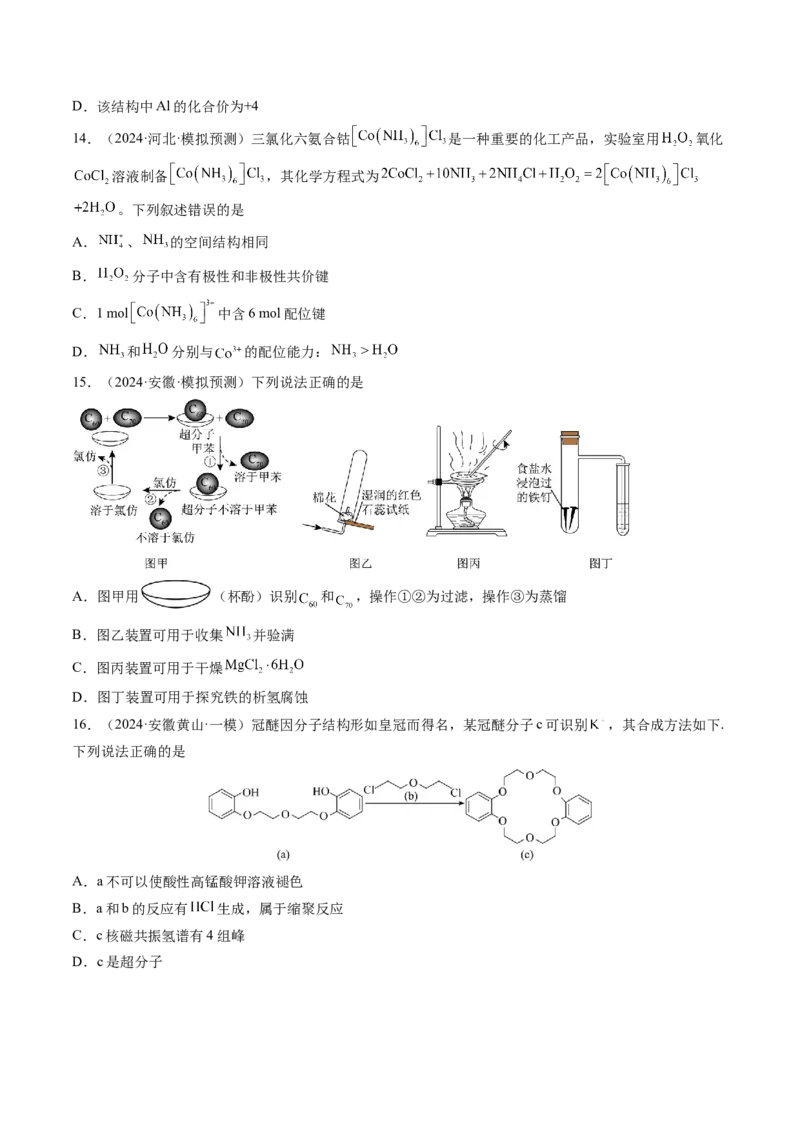
9. 与 在铜催化剂上的反应机理和能量变化如图所示.下列说法正确的是
A.反应Ⅰ、反应Ⅱ均为放热反应
B. 分子中 键和 键数目和 相同
C.选择合适的催化剂可降低反应活化能和焓变
D.该反应机理中涉及物质中有两种非极性分子、三种极性分子10.(2024·重庆·模拟预测)超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
现有某种超分子结构如图所示。下列有关说法正确的是
A.该超分子中C原子均为sp3杂化
B.甲基中的键角∠HCH小于-NH 中的键角∠HNH
2
C.该超分子由一个非极性分子和一个极性分子聚集而成
D.该超分子加热熔化时既破坏氢键,也破坏分子间作用力
11.(2024·北京大兴·三模)下列变化中,主要破坏的微粒间作用力为范德华力的是
A.钠熔化成闪亮的小球
B.干冰升华
C.苯酚晶体久置后变为粉红色
D.工业合成氨,利用氨易液化的特点,从混合气体中分离出来
12.(2024·湖北黄冈·模拟预测)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选
性质差异 结构因素
项
A 沸点:乙醇 高于乙醛 分子间氢键
B 熔点: 熔点远高于 的熔点 分子间作用力
C 键角: 小于 电负性差异
D 分解温度: 高于 键能大小
题型四 配位键、配合物、超分子
13.(2024·江苏南京·模拟预测)由金属钛、铝形成的Tebbe试剂常用作有机反应的烯化试剂,其结构如
图所示。下列说法正确的是
A.Al3+与Cl-具有相同的电子层结构
B.该结构中不存在配位键
C.Tebbe试剂中的Al原子轨道杂化类型为sp3D.该结构中Al的化合价为+4
14.(2024·河北·模拟预测)三氯化六氨合钴 是一种重要的化工产品,实验室用 氧化
溶液制备 ,其化学方程式为
。下列叙述错误的是
A. 、 的空间结构相同
B. 分子中含有极性和非极性共价键
C.1 mol 中含6 mol配位键
D. 和 分别与 的配位能力:
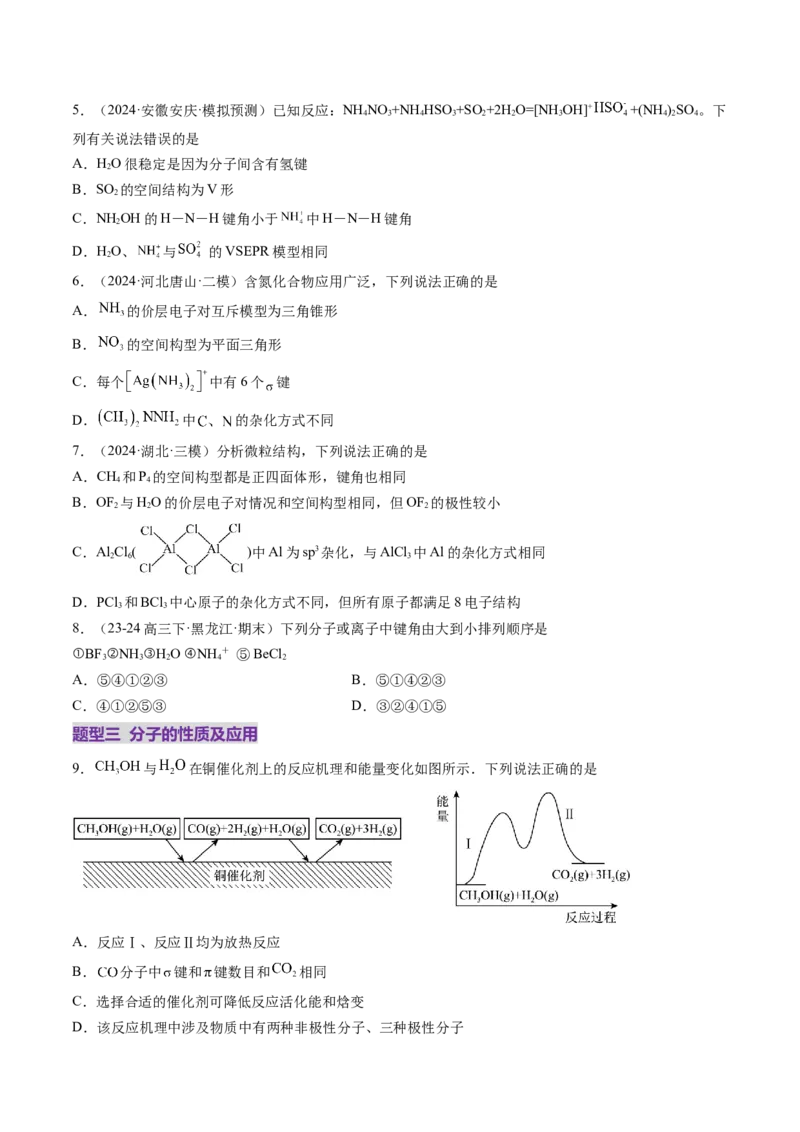
15.(2024·安徽·模拟预测)下列说法正确的是
A.图甲用 (杯酚)识别 和 ,操作①②为过滤,操作③为蒸馏
B.图乙装置可用于收集 并验满
C.图丙装置可用于干燥
D.图丁装置可用于探究铁的析氢腐蚀
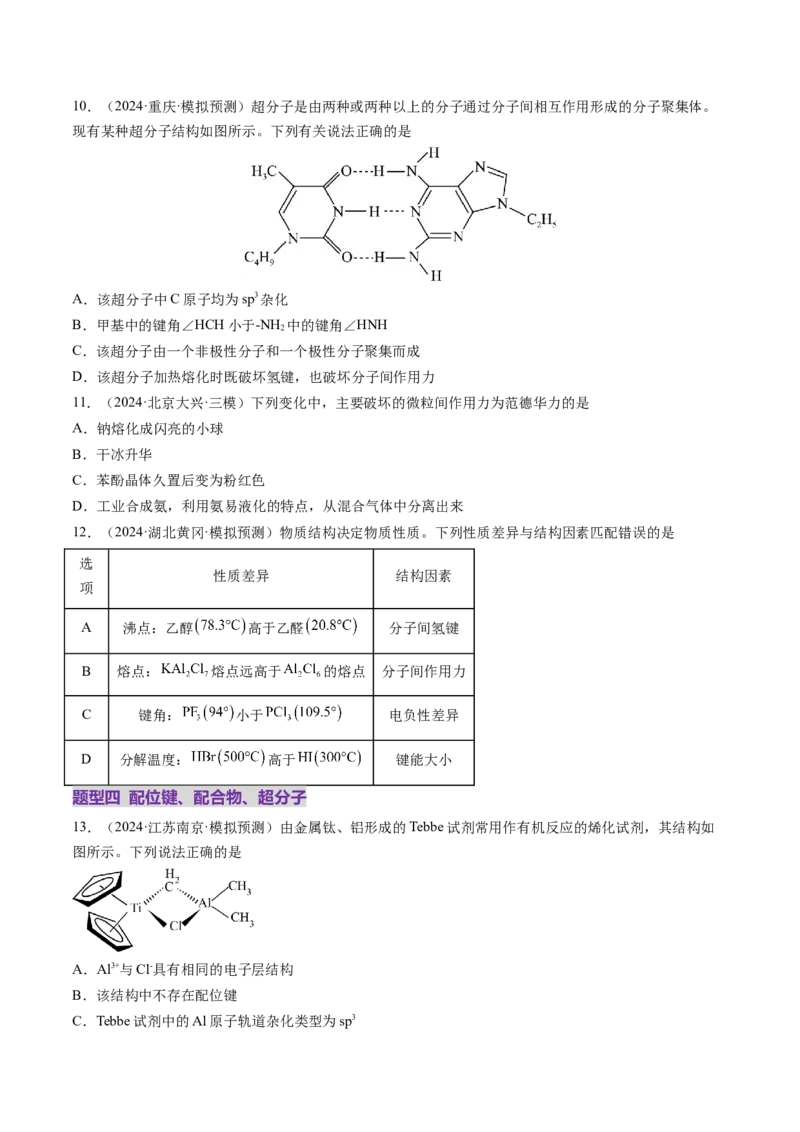
16.(2024·安徽黄山·一模)冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别 ,其合成方法如下.
下列说法正确的是
A.a不可以使酸性高锰酸钾溶液褪色
B.a和b的反应有 生成,属于缩聚反应
C.c核磁共振氢谱有4组峰
D.c是超分子17.(23-24高三下·广东深圳·开学考试)四氯化锗(GeCl )是光导纤维的常用掺杂剂,锗与硅同族。下
4
列说法不正确的是
A.基态Ge原子价层电子排布式为3d104s24p2
B.GeCl 的熔点比SiCl 高
4 4
C.键角:GeCl >H O
4 2
D.第一电离能大小:Cl>Si>Ge
18.(23-24高三上·江苏无锡·阶段考试)下列有关[Ni(NH )]SO 的说法正确的是
3 6 4
A.SO 、ClO 、NO 、CO 离子的中心原子均采用sp3杂化
B.1 mol [Ni(NH)]2+中σ键的数目为18 mol
3 6
C.[Ni(NH )]2+中H—N—H的键角大于NH 中的键角
3 6 3
D.ⅤA族元素单质的晶体类型相同
19.(23-24高三上·湖北·期中)缺电子化合物是指电子数不符合路易斯结构(路易斯结构是通过共用电子
使原子价层电子数达到8,氢原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法正确的是
A. 、 、 均为缺电子化合物
B. 的键角大于 的键角
C. 与 化合反应产物中,B和N的杂化方式不相同
D. 和 都是极性分子
20.(2024·四川眉山·模拟预测)铁元素在地壳中含量丰富,应用广泛。回答下列问题:
(1)原子核外运动的电子有两种相反的自旋状态,若有一种自旋状态用 ,则与之相反的用 ,称
为电子的自旋磁量子数,基态Fe原子核外电子自旋磁量子数的代数和为 。
(2) 水溶液中 可水解生成双核阳离子 ,结构如图所示。该双核阳离子中
键角 (填“大于”、“小于”或“等于”) 中的 键角;若对 水溶
液进行加热,该双核阳离子内部首先断开的是 键(填“a”或“b”)。
(3)三硝酸六尿素合铁【 】是一种重要的配合物,用作有机铁肥,简称铁氮
肥。该配合物中所含非金属元素的第一电离能从大到小的顺序为 , 的空间构型是;尿素晶体的熔点为132.7℃,比相同摩尔质量的乙酸熔点(16.7℃)高116℃,主要原因是 。
1.(2024·山东·高考真题)物质性质决定用途,下列两者对应关系错误的是
A.石灰乳除去废气中二氧化硫,体现了 的碱性
B.氯化铁溶液腐蚀铜电路板,体现了 的氧化性
C.制作豆腐时添加石膏,体现了 的难溶性
D.用氨水配制银氨溶液,体现了 的配位性
2.(2024·湖南·高考真题)下列有关化学概念或性质的判断错误的是
A. 分子是正四面体结构,则 没有同分异构体
B.环己烷与苯分子中 键的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由 与 组成的离子液体常温下呈液态,与其离子的体积较大有关
3.(2024·湖北·高考真题)基本概念和理论是化学思维的基石。下列叙述错误的是
A. 理论认为 模型与分子的空间结构相同
B.元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C.泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D. 杂化轨道由1个s轨道和3个p轨道混杂而成
4.(2024·浙江·高考真题) 中的 原子均通过 杂化轨道成键,与 溶液反应 元素均转化
成 。下列说法不正确的是
A. 分子结构可能是
B. 与水反应可生成一种强酸
C. 与 溶液反应会产生
D. 沸点低于相同结构的
5.(2024·河北·高考真题)从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符
的是
选项 实例 解释A 原子光谱是不连续的线状谱线 原子的能级是量子化的
孤电子对与成键电子对的斥力大于成键电
B 键角依次减小
子对之间的斥力
晶体中 与8个 配位,而 晶体中
C 比 的半径大
与6个 配位
D 逐个断开 中的 键,每步所需能量不同 各步中的 键所处化学环境不同
6.(2024·吉林·高考真题)下列化学用语或表述正确的是
A.中子数为1的氦核素: B. 的晶体类型:分子晶体
C. 的共价键类型: 键 D. 的空间结构:平面三角形
7.(2023·天津·高考真题)常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国卫生
2
组织(WTO)列为Al级高效安全消毒剂。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯
酸钠反应,其反应的化学方程式:CHOH+6NaClO +3H SO =CO ↑+6ClO ↑+3Na SO +5H O,则下列说法正
3 3 2 4 2 2 2 4 2
确的是
A.CO 是非极性分子 B.键角:ClO