文档内容
第 06 讲 氧化还原反应
第一部分:高考真题感悟
1.(2022·山东·高考真题)古医典富载化学知识,下述之物见其氧化性者为
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳( ):“色黄,以苦酒(醋)洗刷则白”
2.(2022·浙江·高考真题)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
3.(2022·浙江·高考真题)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、
C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
4.(2022·湖南·高考真题)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中
的 转化为 进入大气层,反应过程如图所示。下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
5.(2022·湖南·高考真题)为探究 的性质,进行了如下实验( 和 溶液浓度均为
)。
实验 操作与现象
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;将上述混合液分成两份,一份滴加
③
溶液,无蓝色沉淀生;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·北京西城·二模)将氧化还原反应拆解为氧化反应和还原反应的分析过程,蕴含的化学学科的思
想方法是
A.分与合相结合 B.量变与质变相结合
C.化学与社会和谐发展 D.物质变化是有条件的
2.(2022·江苏扬州·模拟预测)从烟道气中分离回收硫的基本反应: 。下列说
法正确的是
A.该反应属于置换反应
B. 、 和 均属于酸性氧化物
C. 在该反应中表现出氧化性
D. , 能将铝土矿中的 还原为
3.(2022·江苏淮安·模拟预测)2022年4月16日,神舟十三号载人飞船返回舱在东风着陆场顺利着陆。
飞船的燃料为偏二甲肼(C HN),发射时发生的反应为:C HN+2N O 3N+2CO +4H O,下列
2 8 2 2 8 2 2 4 2 2 2
说法正确的是
A.偏二甲肼在反应中作还原剂 B.燃烧时吸收大量的热
C.CO 的大量排放会导致酸雨 D.NO 属于酸性氧化物
2 2 4
4.(2022·北京·首都师范大学附属中学三模)下列物质在生活中的应用与氧化还原反应无关的是
A.FeSO 补血剂与维生素C配合使用效果更佳
4
B.用明矾处理污水
C.用84消毒液杀灭细菌
D.还原Fe粉用作食品脱氧剂5.(2022·江苏苏州·模拟预测)工业可通过Al O+N +3C 2AlN+3CO制得高温陶瓷材料AlN。下列说
2 3 2
法正确的是
A.传统陶瓷主要成分是硅酸盐 B.AlN是分子晶体
C.N 发生氧化反应 D.反应为复分解反应
2
6.(2022·北京市第一六一中学三模)下列说法不涉及氧化还原反应的是
A.灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐
B.自然界中硫的转化——含硫化物的矿石转化为硫酸盐
C.干千年,湿万年,不干不湿就半年——青铜器、铁器的保存
D.雷雨肥庄稼——自然固氮
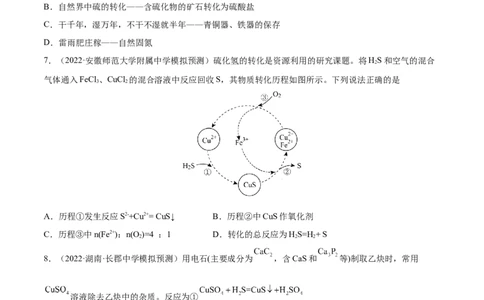
7.(2022·安徽师范大学附属中学模拟预测)硫化氢的转化是资源利用的研究课题。将HS和空气的混合
2
气体通入FeCl 、CuCl 的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的是
3 2
A.历程①发生反应S2-+Cu2+= CuS↓ B.历程②中CuS作氧化剂
C.历程③中n(Fe2+):n(O )=4 :1 D.转化的总反应为HS=H+ S
2 2 2
8.(2022·湖南·长郡中学模拟预测)用电石(主要成分为 ,含CaS和 等)制取乙炔时,常用
溶液除去乙炔中的杂质。反应为①
②
下列分析正确的是
A.可以依据反应①比较硫酸与氢硫酸的酸性强弱
B.反应② 既是氧化产物又是还原产物C.反应②中每 氧化
D.用酸性 溶液验证乙炔还原性时,也可以使用NaOH溶液除杂
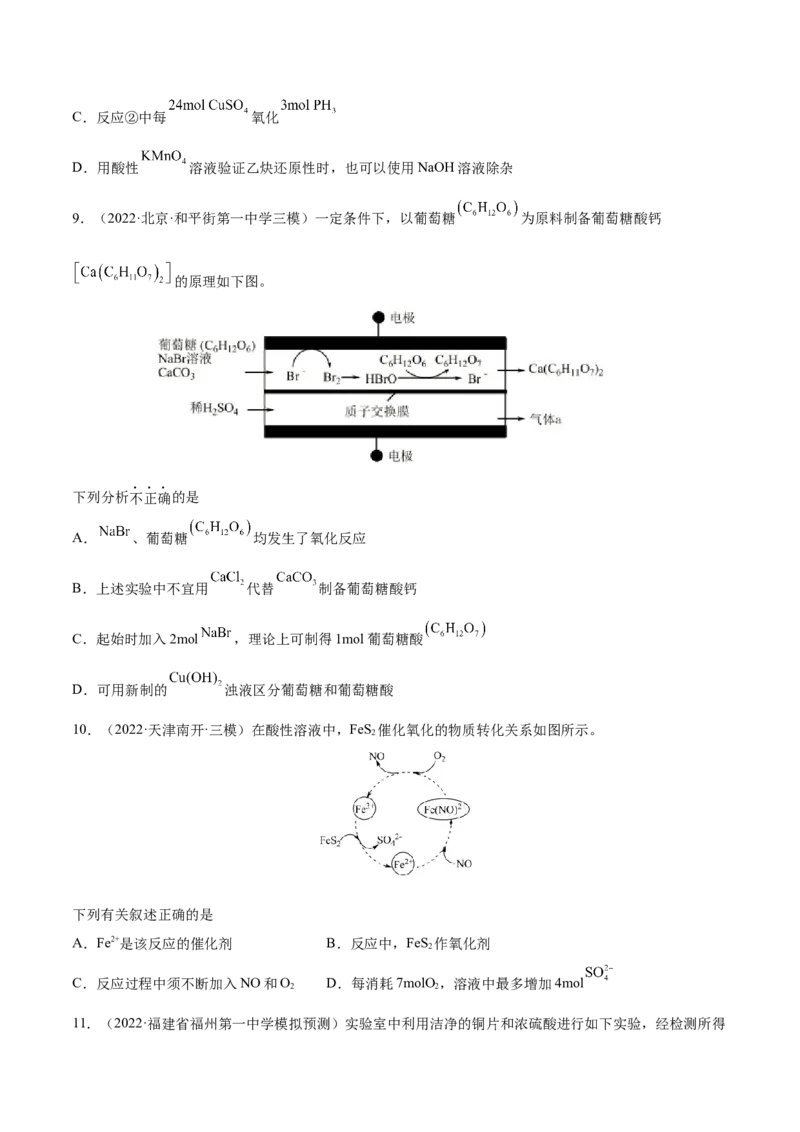
9.(2022·北京·和平街第一中学三模)一定条件下,以葡萄糖 为原料制备葡萄糖酸钙
的原理如下图。
下列分析不正确的是
A. 、葡萄糖 均发生了氧化反应
B.上述实验中不宜用 代替 制备葡萄糖酸钙
C.起始时加入2mol ,理论上可制得1mol葡萄糖酸
D.可用新制的 浊液区分葡萄糖和葡萄糖酸
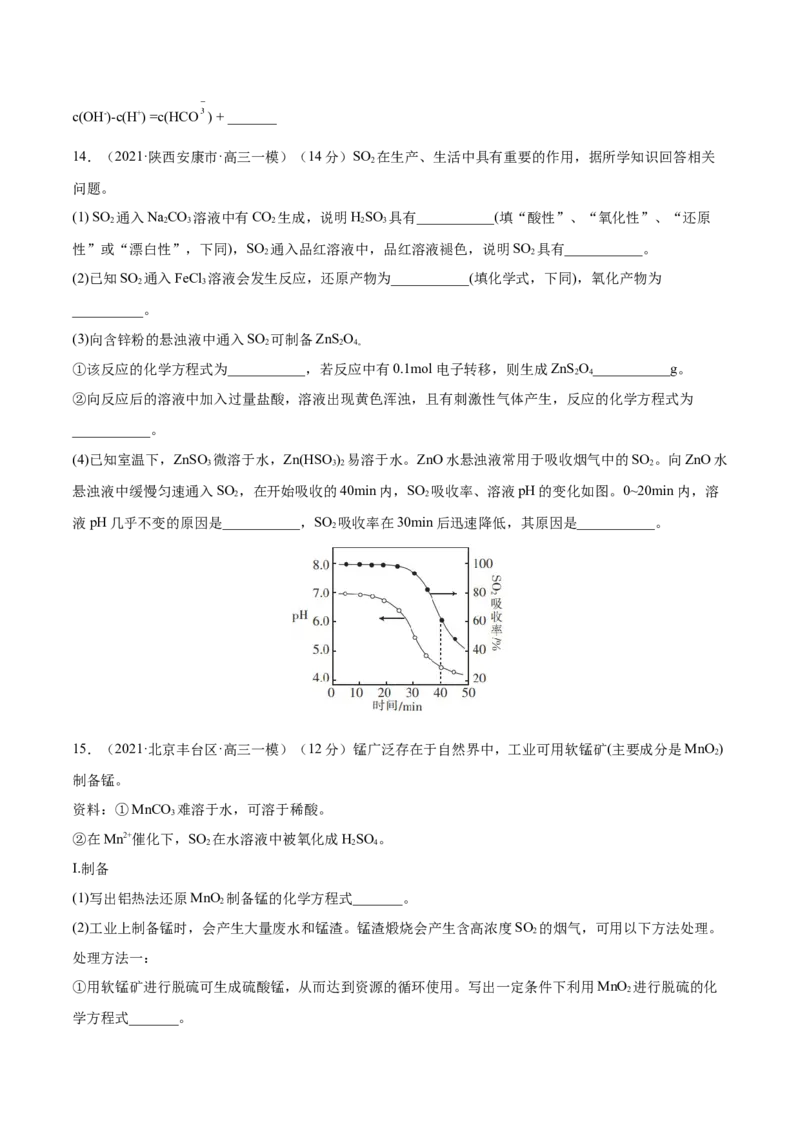
10.(2022·天津南开·三模)在酸性溶液中,FeS 催化氧化的物质转化关系如图所示。
2
下列有关叙述正确的是
A.Fe2+是该反应的催化剂 B.反应中,FeS 作氧化剂
2
C.反应过程中须不断加入NO和O D.每消耗7molO ,溶液中最多增加4mol
2 2
11.(2022·福建省福州第一中学模拟预测)实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中含有Cu S和白色物质X,下列说法正确的是
2
A.X溶液显无色
B.参加反应的浓硫酸中,体现氧化性的占25%
C.NO和Y均为还原产物
D.NO与Y的物质的量之和可能为2mol
12.(2022·山东济南·三模)玻璃仪器内璧残留的硫单质可用热NaOH溶液洗涤除去,发生如下反应:
①3S+ 6NaOH 2NaS+ Na SO + 3H O
2 2 3 2
②(x-1)S+Na S NaS (x=2~6)
2 2 x
③S+ Na SO NaSO
2 3 2 2 3
下列说法正确的是
A.反应①②③中,硫单质的作用相同
B.反应①中,每消耗1 mol硫单质转移4 mol电子
C.0.96g硫单质与amL2mol·L-1热NaOH溶液恰好完全反应,只生成NaS和NaSO ,则a= 60
2 2 3
D.1.28 g硫单质与10 mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS 和NaSO,则x=5
2 x 2 2 3
二、主观题(共3小题,共40分)
13.(2022·上海奉贤·一模)(14分)三氟化氮(NF )是一种无色、无味的气体,它是微电子工业的关键原
3
料之一,可由氨气和氟气反应得到:_______NH +_______F →_______NF +_______NHF。完成下列填空:
3 2 3 4
(1)配平上述反应方程式_______。
(2)F原子的结构示意图是_______,从原子结构角度比较F和N元素的非金属性强弱_______。
(3)写出NH F的电子式_______,溶液中NH 的检验方法是_______。
4
(4)与NH 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是_______,该产
物的水溶液呈_______性,用适当的化学用语解释该溶液酸碱性的原因:_______。其稀溶液中存在关系式:c(OH-)-c(H+) =c(HCO ) + _______
14.(2021·陕西安康市·高三一模)(14分)SO 在生产、生活中具有重要的作用,据所学知识回答相关
2
问题。
(1) SO 通入NaCO 溶液中有CO 生成,说明HSO 具有___________(填“酸性”、“氧化性”、“还原
2 2 3 2 2 3
性”或“漂白性”,下同),SO 通入品红溶液中,品红溶液褪色,说明SO 具有___________。
2 2
(2)已知SO 通入FeCl 溶液会发生反应,还原产物为___________(填化学式,下同),氧化产物为
2 3
__________。
(3)向含锌粉的悬浊液中通入SO 可制备ZnS O
2 2 4。
①该反应的化学方程式为___________,若反应中有0.1mol电子转移,则生成ZnS O___________g。
2 4
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
___________。
(4)已知室温下,ZnSO 微溶于水,Zn(HSO ) 易溶于水。ZnO水悬浊液常用于吸收烟气中的SO 。向ZnO水
3 3 2 2
悬浊液中缓慢匀速通入SO ,在开始吸收的40min内,SO 吸收率、溶液pH的变化如图。0~20min内,溶
2 2
液pH几乎不变的原因是___________,SO 吸收率在30min后迅速降低,其原因是___________。
2
15.(2021·北京丰台区·高三一模)(12分)锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )
2
制备锰。
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
I.制备
(1)写出铝热法还原MnO 制备锰的化学方程式_______。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,可用以下方法处理。
2
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO 进行脱硫的化
2
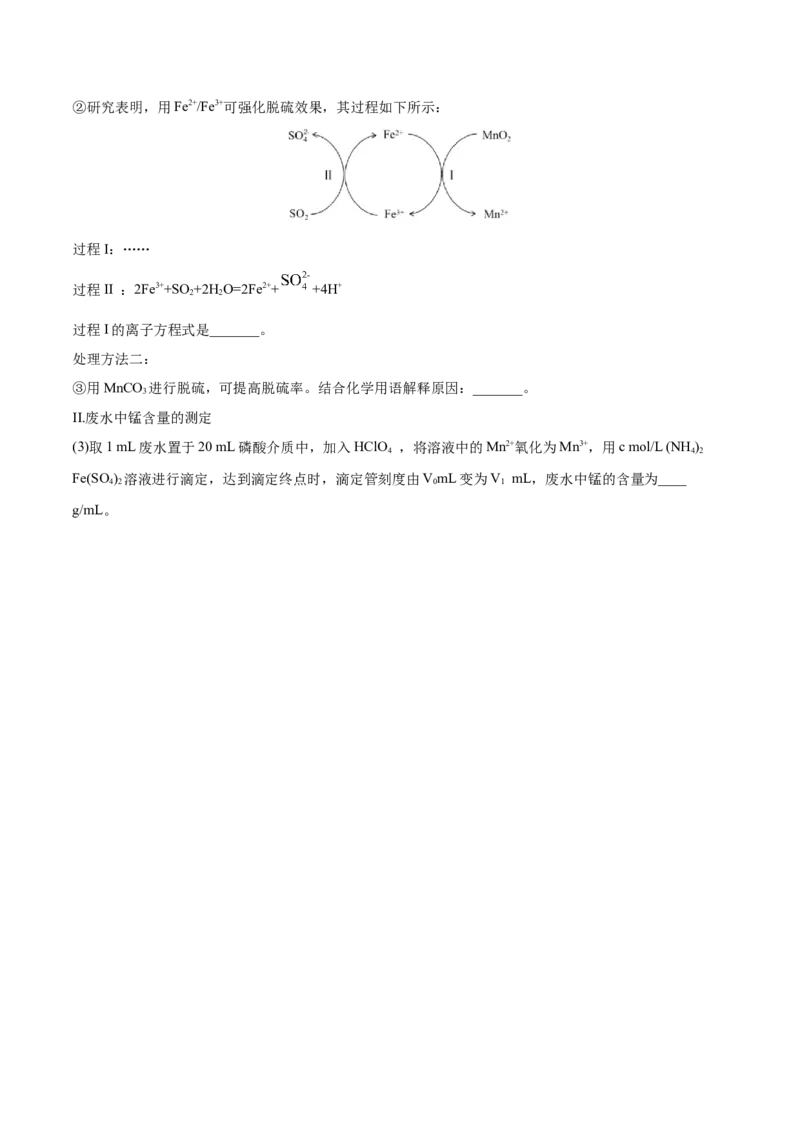
学方程式_______。②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:
过程I:……
过程II :2Fe3++SO+2H O=2Fe2++ +4H+
2 2
过程I的离子方程式是_______。
处理方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______。
3
II.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用c mol/L (NH)
4 4 2
Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由VmL变为V mL,废水中锰的含量为____
4 2 0 1
g/mL。