文档内容
第 08 讲 金属材料
1.化学与工业生产密切相关,下列说法正确的是
A.电冶金工业中,加冰晶石降低 熔融温度
B.炼钢工业中,将炽热的钢水注入留有水的模具
C.电子工业中,以 溶液作为覆铜板腐蚀液
D.硝酸工业中,通过氨的催化氧化实现人工固氮
2.下图为铝的生产原理示意图,下列相关说法不正确的是
A.冰晶石做助熔剂
B.氧化铝属于过渡晶体
C.金属铁、铜的冶炼方法与铝类似
D.铝在工业上是一种很好的还原剂
3.不能使 悬浊液变澄清的是
A.硫酸溶液 B.盐酸 C.氢氧化钠溶液 D.氨水
4.下列反应的离子方程式不正确的是
A.NaSO 溶液中滴入少量氯水:SO +Cl+H O=SO +2H++2Cl-
2 3 2 2
B.Mg(OH) 溶于NH Cl的浓溶液:Mg(OH) +2NH =Mg2++2NH•H O
2 4 2 3 2
C.Al(OH) 溶于NaOH溶液:Al(OH) +OH-=[Al(OH) ]-
3 3 4
D.足量Cu与稀硝酸反应:3Cu+8H++2NO =3Cu2++NO↑+4HO
2
5.对下列劳动项目的解释错误的是
选
劳动项目 解释
项
A 用SO 漂白纸浆 SO 具有还原性
2 2B 用铝制容器贮运浓硝酸 铝遇浓硝酸钝化
C 模具注入熔融钢水之前必须干燥 铁与HO在高温下会反应
2
D 用固体管道疏通剂(主要成分为NaOH和铝粉)疏通管道 与铝粉和NaOH溶液反应产生气体有关
6.常温下,下列各组离子在指定溶液中可能大量共存的是
A.pH=1的溶液中:K+、Na+、 、
B.c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、 、SCN-
C.与铝反应生成氢气的溶液中:Na+、NH +、 、Cl-
4
D.无色溶液中:Na+、Al3+、Cl-、
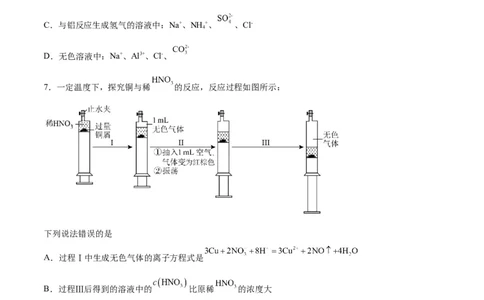
7.一定温度下,探究铜与稀 的反应,反应过程如图所示:
下列说法错误的是
A.过程Ⅰ中生成无色气体的离子方程式是
B.过程Ⅲ后得到的溶液中的 比原稀 的浓度大
C.过程Ⅱ中气体变为红棕色的反应为
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
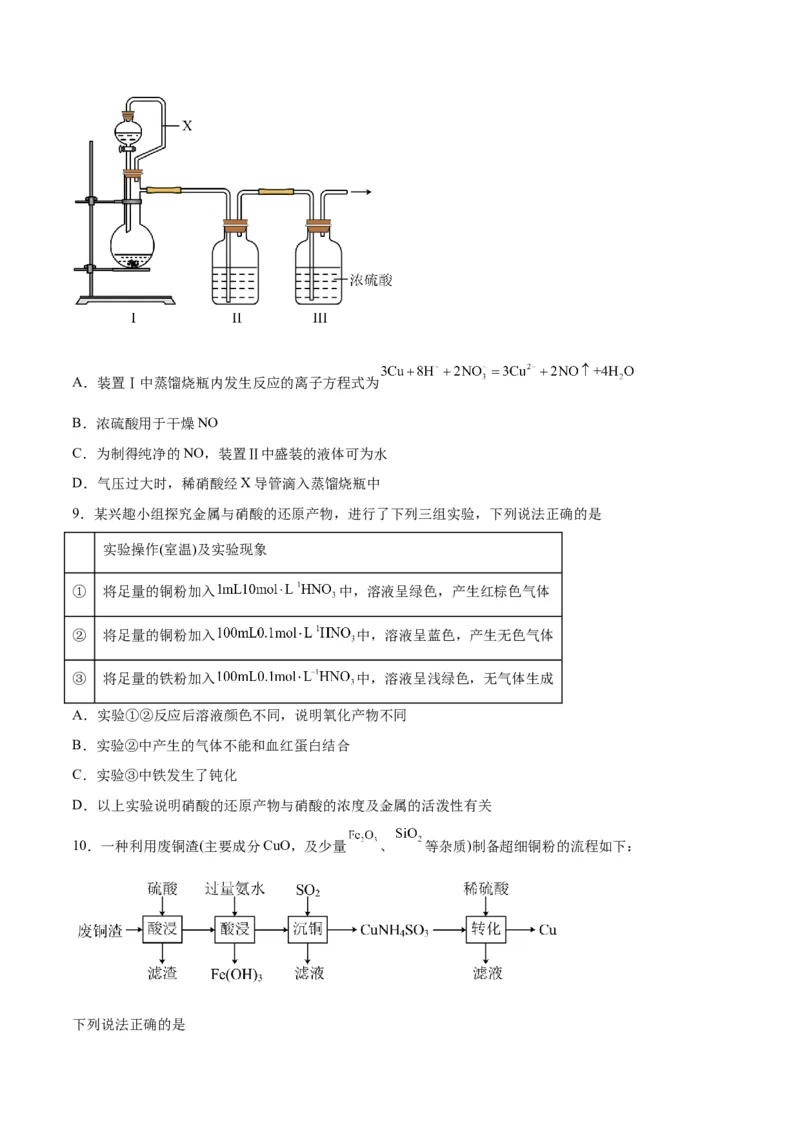
8.某兴趣小组同学用铜与稀硝酸反应制取干燥、纯净的NO气体(装置如图)。下列有关说法错误的是A.装置Ⅰ中蒸馏烧瓶内发生反应的离子方程式为
B.浓硫酸用于干燥NO
C.为制得纯净的NO,装置Ⅱ中盛装的液体可为水
D.气压过大时,稀硝酸经X导管滴入蒸馏烧瓶中
9.某兴趣小组探究金属与硝酸的还原产物,进行了下列三组实验,下列说法正确的是
实验操作(室温)及实验现象
① 将足量的铜粉加入 中,溶液呈绿色,产生红棕色气体
② 将足量的铜粉加入 中,溶液呈蓝色,产生无色气体
③ 将足量的铁粉加入 中,溶液呈浅绿色,无气体生成
A.实验①②反应后溶液颜色不同,说明氧化产物不同
B.实验②中产生的气体不能和血红蛋白结合
C.实验③中铁发生了钝化
D.以上实验说明硝酸的还原产物与硝酸的浓度及金属的活泼性有关
10.一种利用废铜渣(主要成分CuO,及少量 、 等杂质)制备超细铜粉的流程如下:
下列说法正确的是A.“酸浸”所得滤渣的主要成分为
B.若向“沉铁”后所得滤液中加入乙醇,析出的深蓝色晶体为
C.“沉铜”发生的反应为复分解反应
D.“转化”后所得滤液中含有的主要阳离子: 、 、
11.甲、乙两烧杯中分别盛有 浓度均为 的盐酸与 溶液,向两烧杯中分别加入等质量
的铝粉,反应结束后测得同温同压下生成气体的体积之比为 ,则加入铝粉的质量为
A. B. C. D.
12.某固体混合物可能含有Al、 、 、 、 、NaCl中的一种或几种,现对该混合
物做如图实验,所得现象和有关数据如图(气体体积已换算成标准状况下体积)。下列说法不正确的是
A.步骤①中发生了氧化还原反应
B.步骤②和步骤③中反应消耗的 的物质的量之比为3∶1
C.混合物中一定不存在 ,可能含有NaCl、AlCl
3
D.混合物中一定含有 ,且物质的量为0.2mol
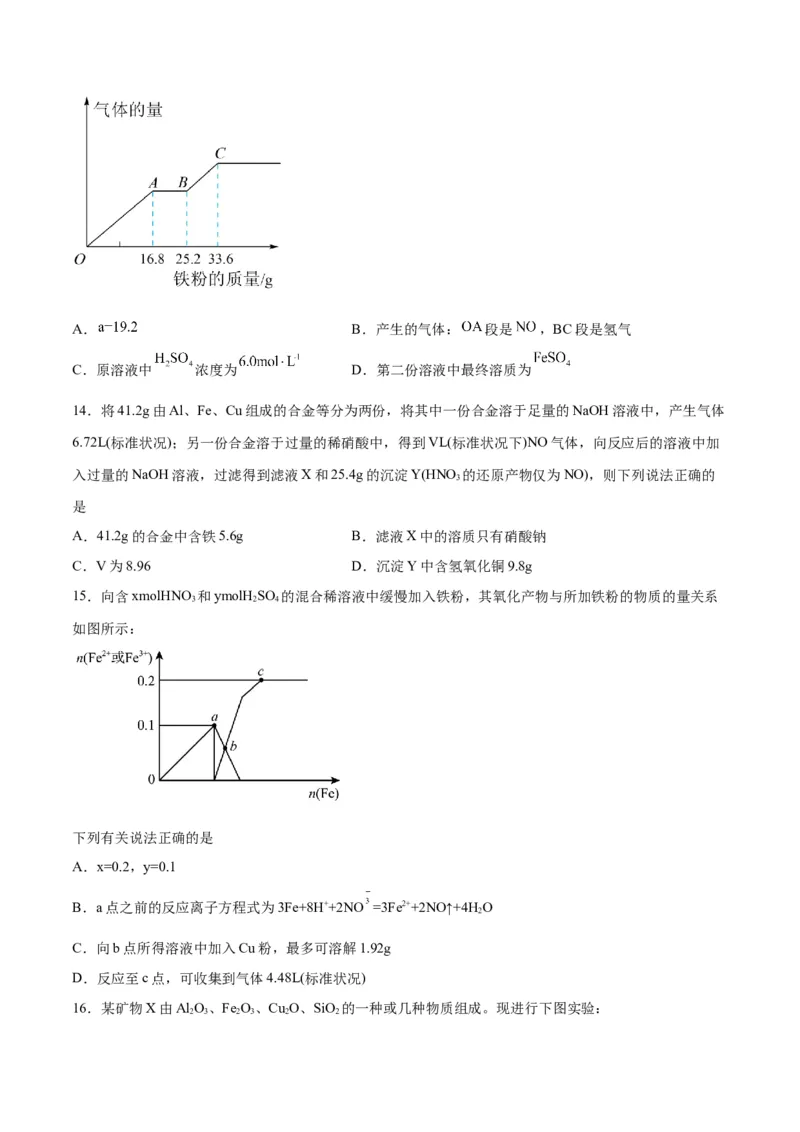
13.某稀硫酸和稀硝酸的混合溶液 ,平均分成两份。向第一份中逐渐加入铜粉,最多能溶解铜粉
;第二份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为 气
体)。下列分析或结果错误的是A. B.产生的气体: 段是 ,BC段是氢气
C.原溶液中 浓度为 D.第二份溶液中最终溶质为
14.将41.2g由Al、Fe、Cu组成的合金等分为两份,将其中一份合金溶于足量的NaOH溶液中,产生气体
6.72L(标准状况);另一份合金溶于过量的稀硝酸中,得到VL(标准状况下)NO气体,向反应后的溶液中加
入过量的NaOH溶液,过滤得到滤液X和25.4g的沉淀Y(HNO 的还原产物仅为NO),则下列说法正确的
3
是
A.41.2g的合金中含铁5.6g B.滤液X中的溶质只有硝酸钠
C.V为8.96 D.沉淀Y中含氢氧化铜9.8g
15.向含xmolHNO 和ymolH SO 的混合稀溶液中缓慢加入铁粉,其氧化产物与所加铁粉的物质的量关系
3 2 4
如图所示:
下列有关说法正确的是
A.x=0.2,y=0.1
B.a点之前的反应离子方程式为3Fe+8H++2NO =3Fe2++2NO↑+4HO
2
C.向b点所得溶液中加入Cu粉,最多可溶解1.92g
D.反应至c点,可收集到气体4.48L(标准状况)
16.某矿物X由Al O、Fe O、Cu O、SiO 的一种或几种物质组成。现进行下图实验:
2 3 2 3 2 2(已知:Cu O+2H+=Cu+Cu2++H O且每步反应都充分)下列说法正确的是
2 2
A.根据上述步骤可以判断矿物X中n(Cu O)/n(Fe O)>1
2 2 3
B.步骤1中减少的固体一定是混合物
C.根据步骤2可以得出蓝色溶液中n(Cu2+)=0.02mol
D.根据步骤1、2可以判断出X中氧化铁的质量分数为50%
17.CuCl用于石油工业脱硫与脱色,还可用作CO吸附剂和脱氧剂。CuCl是一种不溶于水和乙醇的白色粉
末,在潮湿空气中可被迅速氧化。
Ⅰ.利用以下装置可制备CuCl
已知: 为无色溶液,加水稀释即析出CuCl白色固体,回答下列问题:
(1)制取 :A中发生的反应氧化剂和还原剂的物质的量之比为_______,为吸收 尾气,C中可选用试
剂_______(填标号)。
A. 溶液 B.饱和食盐水 C. 溶液 D.浓
(2)制备CuCl:打开分液漏斗旋塞与搅拌器,B中依次发生反应的离子方程式为:
①
②_______
③
观察到_______时停止反应。将B中溶液倾入盛有_______的烧杯中,立即得到白色CuCl沉淀。过滤得
CuCl粗品。(3)洗涤CuCl:洗涤时最好用_______(填序号)洗涤滤饼3~4次,其目的是_______。
a. b.稀硫酸 c.95%的乙醇
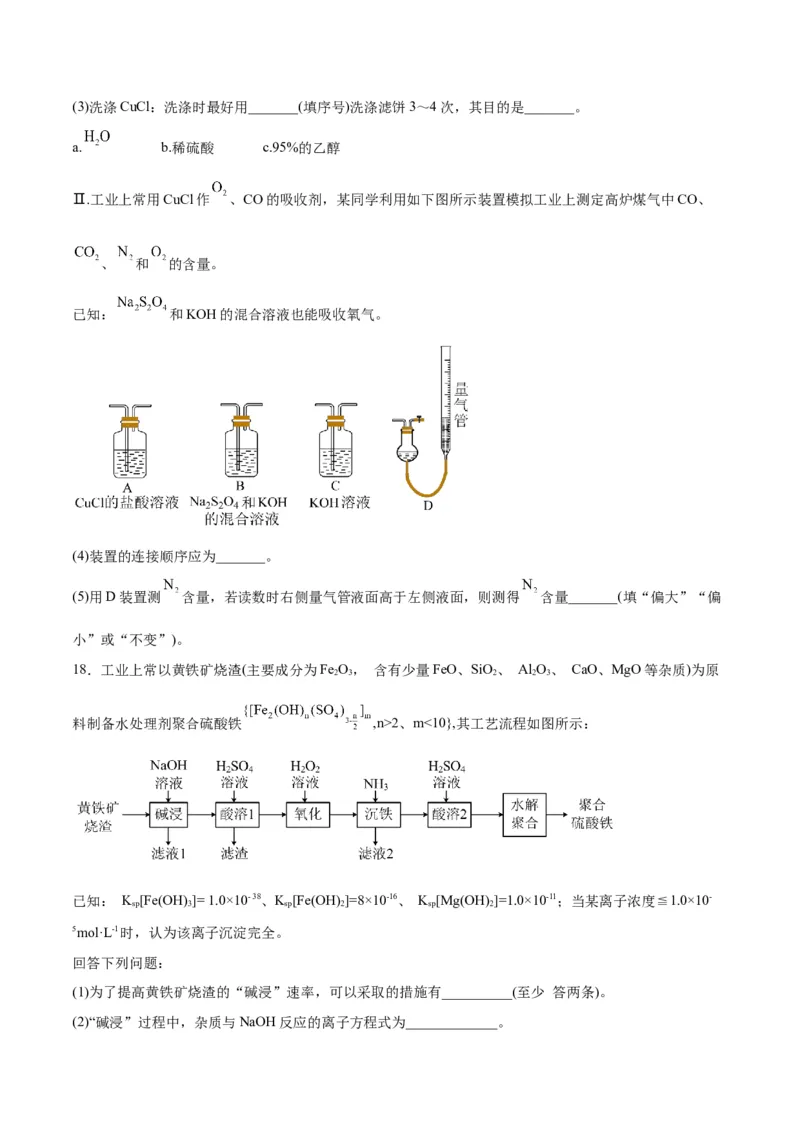
Ⅱ.工业上常用CuCl作 、CO的吸收剂,某同学利用如下图所示装置模拟工业上测定高炉煤气中CO、
、 和 的含量。
已知: 和KOH的混合溶液也能吸收氧气。
(4)装置的连接顺序应为_______。
(5)用D装置测 含量,若读数时右侧量气管液面高于左侧液面,则测得 含量_______(填“偏大”“偏
小”或“不变”)。
18.工业上常以黄铁矿烧渣(主要成分为Fe O, 含有少量FeO、SiO、 Al O、 CaO、MgO等杂质)为原
2 3 2 2 3
料制备水处理剂聚合硫酸铁 ,n>2、m<10},其工艺流程如图所示:
已知: K [Fe(OH) ]= 1.0×10- 38、K [Fe(OH) ]=8×10-16、 K [Mg(OH) ]=1.0×10-11;当某离子浓度≦1.0×10-
sp 3 sp 2 sp 2
5mol·L-1时,认为该离子沉淀完全。
回答下列问题:
(1)为了提高黄铁矿烧渣的“碱浸”速率,可以采取的措施有__________(至少 答两条)。
(2)“碱浸”过程中,杂质与NaOH反应的离子方程式为_____________。(3)“酸溶1”所得滤渣的主要成分为________(填化学式),在实验室中分离出滤渣的操作名称为
___________。
(4)“氧化”工序中加入HO 溶液的目的是________________________。
2 2
(5)若“氧化”后的溶液中Mg2+浓度为0.1 mol·L-1, 则常温下“沉铁”时需满足的pH范围是
_______________。
19.FeCl (易升华)是常见的化学试剂。某学习小组开展了与FeCl 相关的系列实验,回答下列问题:
3 3
I.铁粉制备FeCl (实验装置如图所示)
3
(1)仪器a盛装的物质是为_______(填试剂的名称);装置中F的作用:_______。
(2)硬质玻璃管直接接入收集器的优点是_______。
II.探究FeCl 溶液与Cu的反应
3
(3)配制FeCl 溶液时加入少量盐酸的原因是_______。
3
(4)向FeCl 溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液的红色褪去。用离子
3
方程式解释红色褪去的原因:_______。
(5)已知(4)中除了红色褪去,还产生了白色沉淀。小组成员查阅得知CuCl和CuSCN均为白色沉淀。为探究
白色沉淀的主要成分,小组成员完成了以下实验:向4mL0.1mol/LFeCl 溶液中加入过量Cu粉,静置,取
3
上层清液于试管中,滴加3滴KSCN溶液,有白色沉淀生成。由此现象可知此白色沉淀为_______(填化学
式)。
小组成员进一步查阅资料发现,Cu2+与SCN-可发生如下两种反应。
反应i:Cu2++4SCN-=[Cu(SCN) ]2-(淡黄色)
4
反应ii:2Cu2++4SCN-=2CuSCN↓+(SCN)
2
设计实验如下:
操作 现象
溶液很快由蓝色变为绿色,未观察到白色沉淀;
在盛有2mL0.1mol·L-1CuSO 溶液的试管中滴
4
2h后溶液为绿色,未观察到白色沉淀;24h后,溶液绿色
加KSCN溶液
变浅,试管底部有白色沉淀
由此现象可知,反应速率较快的为_______(填“反应i”或“反应ii”)。小组成员得出结论,反应ii不是CuSCN产生的主要原因。
(6)根据上述分析可知,Cu2+、Fe2+和SCN-可直接发生反应,生成CuSCN和Fe3+,写出反应的离子方程式:
_______。
20.某实验小组在研究硝酸与铜的反应时,发现稀硝酸和铜反应后的混合液为蓝色,而浓硝酸和铜反应后
的混合液为绿色,为此对产生绿色的原因开展探究。按要求完成下列问题:
[猜想假设]
(1)假设1:___________
假设2:硝酸铜溶液中溶解了
[实验操作及现象分析]
实验一:向蒸馏水中不断加入硝酸铜晶体,最终配成饱和溶液。配制过程中溶液颜色始终是蓝色,未见绿
色出现。
甲同学根据实验一的现象证明了假设1不成立,请补全假设。
实验二:
(2)甲同学在实验一的基础上继续开展了实验二,并初步验证了假设2成立,他的实验操作及现象是
___________。
乙同学认为假设2不严谨,用以下实验对假设2进行了深入探究:
实验三:
操作及试剂 现象
向浓硝酸和铜反应后的混合液中通入 大量红棕色气体放出,短时间内溶液仍保持绿色。长时间后变成
蓝色
(3)结合实验三,乙同学认为假设2不严谨的证据是___________
(4)乙同学查阅资料发现:
①铜与浓硝酸反应后溶液呈现绿色是由于HNO(或 )与铜离子作用的结果。
2
②金属和浓HNO 的反应一旦发生后速率不断加快。原因是过程中有HNO 生成。如 和浓HNO 反应,
3 2 3
开始生成的NO 溶于水形成HNO,它再和 反应,速率就大大加快。
2 2
请依据资料完成以下离子反应方程式。
i. ;___________
ii. ;___________iii.
实验四:乙同学通过以下实验证实了反应过程中HNO 的生成。
2
实验 操作 现象
1 向试管a中加入lmL浓硝酸,再插入铜丝 快速产生红棕色气体,溶液变为绿色
2 向试管b中加入1mL浓硝酸,3滴蒸馏水,再插入铜丝 快速产生红棕色气体溶液变为绿色
3 向试管c中加入1mL浓硝酸,3滴 ,再插入铜丝 反应较慢,溶液变为蓝色
(5)结合化学用语,解释实验3产生该现象的原因是___________。