文档内容
第 08 讲 金属材料
1.我国科技事业成果显著,下列成果所涉及的材料不属于金属材料的是
A.“C919”飞机的主体材料——铝合金
B.航天员宇航服的材料——聚酯纤维
C.我国第一艘航空母舰的主体材料——合金钢
D.“奋斗者”号深潜器载人舱的外壳——钛合金
【答案】B
【解析】“C919”飞机的主体材料——铝合金,铝合金为金属铝、镁形成的合金,属于金属材料,A
与题意不符;航天员宇航服的材料——聚酯纤维为由有机二元酸和二元醇缩聚而成的聚酯经纺丝所得的合
成纤维,属于有机高分子材料,B符合题意;我国第一艘航空母舰的主体材料——合金钢,为铁、碳合金,
属于金属材料,C与题意不符;“奋斗者”号深潜器载人舱的外壳——钛合金,为钛与其他金属制成的合
金金属,属于金属材料,D与题意不符;答案为B。
2.下列关于金属镁、铝的说法中正确的是( )
A.铝在地壳中的储量非常丰富,在古代常用来制造兵器
B.大量镁条燃烧引起的火灾不能用干冰灭火器灭火
C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液
D.依据铝热反应原理,能发生反应2Al+3MgO=====3Mg+Al O
2 3
【答案】B
【解析】虽然铝在地壳中的储量非常丰富,但都是以化合态的形式存在,古代没有冶炼金属铝的技术,
A错误;Mg不能溶于NaOH溶液,C错误;Mg的金属性比Al强,故Al与MgO不能发生铝热反应,D错
误。
3.下列有关物质用途的说法中,不正确的是
A.三氧化二铁常用作红色油漆和涂料
B.强化木地板表面的氧化铝具有耐磨与阻燃的作用
C.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是晶体硅
D.过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源
【答案】C
【解析】三氧化二铁是红棕色粉末,常用作红色油漆和涂料,故A正确;氧化铝是熔沸点高、硬度大的不易燃烧的金属氧化物,则强化木地板表面的氧化铝具有耐磨与阻燃的作用,故B正确;光缆的主要成
分是二氧化硅,不是晶体硅,故C错误;过氧化钠能与人呼吸出的二氧化碳和水蒸气反应生成氧气,可用
于呼吸面具或潜水艇中作为氧气的来源,故D正确;故选C。
4.下列关于铝单质的叙述中正确的是( )
A.不能用铝制的器皿来盛放酸梅汤或碱水是因为铝会和酸或碱反应
B.铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质很稳定
C.铝和NaOH溶液反应:Al+2OH-===AlO+2H↑
2
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下来,是
因为金属铝的熔点较低
【答案】A
【解析】A项,无论是铝还是其氧化物都能与酸或碱反应,正确;B项,铝制品在空气中有很强的抗
腐蚀性是因为铝表面形成了致密的氧化膜,错误;C项,电荷、原子均不守恒,正确的离子方程式为2Al
+2OH-+2HO===2AlO+3H↑,错误;D项,打磨后的铝箔在酒精灯上灼烧表面生成Al O ,高熔点的
2 2 2 3
Al O 兜住了熔融的液态铝,不会滴落,错误。
2 3
5.将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
A.稀硝酸 B.稀盐酸
C.硝酸铜溶液 D.氢氧化钠溶液
【答案】C
【解析】铝钝化后表面形成致密的Al O 层,Al O 与Cu(NO ) 溶液不反应。
2 3 2 3 3 2
6.已知:镁的密度为1.738 g·cm-3,铝的密度为2.70 g·cm-3。镁、铝分别与足量的1.0 mol·L-1盐酸发
生反应,下列说法中不正确的是( )
A.相同质量时,镁与盐酸反应产生的氢气少
B.相同质量时,镁与盐酸反应的速率快
C.相同体积时,铝与盐酸反应产生的氢气少
D.相同体积时,铝与盐酸反应产生氢气的体积大(相同条件下)
【答案】C
【解析】相同质量时,设Mg、Al的质量均为1 g,依据反应:Mg+2HCl===MgCl +H↑、2Al+
2 2
6HCl===2AlCl +3H↑可知,Mg、Al产生的氢气分别为 mol、 mol,显然Mg与盐酸反应产生的氢气少,
3 2
A项正确;由于Mg比铝更活泼,与等浓度盐酸反应时,Mg的反应速率更快,B项正确;相同体积时,设
Mg、Al的体积均为1 cm3,则Mg、Al的质量分别为1.738 g、2.70 g,结合上述分析结论“相同质量时,
Al产生的氢气多”,则相同体积时,铝与盐酸反应产生的氢气多,在相同条件下生成气体的体积大,C项错误,D项正确。
7.下列实验探究Cu及其化合物的性质,操作正确且能达到目的的是( )
A.将铜粉和硫粉混合均匀并加热以制取CuS
B.向Cu与过量浓硫酸反应后的试管中加水以观察CuSO 溶液的颜色
4
C.向CuSO 溶液中加入适量的NaOH,过滤、洗涤并收集沉淀充分灼烧以制取CuO
4
D.在淀粉溶液中加入适量稀硫酸微热水解,再加入少量新制Cu(OH) 悬浊液并加热,产生砖红色沉淀
2
【答案】C
【解析】硫的氧化性较弱,只能将铜氧化为+1价生成CuS,A项错误;稀释铜与过量的浓硫酸反应后的
2
溶液,应将反应后的试管中的物质缓慢加入水中,并不断搅拌,B项错误;CuSO 与NaOH溶液反应生成
4
Cu(OH) 沉淀,过滤、洗涤、灼烧后可得CuO,C项正确;淀粉水解后应先加NaOH溶液至溶液呈碱性,然后加
2
入新制Cu(OH) 悬浊液并加热,才会产生砖红色沉淀,D项错误。
2
8.下列除去杂质的方法不正确的是( )
A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.用过量氨水除去Fe3+溶液中的少量Al3+
C.Al(OH) 中混有少量Mg(OH) :加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO 后过
3 2 2
滤
D.MgO中混有少量Al O:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO
2 3
【答案】B
【解析】Al(OH) 不溶于氨水,故向含少量Al3+的Fe3+溶液中加入过量氨水时,Fe3+、Al3+均转化为氢
3
氧化物沉淀,达不到除杂的目的。
9.下列说法正确的是( )
A.向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成
2 3
B.制备Al(OH) 悬浊液:向1 mol·L-1 AlCl 溶液中加过量的6 mol·L-1 NaOH溶液
3 3
C.AlCl 溶液中加入过量稀氨水:Al3++4NH ·H O===AlO+4NH+2HO
3 3 2 2
D.将AlCl 加入Ba(HCO ) 溶液中同时有气体和沉淀产生
3 3 2
【答案】D
【解析】AlO+HCO+HO===Al(OH) ↓+CO,只有沉淀生成,A错误;Al(OH) 是两性氢氧化物,可
2 3 3
以和过量氢氧化钠溶液反应生成偏铝酸钠,故不能制备氢氧化铝悬浊液,B错误;Al(OH) 不溶于过量稀氨
3
水,C错误;Al3+与HCO发生相互促进的水解反应,生成Al(OH) 沉淀和CO 气体,故D正确。
3 2
10.如图是工业利用菱镁矿MgCO (含杂质Al O、FeCO)制取镁的工艺流程。
3 2 3 3回答有关问题:
(1)菱镁矿送入酸浸池前需要粉碎,目的是________________________________。
(2)氧化池中通入氯气的目的是氧化________(填化学式),工业上不选用硝酸作氧化剂的原因是
________________________和________________________。
(3)沉淀混合物为________和________(填化学式)。
(4)利用熔融氯化镁制取金属镁,选用的方法是________(填字母)。
A.电解法 B.氢气还原法
C.碳还原法 D.分解法
【解析】(1)粉碎菱镁矿,可增大固相反应物的接触面积,提高酸浸速率。(2)通入Cl 是为了将Fe2+(或
2
FeCl )氧化为Fe3+(或FeCl ),工业上不用HNO 是因为会产生污染性气体NO,也会引入杂质离子NO。(3)
2 3 3 x
氧化池中存在Al3+、Fe3+、H+,所以加入MgO后MgO与H+反应使溶液碱性增强,Al3+和Fe3+转化为
Al(OH) 和Fe(OH) ,故沉淀池中的沉淀为 Al(OH) 和Fe(OH) 。(4)金属镁比较活泼,一般采用电解熔融
3 3 3 3
MgCl 的方法进行冶炼。
2
【答案】(1)提高酸浸速率
(2)FeCl 会产生污染性气体NO 会引入杂质离子NO
2 x
(3)Al(OH) Fe(OH)
3 3
(4)A
1.实验室通过称量MgSO ·xHO样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的
4 2
是( )
A.实验前试样未经干燥
B.试样中含有少量碳酸氢铵
C.试样中含有少量氯化钠
D.加热过程中有试样迸溅出来
【答案】C
【解析】通过称量MgSO ·xHO样品受热脱水前后的质量来测定x值,实验前试样未经干燥,前后质
4 2量差增大,测定值偏高,A项错误;试样中含有少量碳酸氢铵,碳酸氢铵受热分解生成 NH 、CO 和
3 2
HO,导致前后质量差增大,测定值偏高,B项错误;试样中含有少量氯化钠,导致前后质量差减小,测
2
定值偏低,C项正确;加热过程中有试样迸溅出来,前后质量差增大,测定值偏高,D项错误。
2.下列离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:Fe3++ Cu ═ Fe2+ + Cu2+
B.用氢氧化铝治疗胃酸过多:Al(OH) +3H+ = Al3++3H O
3 2
C.氢氧化钠溶液吸收氯气制漂白液:Cl + OH﹣═ Cl﹣+ HClO
2
D.用氢氧化钠溶液去除铝条表面的氧化膜:Al O+2OH- ═ 2Al3++H O
2 3 2
【答案】B
【解析】电荷不守恒,正确的离子方程式为2Fe3++ Cu ═ 2Fe2+ + Cu2+,A错误;用氢氧化铝治疗胃酸过
多时氢氧化铝与HCl反应生成氯化铝和水,反应的离子方程式为Al(OH) +3H+ = Al3++3H O,B正确;氢
3 2
氧化钠溶液吸收氯气制漂白液时,氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水,反应的离子方程式为
Cl + 2OH﹣═ Cl﹣+ ClO-+H O,C错误;氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为
2 2
Al O+2OH-═2AlO -+H O,D错误;答案选B。
2 3 2 2
3.两份相同质量且均过量的铝,分别放入等体积、等浓度的盐酸和氢氧化钠溶液中,放出的氢气在同
温同压下的体积之比为( )
A.1∶3 B.1∶1
C.2∶3 D.3∶2
【答案】A
【解析】等体积、等浓度的盐酸和氢氧化钠溶液中,n(HCl)=n(NaOH),两份铝的质量相等,且均过
量,HCl、NaOH均反应完全。假设n(HCl)=n(NaOH)=1 mol,发生反应:2Al+6HCl===2AlCl +3H↑、
3 2
2Al+2NaOH+2HO===2NaAlO+3H↑,则Al与盐酸、NaOH溶液反应生成氢气的物质的量分别为 mol、
2 2 2
mol,在同温同压下的体积之比为 mol∶ mol=1∶3。
4.如图所示的反应均是在高温或引燃条件下进行,选项中的物质表示A和B,不合理的是( )
A.CO、Mg B.MgO、Al
2
C.Fe O、Al D.CuO、H
2 3 2
【答案】B【解析】Mg高温下与CO 反应生成C和MgO,C、Mg与足量氧气引燃分别能生成CO 与MgO,故A
2 2
项正确;Al的还原性比Mg弱,故不能置换出Mg,故B项错误;Al与Fe O 高温下反应生成Al O 与Fe,
2 3 2 3
Fe与氧气在高温加热条件下生成Fe O ,故C项正确;H 还原CuO生成HO与Cu,H 、Cu与氧气引燃反
2 3 2 2 2
应分别生成HO和CuO,故D项正确。
2
5.金属材料的发展极大地促进了人类社会的文明程度。如图是两种金属及其化合物的转化关系。下
列说法不正确的是
A.根据反应③可知氧化性:Fe3+>H O
2 2
B.向X溶液中滴入K[Fe(CN) ]溶液,生成蓝色沉淀
3 6
C.反应③中稀硫酸仅表现酸性
D.反应①的离子方程式为Cu+HO+2H+=Cu2++2HO
2 2 2
【答案】A
【解析】由题干中两种金属及其化合物的转化关系图分析可知,物质M为Cu,E为Fe,X为FeSO ,
4
Y为Fe (SO ),W为Fe(SCN) ,Z为Fe(OH) ,据此分析解题。由分析可知,反应③的离子方程式为:2Fe2+
2 4 3 3 3
+2H O+2H+=2Fe3++2H O,可知氧化性:HO > Fe3+,A错误;由分析可知,X溶液中含有Fe2+,故向X
2 2 2 2 2
溶液中滴入K[Fe(CN) ]溶液,生成蓝色沉淀,B正确;根据反应③的离子方程式为:2Fe2+
3 6
+2H O+2H+=2Fe3++2H O可知反应③中稀硫酸仅表现酸性,C正确;由分析可知,反应①的离子方程式为
2 2 2
Cu+HO+2H+=Cu2++2HO,D正确;故答案为A。
2 2 2
6.铝是一种很重要的金属,可以发生一系列反应制备物质,如图所示:
下列说法错误的是( )
A.反应①又称铝热反应,可用于野外焊接铁轨
B.反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等
C.常用反应⑥制备Al(OH) ,方法是向Al (SO ) 溶液中滴加足量的NaOH溶液
3 2 4 3
D.工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度【答案】C
【解析】铝热反应指Al与某些金属氧化物间的置换反应,反应①为铝热反应,因反应剧烈放热,生成
熔融的铁水,可用于野外焊接铁轨,选项A正确;Al既能与酸反应放出氢气又能与碱反应放出氢气,根据
元素化合价的变化,产生等量的氢气时转移的电子数相等,选项B正确;Al(OH) 具有两性,因此制备时
3
不能使用强酸、强碱,用Al (SO ) 溶液制备Al(OH) 沉淀应选用氨水,选项C错误;Al O 熔点高,电解时
2 4 3 3 2 3
要耗费更多的能源,加入冰晶石与氧化铝形成共熔物,可降低氧化铝的熔融温度,选项D正确。
7.通过观察化学实验现象,分析归纳出正确的结论,是学习化学科学最基本的技能之一。下列由实验
现象得出正确结论的是( )
选项 实验现象 结论
把相同大小的一块铝和镁分别投入相同浓度的
A NaOH溶液中:铝溶解有气泡放出,而镁没有任 由此得出:铝的金属性比镁强
何变化
取一块铝箔,用酒精灯点燃:铝箔只熔化成液体
B 由此得出:铝不易燃烧
而没有脱落
向氯化铵溶液中投入一铝片:铝片上产生大量气
C 由此得出:该气体是氨气
泡
向氯化铝溶液中逐滴滴加NaOH溶液至过量:先
由此得出:氢氧化铝能溶于强
D 产生白色沉淀,后沉淀逐渐溶解,最后沉淀完全
碱溶液
消失
【答案】D
【解析】A项,比较金属性的强弱是利用金属单质与水或酸反应产生H 的快慢程度,错误;B项,由
2
于生成了熔点很高的氧化铝,起到隔绝空气的作用,错误;C项,产生的气体应为H 和NH 的混合气体,
2 3
错误。
8.铝热反应常用于冶炼高熔点金属,某小组探究Al粉与Fe O 发生反应所得黑色固体的成分,实验过
3 4
程及现象如下:
下列说法不正确的是( )
A.反应①产生的气体是H
2
B.反应②为Al O+2OH-===2AlO+HO
2 3 2
C.反应③的白色沉淀是Al(OH)
3
D.黑色固体中不含Al和Fe O
3 4
【答案】D
【解析】探究Al粉与Fe O 发生反应所得黑色固体的成分,由实验可知,黑色固体与稀硫酸反应生成
3 4气体,且溶液b加KSCN溶液不变色,可知溶液b不含铁离子;黑色固体与NaOH溶液反应无气体,则一
定不含Al,溶液a与二氧化碳反应生成白色沉淀为氢氧化铝,则黑色固体中一定含氧化铝。由上述分析可
知,黑色固体一定含氧化铝、Fe,一定不含Al,可能含Fe O 。金属与稀硫酸反应生成H ,故A正确;固
3 4 2
体含氧化铝,则反应②为Al O +2OH-===2AlO+HO,故B正确;反应③中AlO与二氧化碳反应,可知
2 3 2
白色沉淀是Al(OH) ,故C正确;黑色固体中不含Al,可能含Fe O,故D错误。
3 3 4
9.某兴趣小组在实验室通过镁粉和空气中的氮气制备氮化镁(可与水发生反应),其装置如图所示。已
知:维生素C具有较强的还原性。下列说法错误的是( )
A.装置①③中盛放的分别是NaOH溶液和浓硫酸
B.装置②的作用为吸收空气中的O
2
C.实验开始时应先通空气再点燃酒精灯
D.装置⑤中碱石灰可以替换为NaCl
【答案】D
【解析】镁可以与空气中的氧气、二氧化碳发生反应,产物氮化镁可以与水发生反应,故应先除去空
气中的二氧化碳、氧气再干燥气体,装置①中盛放NaOH溶液,装置③中装有浓硫酸,故A正确;维生素
C具有还原性,则先除去氧气,故B正确;实验前先通空气,排尽装置中的氧气、二氧化碳等气体,再点
燃酒精灯,使镁与氮气反应,故C正确;装置⑤的作用是防止外界的水蒸气进入装置④中与产物反应,影
响产物的纯度,不能用NaCl替换,故D错误。
10.(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H 的体积之比是________。
2
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生H 的体积之比是
2
________。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者产生的H 相等,
2
则HCl和NaOH的物质的量浓度之比是________。
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,
反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉的质量为________(填字母)。
A.5.4 g B.3.6 g
C.2.7 g D.1.8 g
【解析】(1)根据化学方程式:2Al+6HCl===2AlCl +3H↑、2Al+2NaOH+2HO===2NaAlO +3H↑,
3 2 2 2 2得Al与H 的关系式均为2Al~3H,故只要参加反应的Al的量相等,所得H 的量必相等。
2 2 2
(2)因为在反应中Al过量,产生的H 由HCl和NaOH的量决定。根据化学反应中的关系式:6HCl~
2
3H、2NaOH~3H,故当HCl、NaOH物质的量相等时,二者产生H 的体积比为1∶3。
2 2 2
(3)因为铝足量且产生H 的量相等,根据关系式知n(HCl)∶n(NaOH)=3∶1,又因为两溶液体积相等,
2
故物质的量浓度c(HCl)∶c(NaOH)=n(HCl)∶n(NaOH)=3∶1。
(4)其反应原理分别为2Al+6HCl===2AlCl +3H↑,2Al+2NaOH+2HO===2NaAlO+3H↑。可见当参
3 2 2 2 2
加反应的HCl和NaOH的物质的量一样多时,产生H 的体积比是1∶3,而题设条件体积比为1∶2,说明
2
此题中投入的铝粉对盐酸来说是过量的,而对于NaOH来说是不足的。
2Al+6HCl === 2AlCl + 3H↑
3 2
6 mol 3 mol
3 mol·L-1×0.1 L 0.15 mol
则Al与NaOH反应生成的H 为0.15 mol×2=0.3 mol。
2
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2×27 g 3 mol
5.4 g 0.3 mol
即投入的铝粉为5.4 g。
【答案】(1)1∶1 (2)1∶3 (3)3∶1 (4)A
1.(2021·湖南卷)一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为MgO+C+Cl=====MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
【答案】D
【解析】苦卤水中含有大量镁离子,加入生石灰,生石灰与水反应生成氢氧化钙,氢氧化钙再与镁离
子反应生成氢氧化镁,生石灰来源丰富、价格便宜,常用来做沉镁的沉淀剂,A说法正确;镁为活泼金属,工业上常用电解熔融氯化镁的方法来制备金属镁,B说法正确;根据题给流程图可知,“煅烧”氢氧化镁
得到氧化镁,“氯化”过程中,加入碳和氯气与氧化镁反应,生成无水氯化镁和一种气体,根据原子守恒
和得失电子守恒可得反应的化学方程式为MgO+C+Cl=====MgCl +CO,C说法正确;向“煅烧”后所
2 2
得氧化镁中加稀盐酸,得到氯化镁溶液,由于镁离子会发生水解反应Mg2++2HO Mg(OH) +2H+,直
2 2
接蒸发MgCl 溶液,生成的HCl挥发,最终得到的是氢氧化镁,而不是无水氯化镁,D说法错误。
2
2.(2021·江苏卷)由制铝工业废渣(主要含Fe、Ca、Si、Al等的氧化物)制取聚合硫酸铁铝净水剂的流程
如下。
下列有关说法不正确的是( )
A.控制适当反应温度并不断搅拌,有利于提高铁、铝浸取率
B.Al O 与稀硫酸反应的离子方程式:Al O+6H+===2Al3++3HO
2 3 2 3 2
C.滤液中主要存在的阳离子有:H+、Fe2+、Ca2+、Al3+
D.聚合硫酸铁铝水解形成的胶体具有吸附作用
【答案】C
【解析】控制适当反应温度并不断搅拌,可以加快反应速率,充分反应,有利于提高铁、铝浸取率,
故A正确;Al O 与稀硫酸反应生成硫酸铝和水,离子方程式为Al O +6H+===2Al3++3HO,故B正确;
2 3 2 3 2
双氧水会将亚铁离子氧化,所以滤液中主要存在的阳离子中没有Fe2+,而是Fe3+,故C错误;聚合硫酸铁
铝水解可以生成氢氧化铝和氢氧化铁胶体,具有吸附作用,故D正确。
3.(2020·浙江卷)下列关于铝及其化合物的说法,不正确的是( )
A.明矾可用作净水剂和消毒剂
B.利用铝热反应可冶炼高熔点金属
C.铝可用作包装材料和建筑材料
D.氢氧化铝可用作治疗胃酸过多的药物
【答案】A
【解析】明矾可以用于净水,但没有消毒作用,水的消毒剂是利用物质的强氧化性,如氯气、高铁酸
钠等,故A不正确;由于铝热反应放出大量的热,因此可冶炼高熔点金属,故B正确;铝表面有一层致密
的保护膜且具有良好的延展性,可用作包装材料和建筑材料,故 C正确;胃酸的成分是盐酸,胃酸过多,
可利用氢氧化铝的碱性中和,而且氢氧化铝是弱碱,不会对身体有很大的损伤,所以氢氧化铝可用作治疗胃酸过多的药物,故D正确。
4.(2020·山东卷)以菱镁矿(主要成分为MgCO ,含少量SiO 、Fe O 和Al O)为原料制备高纯镁砂的工
3 2 2 3 2 3
艺流程如下:
已知浸出时产生的废渣中有SiO、Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
【答案】B
【解析】结合流程图分析可知浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO,A项正确;浸
4 2 3 2
出可以在较高温度下进行,促进NH Cl水解和NH 的逸出,但沉镁时应在低温下进行,以减弱氨水分解,
4 3
B项错误;结合流程图可知浸出得到的NH 可转化为氨水,用于沉镁,滤液中含有过量的NH Cl,可用于
3 4
浸出时的反应液,故该流程中NH 和NH Cl可循环使用,C项正确;本流程中分离Mg2+时,Al3+、Fe3+转
3 4
化为沉淀,是利用了它们氢氧化物K 的不同,D项正确。
sp
5.(2019·上海卷)在pH为1的100 mL 0.1 mol·L-1的AlCl 中,加入300 mL 0.1 mol·L-1的氢氧化钠溶
3
液后铝元素的存在形式是( )
A.AlO B.Al3+
C.Al(OH) D.Al3+、Al(OH)
3 3
【答案】D
【解析】pH为1的100 mL 0.1 mol·L-1的AlCl 中,n(H+)=0.1 mol·L-1×0.1 L=0.01 mol。n(Al3+)=0.1
3
mol·L-1×0.1 L=0.01 mol。300 mL 0.1 mol·L-1的氢氧化钠溶液中n(OH-)=0.1 mol·L-1×0.3 L=0.03 mol。其
中0.01 mol的 OH-和0.01 mol的H+发生中和反应,剩下的0.02 mol的OH-和0.01 mol的Al3+反应,氢氧
根离子不足,所以生成Al(OH) 并有Al3+剩余。
3
6.(2018·江苏卷)以高硫铝土矿(主要成分为Al O、Fe O、SiO,少量FeS 和金属硫酸盐)为原料,
2 3 2 3 2 2
生产氧化铝并获得Fe O 的部分工艺流程如下:
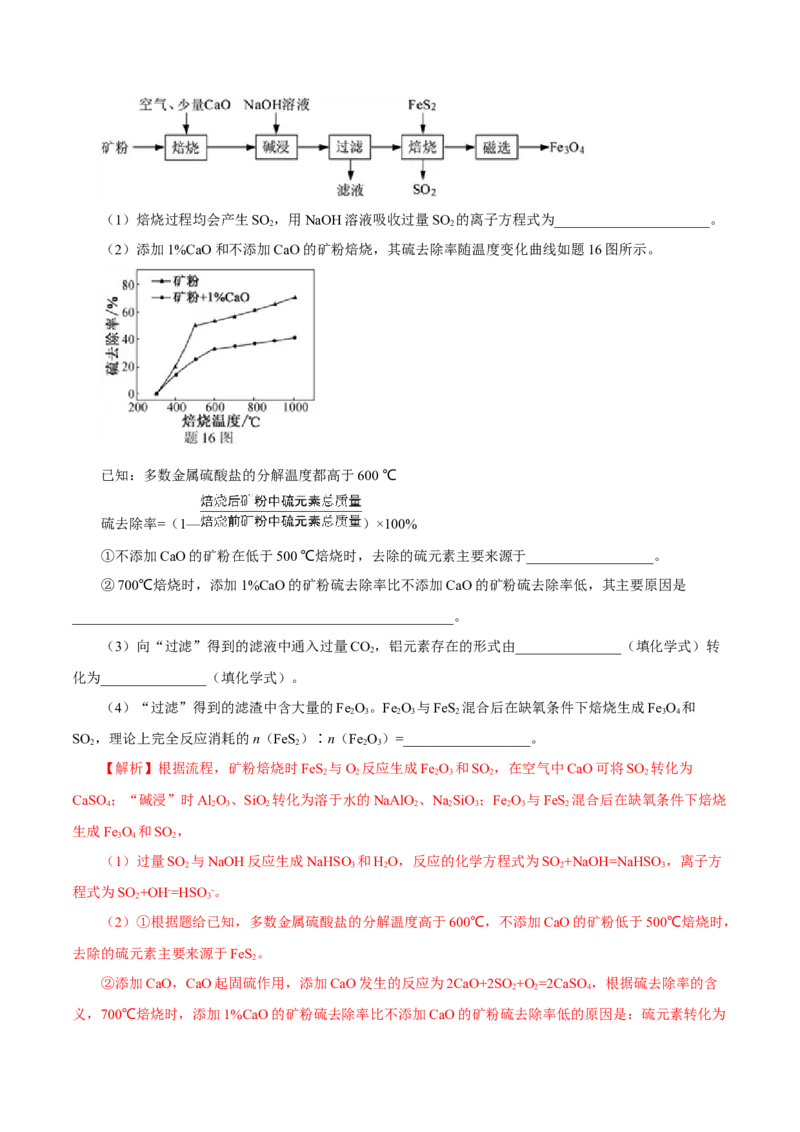
3 4(1)焙烧过程均会产生SO ,用NaOH溶液吸收过量SO 的离子方程式为______________________。
2 2
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题16图所示。
已知:多数金属硫酸盐的分解温度都高于600 ℃
硫去除率=(1— )×100%
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于__________________。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是
______________________________________________________。
(3)向“过滤”得到的滤液中通入过量CO,铝元素存在的形式由_______________(填化学式)转
2
化为_______________(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe O。Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和
2 3 2 3 2 3 4
SO ,理论上完全反应消耗的n(FeS)∶n(Fe O)=__________________。
2 2 2 3
【解析】根据流程,矿粉焙烧时FeS 与O 反应生成Fe O 和SO ,在空气中CaO可将SO 转化为
2 2 2 3 2 2
CaSO;“碱浸”时Al O、SiO 转化为溶于水的NaAlO 、NaSiO;Fe O 与FeS 混合后在缺氧条件下焙烧
4 2 3 2 2 2 3 2 3 2
生成Fe O 和SO ,
3 4 2
(1)过量SO 与NaOH反应生成NaHSO 和HO,反应的化学方程式为SO +NaOH=NaHSO ,离子方
2 3 2 2 3
程式为SO +OH-=HSO -。
2 3
(2)①根据题给已知,多数金属硫酸盐的分解温度高于600℃,不添加CaO的矿粉低于500℃焙烧时,
去除的硫元素主要来源于FeS。
2
②添加CaO,CaO起固硫作用,添加CaO发生的反应为2CaO+2SO+O =2CaSO ,根据硫去除率的含
2 2 4
义,700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低的原因是:硫元素转化为CaSO 留在矿粉中。
4
(3)“碱浸”时Al O、SiO 转化为溶于水的NaAlO 、NaSiO,向“过滤”得到的滤液中通入过量
2 3 2 2 2 3
CO,CO 与NaAlO 反应生成NaHCO 和Al(OH),反应的离子方程式为CO+AlO -+2H O=Al(OH)
2 2 2 3 3 2 2 2
↓+HCO-,即Al元素存在的形式由NaAlO 转化为Al(OH)。
3 3 2 3
(4)Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和SO ,反应的化学方程式为FeS+16Fe O
2 3 2 3 4 2 2 2 3
11Fe O+2SO↑,理论上完全反应消耗的n(FeS):n(Fe O)=1:16。
3 4 2 2 2 3
【答案】
(1)SO +OH−==HSO−
2 3
(2)①FeS
2
②硫元素转化为CaSO 而留在矿粉中
4
(3)NaAlO Al(OH)
2 3
(4)1∶16