文档内容
第 16 讲 元素周期律和元素周期表
第一部分:高考真题感悟
1.(2022·广东·高考真题)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧
化物对应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁
为P。A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;B.根据同
周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;C.甲的氢化物可能为氨气,可
能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、乙烷等,则遇氯化氢不反应,没
有白烟生成,故C错误;D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强
碱反应,故D正确。综上所述,答案为C。
2.(2022·海南·高考真题)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y
是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下
列判断正确的是
A. 是非极性分子
B.简单氢化物沸点:
C.Y与Z形成的化合物是离子化合物
D.X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【解析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且Y是组成水的元
素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,则Z为Na元素,W原子在同周期主族元素中原子半径最小,则W为Cl元素。
A.由分析,X为N元素,W为Cl元素,NCl 分子的空间构型为三角锥形,其正负电荷的中心不重合,属
3
于极性分子,A错误;B.HO和NH 均含有氢键,但HO分子形成的氢键更多,故沸点HO>NH ,B错
2 3 2 2 3
误;C.Y为O元素,Z为Na元素,两者形成的化合物为NaO、NaO 均为离子化合物,C正确;D.N、
2 2 2
O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;答案选C。
3 2
3.(2022·浙江·高考真题)W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y同族,Y的原
子序数是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是
A.非金属性:Y>W B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸 D.X与Y可形成化合物XY
2 3
【答案】D
【解析】X是地壳中含量最多的金属元素,X为Al元素,W和Y同族,Y的原子序数是W的2倍,W为
O元素,Y为S元素,Z为Cl元素。A.非金属性同主族从上至下逐渐减弱:Y<W,A错误;B.氯化铝
是共价化合物,B错误;C.Y、Z的最高价氧化物对应的水化物分别硫酸和高氯酸,两者均为强酸,次氯
酸也是氯的氧化物对应的水化合物,但次氯酸为弱酸,C错误;D.根据化合物的化合价代数和为0可知,
铝与硫元素形成的化合物化学式为Al S,D正确;答案选D。
2 3
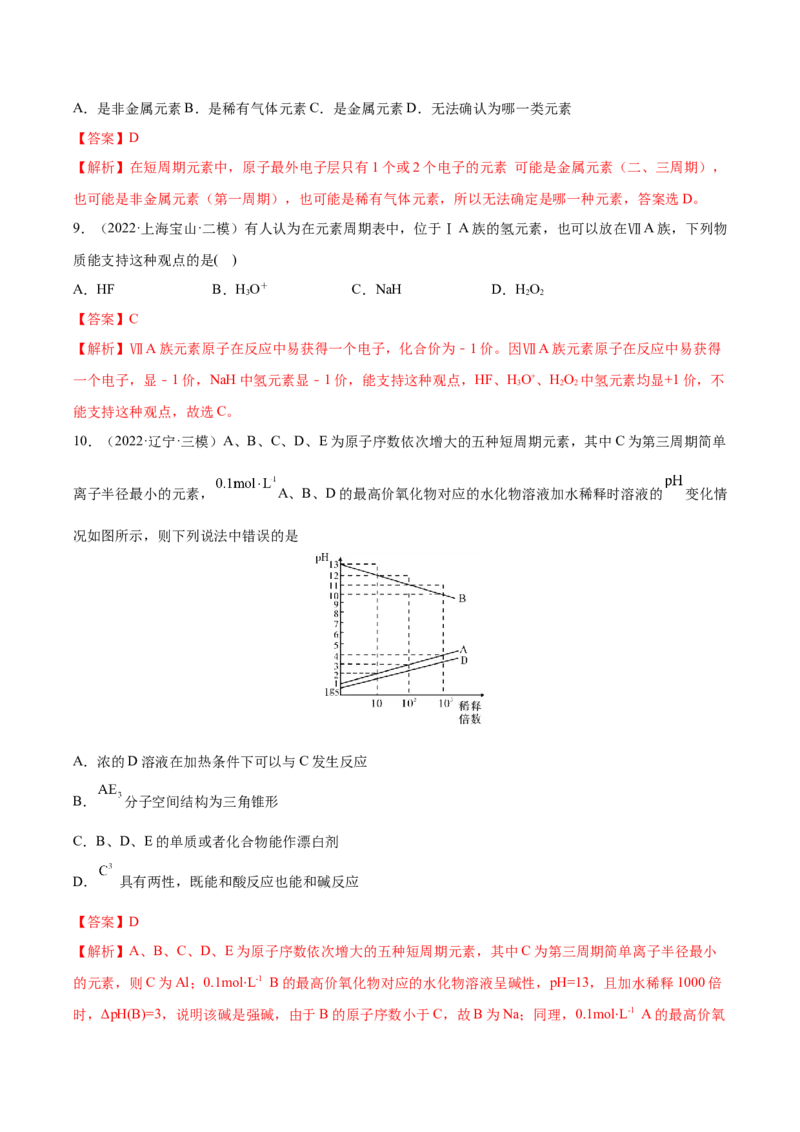
4.(2022·全国·高考真题)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为
短周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数,常温下为气体。该化合物的
热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物的酸性:
C. 阶段热分解失去4个D. 热分解后生成固体化合物
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序
4 5 8 2
数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则
说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序数
2
依次增加,且加和为21,则X为B。A.X(B)的单质常温下为固体,故A错误;B.根据非金属性越强,
其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错误;
3 3 3
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热分解
失去4个HO,则质量分数 ,则说明不是失去4个HO,故C错
2 2
误;
D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到关系
4 5 8 2 2 3 2 3
式2NH B O·4H O~5B O,则固体化合物B O 质量分数为 ,
4 5 8 2 2 3 2 3
说明假设正确,故D正确。综上所述,答案为D。
5.(2022·全国·高考真题)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为
19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说
法正确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的沸点: D.最高价含氧酸的酸性:
【答案】D
【解析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子最外
层电子数为Q原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最外层电子
数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、Y、Z的最外层电
子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的最
外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,则
Z的最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P。A.X为Al,Q为N或O或F,同
一周期从左往右元素非金属性依次增强,同一主族从上往下依次减弱,故非金属性:Q>X,A错误;B.
由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X,B错
误;C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为
2 3
Cl或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在,
2 3
故沸点Q>Z,C错误;D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强
于Si,因此最高价含氧酸酸性:Z>Y,D正确;故答案为:D。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海·格致中学模拟预测)以共价单键相连的非金属单质中,1个原子与相邻原子成键的数目为
8-N个,N为该非金属元素的主族序数,化学家称这一现象为(8-N)规则。如图是某非金属单质结构模型,
构成该单质的元素在元素周期表中位于
A.ⅢA B.ⅣA C.VA D.ⅥA
【答案】A
【解析】根据题意,该单质结构模型中形成了5个共价键,再根据8-N规则,则N=3即为第ⅢA族元素,
故A项正确;故答案选A。
2.(2022·河北保定·二模)中国科学院院士张青莲教授曾主持测定的铟( )等9种元素相对原子质量的
新值,被采用为国际新标准。In与A1同主族。下列说法正确的是
A.In是第四周期ⅢA族元素 B. 与 互为同素异形体
C.原子半径: D.碱性:
【答案】C
【解析】A.In的原子序数为49,原子核外有5个电子层,数目分别为2、8、18、18、3,则In处于第五
周期第ⅢA族,A错误;B. 与 质子数相同,中子数不同,两者互为同位素,B错误;C.Rb位于第五周期第IA族,Rb和In均位于第五周期,同周期主族元素从左到右原子半径递减,则原子半径:
Rb>In,C正确;D.Al位于第三周期第ⅢA族,元素的金属性越强,对应的最高价氧化物的水化物的碱
性越强,同一主族元素从上向下,金属性逐渐增强,则碱性: ,D错误;答案选C。
3.(2022·天津·一模)关于 的反应,下列说法中正确的是
A.反应中 作还原剂 B.X元素的原子最外层上有7个电子
C.X是周期表中第二周期元素 D. 遇淀粉液变蓝
【答案】B
【解析】根据电荷守恒,X的最低价是-1,X是卤素。A. 的化合价由+5降低到0价,作为氧化剂,
故A错误;B.X元素原子的最外层有7个电子,故B正确;C.F没有正价,而X为+5价,故X不可能
位于第二周期,故C错误;D.X若为I,则X 遇淀粉变蓝,但X也可能为Cl,氯气不能使淀粉变蓝,故
2
D错误。故选B。
4.(2022·浙江台州·二模)下列说法正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.原子最外层电子数为2的元素一定处于周期表第ⅡA族
C.同周期中金属性最强的元素是ⅠA族金属元素
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
【答案】C
【解析】A.同主族自上而下非金属性减弱,最高价含氧酸的酸性减弱,不是最高价含氧酸则不一定,故
A错误;B.原子最外层电子数为2的元素不一定处于周期表第ⅡA族,如氦原子最外层电子数为2,它处
于周期表的0族,故B错误;C.同周期元素从左到右金属性逐渐减弱,则第ⅠA族金属元素是同周期中
金属性最强的元素,故C正确;D.周期表中金属和非金属分界线附近的元素可能作半导体材料,过渡元
素位于副族和第VⅢ族,故D错误;答案选C。
5.(2022·湖北武汉·模拟预测)高纯度的锗是半导体材料,下图是锗在周期表中的信息。下列说法正确的
是
32 Ge
锗
4s24p272.63
A.位于Ⅳ族 B.质量数为32 C.价电子数为2 D.相对原子质量为72.63
【答案】D
【解析】元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的
汉字表示元素名称,下边是元素的相对原子质量。A.锗为32号元素,位于ⅣA族,A错误;B.32为原
子序数不是质量数,B错误;C.锗原子的价电子排布为4s24p2,价电子数为4,C错误;D.相对原子质
量为72.63,D正确;故选D。
6.(2022·上海·模拟预测)下列各元素中,一定属于主族元素的是
A.最高价氧化物是酸性氧化物
B.原子最外层电子数为2
C.能形成+7价的含氧酸及其盐
D.简单阴离子最外层满足8个电子稳定结构
【答案】D
【解析】A.最高价氧化物是酸性氧化物的元素不一定是主族元素,如MnO 是酸性氧化物,但Mn是副
2 7
族元素,而SO 、CO 等是酸性氧化物,S、C是主族元素,A不合题意;B.原子最外层电子数为2的元
3 2
素不一定是主族元素,如Mg、Ca为主族元素,而Sc、Ti、V、Zn等则为副族元素,B不合题意;C.能
形成+7价的含氧酸及其盐的元素不一定是主族元素,如HMnO 、KMnO ,但Mn属于副族元素,而
4 4
HClO、KClO,Cl是主族元素,C不合题意;D.能够形成简单阴离子的元素一定是非金属元素,而非金
4 4
属元素都是主族元素,故简单阴离子最外层满足8个电子稳定结构一定是主族元素,D符合题意;故答案
为:D。
7.(2022·上海静安·二模)2021年,我国发布了《医用同位素中长期发展规划》,对提升医用同位素相关
产业能力水平、保障健康中国战略实施具有重要意义。医用同位素有14C、18F、131I等。有关说法正确的是
A.14C位于元素周期表的第二周期第ⅥA族
B.18F和131I具有相同的最外层电子数
C.14C与12C的性质完全相同
D.化合物23Na131I的中子总数为奇数
【答案】B
【解析】A.C原子序数为6,位于元素周期表的第二周期第ⅣA族,故A错误;B.F和I 属于第ⅦA族,
最外层电子数相同,故B正确;C. 14C与12C的化学性质几乎完全相同,但物理性质有差异,故C错误;
D. 23Na131I 的中子总数为(23-11)+(131-53),不为奇数,故D错误。故选B。
8.(2022·上海青浦·一模)在短周期元素中,原子最外电子层只有1个或2个电子的元素A.是非金属元素B.是稀有气体元素C.是金属元素D.无法确认为哪一类元素
【答案】D
【解析】在短周期元素中,原子最外电子层只有1个或2个电子的元素 可能是金属元素(二、三周期),
也可能是非金属元素(第一周期),也可能是稀有气体元素,所以无法确定是哪一种元素,答案选D。
9.(2022·上海宝山·二模)有人认为在元素周期表中,位于ⅠA族的氢元素,也可以放在ⅦA族,下列物
质能支持这种观点的是( )
A.HF B.HO+ C.NaH D.HO
3 2 2
【答案】C
【解析】ⅦA族元素原子在反应中易获得一个电子,化合价为﹣1价。因ⅦA族元素原子在反应中易获得
一个电子,显﹣1价,NaH中氢元素显﹣1价,能支持这种观点,HF、HO+、HO 中氢元素均显+1价,不
3 2 2
能支持这种观点,故选C。
10.(2022·辽宁·三模)A、B、C、D、E为原子序数依次增大的五种短周期元素,其中C为第三周期简单
离子半径最小的元素, A、B、D的最高价氧化物对应的水化物溶液加水稀释时溶液的 变化情
况如图所示,则下列说法中错误的是
A.浓的D溶液在加热条件下可以与C发生反应
B. 分子空间结构为三角锥形
C.B、D、E的单质或者化合物能作漂白剂
D. 具有两性,既能和酸反应也能和碱反应
【答案】D
【解析】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中C为第三周期简单离子半径最小
的元素,则C为Al;0.1molL-1 B的最高价氧化物对应的水化物溶液呈碱性,pH=13,且加水稀释1000倍
时,ΔpH(B)=3,说明该碱是⋅强碱,由于B的原子序数小于C,故B为Na;同理,0.1molL-1 A的最高价氧
⋅化物对应的水化物溶液呈酸性,pH=1,且加水稀释1000倍时,ΔpH(A)=3,说明该酸是强酸,由于A的原
子序数小于C,故A为N;0.1molL-1 D的最高价氧化物对应的水化物溶液呈酸性,pH=0.7,该酸是多元
强酸,则D是S,E是Cl;综上所⋅述,A为N,B为Na,C为Al,D是S,E是Cl。
A.由分析可知,C为Al,D是S,浓HSO 在加热条件下可以和Al发生反应生成Al (SO )、SO 和HO,
2 4 2 4 2 2
A正确;B.由分析可知,A为N,E是Cl;NCl 分子的中心原子N的价层电子对数为3+ =3+1=4,
3
N含有1个孤电子对,则NCl 分子的空间构型为三角锥形,B正确;C.由分析可知,B为Na,D是S,E
3
是Cl;NaO、NaClO等具有强氧化性,可以作漂白剂,SO 能和有色物质反应生成无色物质,也可以作漂
2 2 2
白剂,C正确;D.由分析可知,C为Al,Al3+只能和碱反应,故Al3+不具有两性,D错误;故选D。
11.(2022·河南·二模)X、Y、Z、W四种主族元素,原子序数依次增大,且均不大于20,四种元素核电
荷数之和为46,X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。Z元素是一种
重要的“成盐元素”,其形成的一种盐在海水中含量最高,其单质通过电解该盐溶液获得。下列关于四种
元素说法错误的是
A.XY、ZY、 W(ZY) 均是常见的杀菌消毒剂,三者作用原理相同
2 2 2 2
B.WX 中X元素的检验方法可以将WX 固体置于氧气流中灼烧并将产物通过无水硫酸铜
2 2
C.WZ、WY 两种化合物中阴阳离子个数比均为1 : 2
2 2
D.可以通过XZY、ZY 等物质中的元素化合价来比较Y、Z两种元素的非金属性强弱
2
【答案】C
【解析】X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。则X、Y分别为H、
O。Z形成的一种盐在海水中含量最高,Z为Cl。四种元素核电荷数之和为46,则W为20号元素Ca。
A.三种物质分别为HO、ClO 、Ca(ClO) ,三者均具有较强的氧化性,可利用氧化性进行消毒杀菌,A
2 2 2 2
项正确;B.CaH 与O 反应变为HO遇CuSO 溶液变蓝,说明X为H元素,B项正确;C.WZ、WY 分
2 2 2 4 2 2
别为CaCl 和CaO,前者是由Ca2+和2个Cl-组成阴阳离子之比为1:2,而后者是由Ca2+和 阴阳离子之比
2 2
为1:1,C项错误;D.XZY、ZY 为HClO和ClO 中Cl均呈现出了正价而O均呈现出负价,说明O的电
2 2
子能力强于Cl,所以O的非金属性强于Cl,D项正确;故选C。
12.(2022·湖北·天门市教育科学研究院模拟预测)W、X、Y、Z是原子序数依次增大的短周期主族元素,
其中X和Z同主族,由W、X、Y、Z形成的锂盐结构如图所示,下列说法正确的是A.原子半径: W>X>Y>Z
B.最简单氢化物的稳定性: X<Y
C.Z的单质在过量X 中燃烧生成ZX
2 3
D.该锂盐所有原子最外层均满足8电子稳定结构
【答案】B
【解析】W、X、Y、Z是原子序数依次增大的短周期主族元素,由W、X、Y、Z形成的锂盐结构所示,
X、Z同主族,X可形成Z=X键,Z有6条共价键,则二者位于ⅥA族,则X为O元素,Z是S元素W形
成4条共价键,Y形成一条共价键,则W为C,Y为F元素,W、X、Y、Z分别为C、O、F、S。A.
W、X、Y、Z分别为C、O、F、S,原子半径: Z>W>X>Y,A选项错误;B.X、Y最简单氢化物分别
为HO、HF,由于非金属性F>O,氢化物的稳定性: X<Y,B选项正确;C.Z为S,X为O2,Z的单
2
质在过量X 中燃烧生成SO ,C选项错误;D.该锂盐中C、O、F、S均为最外层8个电子,而Li+最外层
2 2
只有2个电子,D选项错误;答案选B。
二、主观题(共4小题,共40分)
13.(2022·广西柳州·模拟预测)(12分)我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其
构成与地球土壤类似。土壤中含有的短周期元素A、B、C、D,原子序数依次增大,最外层电子数之和为
15。B、C、D为同周期相邻元素,A为地壳中含量最多的元素。回答下列问题:
(1)元素D在周期表中的位置为___,A、C的简单离子半径大小顺序为___ (填离子符号)。
(2)化合物BA的电子式为___(填元素符号)。A和D形成的化合物中的化学键类型为___________。
(3)B和C两元素相比较,金属性较强是___ (填元素符号),可以证明该结论的实验___。
A.比较两种元素的单质与冷的浓硫酸反应的速率
B.比较两种元素最高价氧化物对应的水化物的碱性
C.将相同大小的两种元素单质分别放入沸水中,观察反应现象
D.比较相同物质的量的两种元素的单质与足量稀盐酸反应产生 的多少
【答案】(每空2分)(1) 第3周期第IVA族(或第3周期14列)
(2) 共价键(3)Mg BC
【解析】A为地壳中含量最多的元素,A为O,B、C、D为同周期相邻元素,A、B、C、D原子序数依次
增大,最外层电子数之和为15,则B、C、D最外层电子数之和为9,则B为Mg,C为Al,D为Si。
(1)元素D为Si,在周期表中位置为第三周期ⅣA族。核外电子数相同的情况下,核电荷数越大,离子半
径越小,所以离子半径O2->Al3+。
(2)化合物BA为MgO,电子式为 。A和D形成的化合物为SiO,其中的化学键类型为共价键。
2
(3)Mg和Al相比,金属性较强的为Mg。A项镁能和冷的浓硫酸反应,铝也能和冷的浓硫酸反应,并在表
面形成致密的氧化膜阻止硫酸与铝进一步反应,不能通过两种元素的单质与冷的浓硫酸反应的速率来比较
金属性强弱,A错误;B项元素的金属性越强,其最高价氧化物对应水化物的碱性越强,氢氧化镁碱性强
于氢氧化铝,B正确;镁可与沸水反应生成氢气,反应较为剧烈,铝不能和沸水发生明显的反应,说明金
属性镁强于铝,C正确;D项相同物质的量的两种单质,与足量盐酸反应,铝产生的氢气要多但是铝的金
属性弱于镁,D错误;故答案选BC。
14.(2021·河南·模拟预测)(12分)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性
质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素 ,其原子核内的中子数比核外电子数多_______(填数值)。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
A.沸点:
B.等物质的量浓度溶液的酸性:
C.分解温度:
D.相对分子质量:
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为 ,
前者让: 分解产生黑亮的砷镜(As),后者让 被 溶液氧化为 ,同时还生成Ag单质。
① 的电子式为_______。②Gutzeit试砷法中 被氧化的离子方程式为_______。
(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用 溶液对其进行刻蚀,As元素的化合价变为
+5价,则该反应中还原剂与氧化剂的物质的量之比为_______;砷化镓也可用于制造太阳能电池,该电池
工作时的能量转化形式为_______。
【答案】(每空2分)(1)9
(2)BC
(3)
(4)1:4 太阳能→电能
【解析】(1)根据元素周期表和周期律可推知As的原子序数为33, 的中子数为 ,因此其原
子核内的中子数与核外电子数之差 。
(2)元素的非金属性与氢化物的沸点及相对分子质量无关,A、D项错误;等物质的量浓度溶液的酸性:
,最高价含氧酸的酸性越强,元素的非金属性越强,B项正确;简单氢化物的热稳定性越
强,元素的非金属性越强,因此分解温度 可以判断出N的非金属性强,C项正确;故选BC。
(3)①As原子最外层有5个电子,因此 的电子式为 ;②Gutzeit试砷法中 作氧化剂,
还原产物为银,因此反应的离子方程式为 。
(4)As元素从−3→+5价, 中的O元素从−1→−2价,根据化合价升降相等,可得还原剂与氧化剂的物
质的量之比为1:4;太阳能电池工作时的能量转化形式为太阳能→电能。
15.(2022·湖南·宁乡市教育研究中心模拟预测)(8分)下表为元素周期表的一部分,请参照元素①~⑧
在表中的位置,用化学用语回答下列问题:(1)在此元素周期表的一部分中,金属性最强的元素是_______(填元素符号)。
(2)⑤、⑥的原子半径由大到小的顺序为_______(填元素符号)。
(3)⑦、⑧两种元素的氢化物稳定性较强的是_______ (用化学式表示)。
(4)⑤、⑧的最高价氧化物对应的水化物相互反应的离子方程式为_______。
【答案】(1)Na
(2)Na>Al
(3)HCl
(4)OH-+ H+= H O
2
【解析】根据元素在周期表中的位置,①②③④⑤⑥⑦⑧分别是H元素、C元素、N元素、O元素、Na元
素、Al元素、Si元素、Cl元素。
(1)同主族元素从上到下金属性增强、同周期从右到左元素金属性增强,金属性最强的元素是Na;
(2)同周期元素从左到右,原子半径依次减小,Na、Al的原子半径由大到小的顺序为Na>Al。
(3)同周期元素从左到右非金属性增强,气态氢化物稳定性增强,Si、Cl两种元素的氢化物稳定性较强的是
HCl;
(4)Na的最高价氧化物对应的水化物NaOH、Cl的最高价氧化物对应的水化物是HClO,NaOH是强碱、
4
HClO 是强酸,相互反应的离子方程式为OH-+ H+= H O。
4 2
16.16.(2020·浙江温州·三模)(8分)(1)比较酸性相对强弱:HSO ______HClO(填“>”、“=”或
2 4 4
“<”),已知能发生反应:HSO (浓)+NaClO HClO+NaHSO ,说明该反应能发生的理由_______。
2 4 4 4 4
(2)Al(OH) 具有一元弱酸的性质,在水中电离时产生的含铝微粒具有正四面体结构,写出电离方程式
3
_______。
(3)甘氨酸和硝基乙烷的熔点分别为240°C和-40°C,从物质结构角度解释甘氨酸熔点较高的原因______。
【答案】(每空2分) (1)< HSO 沸点高于HClO
2 4 4(2)Al(OH) +HO Al(OH) -+H+
3 2 4
(3)甘氨酸主要以内盐形式存在,(存在离子键)熔点较高,硝基乙烷是分子晶体,分子间作用力小于离
子键。
【解析】(1)同周期非金属元素的非金属性从左到右逐渐增强,可知非金属性S<Cl;元素的非金属性越强,
其最高价氧化物的水化物的酸性越强,可知酸性HSO <HClO;反应HSO (浓)+NaClO HClO+NaHSO
2 4 4 2 4 4 4 4
能够发生,是由于HSO 沸点高于HClO,高沸点酸制取低沸点酸;
2 4 4
(2)Al(OH) 在水中电离得到Al(OH) -和H+,电离方程式为Al(OH) +HO Al(OH) -+H+;
3 4 3 2 4
(3)甘氨酸的结构简式为NH CHCOOH,具有氨基、羧基;氨基具有碱性,羧基具有酸性;因此甘氨酸主
2 2
要是以内盐形式存在,存在离子键,熔点较高;而硝基乙烷的结构简式为CHCHNO ,是共价分子,分子
3 2 2
间作用力小于离子键。