文档内容
第 16 讲 元素周期律和元素周期表
目录
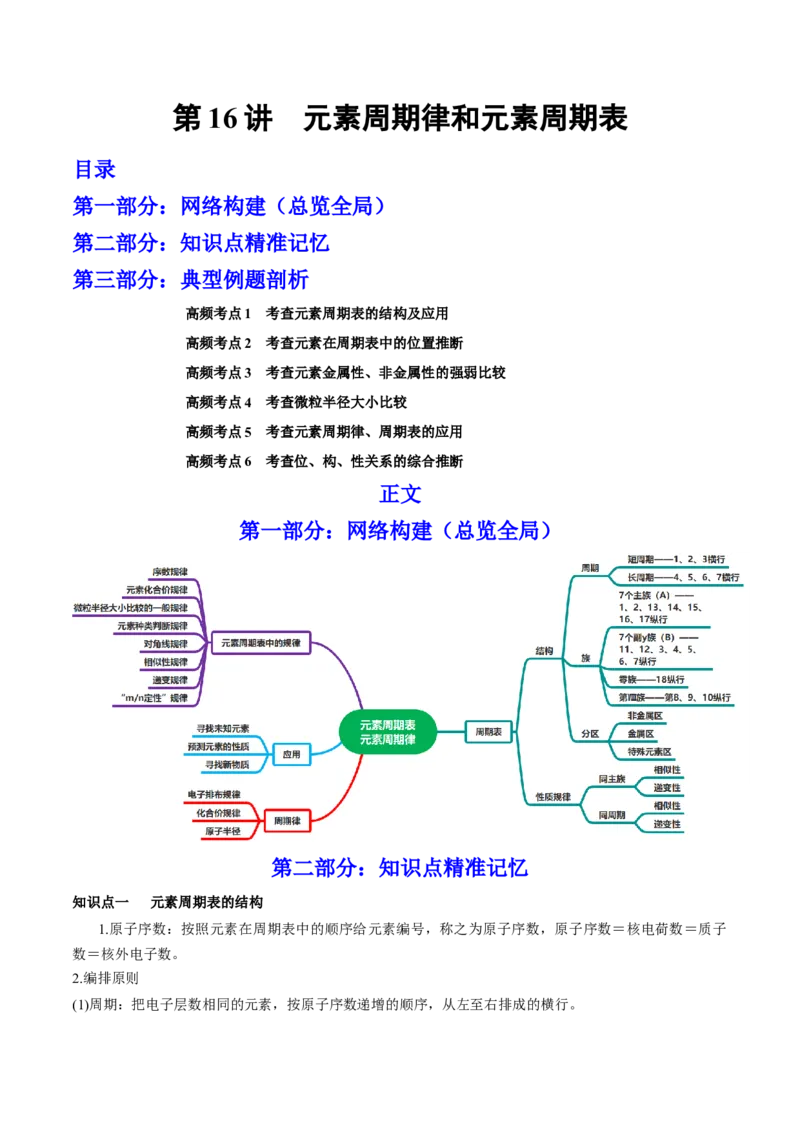
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查元素周期表的结构及应用
高频考点2 考查元素在周期表中的位置推断
高频考点3 考查元素金属性、非金属性的强弱比较
高频考点4 考查微粒半径大小比较
高频考点5 考查元素周期律、周期表的应用
高频考点6 考查位、构、性关系的综合推断
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 元素周期表的结构
1.原子序数:按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电荷数=质子
数=核外电子数。
2.编排原则
(1)周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
3.元素周期表的结构
1)结构
(1)周期(7个横行,7个周期)
短周期 长周期
周期序数 一 二 三 四 五 六 七
元素种数 2 8 8 18 18 32 32
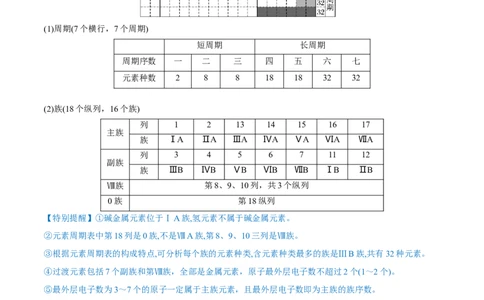
(2)族(18个纵列,16个族)
列 1 2 13 14 15 16 17
主族
族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
列 3 4 5 6 7 11 12
副族
族 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
Ⅷ族 第8、9、10列,共3个纵列
0族 第18纵列
【特别提醒】①碱金属元素位于ⅠA族,氢元素不属于碱金属元素。
②元素周期表中第18列是0族,不是ⅧA族,第8、9、10三列是Ⅷ族。
③根据元素周期表的构成特点,可分析每个族的元素种类,含元素种类最多的族是ⅢB族,共有32种元素。
④过渡元素包括7个副族和第Ⅷ族,全部是金属元素,原子最外层电子数不超过2个(1~2个)。
⑤最外层电子数为3~7个的原子一定属于主族元素,且最外层电子数即为主族的族序数。
⑥电子层数=周期序数,主族序数=价电子数。
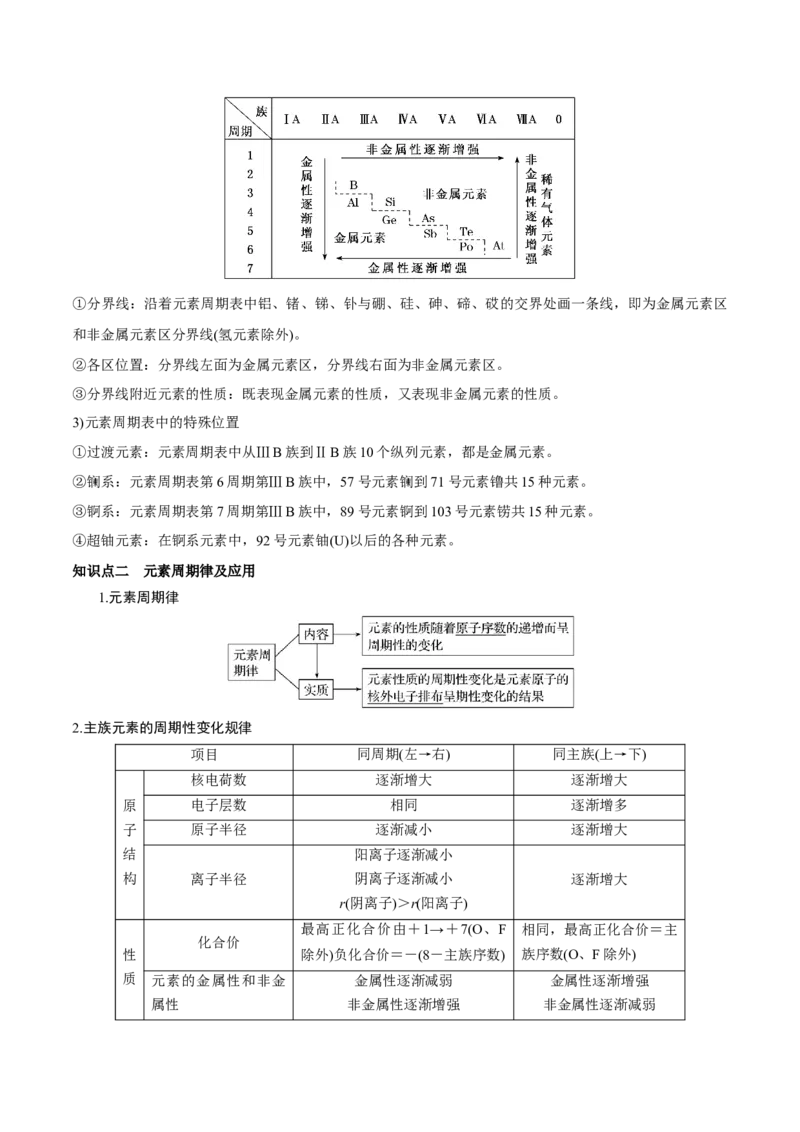
2)分区①分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条线,即为金属元素区
和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左面为金属元素区,分界线右面为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
3)元素周期表中的特殊位置
①过渡元素:元素周期表中从ⅢB族到ⅡB族10个纵列元素,都是金属元素。
②镧系:元素周期表第6周期第ⅢB族中,57号元素镧到71号元素镥共15种元素。
③锕系:元素周期表第7周期第ⅢB族中,89号元素锕到103号元素铹共15种元素。
④超铀元素:在锕系元素中,92号元素铀(U)以后的各种元素。
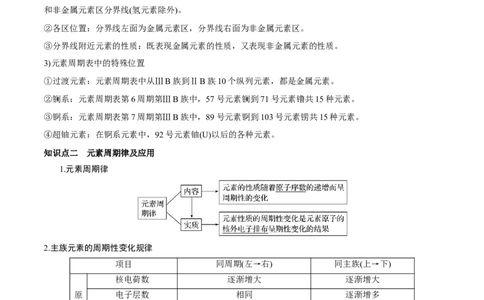
知识点二 元素周期律及应用
1.元素周期律
2.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
原 电子层数 相同 逐渐增多
子 原子半径 逐渐减小 逐渐增大
结 阳离子逐渐减小
构 离子半径 阴离子逐渐减小 逐渐增大
r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F 相同,最高正化合价=主
化合价
性 除外)负化合价=-(8-主族序数) 族序数(O、F除外)
质 元素的金属性和非金 金属性逐渐减弱 金属性逐渐增强
属性 非金属性逐渐增强 非金属性逐渐减弱离子的氧化性、还原 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物的稳定性 逐渐增强 逐渐减弱
最高价氧化物对应的 碱性逐渐减弱 碱性逐渐增强
水化物的酸碱性 酸性逐渐增强 酸性逐渐减弱
3.元素周期表、元素周期律的应用
(1)根据元素周期表中的位置寻找未知元素
(2)预测元素的性质(由递变规律推测)
①比较不同周期、不同主族元素的性质
如:金属性:Mg>Al、Ca>Mg,则碱性:Mg(OH) >Al(OH) 、Ca(OH) >Mg(OH) ,则 Ca(OH) >
2 3 2 2 2
Al(OH) (填“>”“<”或“=”)。
3
②推测未知元素的某些性质
如:已知Ca(OH) 微溶,Mg(OH) 难溶,可推知Be(OH) 难溶;再如:已知卤族元素的性质递变规律,可
2 2 2
推知元素砹(At)应为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt不溶于水等。
(3)启发人们在一定区域内寻找新物质
①半导体元素在金属与非金属分界线附近,如:Si、Ge、Ga等。
②农药中常用元素在右上方,如:F、Cl、S、P、As等。
③催化剂和耐高温、耐腐蚀合金材料主要在过渡元素中找,如:Fe、Ni、Rh、Pt、Pd等。
知识点三 元素周期表中的有关规律
1、原子序数规律
(1)同主族、邻周期元素的原子序数差
同主族相邻两元素中,Z(下)=Z(上)+上一周期
元素周期表中左侧元素(ⅠA、ⅡA族)
元素所在周期的元素种类数目
同主族相邻两元素中,Z(下)=Z(上)+下一周期
元素周期表中右侧元素(ⅢA~ⅦA族)
元素所在周期的元素种类数目
(2)同周期第ⅡA族和第ⅢA族元素原子序数差
周期序数 1 2 3 4 5 6 7
原子序数差 无 1 1 11 11 25 25
2、元素化合价规律
(1)主族元素的最高正化合价=它所在的族序数=最外层电子数(即价电子数),但要注意F无正价,O一般不显正
价。
(2)只有非金属元素才有负价,非金属元素的最高正价与它的负化合价的绝对值之和等于8。
(3)若某原子的最外层电子数为奇数(m),则正常化合价为奇数,从+1价到+m价,若出现偶数则为非正常化合价,
其氧化物为不成盐氧化物,如NO、NO 。
2(4)若某原子的最外层电子数为偶数(n),则元素的正常化合价为一系列偶数,例如-2 +4 +6。
S、S、S
3、微粒半径大小比较的一般规律
(1)同周期(除0族外),随原子序数的递增,原子半径由大到小,如Na>Mg>Al;
(2)同主族,随原子序数的递增,原子半径、离子半径由小到大,如LiZ(B)>Z(A);原子半径r(C)>r(A)>r(B);A、B、C若为非
金属元素,则非金属性B>A>C,单质的氧化性B>A>C等。m
n
8、“ 定性”规律:若主族元素族数为m,周期数为n,则:
m m
n n
① <1时为金属, 值越小,金属性越强;
m m
n n
② >1时是非金属, 越大非金属性越强;
m
n
③ =1时多为两性元素
知识点四 金属性和非金属性强弱的判断方法
元素周期表:金属性“右弱左强,上弱下强,右上弱左下强”;非金属性
“左弱右强,下弱上强,左下弱右上强”
一表
金属活动性顺序:按K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、Hg、
两序 Ag、Pt、Au的顺序,金属性减弱
非金属活动性顺序:按F、O、Cl、Br、I、S的顺序,非金属性减弱
置换反应:强的置换弱的,适合金属也适合非金属
与水或非氧化性酸反应越剧烈,或最高价氧化物对应水化物的碱性越强,
三反应 则金属性越强
与氢气反应越容易,生成的气态氢化物的稳定性越强,或最高价氧化物对
应水化物的酸性越强,则非金属性越强
氧化性 金属离子的氧化性越弱,对应元素的金属性越强
还原性 非金属氢化物或非金属阴离子的还原性越弱,对应元素的非金属性越强
原电池:一般情况下,负极材料的金属性强于正极
两池
电解池:在阳极首先放电的阴离子,其对应元素的非金属性弱;在阴极首
先放电的阳离子,其对应元素的金属性弱;
知识点五 元素位—构—性的关系
元素的原子结构决定了元素在周期表中的位置和元素的主要性质,元素在周期表中的位置反映了元素
的原子结构和元素的主要性质,故三者之间可相互推断。2.三者的推断关系
(1)结构与位置的互推
①明确四个关系式
a.电子层数=周期序数。
b.质子数=原子序数。
c.最外层电子数=主族序数。
d.主族元素的最高正价=最外层电子数。
最低负价=-|8-最外层电子数|。
②熟悉掌握周期表中的一些特殊规律
a.各周期所能容纳元素种数。
b.稀有气体的原子序数及在周期表中的位置。
c.同族上下相邻元素原子序数的关系。
(2)性质与位置互推
熟悉元素周期表中同周期、同主族元素性质的递变规律,根据元素性质可以推知元素在周期表中的位置,
根据元素在周期表中的位置可以推知元素性质。主要包括:
①元素的金属性、非金属性。
②气态氢化物的稳定性。
③最高价氧化物对应水化物的酸碱性。
④金属与HO或酸反应的难易程度。
2
3.结构和性质的互推
(1)最外层电子数是决定元素原子的氧化性和还原性的主要因素。
(2)原子半径决定了元素单质的性质;离子半径决定了元素组成化合物的性质。
(3)同主族元素最外层电子数相同,性质相似。
4.元素推断的一般思路5.推断题要点总结
(1)结构与位置互推是解题的核心
①掌握四个关系式:a.电子层数=周期数;b.质子数=原子序数;c.最外层电子数=主族序数;d.主族元素
的最高正价=主族序数(O、F除外),负价=主族序数-8。
②熟练掌握周期表的结构及周期表中的一些特殊规律
a.“凹”型结构的“三短四长,七主七副八零完”;b.各周期元素种类;c.稀有气体的原子序数及在周期
表中的位置;d.同主族上下相邻元素原子序数的关系。
(2)熟记常见元素及其化合物的特性
①形成化合物种类最多的元素、单质是自然界中存在的硬度最大的物质的元素、气态氢化物中氢的质量分
数最大的元素:C。
②空气中含量最多的元素、气态氢化物水溶液呈碱性的元素:N。
③地壳中含量最多的元素:O。
④常见的具有漂白性的物质:氯水、SO 、NaO、双氧水等。
2 2 2
⑤单质是最活泼的非金属元素、无正价的元素或无含氧酸的非金属元素、气态氢化物的水溶液可腐蚀玻璃
的元素、气态氢化物最稳定的元素、阴离子还原性最弱的元素:F。
⑥单质密度最小的元素:H;密度最小的金属元素:Li。
⑦常温下单质呈液态的非金属元素:Br;金属元素:Hg。
⑧最高价氧化物及其水化物既能与强酸又能与强碱反应的元素:Al。
⑨元素的气态氢化物和它的最高价氧化物对应的水化物能化合的元素:N;能发生氧化还原反应的元素:
S。
○元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
第三部分:典型例题剖析
高频考点1 考查元素周期表的结构及应用
例1.(2021·全国·高三专题练习)1869年俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元
素间的内在联系,成为化学发展史上重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表有7个横行、18个纵列,即有7个周期、18个族
B.在过渡元素中寻找半导体材料
C.俄罗斯专家首次合成了X原子,116号元素位于元素周期表中第7周期ⅥA族
D.ⅠA族的元素全部是金属元素【解析】元素周期表中的Ⅷ族包含8、9、10共3个纵列,因此元素周期表虽然共18个纵列,但共16个族,
A错误;在金属元素和非金属元素的分界线附近寻找半导体材料,B错误;第7周期0族元素为118号,
则116号元素位于元素周期表中第7周期ⅥA族,C正确;ⅠA族的元素包括H和碱金属元素,D错误。
【答案】C
【方法技巧】元素周期表结构巧记口诀
横行叫周期,现有一至七,四长三个短,全部已填满。
纵列称为族,共有十六族,一八依次现①,一零再一遍②。
一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。
镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。
说明:①指ⅠA族、ⅡA族、ⅢB族、ⅣB族、ⅤB族、ⅥB族、ⅦB族、Ⅷ族;
②指ⅠB族、ⅡB族、ⅢA族、ⅣA族、ⅤA族、ⅥA族、ⅦA族、0族。
【变式训练】(2021·湖南汨罗市高三检测)某同学在研究前18号元素时发现,可以将它们排成如下图所示的
“蜗牛”形状,图中每个“·”代表一种元素,其中O点(最中心的点)代表起点元素。下列正确的是( )
A.物质YO可能具有较强的氧化性
B.图中离O点越远的元素,其原子半径一定越大
C.OX、WO 分子内都含有氢键,所以沸点都较高
2 3
D.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的Z元素
【解析】O点代表氢元素,按照原子序数由小到大由里往外延伸,由图可知,W为N元素,X为O元素,
Y为Na元素,Z为P元素,根据元素的种类可知虚线相连的元素处于同一族。A.NaH中氢元素为-1价,
具有较强的还原性,故A错误;B.随原子序数增大距离O点的距离增大,而同周期主族元素,随原子序数
增大原子半径减小,图中离O点越远的元素,其原子半径不一定越大,故 B错误;C.H O、NH 分子间都
2 3
含有氢键,所以沸点都较高,而分子内为共价键,故 C错误;D.As与N元素处于同主族,性质具有相似
性,该As元素最有可能取代了普通DNA链中的Z元素,故D正确。
【答案】D
高频考点2 考查元素在周期表中的位置推断
例2.(2021·全国·高三专题练习)国际理论与应用化学联合会已正式确定了第114号和第116号元素的名称
缩写为Fl、Lv。下列有关这两种元素的说法错误的是( )
A.两种元素位于同一周期B.116号元素位于第ⅥA族
C.两种元素都是活泼的非金属元素
D.114号元素的原子半径比116号元素的大
【解析】A.第114号元素和第116号元素都处于第七周期,A正确;B.118号元素位于0族,则116号
元素位于第ⅥA族,B正确;C.按金属与非金属的分界线划分,第七周期中,只有118号元素为非金属
元素,其余元素都为金属元素,所以114和116号元素都是金属元素,C不正确;D.114号元素和116号
元素为同周期元素,114号元素位于左边,原子半径比116 号元素大,D正确;故选C。
【答案】C
【名师点睛】判断第七周期元素所在周期表中的位置时,常采用倒推法,从118号元素为0族元素开始倒
推,比书写电子排布式更简单。由稀有气体元素的原子序数确定元素在周期表中位置
①原子序数-最邻近的稀有气体元素的原子序数=ΔZ。
②若ΔZ<0,则与稀有气体元素同周期,族序数为8-|ΔZ|;
③若ΔZ>0,则在稀有气体元素下一周期,族序数为ΔZ。
【变式训练】(2022·上海青浦·一模)在短周期元素中,原子最外电子层只有1个或2个电子的元素
A.是非金属元素 B.是稀有气体元素 C.是金属元素 D.无法确认为哪一类元素
【解析】在短周期元素中,原子最外电子层只有1个或2个电子的元素 可能是金属元素(二、三周期),
也可能是非金属元素(第一周期),也可能是稀有气体元素,所以无法确定是哪一种元素,答案选D。
【答案】D
高频考点3 考查金属性、非金属性的强弱比较
例3.(2022·辽宁·东北育才学校三模)下列不能说明氯元素的非金属性比硫元素强的有
①气态HCl比气态HS稳定
2
②HCl溶液的酸性比HS溶液强
2
③沸点:HS>HCl
2
④HS的还原性比HCl强
2
⑤Cl 转化为Cl-得电子的数目比S转化为S2-得电子的数目多
2
⑥铁与Cl 反应生成FeCl ,铁与S反应生成FeS
2 3
⑦Cl 可以和NaS反应生成S
2 2
⑧根据S和Cl 化合生成SCl 中元素化合价判断
2 2
⑨HClO的氧化性比HSO 强
2 4
A.3项 B.4项 C.5项 D.6项
【解析】①同周期从左到右,金属性减弱,非金属性变强,根据非金属性越强,其简单氢化物稳定性越强,气态HCl比气态HS稳定,能说明氯元素的非金属性比硫元素强;
2
②应该比较最高价氧化物对应水化物的酸性强弱,HCl溶液的酸性比HS溶液强,不能说明氯元素的非金
2
属性比硫元素强;③沸点大小,不能说明氯元素的非金属性比硫元素强;④两者为简单氢化物,HS的还
2
原性比HCl强,说明硫离子的还原性强,则硫单质的氧化性弱,能说明氯元素的非金属性比硫元素强;⑤
得电子的数目不是判断非金属性强弱得方法,应该是判断得电子难易程度,故不能说明氯元素的非金属性
比硫元素强;
⑥铁与Cl 反应生成FeCl ,铁与S反应生成FeS,说明氯得电子能力更强,能说明氯元素的非金属性比硫
2 3
元素强;⑦Cl 可以和NaS反应生成S,说明氯气的氧化性大于硫,得电子能力大于硫,能说明氯元素的
2 2
非金属性比硫元素强;⑧根据S和Cl 化合生成SCl 中元素化合价判断,该化合物中氯显负价,说明得电
2 2
子能力更强,能说明氯元素的非金属性比硫元素强;⑨HClO中氯元素不是最高价态,HClO的氧化性比
HSO 强,不能说明氯元素的非金属性比硫元素强;综上所述共4项不能说明氯元素的非金属性比硫元素
2 4
强;故选B
【答案】B
【易错提醒】规避金属性和非金属性判断中的易错点:(1)关注关键词“最高价”,根据元素氧化物对应水
化物的酸碱性的强弱判断元素非金属性或金属性的强弱时,必须是其最高价氧化物的水化物。(2)关注关键
词“难易”,判断元素非金属性或金属性的强弱,依据是元素原子在化学反应中得失电子的难易而不是得
失电子的多少。
【变式训练】(2022·上海市杨浦高级中学高三阶段练习)不能说明碳的非金属性比硅强的是
A.同浓度溶液碱性: NaSiO>NaCO
2 3 2 3
B.键的极性: C-H>Si-H
C.高温下C和SiO 反应生成Si和CO
2
D.SiC中Si是+4价,C是-4价
【解析】A.同浓度溶液碱性:NaSiO>NaCO,则酸性HSiO<HCO,从而表明非金属性碳比硅强,
2 3 2 3 2 3 2 3
A不符合题意;B.键的极性:C-H>Si-H,且共用电子对偏离于H,所以C的非金属性比Si强,B不符合
题意;C.高温下C和SiO 反应生成Si和CO,只能表明高温下C的还原性比Si强,不能表明碳的非金属
2
性比硅强,C符合题意;D.SiC中,由于Si的非金属性比C弱,所以Si显正价,C显负价,再据原子的
最外层电子数,可确定Si是+4价,C是-4价,D不符合题意;故选C。
【答案】C
高频考点4 考查微粒半径大小比较
例4.(2021·全国·高三专题练习)下列粒子半径大小的比较正确的是( )
A.Na+<Mg2+<Al3+<O2-B.S2->Cl->Na+>Al3+
C.Na<Mg<Al<S
D.Cs<Rb<K<Na
【解析】电子层数相同,原子序数越大,半径越小;电子层数不相同,电子层数越多,半径越大;当电子
层数和核电荷数相同时,核外电子数越多,半径越大。A.微粒半径大小关系为:Al3+<Mg2+<Na+<O2-,
A错误;B.微粒半径大小关系为:S2->Cl->Na+>Al3+,B正确;C.微粒半径大小关系为:S<Al<Mg<
Na,C错误;D.微粒半径大小关系为:Cs>Rb>K>Na,D错误;答案为B。
【答案】B
【方法技巧】微粒半径大小的比较规律:①层数相同,核大半径小。即电子层数相同时,结构相似的微粒
中核电荷数大的微粒半径小;②层异,层大半径大。即当微粒的电子层数不同时,结构相似的微粒中,电
子层数大的微粒半径大;③核同,价高半径小。即对同一种元素形成的不同的简单微粒中,化合价高的微
粒的半径小;④电子层结构相同,核电荷数大,则半径小。
【变式训练】(2021·全国·高三专题练习)下列粒子半径大小比较正确的是
A.Mg>Na>Li B.P>S>O
C.Na+<Mg2+<Al3+ D.O2-<F-<Cl-
【解析】A.同周期主族元素自左至右原子半径依次减小,所以半径Mg<Na,A错误;B.同周期主族元
素自左至右原子半径依次减小,所以半径P>S,同主族自上而下原子半径依次增大,所以半径S>O,即
原子半径P>S>O,B正确;C.电子层数相同时,核电荷数越小,离子半径越大,所以半径Na+>Mg2+>
Al3+,C错误;D.电子层数相同时,核电荷数越小,离子半径越大,所以半径O2->F-,D错误;综上所
述答案为B。
【答案】B
高频考点5 考查元素周期律、周期表的应用
例5.(2021·全国·高三专题练习)下列关于元素周期表应用的说法正确的是
A.为元素性质的系统研究提供指导,为新元素的发现提供线索
B.在金属与非金属的交界处,寻找可做催化剂的合金材料
C.在IA、IIA族元素中,寻找制造农药的主要元素
D.在过渡元素中,可以找到半导体材料
【解析】A.元素周期表是元素周期律的具体表现形式,它反映元素原子的内部结构和它们之间相互联系的
规律。为元素性质的系统研究提供指导,为新元素的发现及预测它们的原子结构和性质提供线索,故A正
确;B.在周期表中金属和非金属的分界处可以找到半导体材料,故B错误;C.通常制造农药的主要元素有
F、Cl、S、P等元素,并不在IA、IIA族元素中,故C错误;D.在过渡元素中寻找耐高温、耐腐蚀的合金
材料,并不是半导体材料,故D错误;答案选A。【答案】A
【名师点睛】本题主要考查了周期表的意义,元素周期表在生产方面的应用表现在以下几个方面:①农药
多数是含Cl、P、S、N、As等元素的化合物。
②半导体材料都是周期表里金属与非金属交接界处的元素,如Ge、Si、Ga、Se等。
③催化剂的选择:人们在长期的生产实践中,已发现过渡元素对许多化学反应有良好的催化性能。
④耐高温、耐腐蚀的特种合金材料的制取:在周期表里从ⅢB到ⅣB的过渡元素,如钛、钽、钼、钨、铬,
具有耐高温、耐腐蚀等特点。它们是制作特种合金的优良材料,是制造火箭、导弹、宇宙飞船、飞机、坦
克等的不可缺少的金属。
⑤矿物的寻找:地球上化学元素的分布跟它们在元素周期表里的位置有密切的联系。科学实验发现如下规
律:相对原子质量较小的元素在地壳中含量较多,相对原子质量较大的元素在地壳中含量较少;偶数原子
序数的元素较多,奇数原子序数的元素较少。处于地球表面的元素多数呈现高价,处于岩石深处的元素多
数呈现低价;碱金属一般是强烈的亲石元素,主要富集于岩石圈的最上部;熔点、离子半径、电负性大小
相近的元素往往共生在一起,同处于一种矿石中。
【变式训练】(2021·全国·高三专题练习)下列关于元素周期表应用的说法正确的是( )
A.在过渡元素中,可以找到半导体材料
B.在元素周期表金属和非金属分界线附近可以寻找优良的催化剂
C.为元素性质的系统研究提供指导,为新元素的发现提供线索
D.在金属与非金属的交界处,寻找耐高温、耐腐蚀的合金材料
【解析】A.优良的催化剂含过渡金属元素,则在过渡元素中寻找优良的催化剂,而半导体材料应在金属
与非金属分界处寻找,故A错误;B.在元素周期表的金属和非金属分界线附近寻找半导体材料,催化剂
材料在过渡元素中寻找,故B错误;C.同周期、同族元素性质具有一定相似性、递变性,位置靠近的元
素性质相似,为新元素的发现和预测它们的原子结构和性质提供线索,故C正确;D.在金属与非金属的
交界处,是找到半导体材料,而不是耐高温、耐腐蚀的合金材料,故D错误;故答案为C。
【答案】C
高频考点6 考查位、构、性关系的综合推断
例6.(2022·福建省福州第一中学模拟预测)有M、A、B、D、N、E六种短周期元素原子序数依次增大,
M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期中最大的,A、B、D、E四种元素在周
期表中的相应位置如图所示,E的核电荷数是D的2倍。下列说法不正确的是A.沸点:MD>BM>AM
2 3 4
B.离子半径:r >r >r >r
E B D N
C.化合物AM 分子中既含有极性键又含有非极性键
n 2n
D.B元素的氢化物与D元素的单质在一定条件下能发生置换反应,且氧化剂与还原剂的物质的量之比为
4:3
【解析】由M元素的单质是自然界最轻的气体可得M元素为H元素,M、A、B、D、N、E短周期元素原
子序数依次增大且N元素的原子半径是所在周期中最大,则N为Na,不可能为Li。易知A、B、D位于第
二周期,E位于第三周期,由E的核电荷数是D的2倍可得,D为O元素,E为S元素。则B为N元素,
A为C元素。最终M、A、B、D、N、E六种短周期元素分别为H、C、N、O、Na、S元素。A. 比较沸点
可通过比较范德华力,以及氢键的影响(主要原因),一般情况下相对分子质量越大范德华力越大,沸点
越高,而如果存在氢键则含氢键的物质沸点更高。AM 为CH 只存在范德华力,而MD为HO、BM 为
4 4 2 2 3
NH 两者都存在范德华力以及氢键,都比CH 的沸要高、但水分子形成的氢键比氨气的氢键要强,因此水
3 4
的沸点大于氨气的沸点。最终可判断沸点大小:HO>NH >CH ,故A选项正确;B. 比较离子半径先看电
2 3 4
子层数,电子层数越多,半径越大;电子层数相同时,看电子数,电子数越多,半径越大;电子层数相同
且电子数相同时,看核电荷数,核电荷数越少,半径越大。N3-、O2-与Na+-电子层数相同均为2层,且电子
数相同均为10个电子,但N的核电荷数小于O小于Na,因此离子半径N3->O2-->Na+,而S2-电子层数为3
层,因此S2-半径最大。S2->N3->O2-->Na+-,故离子半径:r >r >r >r ,故B选项正确;C. 共价化合物中根据
E B D N
同种原子间形成非极性共价键,不同种原子间形成极性共价键。化合物AM 为具有一个不饱和度的烃类
n 2n
物质,为共价化合物。其中必然存在碳碳单键、或者碳碳双键都均为非极性共价键、也必然存在碳氢单键,
为极性共价键。因此化合物AM 分子中既含有极性键又含有非极性键,故C选项正确;D. N元素的氢化
n 2n
物其中一种为NH ,D元素的单质可为O,可发生4NH +3O =2N +6H O置换反应,NH 中氮元素化合价
3 2 3 2 2 2 3
由-3价升高到0价,作还原剂。而O 中的氧元素为0价,降到-2价,作氧化剂。根据化学方程式系数可得
2
氧化剂与还原剂的物质的量之比为3:4,故D选项错误;故答案选D选项。
【答案】D
【方法归纳】直接相邻的“┳”型、“┻”型、“╋”型原子序数关系
(1)
(2)
(3)(4)
【变式训练】(2022·江西·上饶市第一中学模拟预测)短周期主族元素W、X、Y、Z原子序数依次增大,
在元素周期表中的相对位置如表所示,其中W元素(非氢元素)最高化合价与最低化合价代数和为0,Y元
素的原子最外层电子数是电子层数的2倍。下列说法不正确的是
A.原子半径大小:XY
C.W元素和氢元素形成的化合物可能与Z的氢化物反应
D.W的氢化物的熔沸点可能高于X的氢化物的熔沸点
【解析】由短周期元素W、X、Y、Z在元素周期表中的相对位置可知,Y元素的原子最外层电子数是电子
层数的2倍,Y位于第三周期可知Y为S,结合元素的相对位置可知,W为C,X为N,Y为S,Z为Cl。
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径为Y>Z>X,故A正确;B.
非金属性越强,对应最高价含氧酸的酸性越强,则最高价氧化物对应水化物的酸性:Z>Y,氧化物对应水化
物的酸性不一定符合,例如酸性HClO