文档内容
第 18 讲 化学键
目录
考情分析 知识点3 σ键与π键的判断
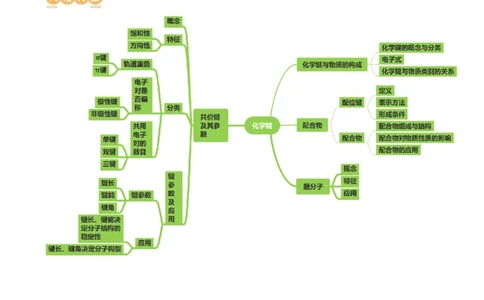
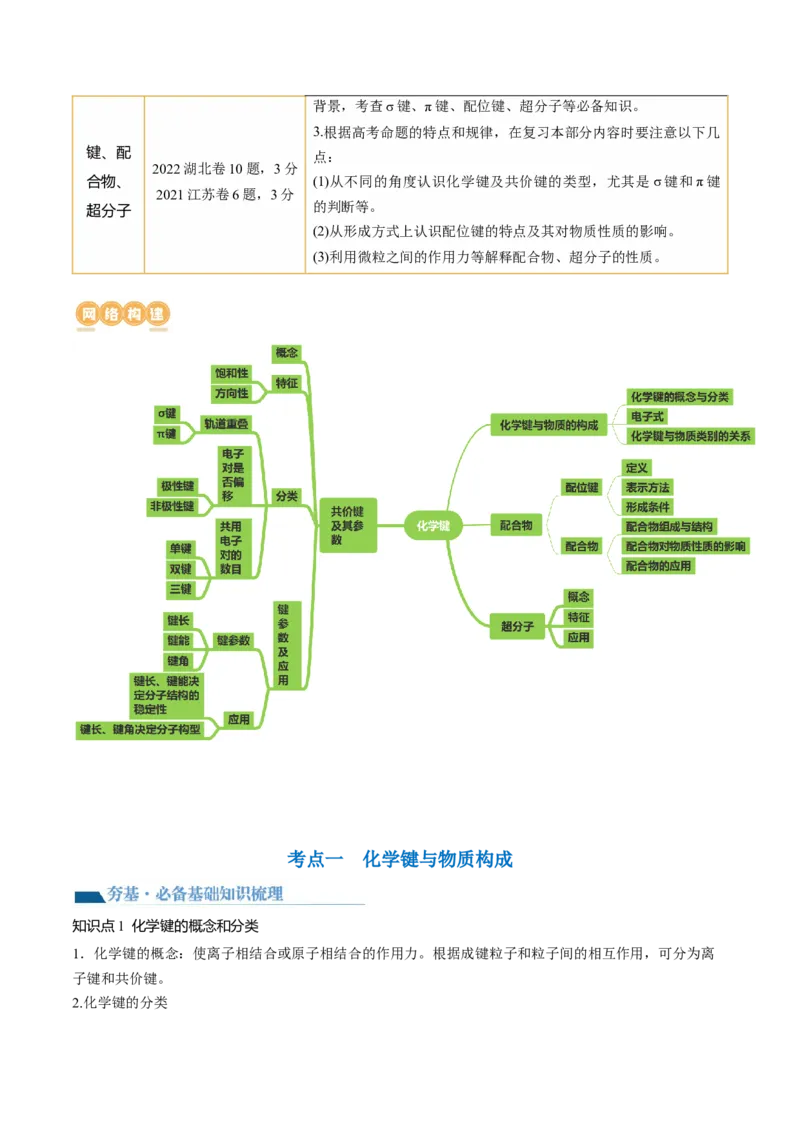
网络构建 知识点4 共价键的键参数
【提升·必考题型归纳】
考点一 化学键与物质构成
考向1 考查共价键的类别及判断
【夯基·必备基础知识梳理】
考向2 考查键参数及其应用
知识点1 化学键的分类
知识点2 电子式
考点三 配位键、配合物、超分子
知识点3 化学键与物质类别的关系
【夯基·必备基础知识梳理】
【提升·必考题型归纳】
知识点1 配位键的形成及配合物的性质
考向1 考查化学键的分类
知识点2 超分子
考向2 考查化学键与物质类别的关系
【提升·必考题型归纳】
考向1 考查配位键、配合物性质
考点二 共价键及其分类
考向2 考查超分子的结构、性质及其应用
【夯基·必备基础知识梳理】
知识点1 共价键的本质和特征
真题感悟
知识点2 共价键的分类
考点要求 考题统计 考情分析
分析近三年高考试题,高考命题在本讲有以下规律:
2023湖北卷5题,3分
化学键 1.从考查题型和内容上看,高考的命题规律主要为非选择题,在
2022湖南卷2题,3分
新高考试题中也会以选择题的形式考查,考查内容主要有以下三
与物质
2021江苏卷2题,3分
个方面:
构成
(1)借助具体的化学物质考查化学键类型(离子键、共价键、配位
共价键 2023山东卷5题,2分
键和金属键)的判断及形成,特别是σ键和π键的判断等;
及其分 2022天津卷4题,3分
(2)考查配位键的特点及其对物质性质的影响。
类
2021海南卷10题,2分
(3)考查超分子的结构、性质及其应用
配位 2023辽宁卷9题,3分 2.从命题思路上看,命题侧重结合新科技,新能源等社会热点为背景,考查σ键、π键、配位键、超分子等必备知识。
3.根据高考命题的特点和规律,在复习本部分内容时要注意以下几
键、配 点:
2022湖北卷10题,3分
合物、 (1)从不同的角度认识化学键及共价键的类型,尤其是σ键和π键
2021江苏卷6题,3分
的判断等。
超分子
(2)从形成方式上认识配位键的特点及其对物质性质的影响。
(3)利用微粒之间的作用力等解释配合物、超分子的性质。
考点一 化学键与物质构成
知识点1 化学键的概念和分类
1.化学键的概念:使离子相结合或原子相结合的作用力。根据成键粒子和粒子间的相互作用,可分为离
子键和共价键。
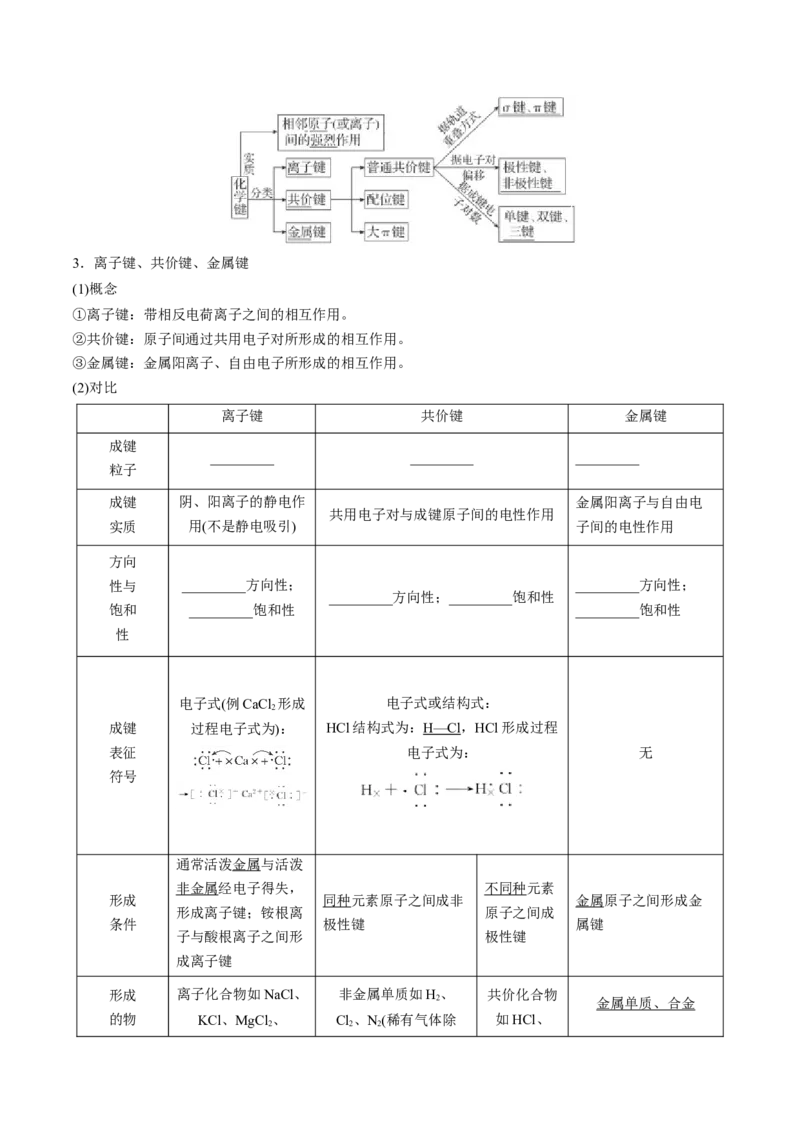
2.化学键的分类3.离子键、共价键、金属键
(1)概念
①离子键:带相反电荷离子之间的相互作用。
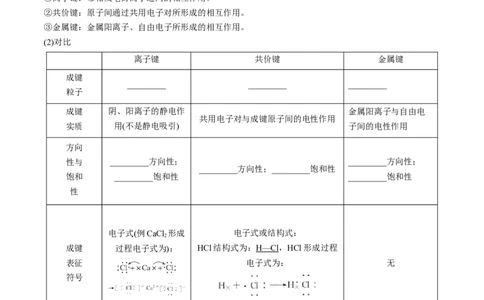
②共价键:原子间通过共用电子对所形成的相互作用。
③金属键:金属阳离子、自由电子所形成的相互作用。
(2)对比
离子键 共价键 金属键
成键
_________ _________ _________
粒子
成键 阴、阳离子的静电作 金属阳离子与自由电
共用电子对与成键原子间的电性作用
实质 用(不是静电吸引) 子间的电性作用
方向
性与 _________方向性; _________方向性;
_________方向性;_________饱和性
饱和 _________饱和性 _________饱和性
性
电子式(例CaCl 形成 电子式或结构式:
2
成键 过程电子式为): HCl结构式为:H—Cl,HCl形成过程
表征 电子式为: 无
符号
通常活泼金属与活泼
非金属经电子得失, 不同种元素
形成 同种元素原子之间成非 金属原子之间形成金
形成离子键;铵根离 原子之间成
条件 极性键 属键
子与酸根离子之间形 极性键
成离子键
形成 离子化合物如NaCl、 非金属单质如H、 共价化合物
2 金属单质、合金
的物 KCl、MgCl 、 Cl、N(稀有气体除 如HCl、
2 2 2CO、CH
2 4
外);某些共价化合物 或离子化合
CaCl 、ZnSO、
2 4
质 (如HO)或离子化合物 物如
2 2
NaOH等
(如NaO) NaOH、
2 2
NH Cl
4
4.化学键类型的判断
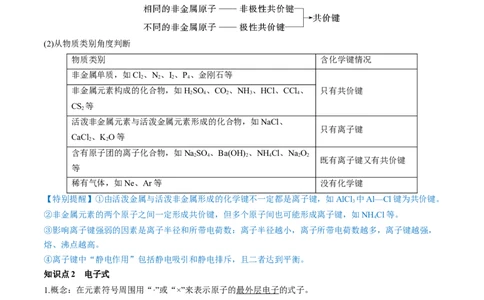
(1)从物质构成角度判断
(2)从物质类别角度判断
物质类别 含化学键情况
非金属单质,如Cl、N、I、P、金刚石等
2 2 2 4
非金属元素构成的化合物,如HSO 、CO、NH 、HCl、CCl 、 只有共价键
2 4 2 3 4
CS 等
2
活泼非金属元素与活泼金属元素形成的化合物,如NaCl、
只有离子键
CaCl 、KO等
2 2
含有原子团的离子化合物,如NaSO 、Ba(OH) 、NH Cl、NaO
2 4 2 4 2 2
既有离子键又有共价键
等
稀有气体,如Ne、Ar等 没有化学键
【特别提醒】①由活泼金属与活泼非金属形成的化学键不一定都是离子键,如AlCl 中Al—Cl键为共价键。
3
②非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键,如NH Cl等。
4
③影响离子键强弱的因素是离子半径和所带电荷数:离子半径越小,离子所带电荷数越多,离子键越强,
熔、沸点越高。
④离子键中“静电作用”包括静电吸引和静电排斥,且二者达到平衡。
知识点2 电子式
1.概念:在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
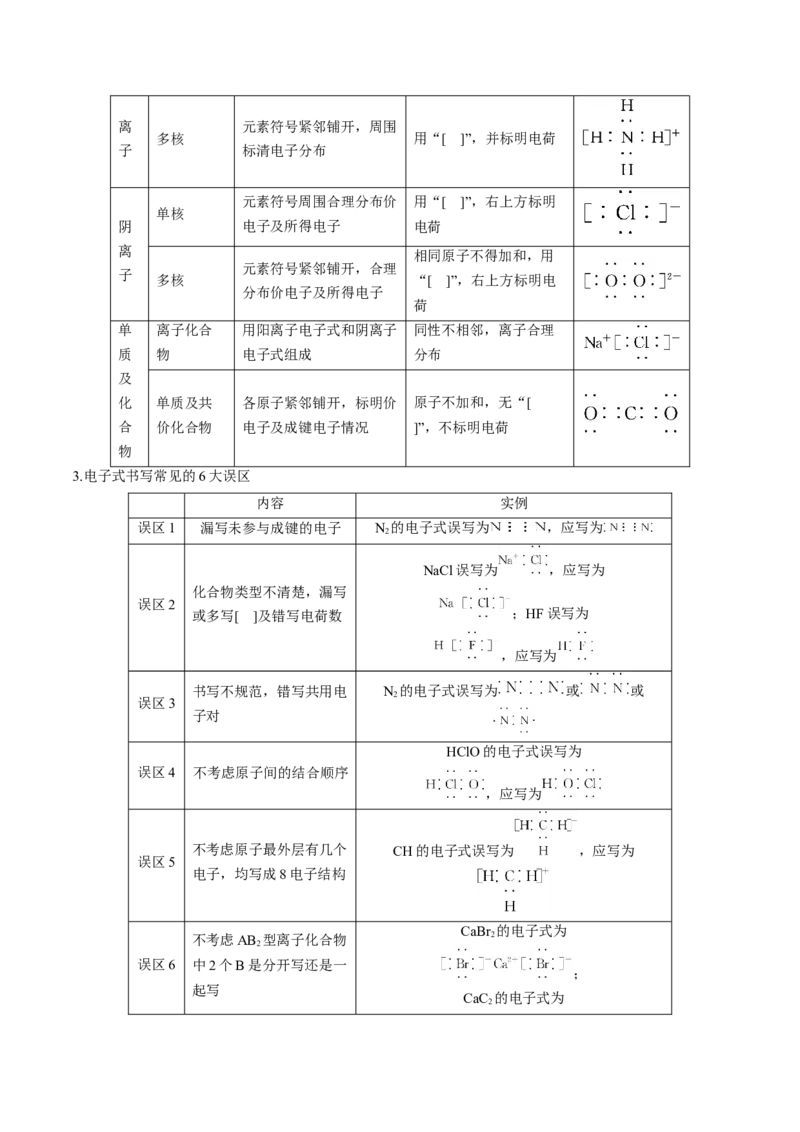
2.电子式的书写
粒子的种类 电子式的表示方法 注意事项 举例
价电子少于4时以单电
原子 元素符号周围标有价电子 子分布,多于4时多出
部分以电子对分布
阳 单核 离子符号 右上方标明电荷 Na+离 元素符号紧邻铺开,周围
多核 用“[ ]”,并标明电荷
子 标清电子分布
元素符号周围合理分布价 用“[ ]”,右上方标明
单核
阴 电子及所得电子 电荷
离
相同原子不得加和,用
元素符号紧邻铺开,合理
子
多核 “[ ]”,右上方标明电
分布价电子及所得电子
荷
单 离子化合 用阳离子电子式和阴离子 同性不相邻,离子合理
质 物 电子式组成 分布
及
化 单质及共 各原子紧邻铺开,标明价 原子不加和,无“[
合 价化合物 电子及成键电子情况 ]”,不标明电荷
物
3.电子式书写常见的6大误区
内容 实例
误区1 漏写未参与成键的电子 N 的电子式误写为 ,应写为
2
NaCl误写为 ,应写为
化合物类型不清楚,漏写
误区2
或多写[ ]及错写电荷数 ;HF误写为
,应写为
书写不规范,错写共用电 N 的电子式误写为 或 或
2
误区3
子对
HClO的电子式误写为
误区4 不考虑原子间的结合顺序
,应写为
不考虑原子最外层有几个 CH的电子式误写为 ,应写为
误区5
电子,均写成8电子结构
CaBr 的电子式为
不考虑AB 型离子化合物 2
2
误区6 中2个B是分开写还是一
;
起写
CaC 的电子式为
24.用电子式表示化合物的形成过程
①离子化合物:左边是原子的电子式,右边是离子化合物的电子式,中间用“―→”连接,相同的原子或
离子不合并。
如NaCl: 。
②共价化合物:左边是原子的电子式,右边是共价化合物的电子式,中间用“―→”连接。
如HCl: 。
5.陌生电子式书写方法
①确定该物质是属于共价化合物还是离子化合物;
②确定该物质中各原子的成键方式;
③根据各原子最外层电子数和成键后各原子达到最外层8(或2)电子稳定结构的要求,分析各原子共用电子
对的情况;
④根据化合物类型、成键方式和原子稳定结构的分析,书写电子式。
知识点3 化学键与物质类别的关系
1.离子化合物与共价化合物
(1)离子化合物与共价化合物的比较
项目 离子化合物 共价化合物
定义 含有_________的化合物 只含有_________的化合物
构成微粒 _________ _________
一定含有_________,可能含有
化学键类型 只含有_________
_________
①含氧酸
①强碱 ②弱碱
②绝大多数盐 ③非金属气态氢化物
物质类别
③金属氧化物 ④非金属氧化物
个例:NaH、CaC 、MgN ⑤极少数盐,如AlCl
2 3 2 3
⑥多数有机物
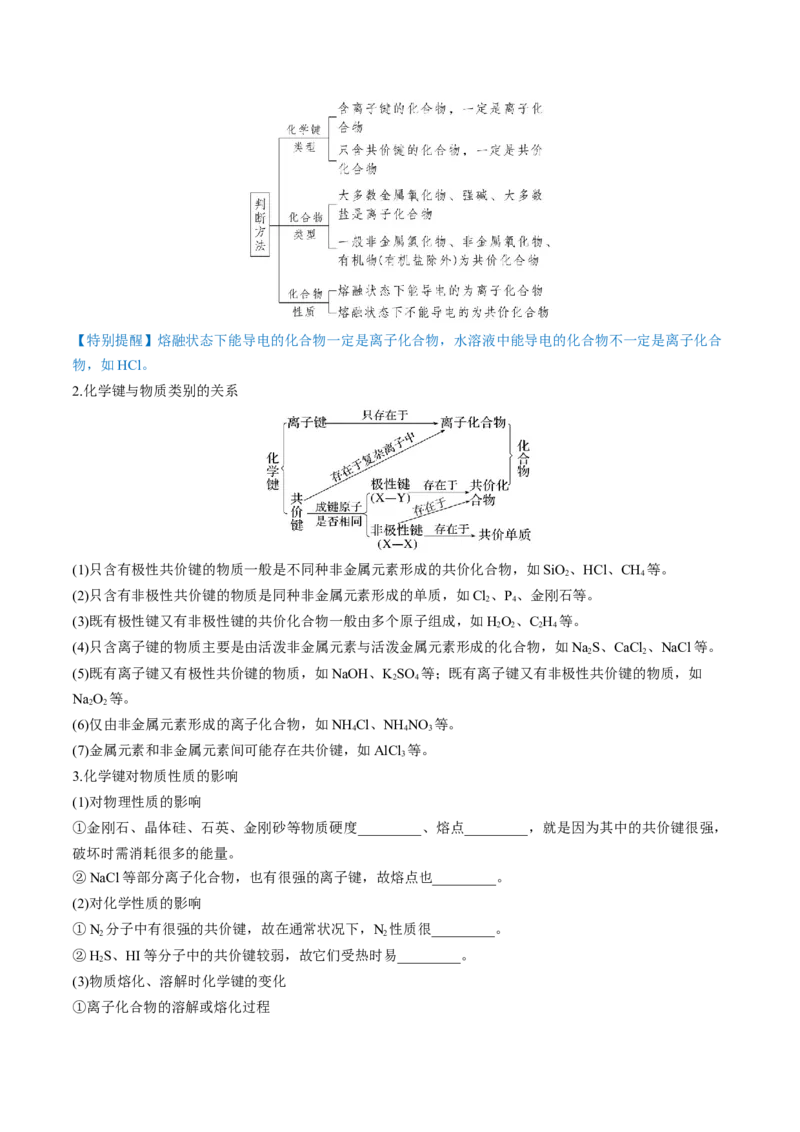
(2)离子化合物和共价化合物的判断方法【特别提醒】熔融状态下能导电的化合物一定是离子化合物,水溶液中能导电的化合物不一定是离子化合
物,如HCl。
2.化学键与物质类别的关系
(1)只含有极性共价键的物质一般是不同种非金属元素形成的共价化合物,如SiO、HCl、CH 等。
2 4
(2)只含有非极性共价键的物质是同种非金属元素形成的单质,如Cl、P、金刚石等。
2 4
(3)既有极性键又有非极性键的共价化合物一般由多个原子组成,如HO、C H 等。
2 2 2 4
(4)只含离子键的物质主要是由活泼非金属元素与活泼金属元素形成的化合物,如NaS、CaCl 、NaCl等。
2 2
(5)既有离子键又有极性共价键的物质,如NaOH、KSO 等;既有离子键又有非极性共价键的物质,如
2 4
NaO 等。
2 2
(6)仅由非金属元素形成的离子化合物,如NH Cl、NH NO 等。
4 4 3
(7)金属元素和非金属元素间可能存在共价键,如AlCl 等。
3
3.化学键对物质性质的影响
(1)对物理性质的影响
①金刚石、晶体硅、石英、金刚砂等物质硬度_________、熔点_________,就是因为其中的共价键很强,
破坏时需消耗很多的能量。
②NaCl等部分离子化合物,也有很强的离子键,故熔点也_________。
(2)对化学性质的影响
①N 分子中有很强的共价键,故在通常状况下,N 性质很_________。
2 2
②HS、HI等分子中的共价键较弱,故它们受热时易_________。
2
(3)物质熔化、溶解时化学键的变化
①离子化合物的溶解或熔化过程离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏。
②共价化合物的溶解过程
A.有些共价化合物溶于水后,能与水反应,其分子内共价键被破坏,如CO 和SO 等。
2 2
B.有些共价化合物溶于水后,与水分子作用形成水合离子,从而发生电离,形成阴、阳离子,其分子内
的共价键被破坏,如HCl、HSO 等。
2 4
C.某些共价化合物溶于水后,其分子内的共价键不被破坏,如蔗糖(C H O )、酒精(C HOH)等。
12 22 11 2 5
③单质的溶解过程
某些活泼的非金属单质溶于水后,能与水反应,其分子内的共价键破坏,如Cl、F 等。
2 2
考向1 考查化学键的分类
例1.(2023·江苏·统考二模)用NaCN溶液浸取矿粉中金的反应为
4Au+2HO+8NaCN+O=4Na[Au(CN) ]+4NaOH。下列说法正确的是
2 2 2
A.HO的空间结构为直线形 B.NaCN中含有离子键和共价键
2
C.1mol[Au(CN) ]-中含有2molσ键 D.NaOH的电子式为
2
【变式训练1】(2022·上海宝山·上海市行知中学校考模拟预测)氮化钠和氢化钙都是离子化合物,与水反
应的化学方程式(末配平)如下: , 。有关它们的
叙述正确的是
A.离子半径的大小:
B.它们与水发生的反应均属于氧化还原反应
C.两种化合物均只含离子键,不含共价键
D.两固体混合物溶于足量盐酸中可得到两种盐
【变式训练2】(2022·上海徐汇·统考三模)下列各组物质中,化学键类型和晶体类型都相同的是
A.Ar和K B.NaCl和NaOH C. 和 D. 和
考向2 考查化学键与物质类别的关系
例2.(2023·浙江杭州·浙江省临安中学校联考一模)熔融状态下能导电且含有极性共价键的化合物是
A. B. C. D.
【变式训练1】(2023·上海静安·统考二模)下列离子化合物含有共价键的是
A.NaO B.CaCl C.KS D.Al O
2 2 2 2 2 3
【变式训练2】(2022·浙江·校联考模拟预测)下列物质中含有极性共价键的离子化合物是
A. B. C. D.
考点二 共价键及其分类知识点1 共价键的本质和特征
1.本质:在原子之间形成共用电子对(电子云的重叠)。
2.特征:具有饱和性和方向性。
知识点2 共价键的分类
分类依据 类型
σ键 电子云“头碰头”重叠
形成共价键的原子轨道重叠方式
π键 电子云“肩并肩”重叠
极性键 共用电子对发生偏移
形成共价键的电子对是否偏移
非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
三键 原子间有三对共用电子对
知识点3 共价键类型的判断
(1)σ键与π键
①依据键强度判断:σ键的强度较大,较稳定;π键活泼,比较容易断裂。
②由物质结构式判断:共价单键都是_________键,共价双键中含有1个_________键、1个_________键,共
价叁键中含有1个_________键、2个_________键。
③由成键轨道类型判断:s轨道形成的共价键全部是_________键;杂化轨道形成的共价键全部为
_________键。
(2)极性键与非极性键
看形成共价键的两原子,不同种元素的原子之间形成的是极性共价键,同种元素的原子之间形成的是非极性
共价键。
【特别提醒】 (1)只有两原子的电负性相差不大时,才能形成共用电子对,形成共价键,当两原子的电负
性相差很大(大于1.7)时,不会形成共用电子对,而形成离子键。
(2)同种元素原子间形成的共价键为非极性键,不同种元素原子间形成的共价键为极性键。
(3)通过物质的结构式,可以快速有效地判断键的种类及数目;判断成键方式时,需掌握:共价单键全为 σ
键,共价双键中有一个σ键和一个π键,共价三键中有一个σ键和两个π键。
知识点4 共价键的键参数
1.概念
①键能:气态基态原子形成1 mol化学键释放的最低能量。
②键长:形成共价键的两个原子之间的核间距。
③键角:两个共价键之间的夹角。
2.键参数对分子性质的影响
①键能越大,键长越短,分子越稳定。②
(3)利用键能(E)计算ΔH的公式:ΔH=E(反应物)-E(生成物)。
【归纳总结】比较键角大小的三种思维模型
(1)杂化轨道类型不同:sp>sp2>sp3。
(2)
(3)在同一分子中,π键电子斥力大,键角大。
考向1 考查共价键的类别及判断
例1.(2023·湖北·校联考模拟预测)科学研究发现新型含碳化合物 和 ,它们的结构类似 ,
均为直线形分子。下列结论中错误的是
A. 是非极性分子, 与 也是非极性分子
B. 、 、 分子中碳原子的杂化方式均为
C. 、 分子中 键与 键的数目之比均为
D. 、 分子中所有原子最外层均满足8电子稳定结构
【变式训练】(2023·重庆·统考三模) (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关
该物质说法错误的是
A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角小
D.铵铁蓝中的配体是 ,该配体中的 键与 键之比是1:2
考向2 考查键参数及其应用
例2.(2023·江苏扬州·统考三模) 可用于钾离子电池的负极材料。冶炼铜时可使 在高温下与
反应转化为 ,生成的 与 进一步反应得到Cu。 在酸性溶液中会转化为Cu和 ;
能被浓硝酸氧化为 。Cu在 存在下能与氨水反应生成 ; 能与
NaOH反应生成 。 、 的沸点分别为 ℃、 ℃。下列说法正确的是
A. 的键角比 的大 B.H—O的键长比H—S的长C. 吸引电子的能力比 的强 D. 分子间作用力比 的大
【变式训练】(2023·辽宁大连·育明高中校考一模)关于 的结构与性质,下列说
法错误的是
A.热稳定性: B. 存在顺反异构现象
C.键角: D. 的沸点依次降低
考点三 配位键、配合物、超分子
知识点1 配位键的形成及配合物的性质
1.孤电子对
分子或离子中没有跟其他原子共用的电子对称孤电子对。
2.配位键
①配位键定义:由一个原子提供孤电子对与另一个接受孤电子对的原子形成的共价键。配位键属于σ键。
②配位键的形成:成键原子一方提供孤电子对,另一方提供空轨道形成共价键。
③成键的性质:共用电子对对两个原子的电性作用。
④配位键的表示:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如NH可表示为 ,在
NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不同,但是一旦形成之后,4个共价键
就完全相同。
⑤配位键的形成条件:
a.配体有孤电子对,如HO、NH 、CO、F-、Cl-、CN-等。
2 3
b.中心原子有空轨道,如Fe3+、Cu2+、Zn2+、Ag+等。
3.配合物
如[Cu(NH )]SO :
3 4 4
(1)中心原子:提供_________接受_________的原子叫中心原子。中心原子一般是带正电荷的金属离子(此
时又叫中心离子),过渡元素最常见
如:Fe3+、Cu2+、Zn2+、Ag+。
(2)配位体:含有并_________的分子或离子,即电子对的给予体。常见的配位体:HO、NH 、SCN-、
2 3
CO、N、X-、OH-、CN-。
2
(3)配位原子:配体中提供孤对电子的原子叫配位原子,如:HO中的O原子,NH 中的N原子。
2 3
(4)配离子:由中心原子(或离子)和配位体组成的离子叫做配离子,如:[Cu(NH )]2+、[Ag(NH)]+。
3 4 3 2
(5)配位数:作为配位体直接与中心原子结合的离子或分子的数目,即形成的配位键的数目称为配位数。如:
[Cu(NH )]2+的配位数为4,[Ag(NH)]+的配位数为2。
3 4 3 2
(6)配离子的电荷数:配离子的电荷数等于中心离子和配位体电荷数的代数和。(7)内界和外界:配合物分为内界和外界,其中配离子称为内界,与内界发生电性匹配的阳离子(或阴离子)
称为外界,如:[Cu(NH )]SO 的内界是[Cu(NH )]2+,外界是SO,配合物在水溶液中电离成内界和外界两
3 4 4 3 4
部分。
即:[Cu(NH )]SO ===[Cu(NH)]2++SO,而内界很难电离,其电离程度很小,[Cu(NH )]2+ Cu2++
3 4 4 3 4 3 4
4NH 。
3
4.配合物的形成对性质的影响
①溶解性:一些难溶于水的金属氯化物、溴化物、碘化物等可溶于含过量的氯离子、溴离子、碘离子和氨
的溶液中,形成可溶的配合物。如:
②颜色:当简单离子形成配合物时,颜色往往会发生变化。如黄色的铁离子溶液与硫氰酸根配合,就形成
血红色的溶液。
③稳定性增强:对于配位化合物稳定性由配位键的强弱决定;配位键的强弱取决于配位体给电子的能力,
配位体给出电子能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定,如:N元素电
负性比O元素电负性小,N原子提供孤电子对的倾向更大,与Co2+形成的配位键更强。配位键的强弱还与
中心粒子空轨道的数目、空间构型,配体空间结构等因素有关,如果形成环状配离子或配体体积较大,则
空轨道数目较多的原子或阳离子才能形成稳定的配离子。
6.配合物的应用
超过百万种的配合物在医药科学、化学催化剂、新型分子材料等领域有广泛的应用。
(1)在生命体中的应用
(2)在生产生活中的应用
(3)在医药中的应用——抗癌药物 、 。
知识点2 超分子
1.概念:由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
【易错提醒】超分子定义中的分子是广义,包括离子。
2.微粒间作用力—非共价键:超分子内部分子之间通过非共价键结合,主要是静电作用、范德华力和氢键、
疏水作用以及一些分子与金属离子之间形成的弱配位键。
3.分子聚集体的大小:超分子这种分子聚集体,有的是有限的,有的是无限伸展的。
4.特征
(1)分子识别
(2)自组装:超分子组装的过程称为分子自组装(Molecular self-assembly),自组装过程(Self-organization)
是使超分子产生高度有序的过程。
5.应用实例(1) “杯酚”分离C 和C :杯酚与C60通过范德华力相结合,通过尺寸匹配实现分子识别。向C 和C 的
60 70 60 70
混合物中加入一种空腔大小适配C 的“杯酚”,再加入甲苯溶剂,溶解未装入“杯酚”的C ,过滤后分离
60 70
C ;再向不溶物中加入氯仿,溶解“杯酚”而将不溶解的C 释放出来并沉淀。
70 60
(2)冠醚识别碱金属离子:冠醚是皇冠状的分子,有不同大小的空穴,能与正离子,尤其是碱金属离子络合,
并随环的大小不同而与不同的金属离子络合,利用此性质可以识别碱金属离子。冠醚环的大小与金属离子
匹配,将阳离子以及对应的阴离子都带入有机溶剂,因而成为有机反应中很好的催化剂。
(3)细胞和细胞器的双分子膜:细胞膜的两侧都是水溶液,水是极性分子,而构成膜的两性分子的头基是极
性基团而尾基是非极性基团。头基为亲水基团,头部会朝向水溶液一侧,从而实现自组装。
(4)DNA分子:核酸的双螺旋结构是靠氢键来保持的。
6.超分子的未来发展
通过对超分子研究,人们可以模拟生物系统,复制出一些新材料,如:新催化剂、新药物、分子器件、
生物传感器等功能材料。
考向1 考查配位键、配合物性质
例1.(2023·安徽·校联考三模)DACP是我国科研工作者合成的一种新型起爆药,结构如图所示。下列关
于该物质的说法正确的是
A.Co3+的配体只有两种,配位数为6
B.1molDACP中含有20molσ键
C.NH 和 中心原子的杂化方式不同
3
D.NH 与 中的键角是前者大于后者
3
【变式训练】(2023·山东滨州·统考二模)整合剂能与人体内有毒的金属离子结合形成稳定整合物,从而
治疗与急性或慢性中毒相关的损伤。乙二胺四乙酸(EDTA)是常见的整合剂之一,其四价阴离子形成的整合
物结构如图,下列说法正确的是A.原子半径:O>N>C>H
B.N、C、O的氢化物分子间均存在氢键
C.Mn+的配位数为6,配位原子为N和O
D.整合物中每两个氮碳键 的夹角均为107.3°
考向2 考查超分子的结构、性质及其应用
例1.(2023·河北衡水·河北武邑中学校考模拟预测)冠醚是由多个二元醇分子之间失水形成的环状醚,X
是其中的一种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧
原子间能形成化学键.下列说法错误的是
A.X形成的晶体为分子晶体 B.Y中 与氧原子间形成的是离子键
C. 不能与X形成超分子 D.电负性:O>C>H>Li
【变式训练】(2023·海南海口·统考模拟预测)下表为几种短周期元素的原子半径及主要化合价。
元素代号 X Y Z Q
原子半径 1.86 1.60 1.02 0.74
最高正价
主要化合
价
最低负价
下列说法不正确的是
A.Y的第一电离能大于Z
B.在 与冠醚形成的超分子中存在范德华力
C.由X和Q两种元素组成的化合物可能含有共价键
D.Q的氢化物分子间含有氢键,所以氢化物稳定性Q>Z
1.(2022·北京·高考真题)由键能数据大小,不能解释下列事实的是
化学键
键能/ 411 318 799 358 452 346 222
A.稳定性: B.键长:
C.熔点: D.硬度:金刚石>晶体硅
2.(2022·湖南·高考真题)下列说法错误的是A.氢键,离子键和共价键都属于化学键
B.化学家门捷列夫编制了第一张元素周期表
C.药剂师和营养师必须具备化学相关专业知识
D.石灰石是制造玻璃和水泥的主要原料之一
3.(2023·山东·统考高考真题)石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF) ,该物
2 x
质仍具润滑性,其单层局部结构如图所示。下列关于该化合物的说法正确的是
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中 的键长比 短
x
D.1mol(CF) 中含有2xmol共价单键
x
4.(2023·湖北·统考高考真题)化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示 的形成:
B.用离子方程式表示 溶于烧碱溶液:
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
5.(2023·辽宁·统考高考真题)某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、
Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电
子数的2倍。下列说法错误的是
A.W与X的化合物为极性分子 B.第一电离能
C.Q的氧化物是两性氧化物 D.该阴离子中含有配位键