文档内容
第 19 讲 电解池 金属的电化学腐蚀与防护
第一部分:高考真题感悟
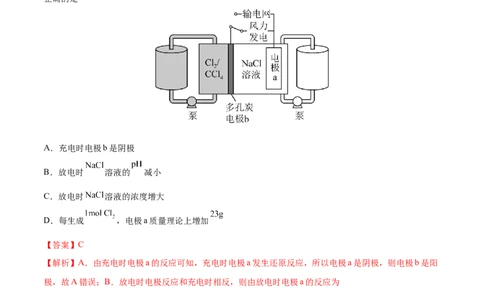
1.(2022·广东·高考真题)科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电
池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法
正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
【答案】C
【解析】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳
极,故A错误;B.放电时电极反应和充电时相反,则由放电时电极a的反应为
可知,NaCl溶液的pH不变,故B错误;C.放电时负极反应为
,正极反应为 ,反应后Na+和Cl-浓度都增大,则
放电时NaCl溶液的浓度增大,故C正确;D.充电时阳极反应为 ,阴极反应为,由得失电子守恒可知,每生成1molCl ,电极a质量理论上增加
2
23g/mol 2mol=46g,故D错误;答案选C。
2.(2022·北京·高考真题)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间后阴
① 极表面有红色固体,气体减少。经检
验电解液中有
阴极表面未观察到气体,一段时间后
② 阴极表面有致密红色固体。经检验电
解液中无 元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B.①中检测到 ,推测可能发生反应:
C.随阴极析出 ,推测②中溶液 减少, 平衡逆移
D.②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
【答案】C
【解析】由实验现象可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚
铁离子、氢气和铜,一段时间后,铜离子在阴极失去电子发生还原反应生成铜;实验②中铜离子与过量氨
水反应生成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到比实验
①更致密的镀层。A.由分析可知,实验①时,铁会先与溶液中的氢离子、铜离子反应,当溶液中氢离子
浓度减小,反应和放电生成的铜覆盖铁电极,阻碍氢离子与铁接触,导致产生的气体减少,故A正确;
B.由分析可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、
氢气和铜,可能发生的反应为 ,故B正确;C.由分析可知,四氨合
铜离子在阴极得到电子缓慢发生还原反应生成铜,随阴极析出铜,四氨合铜离子浓度减小,
平衡向正反应方向移动,故C错误;D.由分析可知,实验②中铜离子与过量氨水反应生成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到
比实验①更致密的镀层,故D正确;故选C。
3.(2022·辽宁·高考真题)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时 透过多孔活性炭电极向 中迁移
C.放电时每转移 电子,理论上 吸收
D.充电过程中, 溶液浓度增大
【答案】A
【解析】放电时负极反应: ,正极反应:Cl+2e-=2Cl-,消耗氯气,
2
放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl。A. 放电时负极失电子,发生氧化反应,电极反应:
2
,故A正确;B. 放电时,阴离子移向负极,放电时 透过多孔
活性炭电极向NaCl中迁移,故B错误;C. 放电时每转移 电子,正极:Cl+2e-=2Cl-,理论上 释
2
放 ,故C错误;D. 充电过程中,阳极:2Cl--2e-=Cl,消耗氯离子, 溶液浓度减小,故D
2
错误;故选A。
4.(2022·海南·高考真题)一种采用 和 为原料制备 的装置示意图如下。下列有关说法正确的是
A.在b电极上, 被还原
B.金属Ag可作为a电极的材料
C.改变工作电源电压,反应速率不变
D.电解过程中,固体氧化物电解质中 不断减少
【答案】A
【解析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此b为
2 3
阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2-+4e-=O ;A.由分析可得,b
2 2 3 2
电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还原,A正确;B.a为阳
2 3 2
极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;C.改变工作电源的电压,电流强度
发生改变,反应速率也会改变,C错误;D.电解过程中,阴极电极反应式为N+3H O+6e-=2NH+3O2-,阳
2 2 3
极电极反应式为2O2-+4e-=O ,因此固体氧化物电解质中O2-不会改变,D错误;答案选A。
2
5.(2022·湖北·高考真题)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图
所示( 为甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
【答案】D
【解析】A.石墨电极发生反应的物质:P→ 化合价升高发生氧化反应,所以石墨电极为阳极,
4
对应的电极反应式为: ,则生成 ,理论上外电路需要转移
电子,A错误;B.阴极上发生还原反应,应该得电子, 为阳极发生的反应, B
错误;C.石墨电极:P→ 发生氧化反应,为阳极,铂电极为阴极, 应该向阳极移动,即
4
移向石墨电极,C错误;D.由所给图示可知HCN在阴极放电,产生 和 ,而HCN中的H来自
,则电解产生的 中的氢元素来自于 ,D正确;故选D。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·新疆·二模)电解合成1 ,2-二氯乙烷的实验装置如图所示。下列说法中不正确的是
A.a为电源正极B.该装置总反应为CH =CH +2NaCl+2H O ClCH CHCl+2NaOH+H
2 2 2 2 2 2
C.X、Y依次为阳离子交换膜、阴离子交换膜
D.液相反应为CH =CH +2CuCl = ClCH CHCl+ 2CuCl(s)
2 2 2 2 2
【答案】C
【解析】图中电源b端所连电极发生反应2HO+2e-=H ↑+2OH-,说明这一极为电解池的阴极,b为电源负
2 2
极,NaCl溶液中的Na+通过阳离子交换膜Y进入右侧阴极区生成NaOH,NaCl溶液中的Cl-通过阴离子交
换膜X进入左侧阳极区发生反应CH =CH +2Cl--2e- = ClCH CHCl。A.据分析可知Cl-在此失电子被氧化,
2 2 2 2
因此a所连电极为电解质的阳极,a为电源正极,A选项正确;B.该装置中阳极反应式CH =CH +2Cl--2e-
2 2
= ClCH CHCl,阴极反应式2HO+2e-=H ↑+2OH-,总反应式为CH =CH +2NaCl+2H O
2 2 2 2 2 2 2
ClCH CHCl+2NaOH+H ,B选项正确;C.据题目分析可知X、Y依次为阴离子交换膜、阳离子交换膜,
2 2 2
C选项错误;D.由物质进出方向可知液相反应为CH =CH +2CuCl = ClCH CHCl+ 2CuCl(s),D选项正
2 2 2 2 2
确;故选 C。
2.(2022·江西·三模)“碳中和”大背景下,一种利用Ag-Cu纳米阴极将CO 电化学转化为C H 或
2 2 4
C HOH的装置如图所示。下列说法正确的是
2 5
A.M极应与外接电源的正极相连
B.装置中离子透过膜为阴离子透过膜
C.装置工作时,N极区SO 的浓度不变(N极为石墨电极)
D.M极生成乙醇的电极反应式为2CO+12H++12e-=C HOH+3H O
2 2 5 2
【答案】D
【解析】该装置为电解池装置,M极二氧化碳转变为乙烯、乙醇等,发生还原反应,故M极为阴极,N极
为阳极。阴极反应:2CO+12H++12e-=C HOH+3H O、2CO+12H++12e-=C H+4H O;阳极为水失电子生成
2 2 5 2 2 2 4 2氧气和氢离子,故氢离子通过交换膜向左移动,为阳离子交换膜。A.M极为阴极,与外接电源的负极相
连,A错误;B.由分析可知,为阳离子交换膜,B错误;C.阳极水失电子,氢离子向左迁移,水减少了,
硫酸根离子浓度增大,C错误;D.由分析可知生成乙醇的电极反应为2CO+12H++12e-=C HOH+3H O,D
2 2 5 2
正确;故选D。
3.(2022·甘肃平凉·二模)某科研小组研制了一种通过电解将草酸(HOOC-COOH)转化为羟基乙酸
(HOCHCOOH)的装置。固体聚合物为两面分别是以YO 为基质的阳极和TiO 涂覆的阴极,H+可通过固体
2 2 3 2
聚合物电解质。其装置如图所示,下列说法错误的是
A.电源的a极为负极
B.电解池工作时,H+通过固体聚合物电解质向右移动
C.为增强阳极电解液的导电性,可在水中添加适量NaSO
2 4
D.阴极上的电极反应式为HOOC-COOH+4H++4e-=HOCH COOH+H O
2 2
【答案】B
【解析】由外接电源,本题主要考查电解池相关知识。A.根据图示,电解池中右侧电极水失电子生成氧
气,右侧点击为电解池阳极,则电源的b极是正极、a极为负极,故A正确;B.电解池左侧为阴极、右侧
为阳极,电解池工作时,H+通过固体聚合物电解质向左(阴极)移动,故B错误;C.右侧电极水失电子生成
氧气,阳极电解液中添加适量NaSO ,电极反应不变,故C正确;D.阴极草酸得电子生成羟基乙酸,电
2 4
极反应式为HOOC-COOH+4H++4e-=HOCH COOH+H O,故D正确;选B。
2 2
4.(2022·四川凉山·三模)如图是利用KCl、NaNO 为原料制取KNO 和NaCl的电化学装置,A、C代表
3 3
不同类别的选择性离子通过膜,M、N为电极,下列有关说法中正确的是A.A为阳离子交换膜,C为阴离子交换膜
B.该装置中电子由电极b流向电极N,电极M流向电极a
C.电解总反应:KCl+NaNO KNO+NaCl
3 3
D.可以用纯铜作为M电极的材料
【答案】B
【解析】M极通入KCl溶液,N极通入NaNO 溶液,整个过程电解制取KNO 和NaCl,则M极上Cl-放电,
3 3
故M为阳极,N为阴极,阴极反应生成为2HO+2e-=H ↑+2OH-,阳极反应式为2Cl--2e-=Cl↑,左1室与右3
2 2 2
室均通入KCl溶液,右1室与左3室均通入NaNO 溶液,由于阳离子向阴极移动、阴离子向阳极移动,故
3
左3室中NO -通过膜A移向左2室、Na+通过膜C移向中间室(左4室),右3室中Cl-通过膜A移中间室(左
3
4室)、K+通过膜C移向右2室,在中间室获得NaCl,则左2室、右2室获得KNO,A膜为阴离子交换膜、
3
C膜为阳离子交换膜。A. 由分析C为阳离子交换膜,A为阴离子交换膜,故A错误;B. M为阳极,N
为阴极,该装置中电子由电极b流向电极N,电极M流向电极a,故B正确;C. 电解总反应:2Cl-+2H O
2
Cl↑+H ↑+2OH-,故C错误;D. 铜的还原性强于氯离子,M为阳极,不可以用纯铜作为M电极的材
2 2
料,故D错误;故选B。
5.(2022·四川雅安·三模)硬水除垢可以让循环冷却水系统稳定运行。某科研团队改进了主动式电化学硬
水处理技术,原理如图 (R表示有机物)所示。下列说法错误是A.a端为电源正极,处理后的水垢沉积在阴极底部
B.处理过程中C1-可以循环利用
C.铂电极M发生的电极反应式:2Cl- +2e- =Cl ↑; 2HO+4e- =O ↑+4H+
2 2 2
D.铂电极M处产生的H+移向铂电极N
【答案】C
【解析】由M极上Cl-失电子生成Cl 可知M为阳极,发生的电极反应式:2Cl- -2e- =Cl ↑; 2HO-4e-
2 2 2
=O ↑+4H+,N为阴极,电极反应式为:2HO+2e- =H ↑+2OH-;A.由M极上Cl-失电子生成Cl 可知M为
2 2 2 2
阳极,则a为电源正极,硬水中存在Mg2+、Ca2+和 ,阴极放电产生OH-,OH-与Mg2+结合生成
Mg(OH) ,OH-与 反应生成 ,Ca2+与 结合生成CaCO ,Mg(OH) 和CaCO 主要沉降在阴极附
2 3 2 3
近,故A正确;B.阳极产生氯气,氯气与水反应生成次氯酸和HCl,HClO能将有机物氧化为二氧化碳和
水,HClO自身被还原为氯离子,Cl-可以循环利用,故B正确;C.铂电极M为阳极,失电子发生氧化反
应,发生的电极反应式:2Cl- -2e- =Cl ↑; 2HO-4e- =O ↑+4H+,故C错误;D.铂电极M为阳极,N为阴
2 2 2
极,阳离子移向阴极,则H+移向铂电极N,故D正确;故选:C。
6.(2022·安徽师范大学附属中学模拟预测)近日,我国学者在Science报道了一种氯离子介导的电化学合
成方法,能将乙烯高效清洁、选择性地转化为环氧乙烷,电化学反应的过程如图所示。在电解结束后,将
阴、阳极电解液输出混合,便可反应生成环氧乙烷。下列叙述错误的是A.电解过程中Cl-透过交换膜向左侧移动
B.电解结束溶液混合后KCl的浓度与电解前的相等
C.每生成1mol环氧乙烷,理论上电路中转移电子数为2N
A
D.工作过程中Ni电极附近的电极反应式为2HO+2e-=2OH-+H ↑
2 2
【答案】B
【解析】由图示可知,在Pt电极附近通入乙烯,所以Pt电极氯离子失电子生成氯气,Pt电极为阳极,Ni
电极为阴极,阴极反应式为 。A.Pt电极为阳极,Ni电极为阴极,电解过程中Cl-透
过交换膜向左侧移动,故A正确;B.总反应为 ,电解结束溶
液混合后,溶剂水的质量减小,所以KCl的浓度比电解前增大,故B错误;C.根据
,每生成1mol环氧乙烷同时生成1mol氢气,理论上电路中转
移电子数为2N ,故C正确;D.Ni电极为阴极,工作过程中Ni电极附近的电极反应式为2HO+2e-=2OH-
A 2
+H ↑,生成KOH生成,故D正确;选B。
2
7.(2022·河南·模拟预测)氯化氢回收氯气技术近年来为科学研究的热点,一种新的氯化氢电解回收氯气
的过程如图。下列说法正确的是
A.石墨电极连接电源正极
B.H+透过交换膜从石墨电极向铂电极移动
C.石墨电极区域的电极反应为Fe3++e- =Fe2+
D.随着反应的进行,阴阳两极电解质溶液pH均升高。
【答案】D【解析】石墨电极中Fe3+转化为Fe2+,得电子则在电解池中作为阴极,连接电源的负极,氧气将生成的
Fe2+氧化为Fe3+;铂电极为阳极,氯化氢失电子产生氯气。A.根据离子转化关系,石墨电极为阴极,连接
电源负极,选项A错误;B.H+透过交换膜从阳极(铂电极)向阴极(石墨电极)移动,选项B错误;C.该过
程Fe3+循环再生,石墨电极实际上是氧气得电子,电极反应为4H++O +4e-=2H O,选项C错误;D.随着反
2 2
应的进行,阳极氢离子向阴极移动,移动过来的H+在阴极又参与反应生成了水,所以阴阳两极电解质溶液
pH均升高,选项D正确;答案选D。
8.(2022·四川省泸县第二中学一模)对氨基苯甲酸( )是一种用途广泛的化工产品和医
药中间体,以对硝基苯甲酸( )为原料,采用电解法合成它的装置如图。下列说法中
正确的是
A.左边电极电势比右边高
B.每转移1mole-时,阳极电解质溶液的质量减少8g
C.阴极的主要电极反应式为 +6e-+6H+→+2H2O
D.反应结束后阳极区pH增大
【答案】C
【解析】金属阳极DSA发生2HO-4e-=O +4H+,阴极的主要电极反应式为 +6e-+6H+→
2 2
+2H O。A.金属阳极DSA发生2HO-4e-=O +4H+,右侧为阳极,左侧为阴极,右边
2 2 2
电极电势比左边高,故A错误;B.阳极发生反应2HO-4e-=O +4H+,氧气逸出,氢离子跨过阳离子交换膜
2 2
移向阴极,当转移4mole-时,阳极电解质溶液减少2mol水,则转移1mole-时,阳极电解质溶液减少0.5mol
水,质量为9g,故B错误;C.阴极上对硝基苯甲酸得电子发生还原反应,生成对氨基苯甲酸,则阴极的
主要电极反应式为 +6e-+6H+→ +2H O,故C正确;D.由B
2项分析知,阳极反应消耗阳极区的水,则反应结束后阳极区硫酸的浓度增大,pH减小,故D错误;故选:
C。
9.(2022·河南河南·模拟预测)一种采用SOEC共电解HO/CO 技术合成CH 的工作原理如图所示。图中
2 2 4
三相界面即电子导体相、离子导体相和气相共存的界面。
下列说法正确的是
A.电解时,M电极与电源的负极相接
B.电解时,阴极电极反应式之一为CO+2e-=CO+O2-
2
C.若电解过程中生成22. 4 L CH ,则转移电子的数目一定为6N
4 A
D.若该装置能为外界提供电力,则M电极为负极
【答案】B
【解析】A. M电极处生成O,应为O2-失去电子生成O,为阳极,与电源的正极相连,故A错误;B.
2 2
阴极电极处,CO→CO,HO→H ,CO→CH,故阴极电极反应式之一为CO+2e-=CO+O2-,故B正确;
2 2 2 2 4 2
C. 没有指明为标准状况,故无法计算甲烷的物质的量,且阴极除了生成甲烷外,还生成氢气和CO,故
不能计算转移电子数,故C错误;D. 若该装置能为外界提供电力,为电解池,O→O2-,M电极为正极,
2
故D错误;故选B。
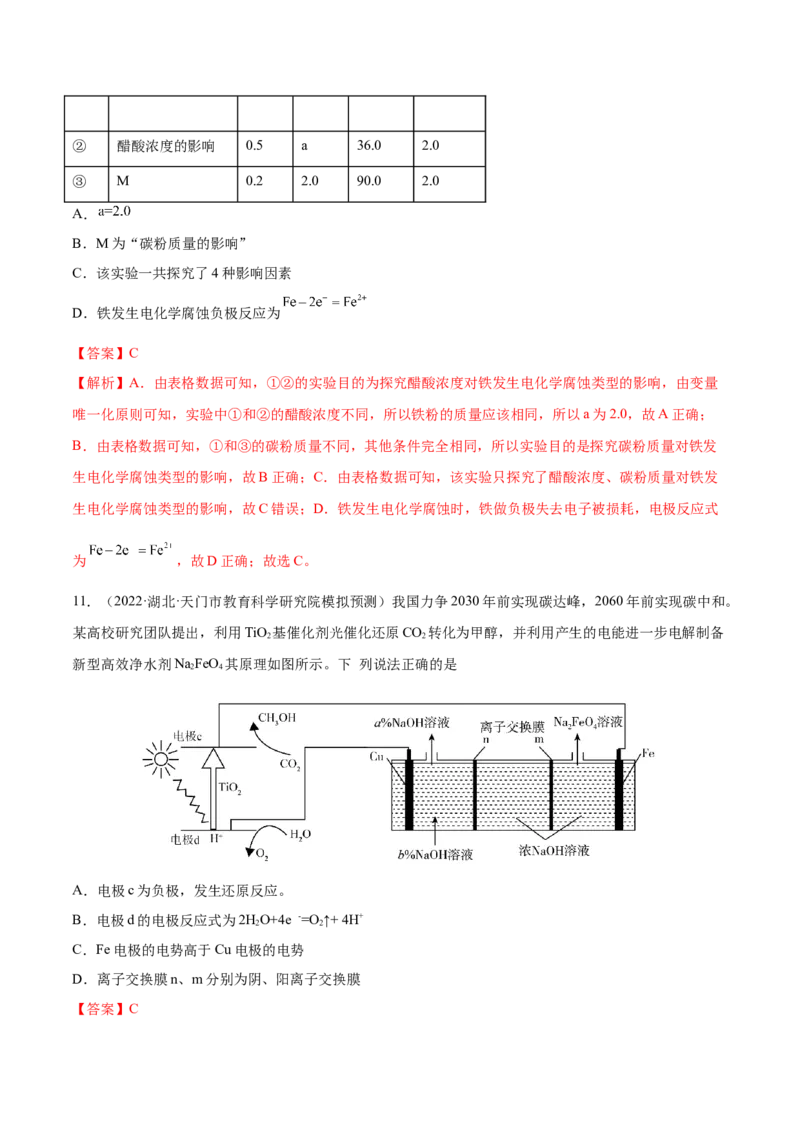
10.(2022·广东广州·三模)某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,设计下
表实验。将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞。从胶头滴管中一次性滴入醋酸溶液,
同时测量容器中的压强变化。下列说法不正确的是
编
实验目的 碳粉/g 铁粉/g 醋酸/ 醋酸/
号
① 为以下实验作参照 0.5 2.0 90.0 2.0② 醋酸浓度的影响 0.5 a 36.0 2.0
③ M 0.2 2.0 90.0 2.0
A.
B.M为“碳粉质量的影响”
C.该实验一共探究了4种影响因素
D.铁发生电化学腐蚀负极反应为
【答案】C
【解析】A.由表格数据可知,①②的实验目的为探究醋酸浓度对铁发生电化学腐蚀类型的影响,由变量
唯一化原则可知,实验中①和②的醋酸浓度不同,所以铁粉的质量应该相同,所以a为2.0,故A正确;
B.由表格数据可知,①和③的碳粉质量不同,其他条件完全相同,所以实验目的是探究碳粉质量对铁发
生电化学腐蚀类型的影响,故B正确;C.由表格数据可知,该实验只探究了醋酸浓度、碳粉质量对铁发
生电化学腐蚀类型的影响,故C错误;D.铁发生电化学腐蚀时,铁做负极失去电子被损耗,电极反应式
为 ,故D正确;故选C。
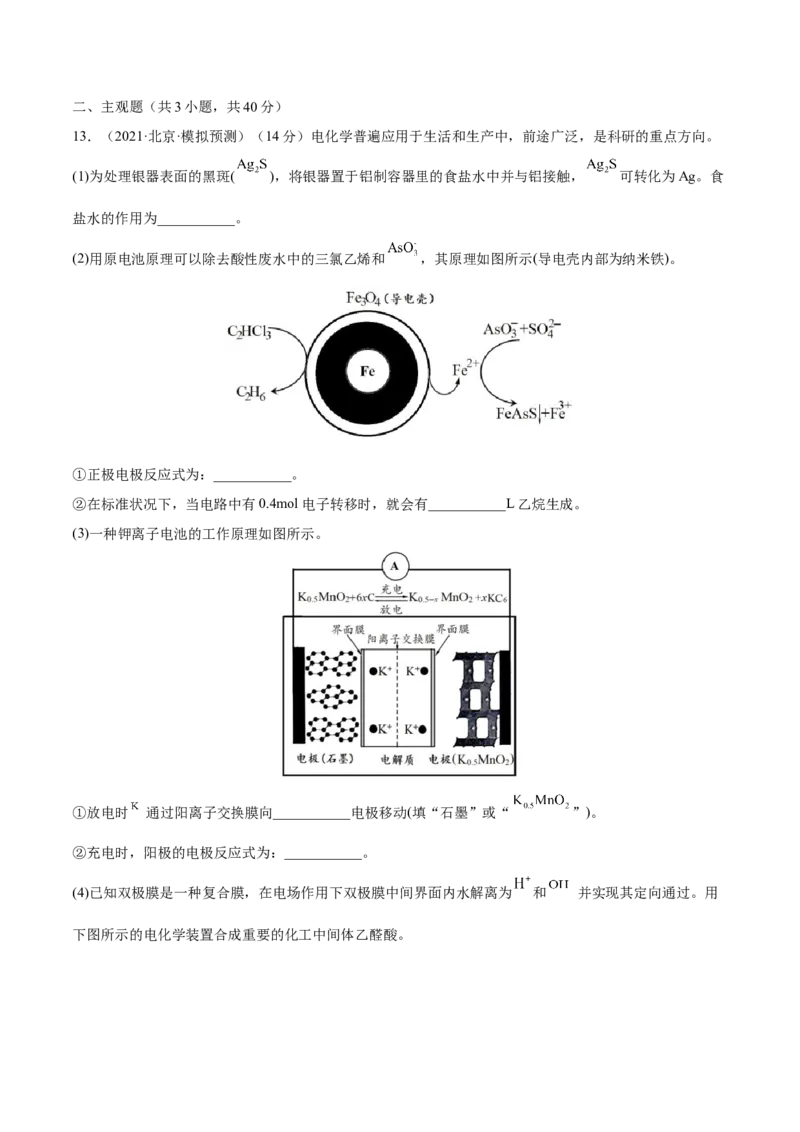
11.(2022·湖北·天门市教育科学研究院模拟预测)我国力争2030年前实现碳达峰,2060年前实现碳中和。
某高校研究团队提出,利用TiO 基催化剂光催化还原CO 转化为甲醇,并利用产生的电能进一步电解制备
2 2
新型高效净水剂NaFeO 其原理如图所示。下 列说法正确的是
2 4
A.电极c为负极,发生还原反应。
B.电极d的电极反应式为2HO+4e -=O ↑+ 4H+
2 2
C.Fe电极的电势高于Cu电极的电势
D.离子交换膜n、m分别为阴、阳离子交换膜
【答案】C【解析】电极c上CO 转化为甲醇其中C元素化合价降低,则c为正极,电极d上水转化为氧气,O元素
2
化合价升高,则d为负极,与电源负极相连的是电解池的阴极,则Cu为阴极,Fe为阳极;A.电极c上
CO 转化为甲醇其中C元素化合价降低,c为正极,A错误;B.电极d上水转化为氧气,O元素化合价升
2
高,则d为负极,发生氧化反应,电极反应式为2HO-4e-=O ↑+ 4H+,B错误;C.与电源负极相连的是电
2 2
解池的阴极,则Cu为阴极,Fe为阳极,则Fe电极的电势高于Cu电极的电势,C正确;D.电解池中阳离
子移向阴极,阴离子移向阳极,则钠离子移向Cu极,n为阳离子交换膜,D错误;故选:C。
12.(2022·江西抚州·模拟预测)含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接
电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是
A.阳极保护法中受保护的金属外接电源的负极
B.电流密度越大,金属受保护程度越好
C.CFD区,金属受到保护
D.外接电势越高,对金属保护性越有效
【答案】C
【解析】A.金属从活态向钝态的转变叫钝化;而通过外接电源而钝化的阳极保护法,指的是使受保护的
金属作为阳极,通过外加电流使阳极极化,电位强烈正移,腐蚀速率大幅度降低,所以,阳极保护法中受
保护的金属外接电源的正极,A错误;B. 代表的是金属钝化的难易程度,即开始的时候电流密度越大,
此时金属溶解,表示金属越难钝化,所以并非电流密度越大,金属受保护程度越好,B错误;C.当外接
电势超过 后,金属开始钝化,从 到 都是金属钝化较稳定的范围,所以CFD区,金属受到保护,C
正确;D.外接电势超过 后,电流密度又持续增加了,腐蚀速度又加快了,所以并非外接电势越高,对
金属保护越有效,D错误;故合理选项为C。二、主观题(共3小题,共40分)
13.(2021·北京·模拟预测)(14分)电化学普遍应用于生活和生产中,前途广泛,是科研的重点方向。
(1)为处理银器表面的黑斑( ),将银器置于铝制容器里的食盐水中并与铝接触, 可转化为Ag。食
盐水的作用为___________。
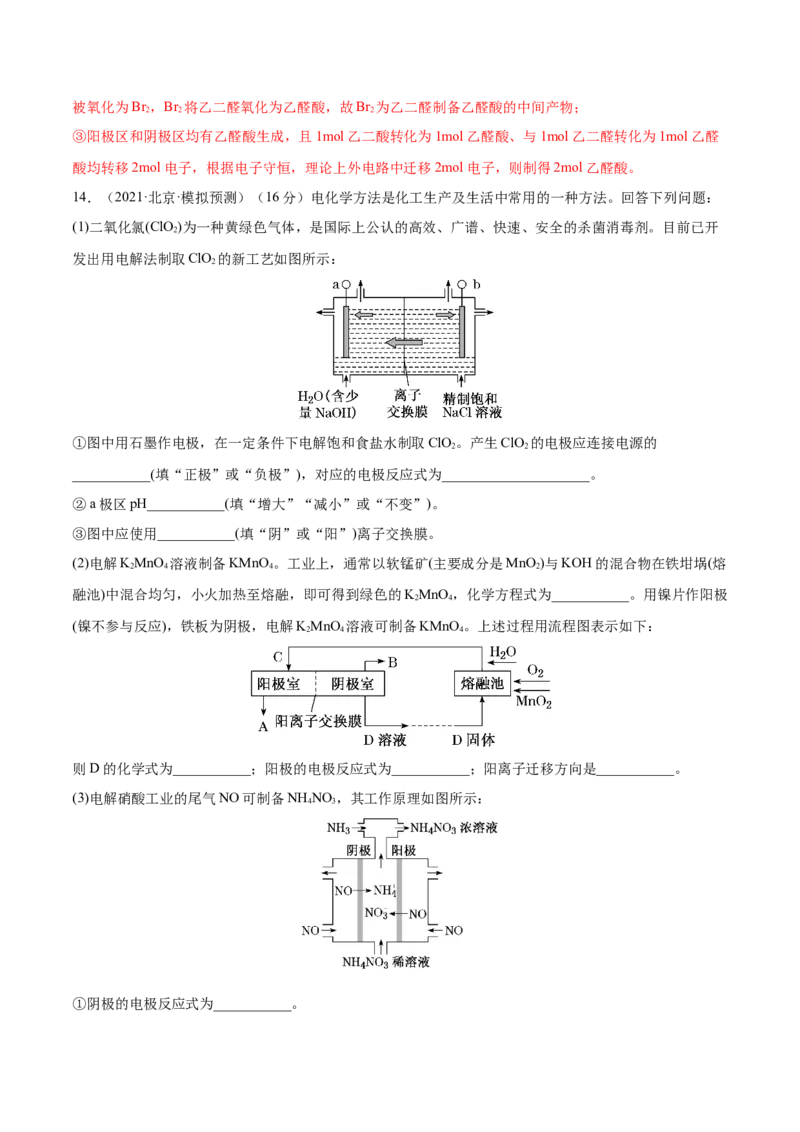
(2)用原电池原理可以除去酸性废水中的三氯乙烯和 ,其原理如图所示(导电壳内部为纳米铁)。
①正极电极反应式为:___________。
②在标准状况下,当电路中有0.4mol电子转移时,就会有___________L乙烷生成。
(3)一种钾离子电池的工作原理如图所示。
①放电时 通过阳离子交换膜向___________电极移动(填“石墨”或“ ”)。
②充电时,阳极的电极反应式为:___________。
(4)已知双极膜是一种复合膜,在电场作用下双极膜中间界面内水解离为 和 并实现其定向通过。用
下图所示的电化学装置合成重要的化工中间体乙醛酸。①阴极电极反应式为___________。
②其中 的作用是___________。
③制得2mol乙醛酸,理论上外电路中迁移了___________mol电子。
【答案】(除标注外,每空2分)(1)作电解质溶液(1分)
(2)① ②1.12
(3)①K MnO (1分) ②
0.5 2
(4)① ②Br 为乙二醛制备乙醛酸的中间产物 ③2
2
【解析】(1)为处理银器表面的黑斑(Ag S),将银器置于铝制容器里的食盐水中并与铝接触,该装置构成原
2
电池,食盐水作电解质溶液,形成原电池,故答案为:作电解质溶液;
(2)①原电池正极得电子发生还原反应,据题图可知在酸性条件下,正极上C HCI ,被还原为乙烷,则电极
2 3
反应式为 ;
②根据电极反应式 ,当电路中有0.4mol电子转移时,就会有0.05mol乙烷生成,
其体积是 ;
(3)①放电时为原电池,K+通过阳离子交换膜由负极石墨电极向正极K MnO 移动;
0.5 2
②充电时为电解池,阴阳极反应与原电池负正极反应相反,即阳极反应式为 ;
(4)①阴极发生还原反应,其电极反应式为 ;
②该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳极上Br-被氧化为Br ,Br 将乙二醛氧化为乙醛酸,故Br 为乙二醛制备乙醛酸的中间产物;
2 2 2
③阳极区和阴极区均有乙醛酸生成,且1mol乙二酸转化为1mol乙醛酸、与1mol乙二醛转化为1mol乙醛
酸均转移2mol电子,根据电子守恒,理论上外电路中迁移2mol电子,则制得2mol乙醛酸。
14.(2021·北京·模拟预测)(16分)电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开
2
发出用电解法制取ClO 的新工艺如图所示:
2
①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO 。产生ClO 的电极应连接电源的
2 2
___________(填“正极”或“负极”),对应的电极反应式为_____________________。
②a极区pH___________(填“增大”“减小”或“不变”)。
③图中应使用___________(填“阴”或“阳”)离子交换膜。
(2)电解KMnO 溶液制备KMnO 。工业上,通常以软锰矿(主要成分是MnO )与KOH的混合物在铁坩埚(熔
2 4 4 2
融池)中混合均匀,小火加热至熔融,即可得到绿色的KMnO ,化学方程式为___________。用镍片作阳极
2 4
(镍不参与反应),铁板为阴极,电解KMnO 溶液可制备KMnO 。上述过程用流程图表示如下:
2 4 4
则D的化学式为___________;阳极的电极反应式为___________;阳离子迁移方向是___________。
(3)电解硝酸工业的尾气NO可制备NH NO ,其工作原理如图所示:
4 3
①阴极的电极反应式为___________。②将电解生成的HNO 全部转化为NH NO ,则通入的NH 与实际参加反应的NO的物质的量之比至少为
3 4 3 3
___________。
【答案】(除标注外,每空2分)
(1)①正极(1分)②Cl--5e-+2HO=ClO ↑+4H+ 增大 (1分)③阳(1分)
2 2
(2)2MnO +4KOH+O 2KMnO +2HO KOH(1分) -e-= K+由阳离子交换膜左侧向右侧迁
2 2 2 4 2
移
(3)①NO+5e-+6H+= +HO ②1∶4
2
【解析】(1)①根据题意可知,Cl-放电生成ClO 的电极为阳极,接电源的正极。根据元素守恒,有水参加
2
反应,同时生成H+,电极反应式为Cl--5e-+2HO=ClO ↑+4H+;②a极区为阴极区,电极反应式:
2 2
2HO+2e-=H ↑+2OH-,阴极区OH-浓度增大,溶液的pH增大;③根据溶液中电荷守恒的规律,图中应
2 2
使用阳离子交换膜。
(2)软锰矿(主要成分是MnO )与KOH小火加热至熔融,得到KMnO ,Mn元素化合价由+4价升为+6价,
2 2 4
则空气中的O 作氧化剂,化学方程式为2MnO +4KOH+O 2KMnO +2HO;电解锰酸钾溶液时,
2 2 2 2 4 2
阴极上水得电子生成氢气和氢氧根离子,电极反应式为2HO+2e-===H↑+2OH-,K+通过阳离子交换膜
2 2
由左侧向右侧迁移,所以D是氢氧化钾溶液,阳极上 失电子生成 ,电极反应式为 -e-
=== 。
(3)①由图示可知,NO在阴极上得电子生成 ,电极反应式为NO+5e-+6H+= +HO;②NO在
2
阳极上失电子生成 ,电极反应式为NO-3e-+2HO = +4H+,电解总反应式为8NO+7HO
2 2
3NH NO +2HNO,故当实际参加反应的NO为8 mol时,要将电解生成的HNO 全部转化为NH NO ,还
4 3 3 3 4 3
应通入2 mol NH ,则n(NH )∶n(NO)=2 mol∶8 mol=1∶4。
3 3
15.(2022·重庆·三模)(10分)回答下列问题:
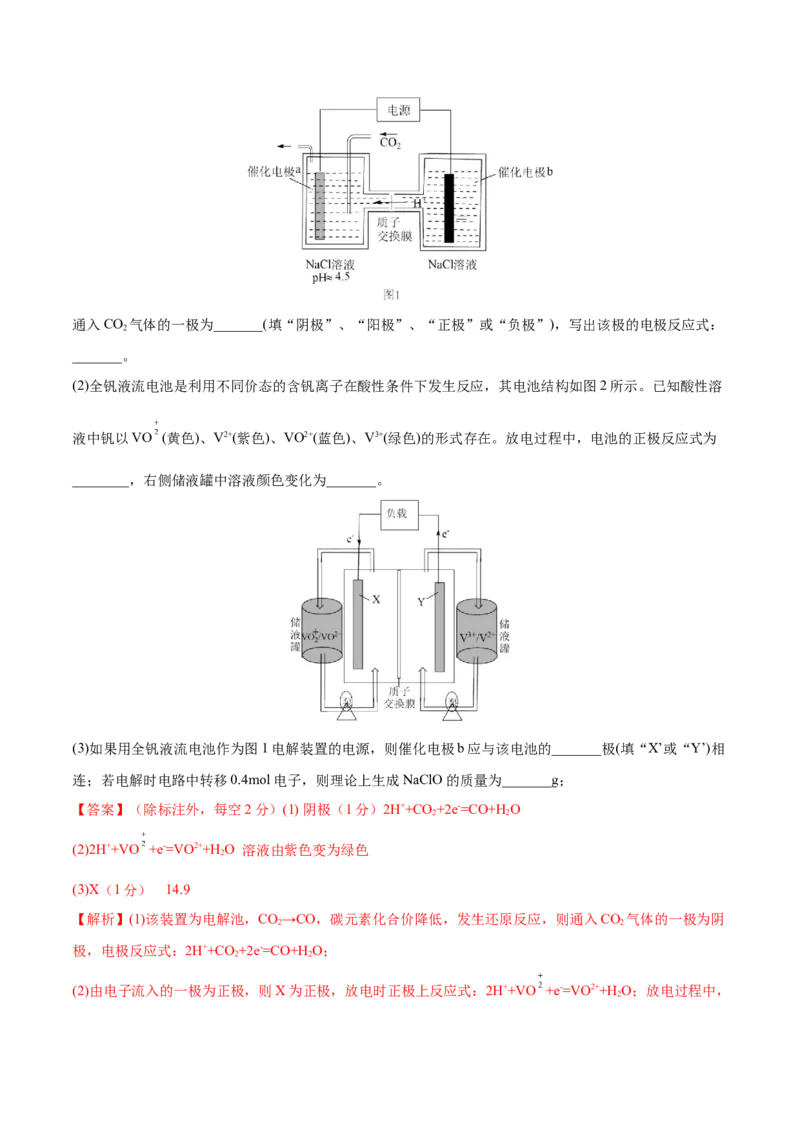
(1)我国某科研团队设计了一种电解装置,将CO 和NaCl高效转化为CO和NaClO,原理如图1所示:
2通入CO 气体的一极为_______(填“阴极”、“阳极”、“正极”或“负极”),写出该极的电极反应式:
2
_______。
(2)全钒液流电池是利用不同价态的含钒离子在酸性条件下发生反应,其电池结构如图2所示。已知酸性溶
液中钒以VO (黄色)、V2+(紫色)、VO2+(蓝色)、V3+(绿色)的形式存在。放电过程中,电池的正极反应式为
________,右侧储液罐中溶液颜色变化为_______。
(3)如果用全钒液流电池作为图1电解装置的电源,则催化电极b应与该电池的_______极(填“X’或“Y’)相
连;若电解时电路中转移0.4mol电子,则理论上生成NaClO的质量为_______g;
【答案】(除标注外,每空2分)(1) 阴极(1分)2H++CO +2e-=CO+H O
2 2
(2)2H++VO +e-=VO2++H O 溶液由紫色变为绿色
2
(3)X(1分) 14.9
【解析】(1)该装置为电解池,CO→CO,碳元素化合价降低,发生还原反应,则通入CO 气体的一极为阴
2 2
极,电极反应式:2H++CO +2e-=CO+H O;
2 2
(2)由电子流入的一极为正极,则X为正极,放电时正极上反应式:2H++VO +e-=VO2++H O;放电过程中,
2右罐为负极,反应式:V2+-e-═V3+,则溶液颜色逐渐由紫色变为绿色;
(3)图2是原电池,Y极电子流出,则Y为负极,X为正极,图1是电解池,催化电极b是阳极,由电解池
的阳极接原电池的正极,则催化电极b应与该电池的X极,催化电极b的电极反应式为:HO+Cl--2e-
2
=HClO+H+,电路中转移0.4mol电子,则理论上生成0.2mol NaClO,质量
为m=nM=0.2mol×74.5g/mol=14.9g。