文档内容
训练(四十八) 物质的分离、提纯与检验
1.(2021·河南洛阳检测)南朝陶弘景在《本草经集注》中记载有鉴别消石(KNO)与朴消
3
(Na SO )之法:“强烧之,紫青烟起,云是真消石也”。该鉴别方法利用的原理是( )
2 4
A.受热升华 B.颜色反应
C.焰色反应 D.丁达尔效应
C [含有钾元素的物质在火焰上灼烧,火焰呈紫色(透过蓝色钴玻璃观察),该原理为焰
色反应,C项正确。]
2.(2021·四川新津中学检测)下列有关操作的说法不正确的是( )
A.《本草经集注》记载了鉴别硝石(KNO)和朴硝(Na SO )的方法:“以火烧之,紫青烟起,
3 2 4
乃真硝石也”,此处运用了物质升华的性质
B.《本草纲目》记载了烧酒的制作工艺: “凡酸坏之酒,皆可蒸烧”,此处用到的操作是
蒸馏
C.《肘后备急方》一书中有“青蒿一握,以水二升渍,绞其汁”,此处用到的操作是溶解
D.唐诗有“千淘万漉虽辛苦,吹尽狂沙始到金”的诗句,此处用到的操作是过滤
A [钾元素的焰色反应为紫色,钠元素的焰色反应为黄色,则硝石(KNO)和朴硝
3
(Na SO )可通过焰色反应来鉴别,A项错误;《本草纲目》中“凡酸坏之酒,皆可蒸烧”,酸坏
2 4
之酒中含有乙酸,利用乙酸和乙醇的沸点不同进行分离,该操作为蒸馏,B项正确;“以水二
升渍”中的“渍”即为浸泡溶解,C项正确;诗句中的“淘”和“漉”的原理和过滤的原理
相同,D项正确。]
3.(2021·山东莱芜一中检测)为提纯下列物质(括号内为杂质),选用的试剂或分离方法错
误的是( )
选项 物质 试剂 分离方法
A 硝酸钾(氯化钠) 蒸馏水 降温结晶
B 二氧化碳(氯化氢) 饱和NaHCO 溶液 洗气
3
C 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
D 乙醇(水) 生石灰 蒸馏
C [KNO 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,可加蒸馏水
3
溶解固体,再通过蒸发浓缩、降温结晶的方法,获得纯净的KNO 固体,A项正确;HCl与饱和
3
NaHCO 溶液反应生成二氧化碳,B项正确;乙烯被酸性KMnO 氧化生成CO,使甲烷中混
3 4 2
入CO 气体,C项错误;加入的生石灰能与水反应生成Ca(OH) ,消耗掉部分水,再通过蒸馏
2 2获得乙醇,D项正确。]
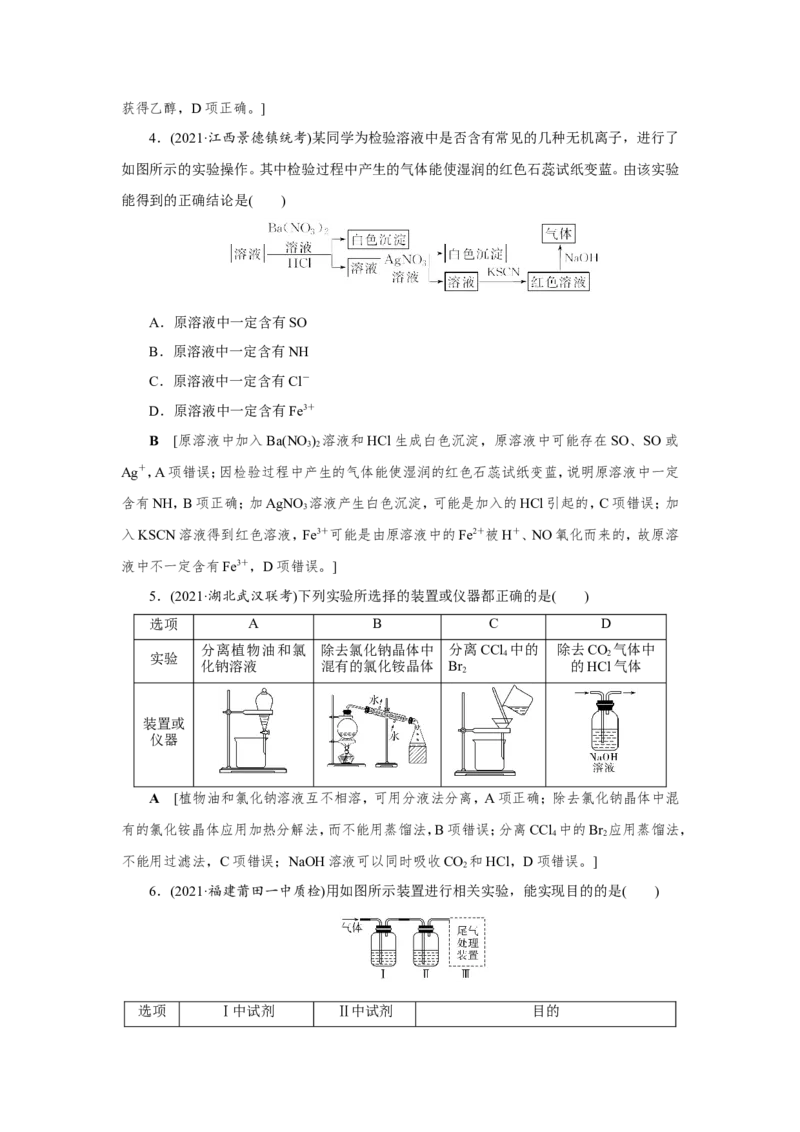
4.(2021·江西景德镇统考)某同学为检验溶液中是否含有常见的几种无机离子,进行了
如图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验
能得到的正确结论是( )
A.原溶液中一定含有SO
B.原溶液中一定含有NH
C.原溶液中一定含有Cl-
D.原溶液中一定含有Fe3+
B [原溶液中加入Ba(NO ) 溶液和HCl生成白色沉淀,原溶液中可能存在SO、SO或
3 2
Ag+,A项错误;因检验过程中产生的气体能使湿润的红色石蕊试纸变蓝,说明原溶液中一定
含有NH,B项正确;加AgNO 溶液产生白色沉淀,可能是加入的HCl引起的,C项错误;加
3
入KSCN溶液得到红色溶液,Fe3+可能是由原溶液中的Fe2+被H+、NO氧化而来的,故原溶
液中不一定含有Fe3+,D项错误。]
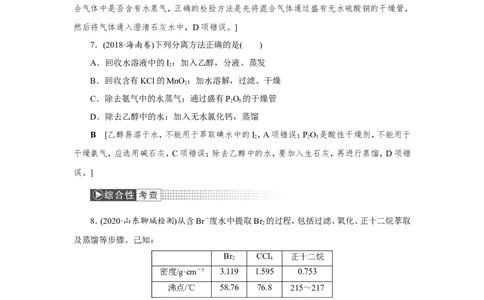
5.(2021·湖北武汉联考)下列实验所选择的装置或仪器都正确的是( )
选项 A B C D
分离植物油和氯 除去氯化钠晶体中 分离CCl 中的 除去CO 气体中
实验 4 2
化钠溶液 混有的氯化铵晶体 Br 的HCl气体
2
装置或
仪器
A [植物油和氯化钠溶液互不相溶,可用分液法分离,A项正确;除去氯化钠晶体中混
有的氯化铵晶体应用加热分解法,而不能用蒸馏法,B项错误;分离CCl 中的Br 应用蒸馏法,
4 2
不能用过滤法,C项错误;NaOH溶液可以同时吸收CO 和HCl,D项错误。]
2
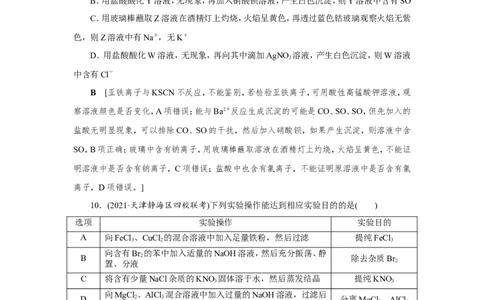
6.(2021·福建莆田一中质检)用如图所示装置进行相关实验,能实现目的的是( )
选项 Ⅰ中试剂 Ⅱ中试剂 目的足量酸性
A 澄清石灰水 检验SO 中是否混有CO 气体
2 2
KMnO 溶液
4
B 溴水 NaOH溶液 检验CH 中是否混有CH===CH 气体
4 2 2
C 饱和NaCO 溶液 浓硫酸 除去CO 中混有的HCl气体
2 3 2
D 澄清石灰水 CuSO 溶液 证明混合气体中含有CO 和水蒸气
4 2
B [SO 、CO 都能与澄清石灰水反应,应先通过酸性KMnO 溶液除去SO 再检验CO,
2 2 4 2 2
A项错误;乙烯与溴水发生加成反应,溴水褪色,可用溴水检验乙烯,B项正确;CO 和HCl都
2
与饱和NaCO 溶液反应,应用饱和NaHCO 溶液除杂,C项错误;不能用CuSO 溶液检验混
2 3 3 4
合气体中是否含有水蒸气,正确的检验方法是先将混合气体通过盛有无水硫酸铜的干燥管,
然后将气体通入澄清石灰水中,D项错误。]
7.(2018·海南卷)下列分离方法正确的是( )
A.回收水溶液中的I:加入乙醇,分液、蒸发
2
B.回收含有KCl的MnO :加水溶解,过滤、干燥
2
C.除去氨气中的水蒸气:通过盛有PO 的干燥管
2 5
D.除去乙醇中的水:加入无水氯化钙,蒸馏
B [乙醇易溶于水,不能用于萃取碘水中的I,A项错误;PO 是酸性干燥剂,不能用于
2 2 5
干燥氨气,应选用碱石灰,C项错误;除去乙醇中的水,要加入生石灰,再进行蒸馏,D项错
误。]
8.(2020·山东聊城检测)从含Br-废水中提取Br 的过程,包括过滤、氧化、正十二烷萃取
2
及蒸馏等步骤。己知:
Br CCl 正十二烷
2 4
密度/g·cm-3 3.119 1.595 0.753
沸点/℃ 58.76 76.8 215~217
下列说法正确的是( )
A.用甲装置过滤时,需不断搅拌
B.丙装置中用正十二烷而不用CCl ,是因为其密度小
4C.用乙装置将Br-氧化为Br
2
D.可用装置丁进行蒸馏,先收集正十二烷再收集Br
2
C [过滤时不需搅拌,A错误;丙装置中用正十二烷而不用CCl ,是因为其沸点与溴相
4
差大,萃取后的溶液可通过蒸馏而分离,B错误;用乙装置利用氯气将Br-氧化为Br ,C正确;
2
可用装置丁进行蒸馏,先收集Br 再收集正十二烷,D错误。]
2
9.(2021·河南郑州一中检测)下列关于物质或离子检验的推断正确的是( )
A.向X溶液中滴加KSCN溶液,溶液显红色,证明X溶液中有Fe3+,无Fe2+
B.用盐酸酸化Y溶液,无现象,再加入硝酸钡溶液,产生白色沉淀,则Y溶液中含有SO
C.用玻璃棒蘸取Z溶液在酒精灯上灼烧,火焰呈黄色,再透过蓝色钴玻璃观察火焰无紫
色,则Z溶液中有Na+,无K+
D.用盐酸酸化W溶液,无现象,再向其中滴加AgNO 溶液,产生白色沉淀,则W溶液
3
中含有Cl-
B [亚铁离子与KSCN不反应,不能鉴别,若检验亚铁离子,可用酸性高锰酸钾溶液,观
察溶液颜色是否变化,A项错误;能与Ba2+反应生成沉淀的可能是CO、SO、SO,但先加入的
盐酸无明显现象,可以排除CO、SO的干扰,然后加入硝酸钡,如果产生沉淀,则溶液中含
SO,B项正确;玻璃中含有钠离子,用玻璃棒蘸取溶液在酒精灯上灼烧,火焰呈黄色,不能证
明溶液中是否含有钠离子,C项错误;盐酸中也含有氯离子,不能证明原溶液中是否含有氯
离子,D项错误。]
10.(2021·天津静海区四校联考)下列实验操作能达到相应实验目的的是( )
选项 实验操作 实验目的
A 向FeCl 、CuCl 的混合溶液中加入足量铁粉,然后过滤 提纯FeCl
3 2 3
向含有Br 的苯中加入适量的NaOH溶液,然后充分振荡、静
B 2 除去杂质Br
置、分液 2
C 将含有少量NaCl杂质的KNO 固体溶于水,然后蒸发结晶 提纯KNO
3 3
向MgCl 、AlCl 混合溶液中加入过量的NaOH溶液,过滤后
D 2 3 分离MgCl 、AlCl
将沉淀溶于适量的盐酸;向滤液中加入适量盐酸 2 3
B [向FeCl 、CuCl 的混合溶液中加入足量铁粉,FeCl 会和Fe反应生成FeCl ,A项错
3 2 3 2
误;Br 和NaOH溶液反应生成易溶于水的NaBr和NaBrO,充分振荡、静置、分液可以除去杂
2
质Br ,B项正确;KNO 的溶解度随温度升高变化较大,而NaCl的溶解度受温度影响不大,
2 3
要提纯KNO,将含有少量NaCl杂质的KNO 固体溶于水,蒸发浓缩、冷却结晶,然后过滤即
3 3
可得较纯净的KNO,C项错误;滤液中含有过量的NaOH溶液,向滤液中加入适量盐酸后会
3
有NaCl生成,D项错误。]11.(2021·安徽“皖南八校”联考)实验室在 500 ℃时隔绝空气加热硫酸亚铁铵
[(NH )Fe(SO )]至分解完全并确定分解产物成分的装置如图所示(已知分解的固体产物中可
4 2 4 2
能有FeO、Fe O 和Fe O,气体产物中可能有NH 、N、HO、SO 和SO )。下列说法正确的是(
2 3 3 4 3 2 2 3 2
)
A.装置②用于检验分解产物中是否有水蒸气生成,试剂X最好选用碱石灰
B.装置③用于检验分解产物中是否有SO 气体生成并除去SO 和NH
3 3 3
C.取①中固体残留物与稀硫酸反应并滴加KSCN溶液,溶液变红,则残留物一定为
Fe O
2 3
D.装置④用于检验分解产物中是否有SO 气体生成,装置⑤用于收集生成的NH 和N
2 3 2
B [装置②的作用是检验分解产物中是否有水蒸气生成,故试剂X应选用无水CuSO ,
4
A项错误;装置③用于检验分解产物中是否有SO 气体生成,若有SO 气体生成,则装置③中
3 3
产生白色沉淀硫酸钡,并用氯化钡和盐酸除去SO 和NH ,B项正确;①中固体残留物中可能
3 3
还含有FeO,可能不含有Fe O 而含有Fe O,不一定为Fe O,C项错误;NH 极易溶于水,若
2 3 3 4 2 3 3
分解产物中有NH ,则NH 被装置③中的溶液吸收,装置⑤中不可能收集到NH ,D项错误。]
3 3 3
12.(2021·河北衡水中学调研)工业品MnCl 溶液中含有杂质,利用锰粉、草酸、硫酸锰分
2
别依次除去Pb2+、Ca2+、Mg2+制得纯净的MnCl 。工艺流程如下:
2
已知:①草酸为二元弱酸,其钠盐、钾盐易溶于水,钙盐难溶于水。
②硫酸镁晶体、硫酸锰的溶解度曲线如下图:回答下列问题:
(1)过滤所需的玻璃仪器主要有____________________,加热搅拌的作用是
________________。
(2)弃渣Ⅰ、Ⅱ、Ⅲ的主要成分分别为________________、____________、______________。
反应①的离子方程式为_______________________________________。
(3)反应②的离子方程式为_____________________________________________。
(4)③加热搅拌、静置过滤时,所选择的温度的范围是______。
a.0~20 ℃ b.20~40 ℃ c.40~60 ℃ d.80~90 ℃
(5)④加入氯化钡溶液主要是为了除去________,检验该离子是否除尽的方法为
________________________________________________________________________
________________________________________________________________________。
(6)已知MnCl 溶液呈弱酸性,操作X为________(填字母)。
2
a.蒸发结晶 b.降温结晶 c.萃取分液 D.蒸馏
解析 (1)过滤所需的玻璃仪器主要有漏斗、烧杯、玻璃棒,加热搅拌的作用是加快反应
速率。
(2)根据题意,结合流程图知,反应①为除Pb2+,则弃渣Ⅰ为铅及少量锰粉;反应③除镁
离子,则弃渣Ⅱ为硫酸镁晶体;反应④为除去引入的硫酸根离子,则弃渣Ⅲ为硫酸钡。
(3)草酸与Ca2+反应生成草酸钙沉淀,注意草酸为弱酸,不能拆写成离子。
(4)根据硫酸锰与硫酸镁晶体的溶解度曲线,可知在80~90 ℃的范围内二者溶解度差别
最大,且硫酸镁晶体的溶解度最小。
(6)MnCl 溶液呈弱酸性,是因为Mn2+水解,不能用蒸发结晶的方法,而用蒸发浓缩、冷
2
却结晶(即降温结晶)的方法。
答案 (1)漏斗、烧杯、玻璃棒 加快反应速率
(2)铅及少量锰粉 MgSO ·7H O 硫酸钡(或BaSO) Mn+Pb2+===Mn2++Pb
4 2 4
(3)H C O+Ca2+===CaC O↓+2H+ (4)d (5)SO 取少量上层澄清溶液于试管中,滴
2 2 4 2 4
加BaCl 溶液,如无沉淀出现则说明SO已除尽,反之则没有除尽 (6)b
2