文档内容
第2课时 必备知识——物质的分离、提纯与检验
[重要操作]①过滤;②蒸馏;③萃取、分液;④蒸发;⑤升华;⑥洗气
知识
清单
[基本规律]①分离及提纯常用物理方法与选择;②分离及提纯常用化学方法与选
择;③常见物质(如Fe3+、NH、SO 等)的检验原理及操作
2
知识点1 分离、提纯的常用物理方法
1.物质分离和提纯的区别
2.根据物理性质选择分离、提纯的方法
(1)“固+固”混合物的分离(提纯)
(2)“固+液”混合物的分离(提纯)
(3)“液+液”混合物的分离(提纯)
3.物质分离、提纯的常用装置
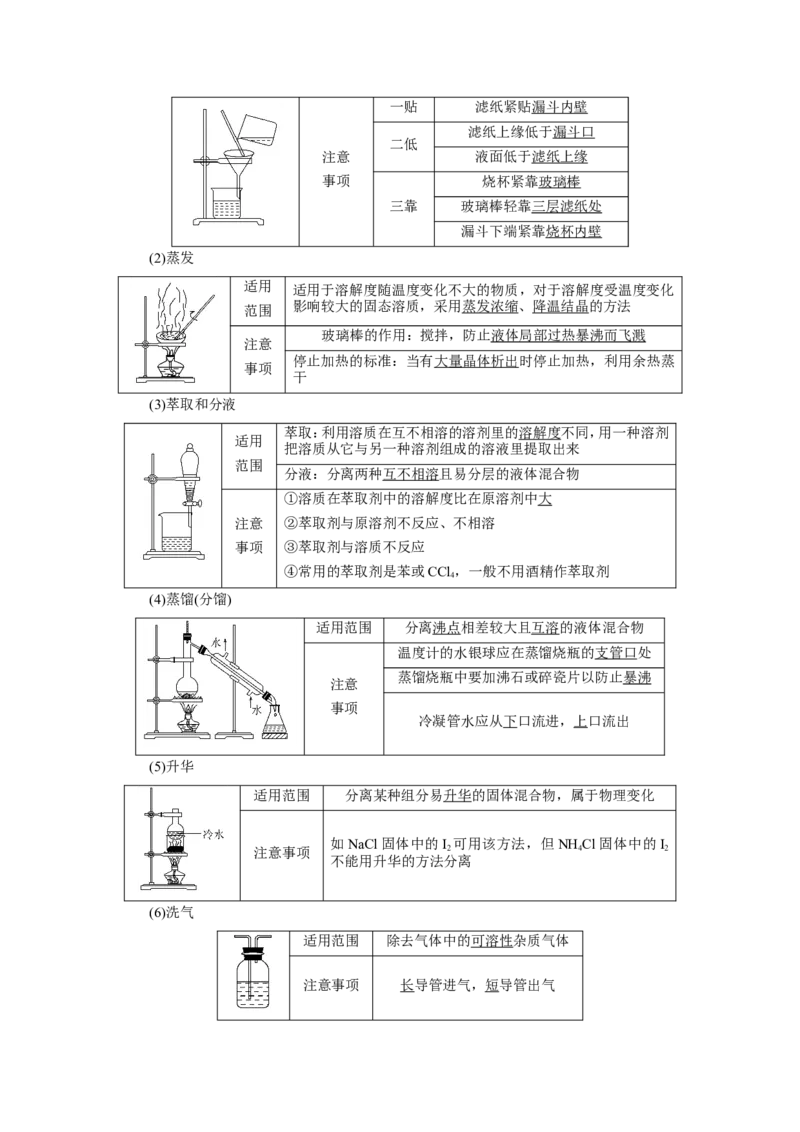
(1)过滤
适用范围 适用于不溶性固体与液体的分离一贴 滤纸紧贴漏斗内壁
滤纸上缘低于漏斗口
二低
注意 液面低于滤纸上缘
事项 烧杯紧靠玻璃棒
三靠 玻璃棒轻靠三层滤纸处
漏斗下端紧靠烧杯内壁
(2)蒸发
适用 适用于溶解度随温度变化不大的物质,对于溶解度受温度变化
范围 影响较大的固态溶质,采用蒸发浓缩、降温结晶的方法
玻璃棒的作用:搅拌,防止液体局部过热暴沸而飞溅
注意
停止加热的标准:当有大量晶体析出时停止加热,利用余热蒸
事项
干
(3)萃取和分液
萃取:利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂
适用
把溶质从它与另一种溶剂组成的溶液里提取出来
范围
分液:分离两种互不相溶且易分层的液体混合物
①溶质在萃取剂中的溶解度比在原溶剂中大
注意 ②萃取剂与原溶剂不反应、不相溶
事项 ③萃取剂与溶质不反应
④常用的萃取剂是苯或CCl ,一般不用酒精作萃取剂
4
(4)蒸馏(分馏)
适用范围 分离沸点相差较大且互溶的液体混合物
温度计的水银球应在蒸馏烧瓶的支管口处
蒸馏烧瓶中要加沸石或碎瓷片以防止暴沸
注意
事项
冷凝管水应从下口流进,上口流出
(5)升华
适用范围 分离某种组分易升华的固体混合物,属于物理变化
如NaCl固体中的I 可用该方法,但NH Cl固体中的I
注意事项 2 4 2
不能用升华的方法分离
(6)洗气
适用范围 除去气体中的可溶性杂质气体
注意事项 长导管进气,短导管出气两种分离操作的创新设计
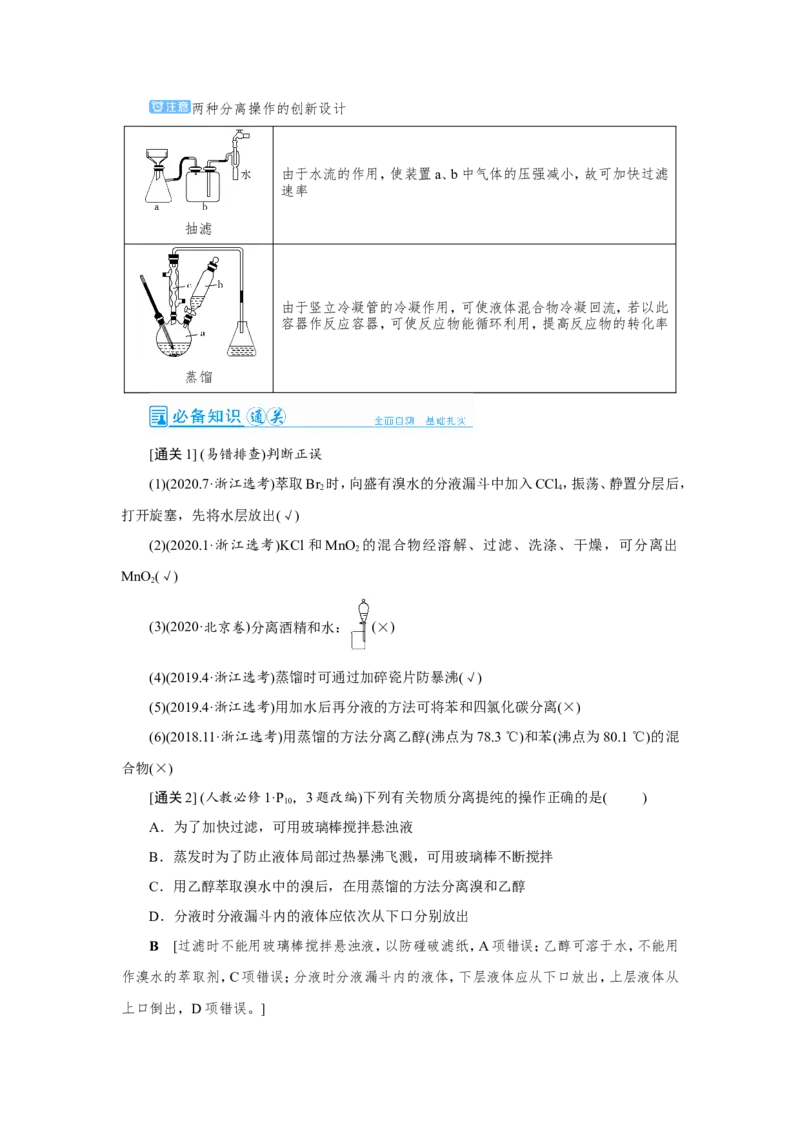
由于水流的作用,使装置a、b中气体的压强减小,故可加快过滤
速率
抽滤
由于竖立冷凝管的冷凝作用,可使液体混合物冷凝回流,若以此
容器作反应容器,可使反应物能循环利用,提高反应物的转化率
蒸馏
[通关1] (易错排查)判断正误
(1)(2020.7·浙江选考)萃取Br 时,向盛有溴水的分液漏斗中加入CCl ,振荡、静置分层后,
2 4
打开旋塞,先将水层放出(√)
(2)(2020.1·浙江选考)KCl和MnO 的混合物经溶解、过滤、洗涤、干燥,可分离出
2
MnO (√)
2
(3)(2020·北京卷)分离酒精和水: (×)
(4)(2019.4·浙江选考)蒸馏时可通过加碎瓷片防暴沸(√)
(5)(2019.4·浙江选考)用加水后再分液的方法可将苯和四氯化碳分离(×)
(6)(2018.11·浙江选考)用蒸馏的方法分离乙醇(沸点为78.3 ℃)和苯(沸点为80.1 ℃)的混
合物(×)
[通关2] (人教必修1·P ,3题改编)下列有关物质分离提纯的操作正确的是( )
10
A.为了加快过滤,可用玻璃棒搅拌悬浊液
B.蒸发时为了防止液体局部过热暴沸飞溅,可用玻璃棒不断搅拌
C.用乙醇萃取溴水中的溴后,在用蒸馏的方法分离溴和乙醇
D.分液时分液漏斗内的液体应依次从下口分别放出
B [过滤时不能用玻璃棒搅拌悬浊液,以防碰破滤纸,A项错误;乙醇可溶于水,不能用
作溴水的萃取剂,C项错误;分液时分液漏斗内的液体,下层液体应从下口放出,上层液体从
上口倒出,D项错误。][通关3] (2020·山东卷)实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeClD-,该配离子在乙醚(Et O,沸点34.6 ℃)中生
2
成缔合物EtO·H+·[FeCl ]-。下列说法错误的是( )
2 4
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
A [萃取时,分液漏斗下口应向上倾斜,A项错误;分液时,下层液体由下口放出,上层
液体从上口倒出,B项正确;萃取、分液后的水相是含Al3+的无色溶液,若含有[FeCl ]-,则水
4
相呈现黄色,说明未分离完全,C项正确;蒸馏时,为便于乙醚冷凝流出,应选用直形冷凝管,
D项正确。]
[通关4] (2019·全国卷Ⅱ)咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5 ℃,100 ℃
以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(K 约为
a
10-6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的
流程如下图所示。
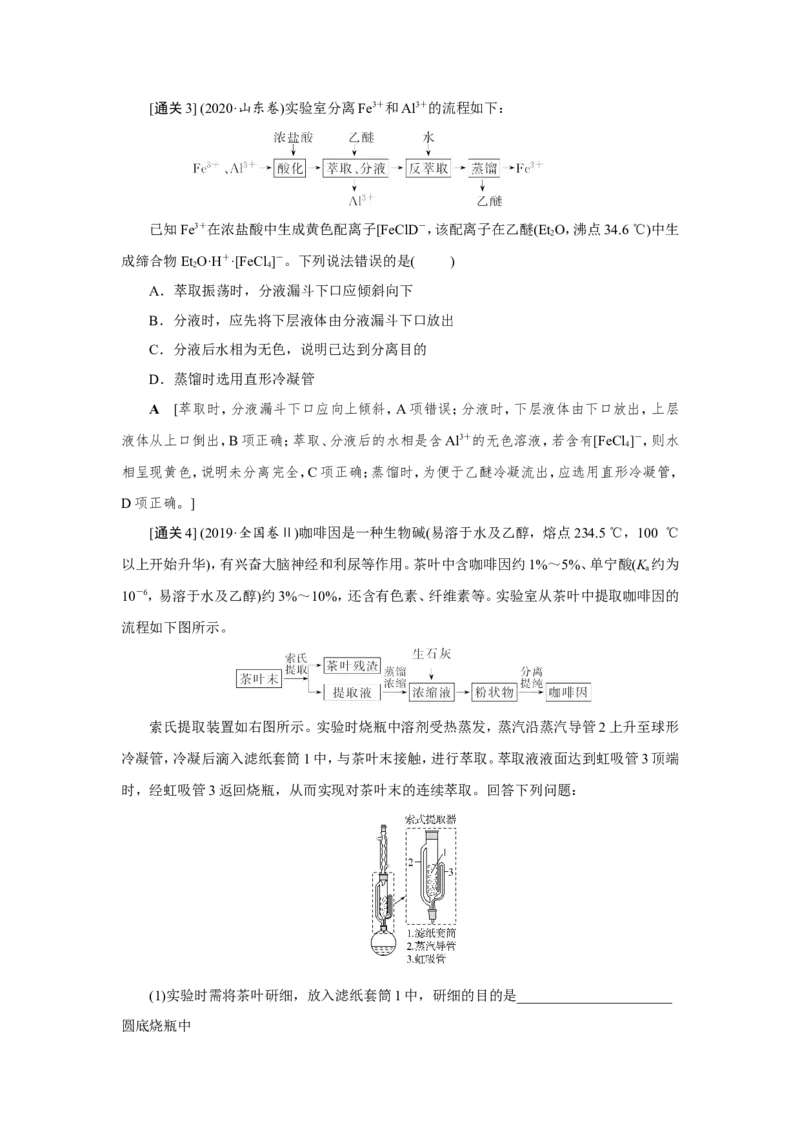
索氏提取装置如右图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形
冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端
时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________________
圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒________。
(2)提取过程不可选用明火直接加热,原因是__________________________。与常规的萃
取相比,采用索氏提取器的优点是____________________________________________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂的优点是
________________________________________________________________________。
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有
________(填标号)。
A.直形冷凝管 B.球形冷凝管
C.接收瓶 D.烧杯
(4)浓缩液加生石灰的作用是中和________和吸收________。
(5)可采用如下图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,
咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是________。
解析 (1)为提高浸取速率,常将反应物研细,增大固体与液体的接触面积;由于有机物
的沸点低,加热时易沸腾,因此常加入沸石,防止液体暴沸。
(2)乙醇的沸点低,易挥发、易燃烧,明火加热温度高,会导致乙醇挥发、燃烧,因此不能
选用明火直接加热。根据索氏萃取的原理描述可知,采用索氏提取器的优点是溶剂的用量减
少,可连续萃取(萃取效率高)。
(3)由于提取液需“蒸馏浓缩”除去大部分溶剂,所以与水相比,乙醇作为萃取剂的优点
是乙醇沸点低,易浓缩。“蒸馏浓缩”需选用的仪器有圆底烧瓶、蒸馏头、温度计、接收管、
直形冷凝管(球形冷凝管的主要用途是使气体冷却回流)、接收瓶等。
(4)茶叶中含单宁酸,加入生石灰的目的是中和单宁酸,同时吸收水分。
(5)粉状的咖啡因在蒸发皿中受热,在扎有小孔的滤纸上凝结变为固体,此过程称为升华。
答案 (1)增加固液接触面积,提取充分 沸石 (2)乙醇易挥发,易燃 使用溶剂少,可
连续萃取(萃取效率高) (3)乙醇沸点低,易浓缩 AC (4)单宁酸 水 (5)升华
知识点2 分离、提纯的常用化学方法1.除杂过程的“四项基本原则”
(1)不增,不得引入新杂质;
(2)不减,尽量不减少被提纯和分离的物质;
(3)易分,应使被提纯或分离的物质与其他物质易分离;
(4)易复原,被提纯物质转化后要易被复原。
2.除杂操作中的“四个注意”
(1)除杂试剂要过量;
(2)过量试剂需除去;
(3)选择的途径要最佳;
(4)除去多种杂质时要考虑加入试剂的先后顺序。
3.物质分离、提纯的常用化学方法
(1)溶解法:除去固体混合物中杂质的常用方法,选择合适的溶剂(酸或碱)将难溶杂质转
化为可溶性物质。例如:
①除去Fe粉(Al粉)[括号内为杂质,下同],可溶解在过量NaOH 溶液里,过滤分离。
②除去SiO(CaCO),可用足量盐酸溶解,过滤分离。
2 3
(2)吸收法:除去气体混合物中杂质的常用方法,例如:
①除去N(O ),可将混合气体通过加热的铜网,将氧气吸收。
2 2
②可用 酸性 KMnO 溶液(或饱和NaHCO 溶液)吸收CO 中的少量SO 气体。
4 3 2 2
(3)沉淀法:除去溶液中某些杂质离子的常用方法,选择合适的沉淀剂,将杂质离子转化
为难溶物质,再过滤分离。例如:
①除去食盐水中的Ca2+、Mg2+、SO等,可依次加入稍过量的NaOH、BaCl 、NaCO 过滤
2 2 3
分离沉淀、再加适量盐酸调pH。
②除去MgCl 溶液(Fe3+),可通过加MgO调pH,使 Fe 3 + 转化为 Fe(OH) 沉淀,再过滤分
2 3
离。
(4)气化法:将混合物中的杂质转化为气体的方法,例如:
①除去食盐水中的少量CO,可加适量盐酸除去。
②除去NaCl固体(NH Cl),可通过加热使NH Cl分解的方法除去。
4 4
(5)转化法:将杂质转化为被提纯的物质的方法。例如:
①除去CO(CO),将混合气体通过 加热的 CuO 。
2
②除去CO(HCl),将混合气体通过 饱和 NaHCO 溶液。
2 3③除去NaCO 固体(NaHCO ),通过加热灼烧固体混合物,使NaHCO 分解为NaCO。
2 3 3 3 2 3
④除去FeCl 溶液(Fe2+),在溶液中通入适量氯气,将Fe2+转化为Fe3+。
3
[通关1] (易错排查)判断正误
(1)(2019·全国卷Ⅲ)除去乙酸乙酯中的少量乙酸:加入饱和碳酸钠溶液洗涤、分液(√)
(2)(2019·天津卷)将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl(√)
2 2
(3)(2018.4·浙江选考)可用灼烧法除去氧化铜中混有的铜粉(√)
(4)(2017·天津卷)除去NaHCO 固体中的NaCO:将固体加热至恒重(×)
3 2 3
(5)(2017·天津卷)重结晶提纯苯甲酸:将粗品水溶、过滤、蒸发、结晶(×)
(6)(全国卷Ⅱ)除去Cu粉中混有CuO的实验操作是加入稀硝酸溶解、过滤、洗涤、干燥
(×)
[通关2] (2020·全国卷Ⅰ)下列气体去除杂质的方法中,不能实现目的的是( )
气体(杂质) 方法
A SO (H S) 通过酸性高锰酸钾溶液
2 2
B Cl(HCl) 通过饱和的食盐水
2
C N(O ) 通过灼热的铜丝网
2 2
D NO(NO ) 通过氢氧化钠溶液
2
A [SO 和HS均具有较强的还原性,都可以与酸性高锰酸钾溶液反应,A错误;Cl 难
2 2 2
溶于饱和食盐水,HCl易溶于饱和食盐水,B正确;二者通过灼热的铜丝网,只有O 与铜反应
2
生成氧化铜,C 正确;NO 和 NO 可以共同与氢氧化钠溶液发生反应 2NaOH+NO+
2
NO ===2NaNO +HO,因杂质含量少,虽消耗少量的NO,但除杂的目的可以实现,D正确。]
2 2 2
[通关3] (2019·北京卷)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是(
)
选项 物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
B [发生反应2Fe3++Fe===3Fe2+,但属于氧化还原反应,A项错误;发生Mg2+与OH-
生成Mg(OH) 沉淀的反应,过量的NaOH溶液用稀盐酸中和而除去,仅发生复分解反应,B
2
项正确;Cl 中混有HCl,应通过饱和食盐水除去,C项错误;发生NO 与水的反应:3NO +
2 2 2
HO===2HNO +NO,属于氧化还原反应,D项错误。]
2 3[通关4] (2021·河南部分重点校联考)下列实验的试剂、装置选用不合理的是( )
汈汈汈汈汈
选项 实验目的 选用试剂 选用装置
A 除去Cl 中少量的HCl、HO 试剂a为饱和氯化钠溶液 甲
2 2
B 除去NH 中少量的HO 试剂b为无水氯化钙 乙
3 2
C 除去H 中少量的HCl、HO 试剂b为碱石灰 乙
2 2
D 除去N 中少量的O 足量铜网 丙
2 2
B [甲装置中饱和氯化钠溶液可除去HCl,浓硫酸可除去HO,A正确;干燥管中的无水
2
氯化钙在除去水的同时也吸收NH ,B错误;干燥管中的碱石灰的主要成分为生石灰与氢氧
3
化钠,可除去HCl和HO,C正确;在加热条件下,O 可与丙装置中的铜网反应而被除去,D
2 2
正确。]
[通关5] (2021·江西九江六校联考)通过海水晾晒可以得到粗盐,粗盐除含有NaCl外,还
含有MgCl 、CaCl 、NaSO 以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,各步
2 2 2 4
操作流程如图。下列说法正确的是( )
A.实验过程中①、⑤步骤的操作分别是溶解、过滤
B.实验过程中步骤④的目的仅是除去溶液中的Ca2+
C.实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、铁架台(带铁圈)
D.实验过程中②、④步骤互换,对实验结果不影响
A [由实验流程可知,①为粗盐溶解,②中硫酸根离子用钡离子转化为沉淀,③中镁离
子用氢氧根离子沉淀,④中钙离子及过量钡离子用碳酸根离子沉淀,⑤为过滤,过滤分离出
所有的沉淀,滤液含NaCl、NaOH、NaCO,⑥中用盐酸处理溶液中的碳酸根离子和氢氧根离
2 3
子,⑦为蒸发、结晶、烘干,得到精盐。]知识点3 常见物质的检验方法
1.常见气体的检验方法
气体 特征性质 注意事项
O 使带火星的木条复燃 —
2
纯净的H 在空气中燃烧发出淡蓝色火焰,
2
H 在火焰上方罩一个干而冷的烧杯,烧杯的 产物只有水
2
内壁有水雾生成
在空气中燃烧产生淡蓝色火焰,生成无色
CO 产物只有二氧化碳
无味且能使澄清石灰水变浑浊的气体
无色,具有刺激性气味;能使品红溶液褪 SO 的漂白原理与新制氯水的漂白
SO 2
2 色,加热后恢复红色 原理不同
能使澄清石灰水变浑浊,能使燃着的木条 SO 也能使澄清石灰水变浑浊,N
CO 2 2
2 熄灭 也能使燃着的木条熄灭
黄绿色,有刺激性气味,能使湿润的淀粉碘
Cl Cl 有毒,注意闻气味的方法
2 化钾试纸变蓝 2
无色,有刺激性气味,能使湿润的红色石蕊
NH 极易溶于水,做相关实验时应
NH 试纸变蓝;用蘸有浓盐酸的玻璃棒靠近时 3
3 防倒吸
冒白烟
2.常见阳离子的检验
常见阳离子 试剂或方法 实验现象
①紫色石蕊试液 ①变红
H+
②活泼金属(如Zn)或碳酸盐 ②有无色无味气体产生
Na+ 焰色反应 黄色火焰
K+ 焰色反应 紫色火焰(透过蓝色钴玻璃)Mg2+ NaOH溶液 白色沉淀,不溶于过量的碱
Al3+ NaOH溶液 白色沉淀,溶于过量的强碱
①NaOH溶液 ①白色沉淀→灰绿色→红褐色
Fe2+
②先加KSCN溶液,再加氯水 ②无明显变化,滴加氯水后变血红色
①NaOH溶液 ①生成红褐色沉淀
Fe3+
②KSCN溶液 ②溶液呈红色
3.常见阴离子的检验
→
→
→
→
→
→
[通关1] (易错排查)判断正误
(1)(2020.7·浙江选考)可用AgNO 溶液和稀HNO 区分NaCl、NaNO 和NaNO (√)
3 3 2 3
(2)(2020.1·浙江选考)火柴头的浸泡液中滴加AgNO 溶液、稀HNO 和NaNO 溶液,可检
3 3 2
验火柴头是否含有氯元素(√)
(3)(2018·全国卷Ⅲ)用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+
(√)
(4)(2018·天津卷)某溶液中滴加K[Fe(CN) ]溶液,产生蓝色沉淀,则原溶液中有Fe2+、无
3 6
Fe3+(×)(5)(2018·天津卷)某溶液中加入Ba(NO ) 溶液,产生白色沉淀,再加足量盐酸,仍有白色
3 2
沉淀,则原溶液中有SO(×)
[通关2] (2020·天津卷)检验下列物质所选用的试剂正确的是( )
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的NH NaOH溶液,湿润的蓝色石蕊试纸
C [淀粉遇碘单质变蓝色,而海水中碘元素的存在形式为I—,A项错误;CO 和SO 与澄
2 2
清石灰水反应现象相同,B项错误;向含Cu2+的溶液中滴加氨水首先产生蓝色沉淀,继续添
加氨水,沉淀溶解,得到深蓝色的透明溶液,C项正确;检验氨气应用湿润的红色石蕊试纸,D
项错误。]
[通关3](2021·福建福州质检)向四支试管中分别加入少量不同的无色溶液进行如下操作,
结论正确的是( )
选项 操作 现象 结论
A 滴加BaCl 溶液 生成白色沉淀 原溶液中有SO
2
B 滴加稀硫酸 有刺激性气味的气体产生 原溶液中有SO
用洁净铂丝蘸取溶液进行焰 火焰呈紫色(透过蓝色钴玻
C 原溶液中有K+
色反应 璃)
滴加NaOH溶液,将湿润的红
D 试纸不变蓝 原溶液中无NH
色石蕊试纸置于试管口
C [加入BaCl 溶液得到白色沉淀,原溶液中可能含有SO或SO或Ag+,A错误;HSO
2
也有同样的现象,B错误;,观察K+的焰色反应应透过蓝色钴玻璃,排除Na+的干扰,C正确;
检验NH应加入浓NaOH溶液,且需要加热,D错误。]
离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施
SO 加过量的Ba(NO ) 溶液
3 2
Cl- CO
加稀硝酸酸化
OH-
CO
SO SO 加盐酸酸化
Ag+
SO CO 加盐酸后将产生的气体通入品红溶液中CO SO 加硝酸后将产生的无色无味气体通入澄清石灰水,变浑浊
[通关4] (2018·全国卷Ⅱ)在三草酸合铁酸钾的热分解产物含有FeO和Fe O,检验Fe O
2 3 2 3
存在的方法是:______________________________________________________________
________________________________________________________________________。
答案 取少量装置残留物放入试管中,加入稀硫酸溶解,再滴加几滴KSCN溶液,若观
察到溶液变红,则证明残留物中含Fe O
2 3
训练(四十八) 物质的分离、提纯与检验
1.(2021·河南洛阳检测)南朝陶弘景在《本草经集注》中记载有鉴别消石(KNO)与朴消
3
(Na SO )之法:“强烧之,紫青烟起,云是真消石也”。该鉴别方法利用的原理是( )
2 4
A.受热升华 B.颜色反应
C.焰色反应 D.丁达尔效应
C [含有钾元素的物质在火焰上灼烧,火焰呈紫色(透过蓝色钴玻璃观察),该原理为焰
色反应,C项正确。]
2.(2021·四川新津中学检测)下列有关操作的说法不正确的是( )
A.《本草经集注》记载了鉴别硝石(KNO)和朴硝(Na SO )的方法:“以火烧之,紫青烟起,
3 2 4
乃真硝石也”,此处运用了物质升华的性质
B.《本草纲目》记载了烧酒的制作工艺: “凡酸坏之酒,皆可蒸烧”,此处用到的操作是
蒸馏
C.《肘后备急方》一书中有“青蒿一握,以水二升渍,绞其汁”,此处用到的操作是溶解
D.唐诗有“千淘万漉虽辛苦,吹尽狂沙始到金”的诗句,此处用到的操作是过滤
A [钾元素的焰色反应为紫色,钠元素的焰色反应为黄色,则硝石(KNO)和朴硝
3(Na SO )可通过焰色反应来鉴别,A项错误;《本草纲目》中“凡酸坏之酒,皆可蒸烧”,酸坏
2 4
之酒中含有乙酸,利用乙酸和乙醇的沸点不同进行分离,该操作为蒸馏,B项正确;“以水二
升渍”中的“渍”即为浸泡溶解,C项正确;诗句中的“淘”和“漉”的原理和过滤的原理
相同,D项正确。]
3.(2021·山东莱芜一中检测)为提纯下列物质(括号内为杂质),选用的试剂或分离方法错
误的是( )
选项 物质 试剂 分离方法
A 硝酸钾(氯化钠) 蒸馏水 降温结晶
B 二氧化碳(氯化氢) 饱和NaHCO 溶液 洗气
3
C 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
D 乙醇(水) 生石灰 蒸馏
C [KNO 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,可加蒸馏水
3
溶解固体,再通过蒸发浓缩、降温结晶的方法,获得纯净的KNO 固体,A项正确;HCl与饱和
3
NaHCO 溶液反应生成二氧化碳,B项正确;乙烯被酸性KMnO 氧化生成CO,使甲烷中混
3 4 2
入CO 气体,C项错误;加入的生石灰能与水反应生成Ca(OH) ,消耗掉部分水,再通过蒸馏
2 2
获得乙醇,D项正确。]
4.(2021·江西景德镇统考)某同学为检验溶液中是否含有常见的几种无机离子,进行了
如图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验
能得到的正确结论是( )
A.原溶液中一定含有SO
B.原溶液中一定含有NH
C.原溶液中一定含有Cl-
D.原溶液中一定含有Fe3+
B [原溶液中加入Ba(NO ) 溶液和HCl生成白色沉淀,原溶液中可能存在SO、SO或
3 2
Ag+,A项错误;因检验过程中产生的气体能使湿润的红色石蕊试纸变蓝,说明原溶液中一定
含有NH,B项正确;加AgNO 溶液产生白色沉淀,可能是加入的HCl引起的,C项错误;加
3
入KSCN溶液得到红色溶液,Fe3+可能是由原溶液中的Fe2+被H+、NO氧化而来的,故原溶
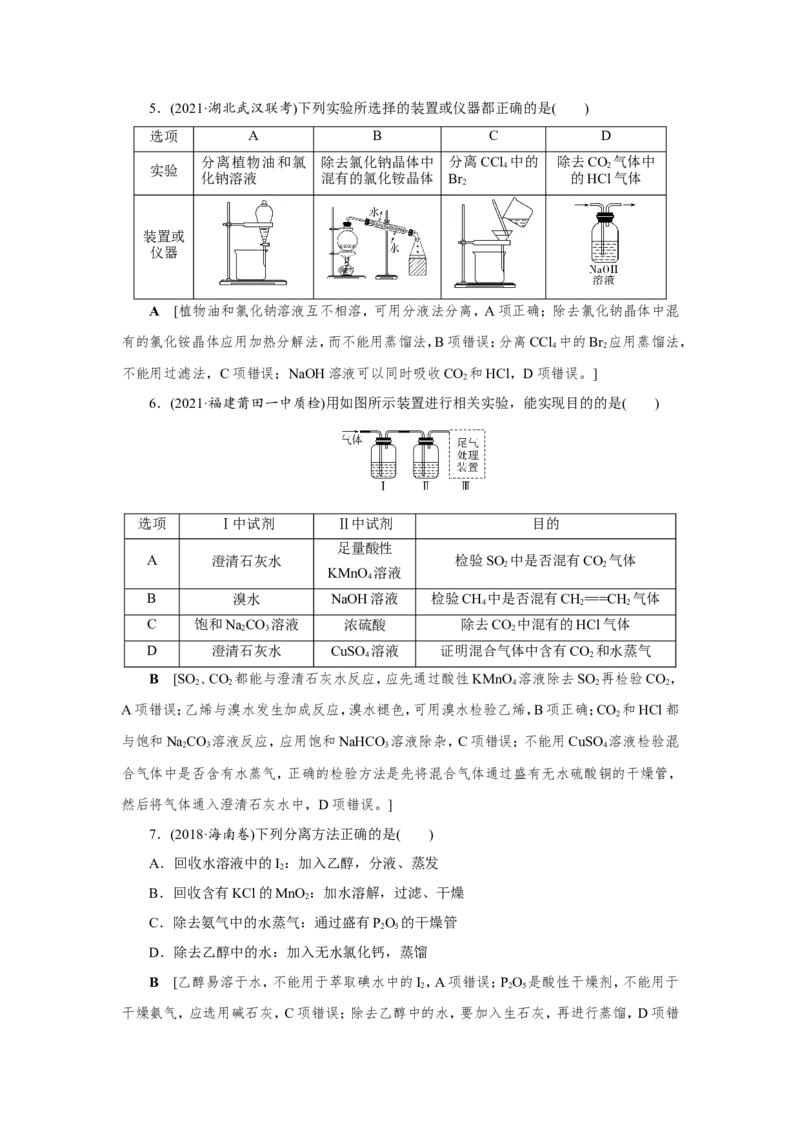
液中不一定含有Fe3+,D项错误。]5.(2021·湖北武汉联考)下列实验所选择的装置或仪器都正确的是( )
选项 A B C D
分离植物油和氯 除去氯化钠晶体中 分离CCl 中的 除去CO 气体中
实验 4 2
化钠溶液 混有的氯化铵晶体 Br 的HCl气体
2
装置或
仪器
A [植物油和氯化钠溶液互不相溶,可用分液法分离,A项正确;除去氯化钠晶体中混
有的氯化铵晶体应用加热分解法,而不能用蒸馏法,B项错误;分离CCl 中的Br 应用蒸馏法,
4 2
不能用过滤法,C项错误;NaOH溶液可以同时吸收CO 和HCl,D项错误。]
2
6.(2021·福建莆田一中质检)用如图所示装置进行相关实验,能实现目的的是( )
选项 Ⅰ中试剂 Ⅱ中试剂 目的
足量酸性
A 澄清石灰水 检验SO 中是否混有CO 气体
2 2
KMnO 溶液
4
B 溴水 NaOH溶液 检验CH 中是否混有CH===CH 气体
4 2 2
C 饱和NaCO 溶液 浓硫酸 除去CO 中混有的HCl气体
2 3 2
D 澄清石灰水 CuSO 溶液 证明混合气体中含有CO 和水蒸气
4 2
B [SO 、CO 都能与澄清石灰水反应,应先通过酸性KMnO 溶液除去SO 再检验CO,
2 2 4 2 2
A项错误;乙烯与溴水发生加成反应,溴水褪色,可用溴水检验乙烯,B项正确;CO 和HCl都
2
与饱和NaCO 溶液反应,应用饱和NaHCO 溶液除杂,C项错误;不能用CuSO 溶液检验混
2 3 3 4
合气体中是否含有水蒸气,正确的检验方法是先将混合气体通过盛有无水硫酸铜的干燥管,
然后将气体通入澄清石灰水中,D项错误。]
7.(2018·海南卷)下列分离方法正确的是( )
A.回收水溶液中的I:加入乙醇,分液、蒸发
2
B.回收含有KCl的MnO :加水溶解,过滤、干燥
2
C.除去氨气中的水蒸气:通过盛有PO 的干燥管
2 5
D.除去乙醇中的水:加入无水氯化钙,蒸馏
B [乙醇易溶于水,不能用于萃取碘水中的I,A项错误;PO 是酸性干燥剂,不能用于
2 2 5
干燥氨气,应选用碱石灰,C项错误;除去乙醇中的水,要加入生石灰,再进行蒸馏,D项错误。]
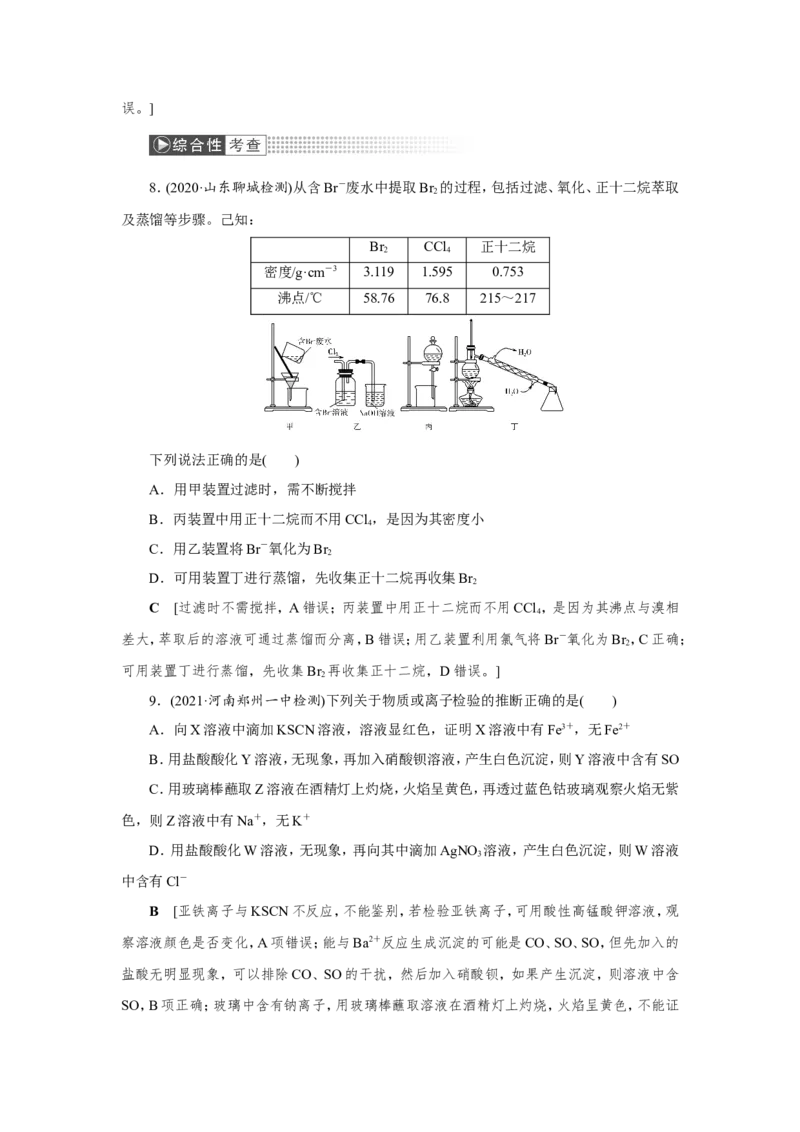
8.(2020·山东聊城检测)从含Br-废水中提取Br 的过程,包括过滤、氧化、正十二烷萃取
2
及蒸馏等步骤。己知:
Br CCl 正十二烷
2 4
密度/g·cm-3 3.119 1.595 0.753
沸点/℃ 58.76 76.8 215~217
下列说法正确的是( )
A.用甲装置过滤时,需不断搅拌
B.丙装置中用正十二烷而不用CCl ,是因为其密度小
4
C.用乙装置将Br-氧化为Br
2
D.可用装置丁进行蒸馏,先收集正十二烷再收集Br
2
C [过滤时不需搅拌,A错误;丙装置中用正十二烷而不用CCl ,是因为其沸点与溴相
4
差大,萃取后的溶液可通过蒸馏而分离,B错误;用乙装置利用氯气将Br-氧化为Br ,C正确;
2
可用装置丁进行蒸馏,先收集Br 再收集正十二烷,D错误。]
2
9.(2021·河南郑州一中检测)下列关于物质或离子检验的推断正确的是( )
A.向X溶液中滴加KSCN溶液,溶液显红色,证明X溶液中有Fe3+,无Fe2+
B.用盐酸酸化Y溶液,无现象,再加入硝酸钡溶液,产生白色沉淀,则Y溶液中含有SO
C.用玻璃棒蘸取Z溶液在酒精灯上灼烧,火焰呈黄色,再透过蓝色钴玻璃观察火焰无紫
色,则Z溶液中有Na+,无K+
D.用盐酸酸化W溶液,无现象,再向其中滴加AgNO 溶液,产生白色沉淀,则W溶液
3
中含有Cl-
B [亚铁离子与KSCN不反应,不能鉴别,若检验亚铁离子,可用酸性高锰酸钾溶液,观
察溶液颜色是否变化,A项错误;能与Ba2+反应生成沉淀的可能是CO、SO、SO,但先加入的
盐酸无明显现象,可以排除CO、SO的干扰,然后加入硝酸钡,如果产生沉淀,则溶液中含
SO,B项正确;玻璃中含有钠离子,用玻璃棒蘸取溶液在酒精灯上灼烧,火焰呈黄色,不能证明溶液中是否含有钠离子,C项错误;盐酸中也含有氯离子,不能证明原溶液中是否含有氯
离子,D项错误。]
10.(2021·天津静海区四校联考)下列实验操作能达到相应实验目的的是( )
选项 实验操作 实验目的
A 向FeCl 、CuCl 的混合溶液中加入足量铁粉,然后过滤 提纯FeCl
3 2 3
向含有Br 的苯中加入适量的NaOH溶液,然后充分振荡、静
B 2 除去杂质Br
置、分液 2
C 将含有少量NaCl杂质的KNO 固体溶于水,然后蒸发结晶 提纯KNO
3 3
向MgCl 、AlCl 混合溶液中加入过量的NaOH溶液,过滤后
D 2 3 分离MgCl 、AlCl
将沉淀溶于适量的盐酸;向滤液中加入适量盐酸 2 3
B [向FeCl 、CuCl 的混合溶液中加入足量铁粉,FeCl 会和Fe反应生成FeCl ,A项错
3 2 3 2
误;Br 和NaOH溶液反应生成易溶于水的NaBr和NaBrO,充分振荡、静置、分液可以除去杂
2
质Br ,B项正确;KNO 的溶解度随温度升高变化较大,而NaCl的溶解度受温度影响不大,
2 3
要提纯KNO,将含有少量NaCl杂质的KNO 固体溶于水,蒸发浓缩、冷却结晶,然后过滤即
3 3
可得较纯净的KNO,C项错误;滤液中含有过量的NaOH溶液,向滤液中加入适量盐酸后会
3
有NaCl生成,D项错误。]
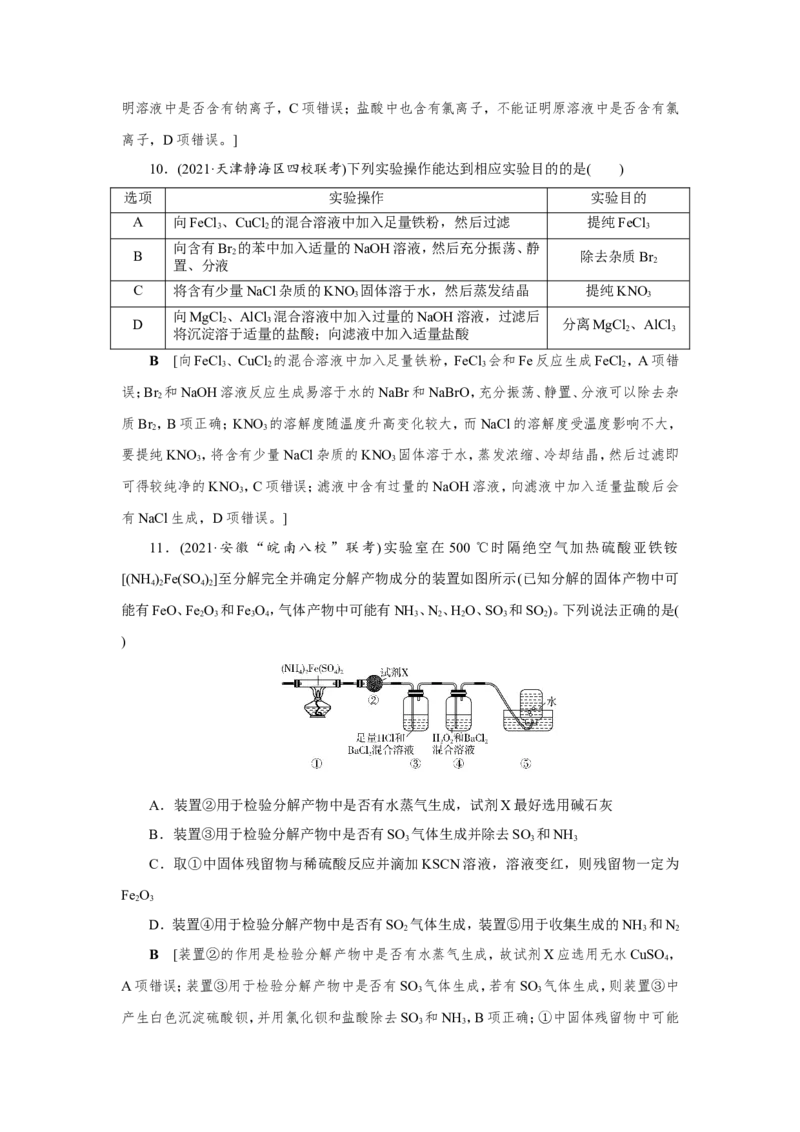
11.(2021·安徽“皖南八校”联考)实验室在 500 ℃时隔绝空气加热硫酸亚铁铵
[(NH )Fe(SO )]至分解完全并确定分解产物成分的装置如图所示(已知分解的固体产物中可
4 2 4 2
能有FeO、Fe O 和Fe O,气体产物中可能有NH 、N、HO、SO 和SO )。下列说法正确的是(
2 3 3 4 3 2 2 3 2
)
A.装置②用于检验分解产物中是否有水蒸气生成,试剂X最好选用碱石灰
B.装置③用于检验分解产物中是否有SO 气体生成并除去SO 和NH
3 3 3
C.取①中固体残留物与稀硫酸反应并滴加KSCN溶液,溶液变红,则残留物一定为
Fe O
2 3
D.装置④用于检验分解产物中是否有SO 气体生成,装置⑤用于收集生成的NH 和N
2 3 2
B [装置②的作用是检验分解产物中是否有水蒸气生成,故试剂X应选用无水CuSO ,
4
A项错误;装置③用于检验分解产物中是否有SO 气体生成,若有SO 气体生成,则装置③中
3 3
产生白色沉淀硫酸钡,并用氯化钡和盐酸除去SO 和NH ,B项正确;①中固体残留物中可能
3 3还含有FeO,可能不含有Fe O 而含有Fe O,不一定为Fe O,C项错误;NH 极易溶于水,若
2 3 3 4 2 3 3
分解产物中有NH ,则NH 被装置③中的溶液吸收,装置⑤中不可能收集到NH ,D项错误。]
3 3 3
12.(2021·河北衡水中学调研)工业品MnCl 溶液中含有杂质,利用锰粉、草酸、硫酸锰分
2
别依次除去Pb2+、Ca2+、Mg2+制得纯净的MnCl 。工艺流程如下:
2
已知:①草酸为二元弱酸,其钠盐、钾盐易溶于水,钙盐难溶于水。
②硫酸镁晶体、硫酸锰的溶解度曲线如下图:
回答下列问题:
(1)过滤所需的玻璃仪器主要有____________________,加热搅拌的作用是
________________。
(2)弃渣Ⅰ、Ⅱ、Ⅲ的主要成分分别为________________、____________、______________。
反应①的离子方程式为________________________________________________________。
(3)反应②的离子方程式为_____________________________________________。
(4)③加热搅拌、静置过滤时,所选择的温度的范围是______。
a.0~20 ℃ b.20~40 ℃ c.40~60 ℃ d.80~90 ℃
(5)④加入氯化钡溶液主要是为了除去________,检验该离子是否除尽的方法为
________________________________________________________________________
________________________________________________________________________。
(6)已知MnCl 溶液呈弱酸性,操作X为________(填字母)。
2a.蒸发结晶 b.降温结晶 c.萃取分液 D.蒸馏
解析 (1)过滤所需的玻璃仪器主要有漏斗、烧杯、玻璃棒,加热搅拌的作用是加快反应
速率。
(2)根据题意,结合流程图知,反应①为除Pb2+,则弃渣Ⅰ为铅及少量锰粉;反应③除镁
离子,则弃渣Ⅱ为硫酸镁晶体;反应④为除去引入的硫酸根离子,则弃渣Ⅲ为硫酸钡。
(3)草酸与Ca2+反应生成草酸钙沉淀,注意草酸为弱酸,不能拆写成离子。
(4)根据硫酸锰与硫酸镁晶体的溶解度曲线,可知在80~90 ℃的范围内二者溶解度差别
最大,且硫酸镁晶体的溶解度最小。
(6)MnCl 溶液呈弱酸性,是因为Mn2+水解,不能用蒸发结晶的方法,而用蒸发浓缩、冷
2
却结晶(即降温结晶)的方法。
答案 (1)漏斗、烧杯、玻璃棒 加快反应速率
(2)铅及少量锰粉 MgSO ·7H O 硫酸钡(或BaSO) Mn+Pb2+===Mn2++Pb
4 2 4
(3)H C O+Ca2+===CaC O↓+2H+ (4)d (5)SO 取少量上层澄清溶液于试管中,滴
2 2 4 2 4
加BaCl 溶液,如无沉淀出现则说明SO已除尽,反之则没有除尽 (6)b
2