文档内容
第 11 讲 物质的分离与提纯
[复习目标] 1.掌握常见物质分离和提纯的方法。2.能综合运用物质的不同性质对常见的物
质进行分离和提纯。
考点一 物质分离、提纯的常用物理方法及装置
(一)物质分离与提纯的区别
分离 将混合物的各组分分开,获得几种纯净物的过程
将混合物中的杂质______而得到______的过程,又叫
提纯
物质的净化或除杂
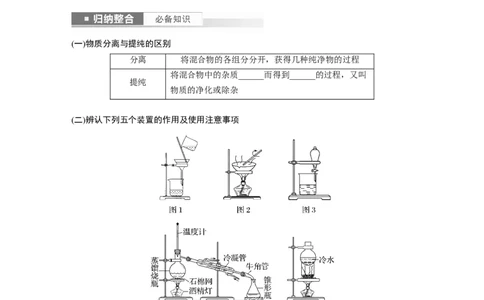
(二)辨认下列五个装置的作用及使用注意事项
1.固液分离
(1)图1为________装置,适用于____________与液体的分离。操作注意:一贴、二低、三
靠。
(2)图2为蒸发装置,溶解度随温度变化不大的易溶性固体溶质,采用蒸发结晶;溶解度受
温度变化较大的易溶性固体溶质,采用蒸发浓缩、降温结晶的方法。
注意:在蒸发结晶操作中:①玻璃棒的作用:搅拌,防止液体局部过热而飞溅;②当有大量
晶体析出时,停止加热,利用余热蒸干而不能直接蒸干。2.液液分离
(1)图3为分液装置,分离两种____________且易分层的液体。
注意:下层液体从________放出,上层液体由________倒出。
(2)图4为蒸馏装置,分离________相差较大且互溶的液体混合物。
注意:①温度计的水银球在蒸馏烧瓶的支管口处;②蒸馏烧瓶中要加沸石或碎瓷片,目的是
防止暴沸;③冷凝管水流方向为下口进,上口出。
3.固固分离
图5为升华装置,适应于某种组分易________的混合物的分离。
1.过滤时,为加快过滤速度,应用玻璃棒不断搅拌漏斗中的液体( )
2.根据食用油和汽油的密度不同,可选用分液的方法分离( )
3.用乙醇萃取出溴水中的溴,再用蒸馏的方法分离溴与乙醇( )
4.在蒸馏过程中,若发现忘加沸石,应停止加热立即补加( )
5.利用加热的方法分离NH Cl和I 的固体混合物( )
4 2
6.制取无水乙醇可向乙醇中加入CaO之后过滤( )
1.利用物质的溶解度对物质进行分离、提纯
图甲、图乙所示为一些物质的溶解度随温度变化的曲线。
(1) A点KNO 溶液是__________(填“饱和溶液”或“不饱和溶液”)。
3
(2)将B点KNO 溶液变成饱和溶液的方法有__________________________________
3
________________________________________________________________________。
(3)常温下,由NaCl稀溶液获取NaCl固体的方法是__________。
(4)常温下由KNO 稀溶液获取KNO 固体的方法是____________________________。
3 3
(5) NaCl固体中含少量KNO,提纯NaCl固体的方式是__________________________。
3
(6) KNO 固体中含少量NaCl,提纯KNO 固体的方式是____________________________。
3 3
(7)图乙所示为NaSO 的溶解度随温度的变化曲线。常温下由 NaSO 稀溶液获取NaSO 固
2 3 2 3 2 3
体的方法是什么?_________________________________________________________。
2.物质分离操作注意事项(1) 从MgSO 溶液中得到MgSO 固体的实验操作包括________、冷却结晶、________、洗
4 4
涤、干燥等一系列操作,在此过程中玻璃棒的作用是________(填序号)。
①引流 ②搅拌加速溶解 ③搅拌使溶液受热均匀,防止暴沸
(2)过滤后,若滤液浑浊,需__________________________________________________。
浑浊的原因可能是___________________________________________________________。
(3)硫酸铝和硫酸铵的混合液经蒸发浓缩至溶液表面刚出现薄层晶体时即停止加热,然后冷
却 结 晶 , 得 到 铵 明 矾 晶 体 [NH Al(SO )·12H O] 。 溶 液 不 能 蒸 干 的 原 因 是
4 4 2 2
___________________。
(4)分液时,分液漏斗中的液体很难滴下,可能的原因是_______________________________。
考点二 物质分离、提纯的化学方法
1.除杂“四原则”
(1)不增,不得引入新杂质。
(2)不减,尽量不减少被提纯和分离的物质。
(3)易分,应使被提纯或分离的物质与其他物质易分离。
(4)易复原,被提纯物质转化后要易被复原。
2.除杂操作“四注意”
(1)除杂试剂要过量。
(2)过量试剂需除去。
(3)选择的途径要最佳。
(4)除去多种杂质时要考虑加入试剂的先后顺序。
3.物质分离提纯常用的化学方法
方法 原理
当混合物中混有热稳定性差的物质时,可直接加热,使热稳定性差的物
加热法
质受热分解而分离出,如NaCO 固体中的NaHCO
2 3 3
当某气体中含有杂质气体时,可把混合气体通入某溶液中而除去,或转
洗气法
化成该气体,如乙烷中的乙烯可通过溴水而除去
在混合物中加入某种试剂,使其中一种以沉淀的形式分离出去的方法。
沉淀法 使用该方法一定要注意不能引入新的杂质,如可用适量的BaCl 除去
2
NaCl中的NaSO
2 4
氧化还原 如果混合物中混有氧化性杂质,可以加入适当的还原剂使其还原为被提
反应法 纯物质,如可用过量的铁粉除去FeCl 溶液中的FeCl
2 3
电解法 利用电解原理来分离、提纯物质,如电解精炼铜通过加入试剂来调节溶液的pH,使溶液中某组分沉淀而分离的方法,
调节pH法 一般是加入相应的难溶或微溶物来调节,如除去CuCl 中的FeCl ,可加
2 3
入CuO,使Fe3+生成Fe(OH) 过滤除去
3
4.物质分离提纯常用化学方法应用举例
主要成分(杂质) 除杂试剂 主要操作方法
N(O )
2 2
用固体转化气体
CO(CO)
2
CO(CO ) 洗气或用固体转化气体
2
CO(HCl)
2
CO(SO ) 洗气
2 2
SO (HCl)
2
NaHCO 溶液(Na CO)
3 2 3
杂转纯
FeCl 溶液(FeCl )
3 2
MgCl 溶液(FeCl ) 调pH转为沉淀,过滤
2 3
粗铜 精铜、CuSO 溶液 电解精炼
4
1.CO 中的HCl可通过饱和NaCO 溶液除去( )
2 2 3
2.分离Fe O、Al O 的操作依次为溶解、过滤、灼烧( )
2 3 2 3
3.蒸馏、过滤、分液、洗气四种分离物质的方法,均不可能发生化学变化( )
4.向MgCl 溶液中加入CaCO 粉末,充分搅拌后过滤可除去杂质FeCl ( )
2 3 3
5.将Cl 和HCl的混合气体通过饱和食盐水可得到纯净的Cl( )
2 2
6.除去NaCl溶液中少量的NaS,可加入AgCl后再过滤( )
2
一、常见物质分离操作方法、装置的选择
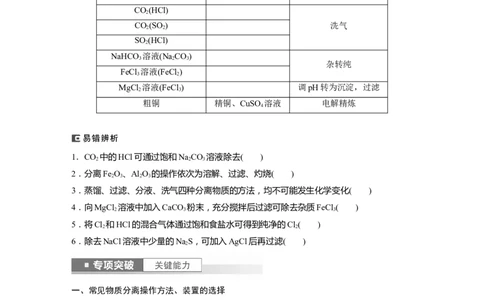
1.常见气体除杂装置的选择
除去气体中的杂质通常有如下3套装置,请选择合适的装置序号填入下列空格中。注:括号内为杂质气体
(1)CO (HCl):________。(2)CO (CO):________。
2 2
(3)CO(CO ):________。
2
2.常见固体混合物除杂
请按要求填写合适的除杂方法或化学方程式(括号内为杂质)
(1)NaCl(I ):______________________________________________________________。
2
(2)Fe O(AlO):加过量NaOH溶液,过滤、洗涤,离子方程式:____________________。
2 3 2 3
(3)CuO(C):________________,化学方程式:_____________________________________。
(4)镁粉(铝粉):_______________________________,化学方程式:___________________。
二、沉淀分离操作的规范解答
3.在测定NaSO 和NaCl的混合物中 NaSO 的质量分数时,可以在混合物中加入过量
2 4 2 4
BaCl 溶液,沉淀SO,然后过滤、洗涤、烘干、称量得到BaSO 的质量,试问:
2 4
(1)怎样判断SO是否沉淀完全?
______________________________________________________________________________
(2)过滤完毕后,为什么要洗涤沉淀(即洗涤沉淀的目的)?
______________________________________________________________________________
(3)沉淀的洗涤方法?
______________________________________________________________________________
(4)怎样判断沉淀是否洗净?
______________________________________________________________________________
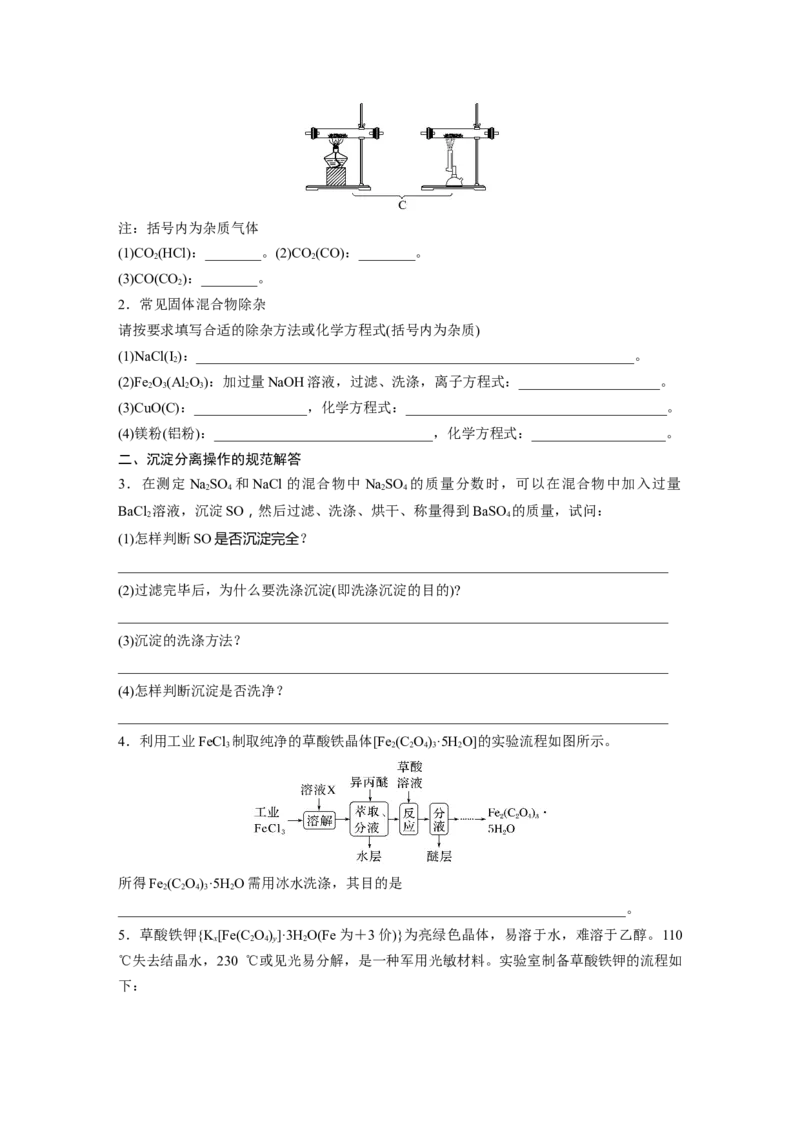
4.利用工业FeCl 制取纯净的草酸铁晶体[Fe (C O)·5H O]的实验流程如图所示。
3 2 2 4 3 2
所得Fe (C O)·5H O需用冰水洗涤,其目的是
2 2 4 3 2
________________________________________________________________________。
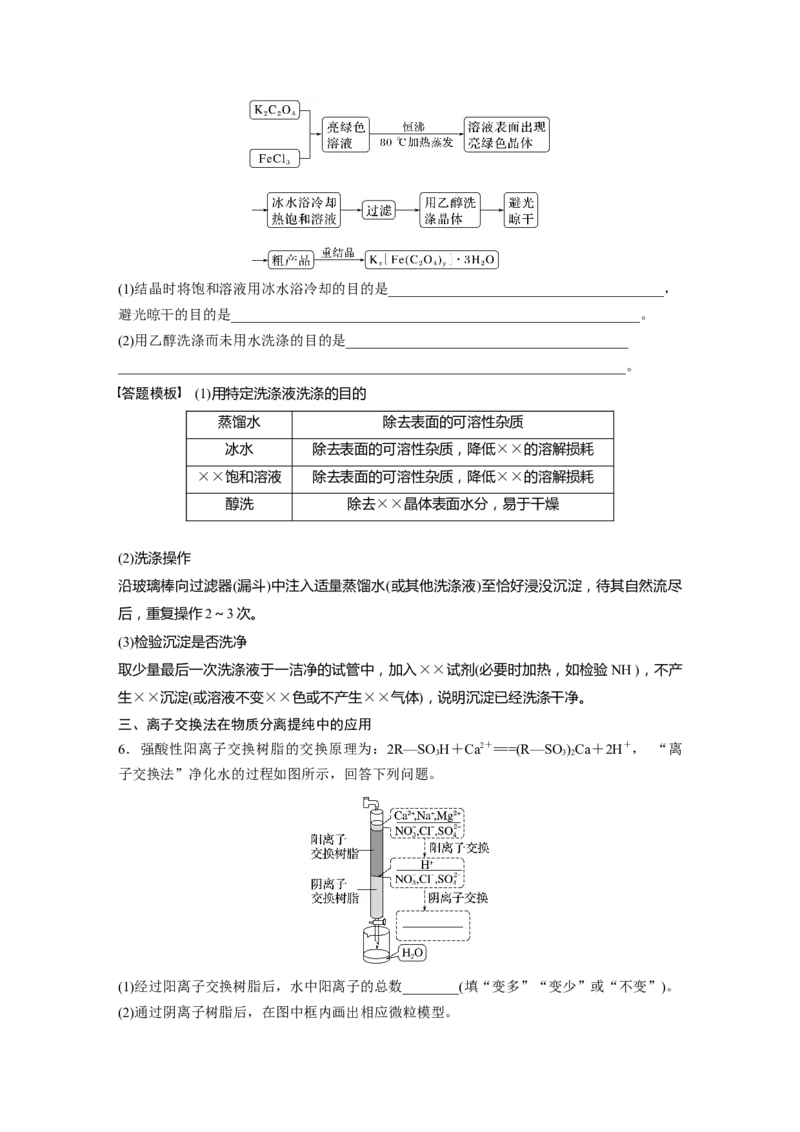
5.草酸铁钾{K[Fe(C O)]·3H O(Fe为+3价)}为亮绿色晶体,易溶于水,难溶于乙醇。110
x 2 4 y 2
℃失去结晶水,230 ℃或见光易分解,是一种军用光敏材料。实验室制备草酸铁钾的流程如
下:(1)结晶时将饱和溶液用冰水浴冷却的目的是_______________________________________,
避光晾干的目的是__________________________________________________________。
(2)用乙醇洗涤而未用水洗涤的目的是________________________________________
________________________________________________________________________。
答题模板 (1)用特定洗涤液洗涤的目的
蒸馏水 除去表面的可溶性杂质
冰水 除去表面的可溶性杂质,降低××的溶解损耗
××饱和溶液 除去表面的可溶性杂质,降低××的溶解损耗
醇洗 除去××晶体表面水分,易于干燥
(2)洗涤操作
沿玻璃棒向过滤器(漏斗)中注入适量蒸馏水(或其他洗涤液)至恰好浸没沉淀,待其自然流尽
后,重复操作2~3次。
(3)检验沉淀是否洗净
取少量最后一次洗涤液于一洁净的试管中,加入××试剂(必要时加热,如检验NH ),不产
生××沉淀(或溶液不变××色或不产生××气体),说明沉淀已经洗涤干净。
三、离子交换法在物质分离提纯中的应用
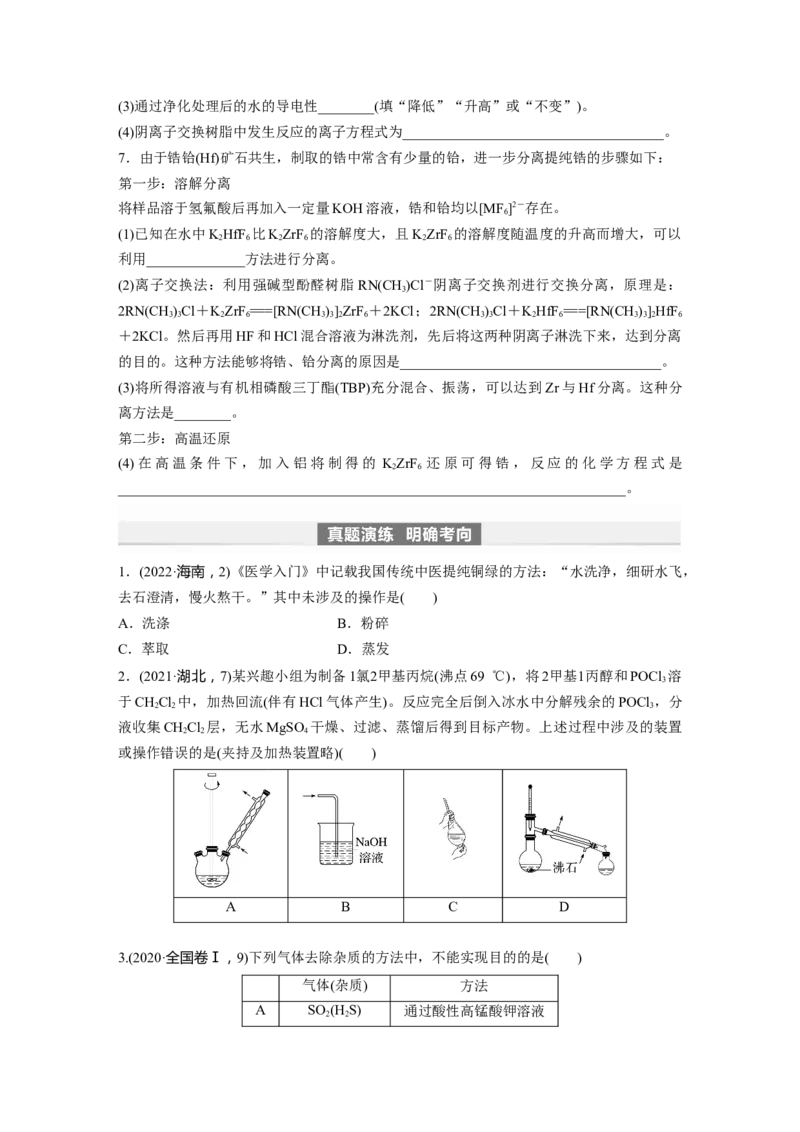
6.强酸性阳离子交换树脂的交换原理为:2R—SO H+Ca2+===(R—SO )Ca+2H+, “离
3 3 2
子交换法”净化水的过程如图所示,回答下列问题。
(1)经过阳离子交换树脂后,水中阳离子的总数________(填“变多”“变少”或“不变”)。
(2)通过阴离子树脂后,在图中框内画出相应微粒模型。(3)通过净化处理后的水的导电性________(填“降低”“升高”或“不变”)。
(4)阴离子交换树脂中发生反应的离子方程式为_____________________________________。
7.由于锆铪(Hf)矿石共生,制取的锆中常含有少量的铪,进一步分离提纯锆的步骤如下:
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF ]2-存在。
6
(1)已知在水中KHfF 比KZrF 的溶解度大,且KZrF 的溶解度随温度的升高而增大,可以
2 6 2 6 2 6
利用______________方法进行分离。
(2)离子交换法:利用强碱型酚醛树脂 RN(CH )Cl-阴离子交换剂进行交换分离,原理是:
3
2RN(CH )Cl+KZrF ===[RN(CH )]ZrF +2KCl;2RN(CH )Cl+KHfF ===[RN(CH )]HfF
3 3 2 6 3 3 2 6 3 3 2 6 3 3 2 6
+2KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离
的目的。这种方法能够将锆、铪分离的原因是_____________________________________。
(3)将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分
离方法是________。
第二步:高温还原
(4)在高温条件下,加入铝将制得的 KZrF 还原可得锆,反应的化学方程式是
2 6
________________________________________________________________________。
1.(2022·海南,2)《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,
去石澄清,慢火熬干。”其中未涉及的操作是( )
A.洗涤 B.粉碎
C.萃取 D.蒸发
2.(2021·湖北,7)某兴趣小组为制备1氯2甲基丙烷(沸点69 ℃),将2甲基1丙醇和POCl 溶
3
于CHCl 中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分
2 2 3
液收集CHCl 层,无水MgSO 干燥、过滤、蒸馏后得到目标产物。上述过程中涉及的装置
2 2 4
或操作错误的是(夹持及加热装置略)( )
A B C D
3.(2020·全国卷Ⅰ,9)下列气体去除杂质的方法中,不能实现目的的是( )
气体(杂质) 方法
A SO (H S) 通过酸性高锰酸钾溶液
2 2B Cl(HCl) 通过饱和的食盐水
2
C N(O ) 通过灼热的铜丝网
2 2
D NO(NO ) 通过氢氧化钠溶液
2
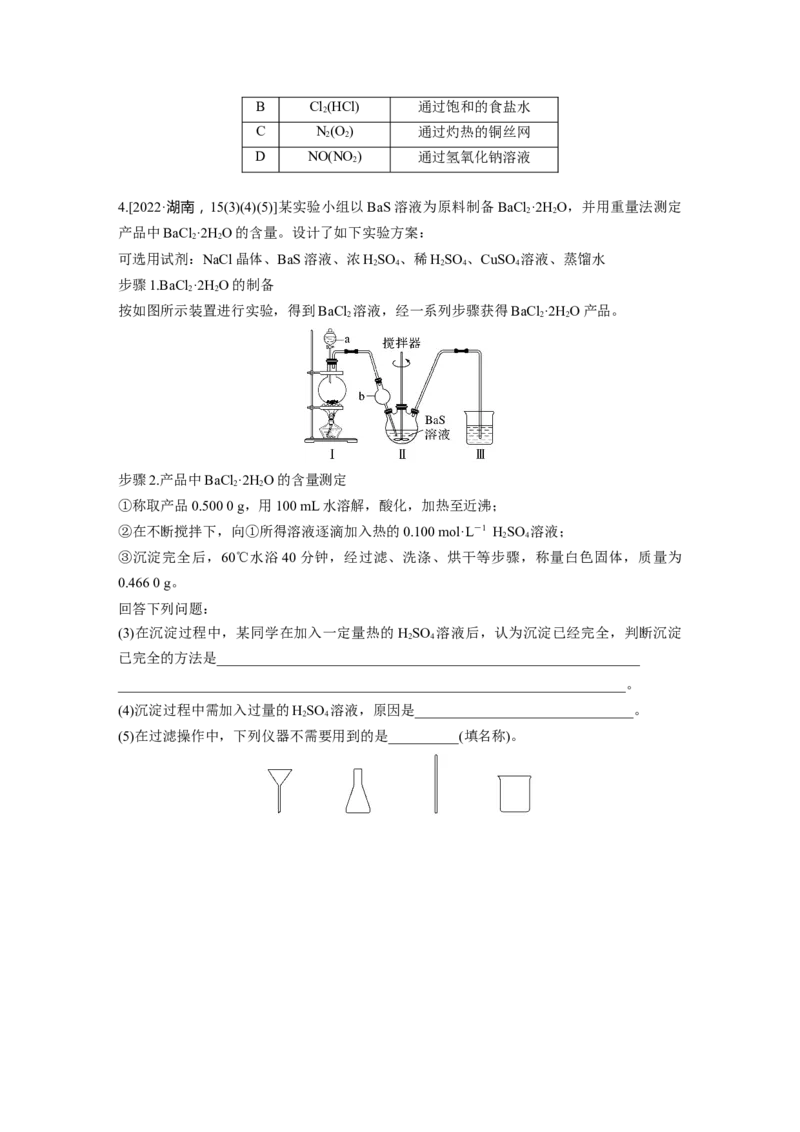
4.[2022·湖南,15(3)(4)(5)]某实验小组以BaS溶液为原料制备BaCl ·2H O,并用重量法测定
2 2
产品中BaCl ·2H O的含量。设计了如下实验方案:
2 2
可选用试剂:NaCl晶体、BaS溶液、浓HSO 、稀HSO 、CuSO 溶液、蒸馏水
2 4 2 4 4
步骤1.BaCl ·2H O的制备
2 2
按如图所示装置进行实验,得到BaCl 溶液,经一系列步骤获得BaCl ·2H O产品。
2 2 2
步骤2.产品中BaCl ·2H O的含量测定
2 2
①称取产品0.500 0 g,用100 mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100 mol·L-1 HSO 溶液;
2 4
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
0.466 0 g。
回答下列问题:
(3)在沉淀过程中,某同学在加入一定量热的HSO 溶液后,认为沉淀已经完全,判断沉淀
2 4
已完全的方法是____________________________________________________________
________________________________________________________________________。
(4)沉淀过程中需加入过量的HSO 溶液,原因是_______________________________。
2 4
(5)在过滤操作中,下列仪器不需要用到的是__________(填名称)。