文档内容
训练(八) 离子共存与离子推断
1.(2020·江苏南京、盐城二模)常温下,下列各组离子在指定溶液中能大量共存的是(
)
A.澄清透明的酸性溶液中:Fe3+、Cu2+、SCN-、SO
B.能使酚酞变红的溶液中:K+、NH、Cl-、NO
C.=10-12 mol·L-1的溶液中:Na+、Al3+、Cl-、SO
D.c(HCO)=0.1 mol·L-1的溶液中:H+、Mg2+ 、SO、NO
C [Fe3+和SCN-反应生成弱电解质Fe(SCN) 而不能大量共存,A项错误;能使酚酞变
3
红的溶液呈碱性,NH和OH-结合生成NH ·HO而不能大量共存,B项错误;常温下,c(OH
3 2
-)==10-12 mol·L-1,则该溶液中c(H+)=10-2mol/L,溶液呈强酸性,四种离子可以大量共
存,C项正确;HCO和H+反应生成CO 和HO而不能大量共存,D项错误。]
2 2
2.(2021·山东临沂检测)常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.“84”消毒液中:SiO、CO、Na+、K+
B.=10-12 的溶液中:NH、Ca2+、Cl-、NO
C.0.1 mol·L-1 NaAlO 溶液中:HCO、NH、SO、Fe3+
2
D.pH=1的溶液中:Na+、K+、Cl-、SO
2
A [“84”消毒液的主要成分是NaClO,溶液呈碱性,SiO、CO、Na+、K+四种离子不反应,
可以大量共存,A项正确;常温下,=10-12 的溶液中c(OH-)=0.1 mol·L-1,溶液呈强碱性,
NH与OH-生成NH ·HO而不能大量共存,B项错误;在NaAlO 溶液中含大量AlO,HCO
3 2 2
与AlO发生反应生成Al(OH) 和CO而不能大量共存,C项错误;pH=1的溶液呈强酸性,
3
SO与H+发生反应:SO+2H+===S↓+SO ↑+HO,不能大量共存,D项错误。]
2 2 2 2
3.(2020·江苏七市第二次调研)室温下,下列各组离子在指定溶液中一定能大量共存的
是( )
A.c(Al3+)=0.1 mol·L-1的溶液:Na+、NH、SO、NO
B.c(Fe3+)=0.1 mol·L-1的溶液:K+、Ba2+、OH-、SCN-
C.c(NO)=0.1 mol/L的溶液:H+、K+、I-、Cl-
D.水电离的c(H+)=1×10-13mol/L的溶液:Na+、Mg2+、SO、HCO
A [Fe3+与OH-、SCN-均发生反应而不能大量共存,B项错误;NO、I-、H+发生氧化还
原反应而不能大量共存,C项错误;室温下,水电离的c(H+)=1×10-13mol/L的溶液中水的电
离受到抑制,该溶液可能是强酸性或强碱性溶液,HCO一定不能大量共存,D项错误。]
4.(2021·湖南益阳检测)常温下,下列各组离子在指定溶液中能大量共存的是( )
A.中性溶液中: Ca2+、Cu2+、Br-、Cl-
B.c(ClO-)=1 mol·L-1的溶液中:Fe2+、Al3+、Cl-、I-
C.能使酚酞变红的溶液中: K+、Na+、SiO、SO
D.=0.1 mol·L-1的溶液中: NH、Mg2+、SO、CHCOO-
3C [由于Cu2+发生水解反应,含有Cu2+的溶液呈弱酸性,故中性溶液中Cu2+不能大量
存在,A项错误;ClO-与Fe2+、I-发生氧化还原反应而不能大量共存,B项错误;使酚酞变红
的溶液呈较强碱性,K+、Na+、SiO、SO不发生反应,可以大量共存,C项正确;=0.1 mol·L-1
的溶液中c(H+)=0.1 mol·L-1,CHCOO-与H+反应生成CHCOOH而不能大量共存,D项错
3 3
误。]
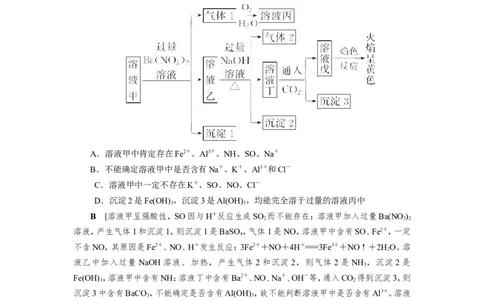
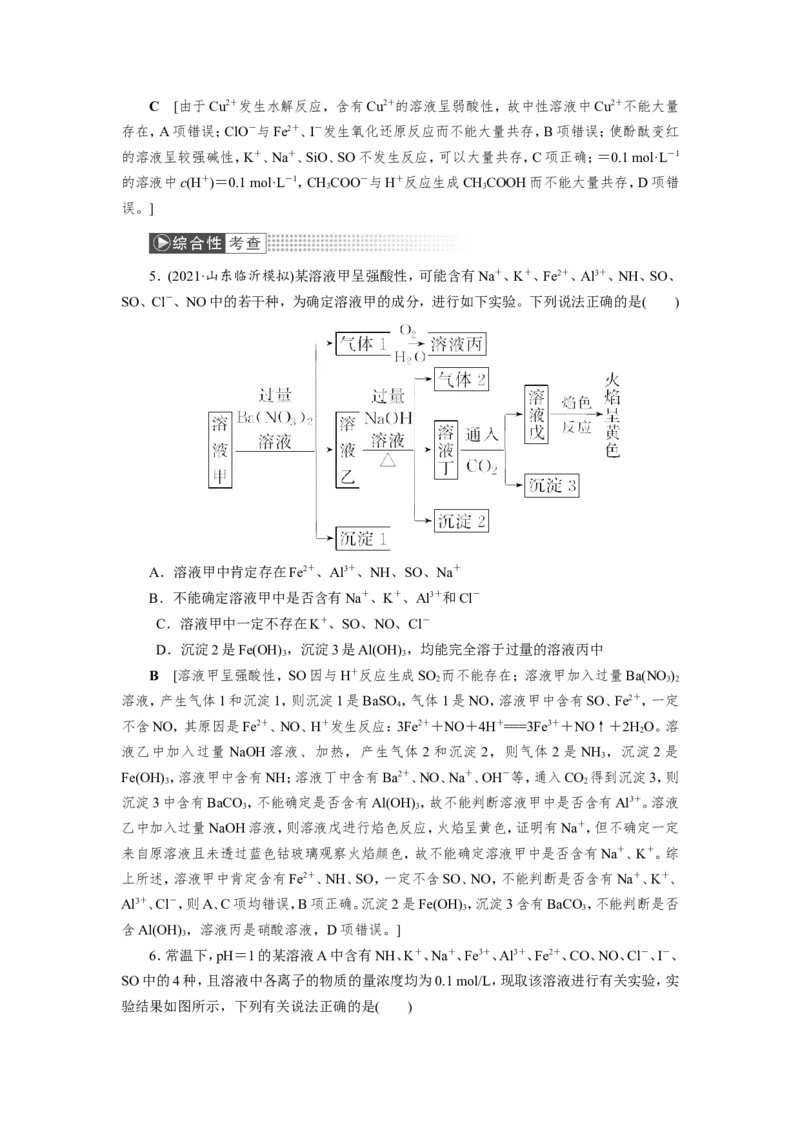
5.(2021·山东临沂模拟)某溶液甲呈强酸性,可能含有Na+、K+、Fe2+、Al3+、NH、SO、
SO、Cl-、NO中的若干种,为确定溶液甲的成分,进行如下实验。下列说法正确的是( )
A.溶液甲中肯定存在Fe2+、Al3+、NH、SO、Na+
B.不能确定溶液甲中是否含有Na+、K+、Al3+和Cl-
C.溶液甲中一定不存在K+、SO、NO、Cl-
D.沉淀2是Fe(OH) ,沉淀3是Al(OH) ,均能完全溶于过量的溶液丙中
3 3
B [溶液甲呈强酸性,SO因与H+反应生成SO 而不能存在;溶液甲加入过量Ba(NO )
2 3 2
溶液,产生气体1和沉淀1,则沉淀1是BaSO,气体1是NO,溶液甲中含有SO、Fe2+,一定
4
不含NO,其原因是Fe2+、NO、H+发生反应:3Fe2++NO+4H+===3Fe3++NO↑+2HO。溶
2
液乙中加入过量 NaOH溶液、加热,产生气体2和沉淀2,则气体2是NH ,沉淀2是
3
Fe(OH) ,溶液甲中含有NH;溶液丁中含有Ba2+、NO、Na+、OH-等,通入CO 得到沉淀3,则
3 2
沉淀3中含有BaCO ,不能确定是否含有Al(OH) ,故不能判断溶液甲中是否含有Al3+。溶液
3 3
乙中加入过量NaOH溶液,则溶液戊进行焰色反应,火焰呈黄色,证明有Na+,但不确定一定
来自原溶液且未透过蓝色钴玻璃观察火焰颜色,故不能确定溶液甲中是否含有Na+、K+。综
上所述,溶液甲中肯定含有Fe2+、NH、SO,一定不含SO、NO,不能判断是否含有Na+、K+、
Al3+、Cl-,则A、C项均错误,B项正确。沉淀2是Fe(OH) ,沉淀3含有BaCO ,不能判断是否
3 3
含Al(OH) ,溶液丙是硝酸溶液,D项错误。]
3
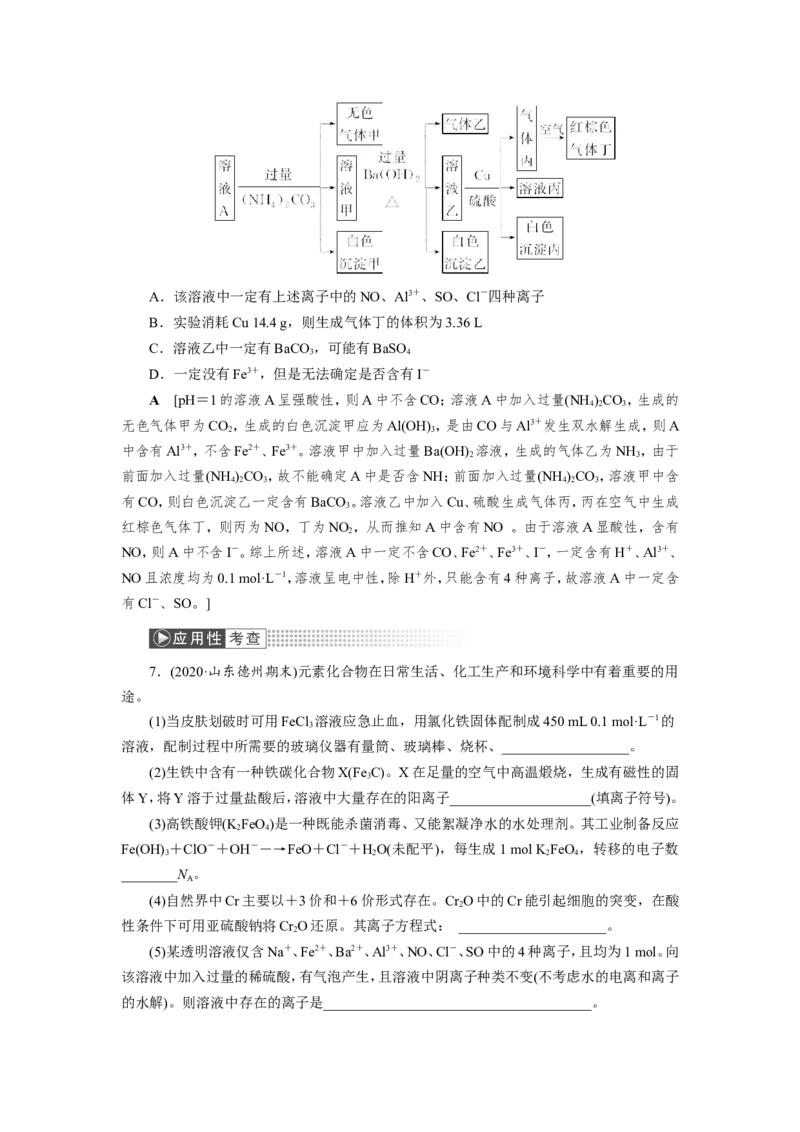
6.常温下,pH=1的某溶液A中含有NH、K+、Na+、Fe3+、Al3+、Fe2+、CO、NO、Cl-、I-、
SO中的4种,且溶液中各离子的物质的量浓度均为0.1 mol/L,现取该溶液进行有关实验,实
验结果如图所示,下列有关说法正确的是( )A.该溶液中一定有上述离子中的NO、Al3+、SO、Cl-四种离子
B.实验消耗Cu 14.4 g,则生成气体丁的体积为3.36 L
C.溶液乙中一定有BaCO ,可能有BaSO
3 4
D.一定没有Fe3+,但是无法确定是否含有I-
A [pH=1的溶液A呈强酸性,则A中不含CO;溶液A中加入过量(NH )CO,生成的
4 2 3
无色气体甲为CO,生成的白色沉淀甲应为Al(OH) ,是由CO与Al3+发生双水解生成,则A
2 3
中含有Al3+,不含Fe2+、Fe3+。溶液甲中加入过量Ba(OH) 溶液,生成的气体乙为NH ,由于
2 3
前面加入过量(NH )CO,故不能确定A中是否含NH;前面加入过量(NH )CO,溶液甲中含
4 2 3 4 2 3
有CO,则白色沉淀乙一定含有BaCO 。溶液乙中加入Cu、硫酸生成气体丙,丙在空气中生成
3
红棕色气体丁,则丙为NO,丁为NO ,从而推知A中含有NO 。由于溶液A显酸性,含有
2
NO,则A中不含I-。综上所述,溶液A中一定不含CO、Fe2+、Fe3+、I-,一定含有H+、Al3+、
NO且浓度均为0.1 mol·L-1,溶液呈电中性,除H+外,只能含有4种离子,故溶液A中一定含
有Cl-、SO。]
7.(2020·山东德州期末)元素化合物在日常生活、化工生产和环境科学中有着重要的用
途。
(1)当皮肤划破时可用FeCl 溶液应急止血,用氯化铁固体配制成450 mL 0.1 mol·L-1的
3
溶液,配制过程中所需要的玻璃仪器有量筒、玻璃棒、烧杯、__________________。
(2)生铁中含有一种铁碳化合物X(Fe C)。X在足量的空气中高温煅烧,生成有磁性的固
3
体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子____________________(填离子符号)。
(3)高铁酸钾(K FeO)是一种既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反应
2 4
Fe(OH) +ClO-+OH-―→FeO+Cl-+HO(未配平),每生成1 mol K FeO ,转移的电子数
3 2 2 4
________N 。
A
(4)自然界中Cr主要以+3价和+6价形式存在。Cr O中的Cr能引起细胞的突变,在酸
2
性条件下可用亚硫酸钠将Cr O还原。其离子方程式: _____________________。
2
(5)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、NO、Cl-、SO中的4种离子,且均为1 mol。向
该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子
的水解)。则溶液中存在的离子是______________________________________。解析 (2)Fe C在足量空气中高温煅烧,生成有磁性的固体Y,则Y是Fe O,溶于过量
3 3 4
盐酸,发生反应:Fe O+8HCl===2FeCl +FeCl +4HO,则溶液中大量存在的阳离子是Fe2
3 4 3 2 2
+、Fe3+及剩余H+。
(3)该反应中,Fe元素由+3价升高到+6价,则生成1mol KFeO 转移电子为2mol×(6
2 4
-3)=3mol,即转移电子数为3N 。
A
(4)在酸性条件下,NaSO 可将Cr O还原为Cr3+,SO则被氧化为SO,结合得失电子、电
2 3 2
荷及原子守恒写出离子方程式:Cr O+3SO+8H+===2Cr3++3SO+4HO。
2 2
(5)溶液中加入过量稀硫酸,有气泡产生则发生反应:3Fe2++NO+4H+===3Fe3++NO↑
+2HO,则溶液中含有Fe2+、NO;又知“溶液中阴离子种类不变”,则原溶液含有SO,则不
2
含Ba2+;原溶液中四种离子均为1 mol,结合电荷守恒推知,还含有Na+,综上所述,原溶液中
存在的4种离子是Fe2+、NO、SO、Na+。
答案 (1)500 mL容量瓶、胶头滴管
(2) Fe2+、Fe3+、H+
(3)3
(4)Cr O+3SO+8H+===2Cr3++3SO+4HO
2 2
(5)Na+、Fe2+、NO、SO