文档内容
第5课时 必备知识——电解原理及应用
[基本规律]①电解池的工作原理;②利用惰性电极电解电解质溶液的规律;
知识清单 ③电解质溶液的复原规律
[重要应用]①电解饱和食盐水;②电镀;③电冶金
知识点1 电解池的构成及工作原理
1.电解和电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
(2)电解池:将电能转化为化学能的装置。
(3)电解池的构成
①有与电源相连的两个电极。
②电解质溶液(或熔融电解质)。
③形成闭合回路。
2.电解池的工作原理
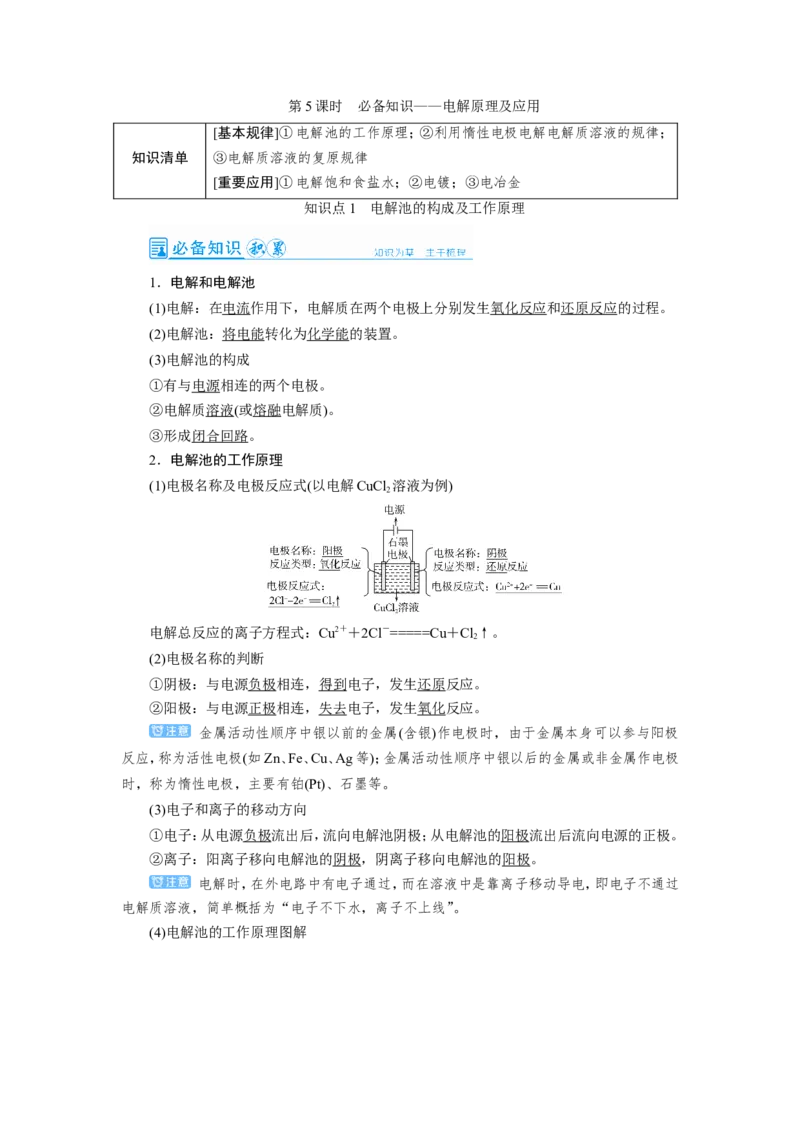
(1)电极名称及电极反应式(以电解CuCl 溶液为例)
2
电解总反应的离子方程式:Cu2++2Cl-=====Cu+Cl↑。
2
(2)电极名称的判断
①阴极:与电源负极相连,得到电子,发生还原反应。
②阳极:与电源正极相连,失去电子,发生氧化反应。
金属活动性顺序中银以前的金属(含银)作电极时,由于金属本身可以参与阳极
反应,称为活性电极(如Zn、Fe、Cu、Ag等);金属活动性顺序中银以后的金属或非金属作电极
时,称为惰性电极,主要有铂(Pt)、石墨等。
(3)电子和离子的移动方向
①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流出后流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。
电解时,在外电路中有电子通过,而在溶液中是靠离子移动导电,即电子不通过
电解质溶液,简单概括为“电子不下水,离子不上线”。
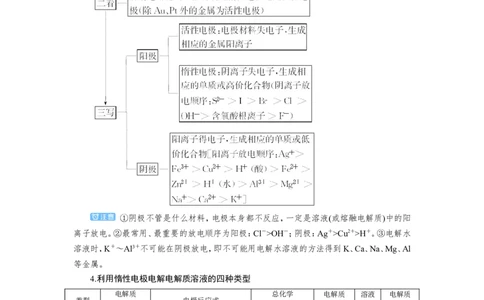
(4)电解池的工作原理图解3.电解池中电极反应式的书写
①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳
离子放电。②最常用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。③电解水
溶液时,K+~Al3+不可能在阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al
等金属。
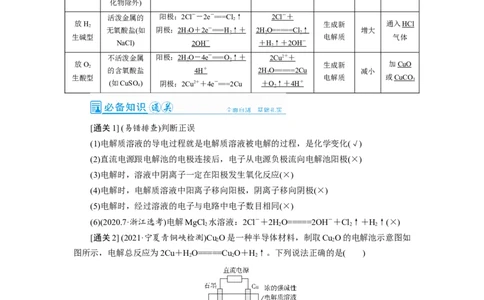
4.利用惰性电极电解电解质溶液的四种类型
电解质 总化学 电解质 溶液 电解质
类型 电极反应式
(水溶液) (或离子)方程式 溶液浓度 pH 溶液复原
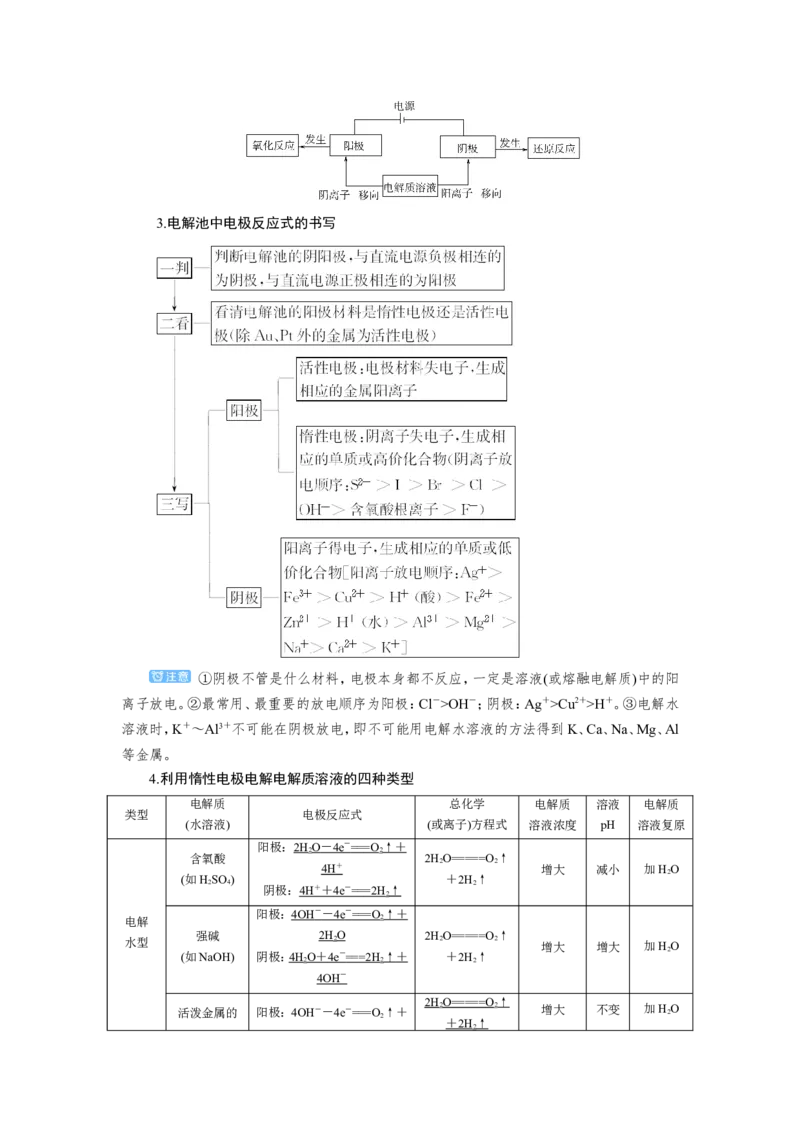
阳极:2H O - 4e - == =O ↑ +
2 2
含氧酸 2HO=====O↑
2 2
4H + 增大 减小 加HO
2
(如HSO) +2H↑
2 4 2
阴极: 4H + + 4e - == =2H ↑
2
阳极: 4OH - - 4e - == =O ↑ +
电解 2
强碱 2HO 2HO=====O↑
水型 2 2 2 增大 增大 加HO
(如NaOH) 阴极:4H O + 4e - == =2H ↑ + +2H↑ 2
2 2 2
4OH -
2H O ===== O ↑
活泼金属的 阳极:4OH--4e-===O 2 ↑+ 2 2 增大 不变 加H 2 O
+ 2H ↑
2含
氧酸盐(如 2HO
2
KNO、 阴极:4H++4e-===2H↑
3 2
NaSO)
2 4
无氧酸(如
阳极:2Cl--2e-===Cl↑ 2HCl=====Cl↑ 通入HCl
2 2
HCl,除HF 减小 增大
阴极:2H++2e-===H↑ +H↑ 气体
2 2
电解 外)
电解 不活泼金属
质型 的无氧酸盐 阳极:2Cl--2e-===Cl↑ CuCl=====_Cu
2 2
减小 — 加CuCl
(如CuCl
2
,氟 阴极:Cu2++2e-===Cu + C l
2
↑ 2
化物除外)
活泼金属的 阳极:2Cl--2e-===Cl↑ 2Cl - +
2
放H 生成新 通入HCl
2 无氧酸盐(如 阴极:2H O + 2e - == =H ↑ + 2H O ===== Cl ↑ 增大
2 2 2 2
生碱型 电解质 气体
NaCl) 2OH - + H ↑ + 2OH -
2
不活泼金属 阳极:2H O - 4e - == =O ↑ + 2Cu 2 + +
2 2
放O 生成新 加CuO
2 的含氧酸盐 4H + 2H O ===== 2Cu 减小
2
生酸型 电解质 或CuCO
(如CuSO
4
) 阴极:2Cu2++4e-===2Cu + O
2
↑ + 4H + 3
[通关1] (易错排查)判断正误
(1)电解质溶液的导电过程就是电解质溶液被电解的过程,是化学变化(√)
(2)直流电源跟电解池的电极连接后,电子从电源负极流向电解池阳极(×)
(3)电解时,溶液中阴离子一定在阳极发生氧化反应(×)
(4)电解时,电解质溶液中阳离子移向阳极,阴离子移向阴极(×)
(5)电解时,经过溶液的电子与电路中电子数目相同(×)
(6)(2020.7·浙江选考)电解MgCl 水溶液:2Cl-+2HO=====2OH-+Cl↑+H↑(×)
2 2 2 2
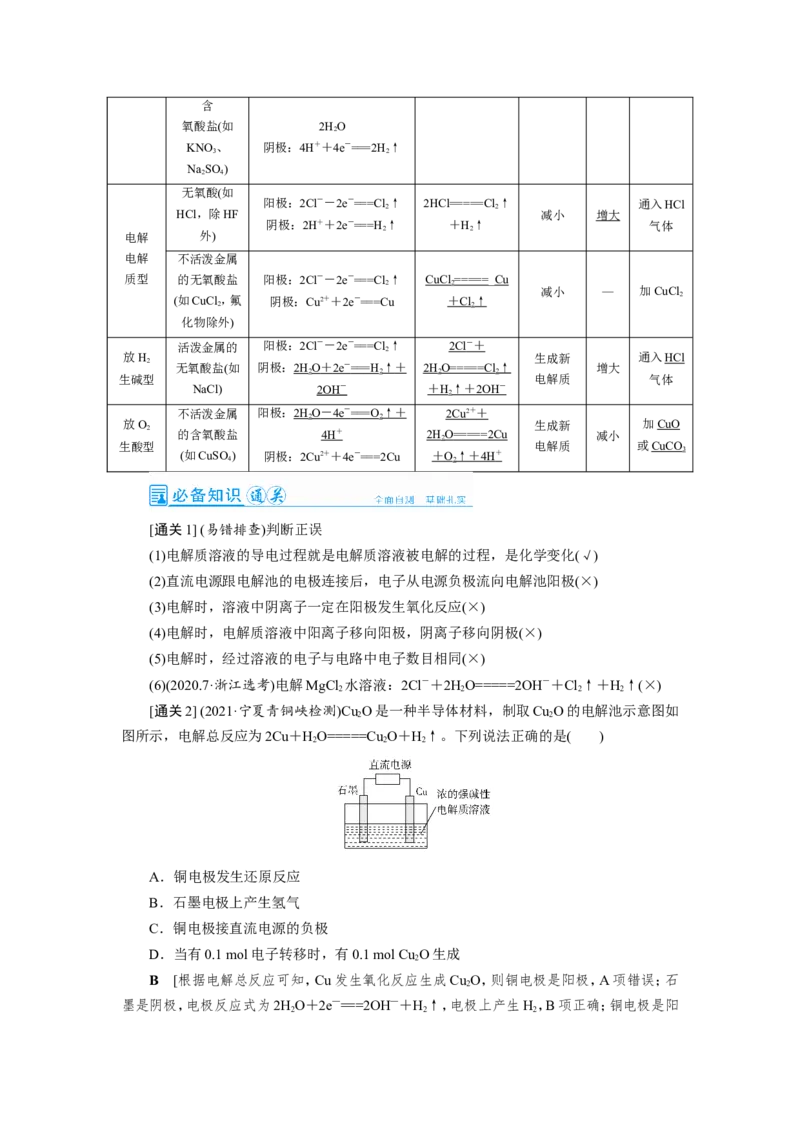
[通关2] (2021·宁夏青铜峡检测)Cu O是一种半导体材料,制取Cu O的电解池示意图如
2 2
图所示,电解总反应为2Cu+HO=====Cu O+H↑。下列说法正确的是( )
2 2 2
A.铜电极发生还原反应
B.石墨电极上产生氢气
C.铜电极接直流电源的负极
D.当有0.1 mol电子转移时,有0.1 mol Cu O生成
2
B [根据电解总反应可知,Cu发生氧化反应生成Cu O,则铜电极是阳极,A项错误;石
2
墨是阴极,电极反应式为2HO+2e—===2OH—+H↑,电极上产生H,B项正确;铜电极是阳
2 2 2极,连接直流电源的正极,C项错误;生成1 mol Cu O转移2 mol 电子,故有0.1 mol 电子转
2
移时,有0.05 mol Cu O生成,D项错误。]
2
[通关3] (2020·北京平谷区检测)某同学将电解池工作时电子、离子流动方向及电极种类
等信息表示在下图中,下列有关分析完全正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极
d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
B [电子从电源的负极流出,故a是阴极,d是正极,溶液中阳离子Q移向阴极a。]
[通关4] (2020·全国卷Ⅱ)电致变色器件可智能调控太阳光透过率,从而实现节能。下图
是某电致变色器件的示意图。当通电时,Ag+注入到无色WO 薄膜中,生成AgWO,器件呈
3 x 3
现蓝色,对于该变化过程,下列叙述错误的是( )
A.Ag为阳极
B.Ag+由银电极向变色层迁移
C.W元素的化合价升高
D.总反应为WO+xAg===AgWO
3 x 3
C [根据图示及信息,Ag失去电子转化为Ag+,Ag 为阳极,A项正确;通电时,Ag+注
入到无色WO 薄膜中,生成AgWO,B项正确;转化过程中,WO 转化为AgWO,W的化合
3 x 3 3 x 3
价降低,C项错误;根据题意,总反应为WO+xAg===AgWO,D项正确。]
3 x 3
[通关5] (深度思考)结合电解原理,按要求书写电极反应式和总反应方程式:
(1)用惰性电极电解MgCl 溶液
2
阳极反应式:_____________________________________________;
阴极反应式:________________________________________________;
总反应离子方程式:_________________________________________________。
(2)用Al作电极电解NaOH溶液
阳极反应式:___________________________________________________________;
阴极反应式:__________________________________________________________;
总反应离子方程式:________________________________________________________
________________________________________________________________________。
(3)以铝材为阳极,电解HSO 溶液,铝材表面形成氧化膜
2 4阳极反应式:______________________________________________________;
阴极反应式:_______________________________________________________;
总反应方程式:_________________________________________________。
(4)离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al Cl和AlCl组成的离子
2
液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的________极,已知电镀过程中不
产生其他离子且有机阳离子不参与电极反应,阴极反应式为___________。若改用AlCl 水溶
3
液作电解液,则阴极产物为________。
解析 (4)电镀时,镀件作阴极,即钢制品作阴极,接电源负极,根据阴极生成Al可知反
应式为4Al Cl+3e-===Al+7AlCl。若改用AlCl 水溶液作电解液,阴极反应为2H++2e-
2 3
===H ↑,产物为H。
2 2
答案 (1)2Cl--2e-===Cl↑ 2H++2e-===H ↑或2HO+2e-===H ↑+2OH- Mg2
2 2 2 2
++2Cl-+2HO=====Mg(OH) ↓+Cl↑+H↑
2 2 2 2
(2)2Al-6e-+8OH-===2AlO+4HO 6HO+6e-===3H ↑+6OH- 2Al+2HO+
2 2 2 2
2OH-=====2AlO+3H↑
2
(3)2Al-6e-+3HO===AlO +6H+ 6H++6e-===3H ↑ 2Al+3HO=====Al O +
2 2 3 2 2 2 3
3H↑
2
(4)负 4Al Cl+3e-===Al+7AlCl H
2 2
知识点2 电解原理的应用
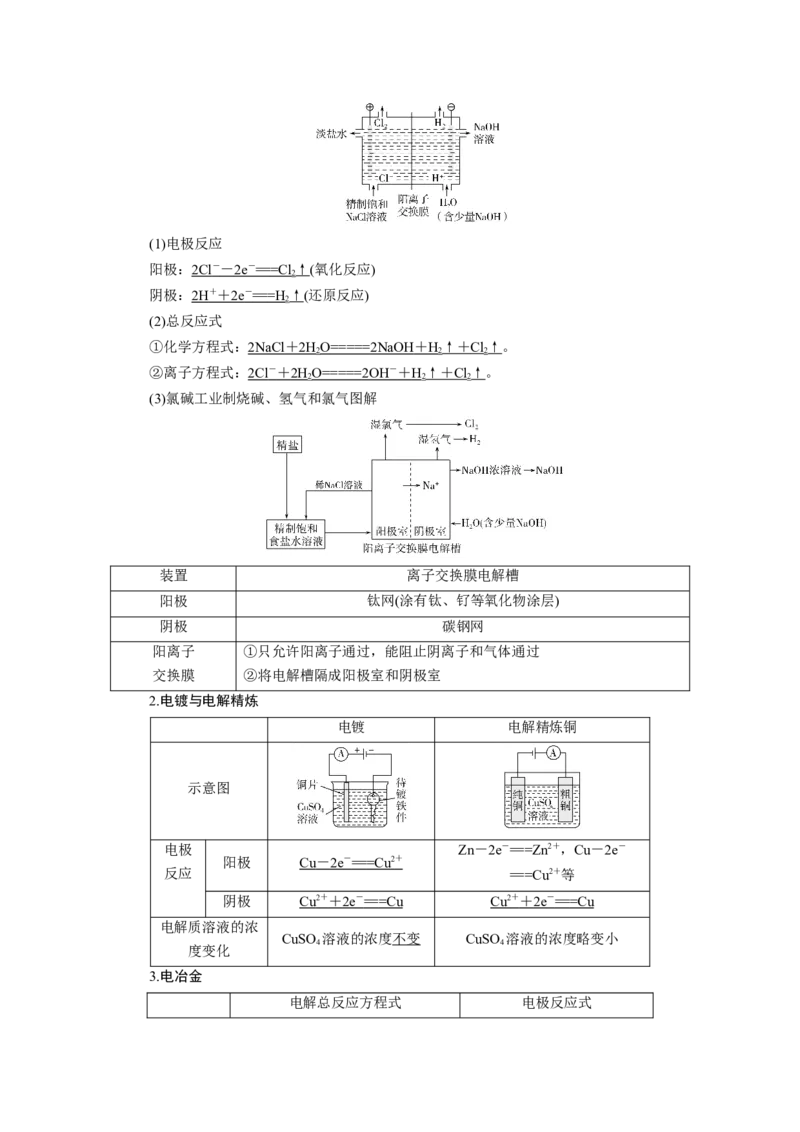
1.氯碱工业(1)电极反应
阳极: 2Cl - - 2e - == =Cl ↑(氧化反应)
2
阴极: 2H + + 2e - == =H ↑(还原反应)
2
(2)总反应式
①化学方程式: 2NaCl + 2H O ===== 2NaOH + H ↑ + C l↑。
2 2 2
②离子方程式: 2Cl - + 2H O ===== 2OH - + H ↑ + C l↑。
2 2 2
(3)氯碱工业制烧碱、氢气和氯气图解
装置 离子交换膜电解槽
阳极 钛网(涂有钛、钌等氧化物涂层)
阴极 碳钢网
阳离子 ①只允许阳离子通过,能阻止阴离子和气体通过
交换膜 ②将电解槽隔成阳极室和阴极室
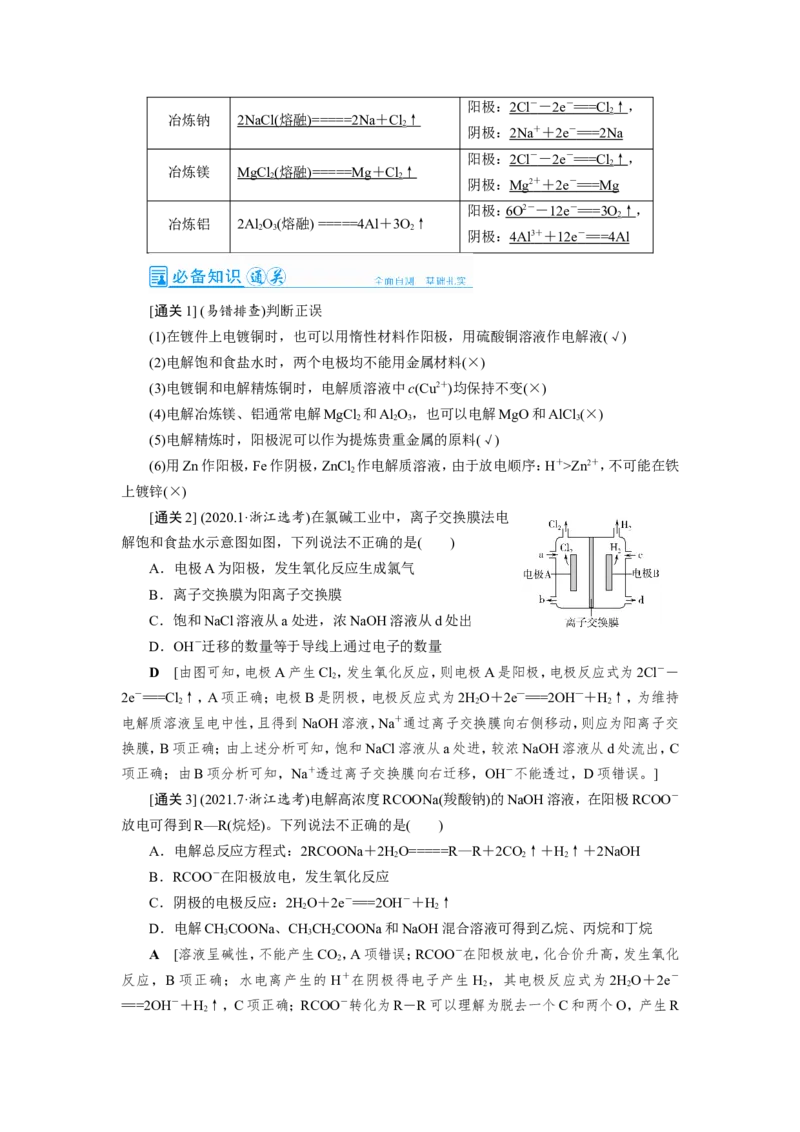
2.电镀与电解精炼
电镀 电解精炼铜
示意图
电极 Zn-2e-===Zn2+,Cu-2e-
阳极 Cu - 2e - == =Cu 2 +
反应 ===Cu2+等
阴极 Cu 2 + + 2e - == =Cu Cu 2 + + 2e - == =Cu
电解质溶液的浓
CuSO 溶液的浓度不变 CuSO 溶液的浓度略变小
4 4
度变化
3.电冶金
电解总反应方程式 电极反应式阳极: 2Cl - - 2e - == =Cl ↑,
2
冶炼钠 2NaCl( 熔融 ) ===== 2Na + Cl ↑
2
阴极: 2Na + + 2e - == =2Na
阳极: 2Cl - - 2e - == =Cl ↑,
2
冶炼镁 MgCl ( 熔融 ) ===== Mg + Cl ↑
2 2
阴极: Mg 2 + + 2e - == =Mg
阳极: 6O 2 - - 12e - == =3O ↑,
2
冶炼铝 2Al O(熔融) =====4Al+3O↑
2 3 2
阴极: 4Al 3 + + 12e - == =4Al
[通关1] (易错排查)判断正误
(1)在镀件上电镀铜时,也可以用惰性材料作阳极,用硫酸铜溶液作电解液(√)
(2)电解饱和食盐水时,两个电极均不能用金属材料(×)
(3)电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变(×)
(4)电解冶炼镁、铝通常电解MgCl 和Al O,也可以电解MgO和AlCl (×)
2 2 3 3
(5)电解精炼时,阳极泥可以作为提炼贵重金属的原料(√)
(6)用Zn作阳极,Fe作阴极,ZnCl 作电解质溶液,由于放电顺序:H+>Zn2+,不可能在铁
2
上镀锌(×)
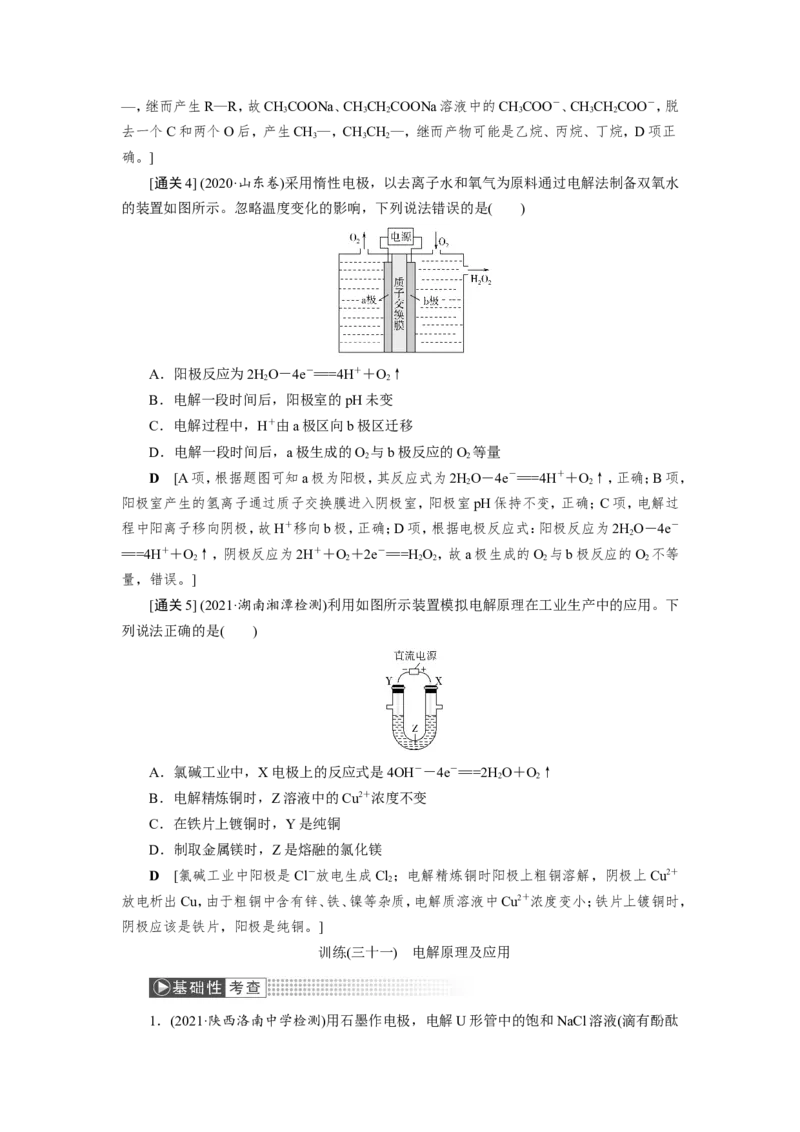
[通关2] (2020.1·浙江选考)在氯碱工业中,离子交换膜法电
解饱和食盐水示意图如图,下列说法不正确的是( )
A.电极A为阳极,发生氧化反应生成氯气
B.离子交换膜为阳离子交换膜
C.饱和NaCl溶液从a处进,浓NaOH溶液从d处出
D.OH-迁移的数量等于导线上通过电子的数量
D [由图可知,电极A产生Cl,发生氧化反应,则电极A是阳极,电极反应式为2Cl--
2
2e-===Cl↑,A项正确;电极B是阴极,电极反应式为2HO+2e—===2OH—+H↑,为维持
2 2 2
电解质溶液呈电中性,且得到NaOH溶液,Na+通过离子交换膜向右侧移动,则应为阳离子交
换膜,B项正确;由上述分析可知,饱和NaCl溶液从a处进,较浓NaOH溶液从d处流出,C
项正确;由B项分析可知,Na+透过离子交换膜向右迁移,OH-不能透过,D项错误。]
[通关3] (2021.7·浙江选考)电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO-
放电可得到R—R(烷烃)。下列说法不正确的是( )
A.电解总反应方程式:2RCOONa+2HO=====R—R+2CO↑+H↑+2NaOH
2 2 2
B.RCOO-在阳极放电,发生氧化反应
C.阴极的电极反应:2HO+2e-===2OH-+H↑
2 2
D.电解CHCOONa、CHCHCOONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
A [溶液呈碱性,不能产生CO,A项错误;RCOO-在阳极放电,化合价升高,发生氧化
2
反应,B项正确;水电离产生的H+在阴极得电子产生H ,其电极反应式为2HO+2e-
2 2
===2OH-+H↑,C项正确;RCOO-转化为R-R可以理解为脱去一个C和两个O,产生R
2—,继而产生R—R,故CHCOONa、CHCHCOONa溶液中的CHCOO-、CHCHCOO-,脱
3 3 2 3 3 2
去一个C和两个O后,产生CH—,CHCH—,继而产物可能是乙烷、丙烷、丁烷,D项正
3 3 2
确。]
[通关4] (2020·山东卷)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水
的装置如图所示。忽略温度变化的影响,下列说法错误的是( )
A.阳极反应为2HO-4e-===4H++O↑
2 2
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
D [A项,根据题图可知a极为阳极,其反应式为2HO-4e-===4H++O↑,正确;B项,
2 2
阳极室产生的氢离子通过质子交换膜进入阴极室,阳极室pH保持不变,正确;C项,电解过
程中阳离子移向阴极,故H+移向b极,正确;D项,根据电极反应式:阳极反应为2HO-4e-
2
===4H++O↑,阴极反应为2H++O+2e-===H O,故a极生成的O 与b极反应的O 不等
2 2 2 2 2 2
量,错误。]
[通关5] (2021·湖南湘潭检测)利用如图所示装置模拟电解原理在工业生产中的应用。下
列说法正确的是( )
A.氯碱工业中,X电极上的反应式是4OH--4e-===2H O+O↑
2 2
B.电解精炼铜时,Z溶液中的Cu2+浓度不变
C.在铁片上镀铜时,Y是纯铜
D.制取金属镁时,Z是熔融的氯化镁
D [氯碱工业中阳极是Cl-放电生成Cl;电解精炼铜时阳极上粗铜溶解,阴极上Cu2+
2
放电析出Cu,由于粗铜中含有锌、铁、镍等杂质,电解质溶液中Cu2+浓度变小;铁片上镀铜时,
阴极应该是铁片,阳极是纯铜。]
训练(三十一) 电解原理及应用
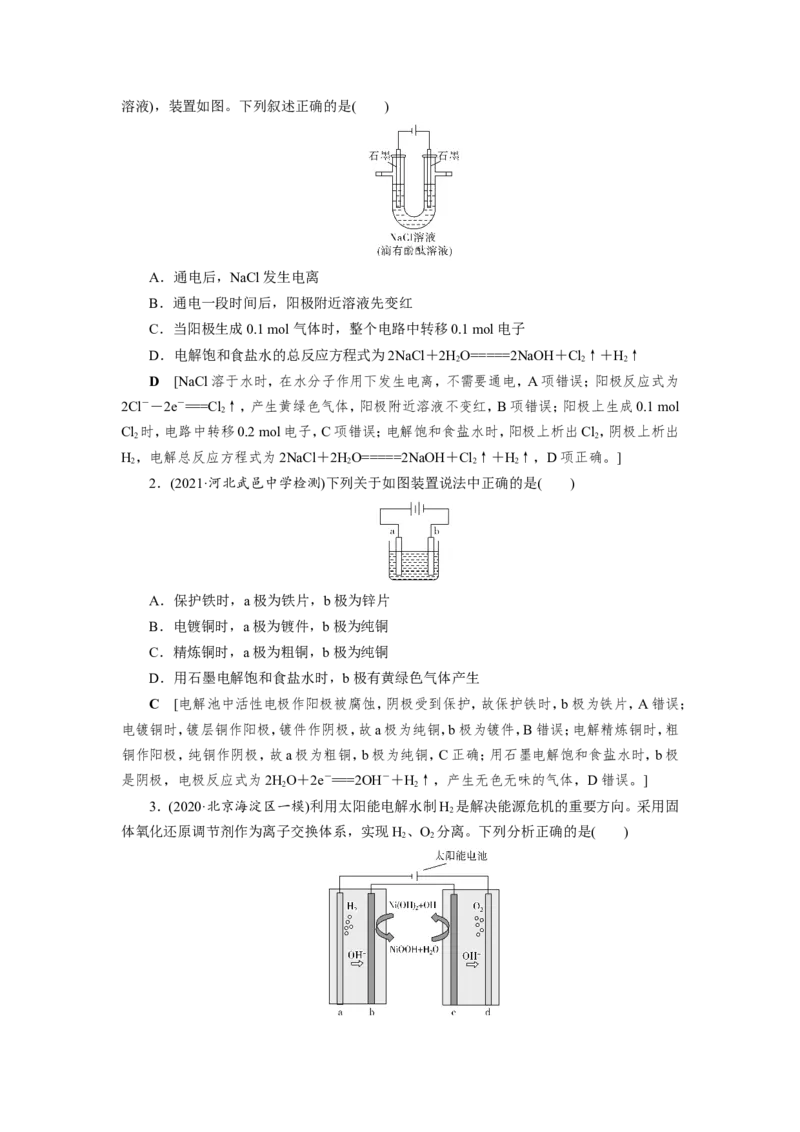
1.(2021·陕西洛南中学检测)用石墨作电极,电解U形管中的饱和NaCl溶液(滴有酚酞溶液),装置如图。下列叙述正确的是( )
A.通电后,NaCl发生电离
B.通电一段时间后,阳极附近溶液先变红
C.当阳极生成0.1 mol 气体时,整个电路中转移0.1 mol电子
D.电解饱和食盐水的总反应方程式为2NaCl+2HO=====2NaOH+Cl↑+H↑
2 2 2
D [NaCl溶于水时,在水分子作用下发生电离,不需要通电,A项错误;阳极反应式为
2Cl--2e-===Cl↑,产生黄绿色气体,阳极附近溶液不变红,B项错误;阳极上生成0.1 mol
2
Cl 时,电路中转移0.2 mol电子,C项错误;电解饱和食盐水时,阳极上析出Cl,阴极上析出
2 2
H,电解总反应方程式为2NaCl+2HO=====2NaOH+Cl↑+H↑,D项正确。]
2 2 2 2
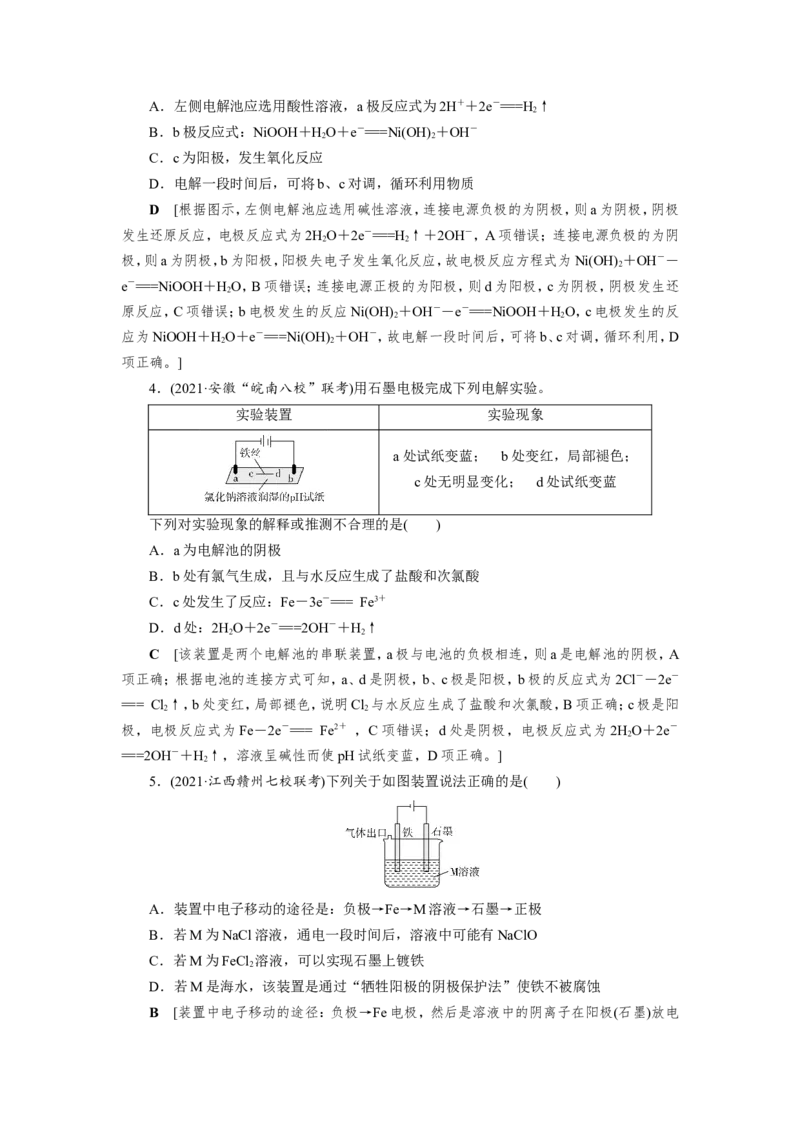
2.(2021·河北武邑中学检测)下列关于如图装置说法中正确的是( )
A.保护铁时,a极为铁片,b极为锌片
B.电镀铜时,a极为镀件,b极为纯铜
C.精炼铜时,a极为粗铜,b极为纯铜
D.用石墨电解饱和食盐水时,b极有黄绿色气体产生
C [电解池中活性电极作阳极被腐蚀,阴极受到保护,故保护铁时,b极为铁片,A错误;
电镀铜时,镀层铜作阳极,镀件作阴极,故a极为纯铜,b极为镀件,B错误;电解精炼铜时,粗
铜作阳极,纯铜作阴极,故a极为粗铜,b极为纯铜,C正确;用石墨电解饱和食盐水时,b极
是阴极,电极反应式为2HO+2e-===2OH-+H↑,产生无色无味的气体,D错误。]
2 2
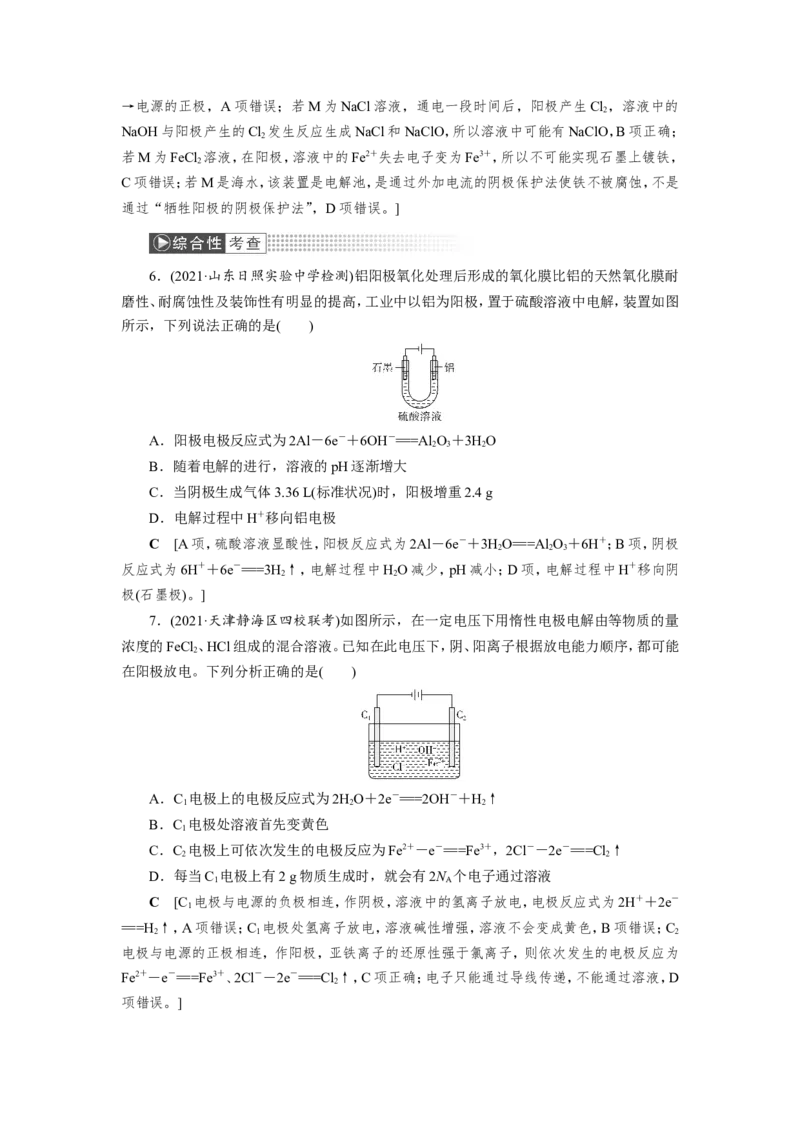
3.(2020·北京海淀区一模)利用太阳能电解水制H 是解决能源危机的重要方向。采用固
2
体氧化还原调节剂作为离子交换体系,实现H、O 分离。下列分析正确的是( )
2 2A.左侧电解池应选用酸性溶液,a极反应式为2H++2e-===H ↑
2
B.b极反应式:NiOOH+HO+e-===Ni(OH) +OH-
2 2
C.c为阳极,发生氧化反应
D.电解一段时间后,可将b、c对调,循环利用物质
D [根据图示,左侧电解池应选用碱性溶液,连接电源负极的为阴极,则a为阴极,阴极
发生还原反应,电极反应式为2HO+2e-===H ↑+2OH-,A项错误;连接电源负极的为阴
2 2
极,则a为阴极,b为阳极,阳极失电子发生氧化反应,故电极反应方程式为Ni(OH) +OH--
2
e-===NiOOH+HO,B项错误;连接电源正极的为阳极,则d为阳极,c为阴极,阴极发生还
2
原反应,C项错误;b电极发生的反应Ni(OH) +OH--e-===NiOOH+HO,c电极发生的反
2 2
应为NiOOH+HO+e-===Ni(OH) +OH-,故电解一段时间后,可将b、c对调,循环利用,D
2 2
项正确。]
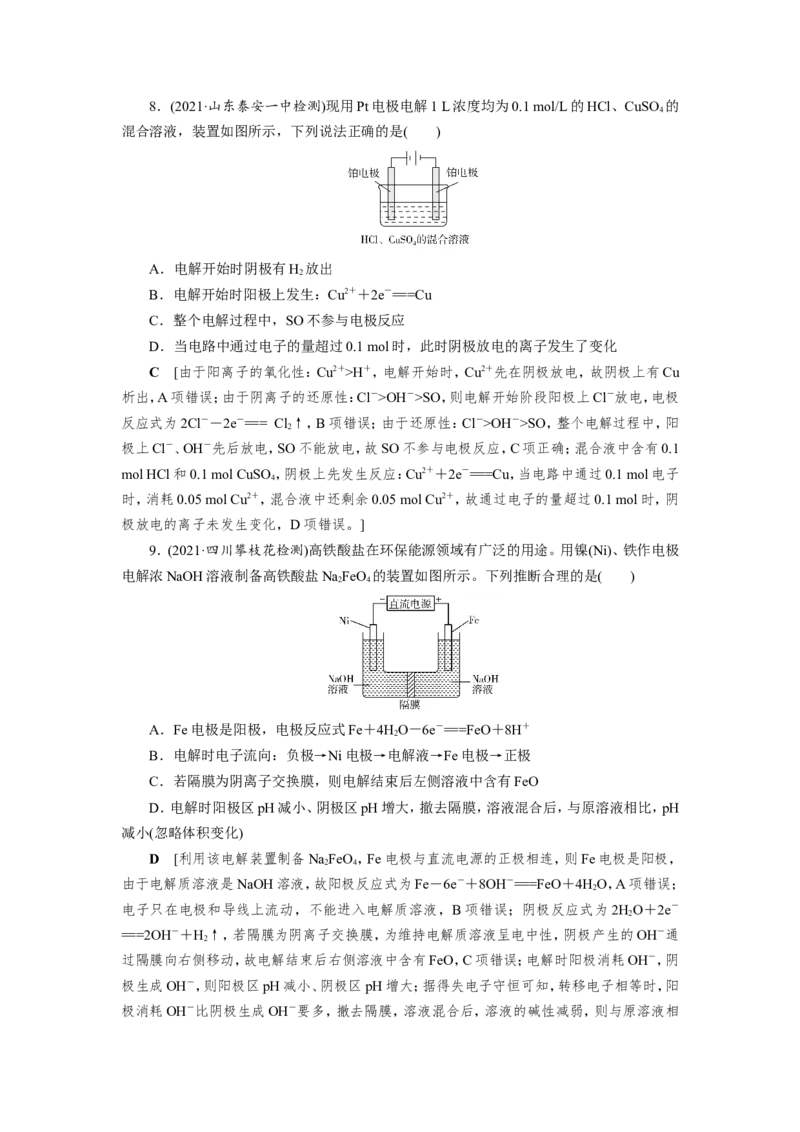
4.(2021·安徽“皖南八校”联考)用石墨电极完成下列电解实验。
实验装置 实验现象
a处试纸变蓝; b处变红,局部褪色;
c处无明显变化; d处试纸变蓝
下列对实验现象的解释或推测不合理的是( )
A.a为电解池的阴极
B.b处有氯气生成,且与水反应生成了盐酸和次氯酸
C.c处发生了反应:Fe-3e-=== Fe3+
D.d处:2HO+2e-===2OH-+H↑
2 2
C [该装置是两个电解池的串联装置,a极与电池的负极相连,则a是电解池的阴极,A
项正确;根据电池的连接方式可知,a、d是阴极,b、c极是阳极,b极的反应式为2Cl--2e-
=== Cl↑,b处变红,局部褪色,说明Cl 与水反应生成了盐酸和次氯酸,B项正确;c极是阳
2 2
极,电极反应式为Fe-2e-=== Fe2+ ,C项错误;d处是阴极,电极反应式为2HO+2e-
2
===2OH-+H↑,溶液呈碱性而使pH试纸变蓝,D项正确。]
2
5.(2021·江西赣州七校联考)下列关于如图装置说法正确的是( )
A.装置中电子移动的途径是:负极→Fe→M溶液→石墨→正极
B.若M为NaCl溶液,通电一段时间后,溶液中可能有NaClO
C.若M为FeCl 溶液,可以实现石墨上镀铁
2
D.若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
B [装置中电子移动的途径:负极→Fe电极,然后是溶液中的阴离子在阳极(石墨)放电→电源的正极,A项错误;若M为NaCl溶液,通电一段时间后,阳极产生Cl ,溶液中的
2
NaOH与阳极产生的Cl 发生反应生成NaCl和NaClO,所以溶液中可能有NaClO,B项正确;
2
若M为FeCl 溶液,在阳极,溶液中的Fe2+失去电子变为Fe3+,所以不可能实现石墨上镀铁,
2
C项错误;若M是海水,该装置是电解池,是通过外加电流的阴极保护法使铁不被腐蚀,不是
通过“牺牲阳极的阴极保护法”,D项错误。]
6.(2021·山东日照实验中学检测)铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐
磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图
所示,下列说法正确的是( )
A.阳极电极反应式为2Al-6e-+6OH-===AlO+3HO
2 3 2
B.随着电解的进行,溶液的pH逐渐增大
C.当阴极生成气体3.36 L(标准状况)时,阳极增重2.4 g
D.电解过程中H+移向铝电极
C [A项,硫酸溶液显酸性,阳极反应式为2Al-6e-+3HO===AlO+6H+;B项,阴极
2 2 3
反应式为6H++6e-===3H ↑,电解过程中HO减少,pH减小;D项,电解过程中H+移向阴
2 2
极(石墨极)。]
7.(2021·天津静海区四校联考)如图所示,在一定电压下用惰性电极电解由等物质的量
浓度的FeCl 、HCl组成的混合溶液。已知在此电压下,阴、阳离子根据放电能力顺序,都可能
2
在阳极放电。下列分析正确的是( )
A.C 电极上的电极反应式为2HO+2e-===2OH-+H↑
1 2 2
B.C 电极处溶液首先变黄色
1
C.C 电极上可依次发生的电极反应为Fe2+-e-===Fe3+,2Cl--2e-===Cl↑
2 2
D.每当C 电极上有2 g物质生成时,就会有2N 个电子通过溶液
1 A
C [C 电极与电源的负极相连,作阴极,溶液中的氢离子放电,电极反应式为2H++2e-
1
===H ↑,A项错误;C 电极处氢离子放电,溶液碱性增强,溶液不会变成黄色,B项错误;C
2 1 2
电极与电源的正极相连,作阳极,亚铁离子的还原性强于氯离子,则依次发生的电极反应为
Fe2+-e-===Fe3+、2Cl--2e-===Cl↑,C项正确;电子只能通过导线传递,不能通过溶液,D
2
项错误。]8.(2021·山东泰安一中检测)现用Pt电极电解1 L浓度均为0.1 mol/L的HCl、CuSO 的
4
混合溶液,装置如图所示,下列说法正确的是( )
A.电解开始时阴极有H 放出
2
B.电解开始时阳极上发生:Cu2++2e-===Cu
C.整个电解过程中,SO不参与电极反应
D.当电路中通过电子的量超过0.1 mol时,此时阴极放电的离子发生了变化
C [由于阳离子的氧化性:Cu2+>H+,电解开始时,Cu2+先在阴极放电,故阴极上有Cu
析出,A项错误;由于阴离子的还原性:Cl->OH->SO,则电解开始阶段阳极上Cl-放电,电极
反应式为2Cl--2e-=== Cl↑,B项错误;由于还原性:Cl->OH->SO,整个电解过程中,阳
2
极上Cl-、OH-先后放电,SO不能放电,故SO不参与电极反应,C项正确;混合液中含有0.1
mol HCl和0.1 mol CuSO ,阴极上先发生反应:Cu2++2e-===Cu,当电路中通过0.1 mol电子
4
时,消耗0.05 mol Cu2+,混合液中还剩余0.05 mol Cu2+,故通过电子的量超过0.1 mol时,阴
极放电的离子未发生变化,D项错误。]
9.(2021·四川攀枝花检测)高铁酸盐在环保能源领域有广泛的用途。用镍(Ni)、铁作电极
电解浓NaOH溶液制备高铁酸盐NaFeO 的装置如图所示。下列推断合理的是( )
2 4
A.Fe电极是阳极,电极反应式Fe+4HO-6e-===FeO+8H+
2
B.电解时电子流向:负极→Ni电极→电解液→Fe电极→正极
C.若隔膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO
D.电解时阳极区pH减小、阴极区pH增大,撤去隔膜,溶液混合后,与原溶液相比,pH
减小(忽略体积变化)
D [利用该电解装置制备NaFeO,Fe电极与直流电源的正极相连,则Fe电极是阳极,
2 4
由于电解质溶液是NaOH溶液,故阳极反应式为Fe-6e-+8OH-===FeO+4HO,A项错误;
2
电子只在电极和导线上流动,不能进入电解质溶液,B项错误;阴极反应式为2HO+2e-
2
===2OH-+H↑,若隔膜为阴离子交换膜,为维持电解质溶液呈电中性,阴极产生的OH-通
2
过隔膜向右侧移动,故电解结束后右侧溶液中含有FeO,C项错误;电解时阳极消耗OH-,阴
极生成OH-,则阳极区pH减小、阴极区pH增大;据得失电子守恒可知,转移电子相等时,阳
极消耗OH-比阴极生成OH-要多,撤去隔膜,溶液混合后,溶液的碱性减弱,则与原溶液相比,pH减小,D项正确。]
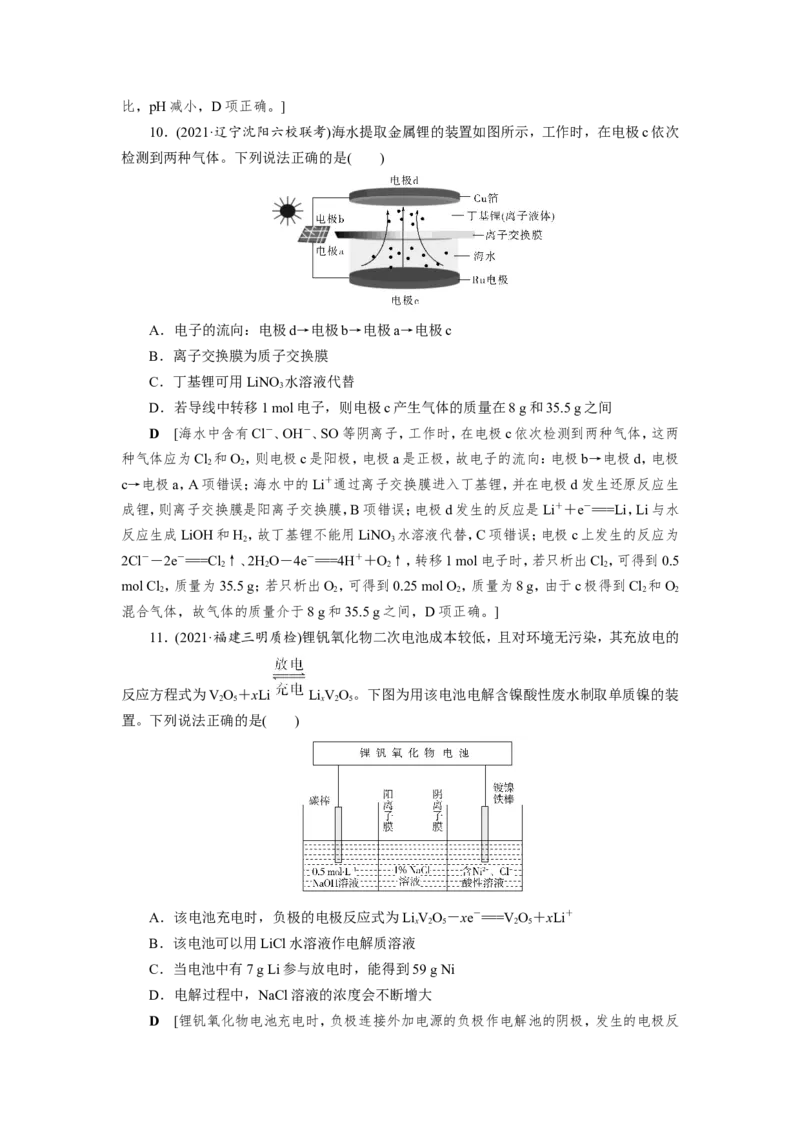
10.(2021·辽宁沈阳六校联考)海水提取金属锂的装置如图所示,工作时,在电极c依次
检测到两种气体。下列说法正确的是( )
A.电子的流向:电极d→电极b→电极a→电极c
B.离子交换膜为质子交换膜
C.丁基锂可用LiNO 水溶液代替
3
D.若导线中转移1 mol电子,则电极c产生气体的质量在8 g和35.5 g之间
D [海水中含有Cl-、OH-、SO等阴离子,工作时,在电极c依次检测到两种气体,这两
种气体应为Cl 和O,则电极c是阳极,电极a是正极,故电子的流向:电极b→电极d,电极
2 2
c→电极a,A项错误;海水中的Li+通过离子交换膜进入丁基锂,并在电极d发生还原反应生
成锂,则离子交换膜是阳离子交换膜,B项错误;电极d发生的反应是Li++e-===Li,Li与水
反应生成LiOH和H,故丁基锂不能用LiNO 水溶液代替,C项错误;电极c上发生的反应为
2 3
2Cl--2e-===Cl↑、2HO-4e-===4H++O↑,转移1 mol电子时,若只析出Cl,可得到0.5
2 2 2 2
mol Cl ,质量为35.5 g;若只析出O,可得到0.25 mol O,质量为8 g,由于c极得到Cl 和O
2 2 2 2 2
混合气体,故气体的质量介于8 g和35.5 g之间,D项正确。]
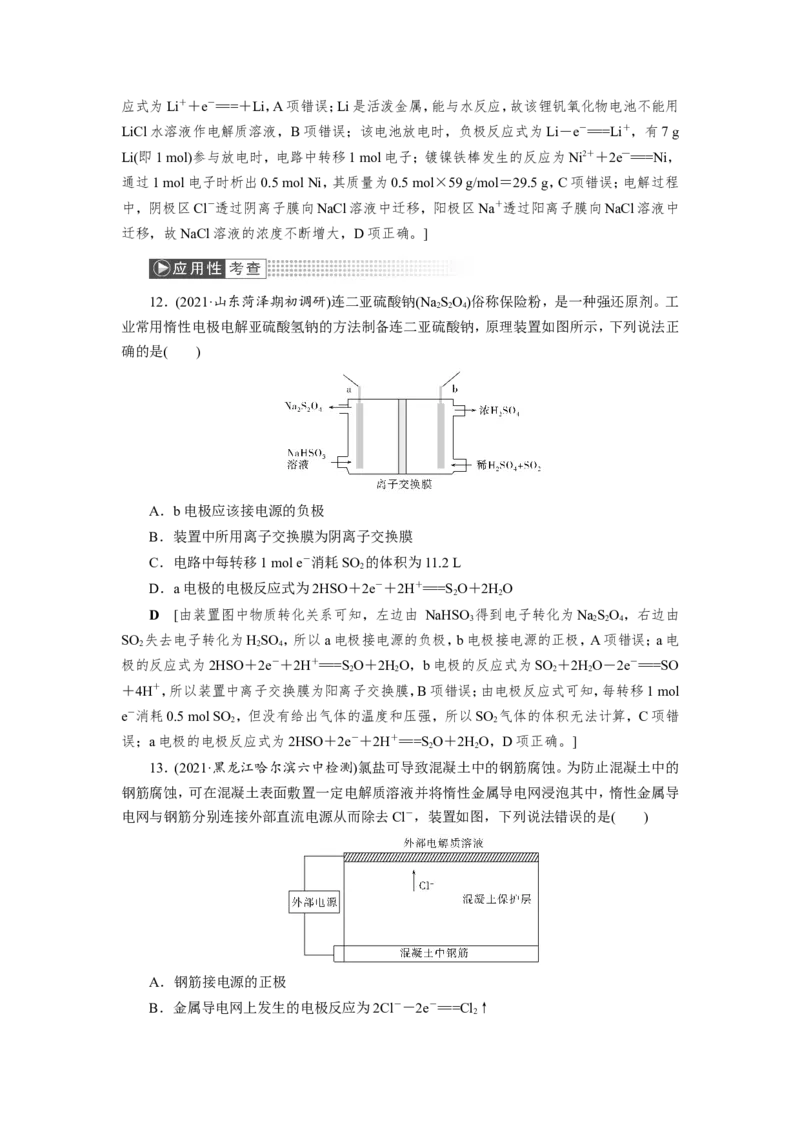
11.(2021·福建三明质检)锂钒氧化物二次电池成本较低,且对环境无污染,其充放电的
反应方程式为VO +xLi LiVO 。下图为用该电池电解含镍酸性废水制取单质镍的装
2 5 x 2 5
置。下列说法正确的是( )
A.该电池充电时,负极的电极反应式为LiVO-xe-===V O+xLi+
x 2 5 2 5
B.该电池可以用LiCl水溶液作电解质溶液
C.当电池中有7 g Li参与放电时,能得到59 g Ni
D.电解过程中,NaCl溶液的浓度会不断增大
D [锂钒氧化物电池充电时,负极连接外加电源的负极作电解池的阴极,发生的电极反应式为Li++e-===+Li,A项错误;Li是活泼金属,能与水反应,故该锂钒氧化物电池不能用
LiCl水溶液作电解质溶液,B项错误;该电池放电时,负极反应式为Li-e-===Li+,有7 g
Li(即1 mol)参与放电时,电路中转移1 mol电子;镀镍铁棒发生的反应为Ni2++2e—===Ni,
通过1 mol电子时析出0.5 mol Ni,其质量为0.5 mol×59 g/mol=29.5 g,C项错误;电解过程
中,阴极区Cl-透过阴离子膜向NaCl溶液中迁移,阳极区Na+透过阳离子膜向NaCl溶液中
迁移,故NaCl溶液的浓度不断增大,D项正确。]
12.(2021·山东菏泽期初调研)连二亚硫酸钠(Na SO)俗称保险粉,是一种强还原剂。工
2 2 4
业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正
确的是( )
A.b电极应该接电源的负极
B.装置中所用离子交换膜为阴离子交换膜
C.电路中每转移1 mol e-消耗SO 的体积为11.2 L
2
D.a电极的电极反应式为2HSO+2e-+2H+===S O+2HO
2 2
D [由装置图中物质转化关系可知,左边由 NaHSO 得到电子转化为NaSO,右边由
3 2 2 4
SO 失去电子转化为HSO ,所以a电极接电源的负极,b电极接电源的正极,A项错误;a电
2 2 4
极的反应式为2HSO+2e-+2H+===S O+2HO,b电极的反应式为SO +2HO-2e-===SO
2 2 2 2
+4H+,所以装置中离子交换膜为阳离子交换膜,B项错误;由电极反应式可知,每转移1 mol
e-消耗0.5 mol SO ,但没有给出气体的温度和压强,所以SO 气体的体积无法计算,C项错
2 2
误;a电极的电极反应式为2HSO+2e-+2H+===S O+2HO,D项正确。]
2 2
13.(2021·黑龙江哈尔滨六中检测)氯盐可导致混凝土中的钢筋腐蚀。为防止混凝土中的
钢筋腐蚀,可在混凝土表面敷置一定电解质溶液并将惰性金属导电网浸泡其中,惰性金属导
电网与钢筋分别连接外部直流电源从而除去Cl-,装置如图,下列说法错误的是( )
A.钢筋接电源的正极
B.金属导电网上发生的电极反应为2Cl--2e-===Cl↑
2C.混凝土中的钙离子向钢筋方向移动
D.电解一段时间后钢筋附近溶液的pH增大
A [由Cl-移动的方向可知钢筋接电源的负极,A项错误;金属导电网为阳极,发生的电
极反应为2Cl--2e-===Cl↑,B项正确; 混凝土一端为阴极,钙离子为阳离子,所以向钢筋
2
方向移动,C项正确;钢筋附近发生的电极反应为2HO+2e-===H ↑+2OH-,所以电解一
2 2
段时间后钢筋附近溶液的pH增大,D项正确。]
14.(2021·江西九江六校联考)最近某科研小组创建了一种通过连续电解将能量储存为
化学能的装置。在氧化钇基质的阳极和二氧化钛涂覆的钛阴极之间是可通过H+的固体聚合
物电解质,其结构如图所示。下列说法正确的是( )
A.电源的b极为负极
B.在能量转化过程中,固体电解质中H+由阴极向阳极移动
C.阴极的电极反应式为:OX+4H++4e-===GC+HO
2
D.为增强阳极电解液导电性,可在水中添加适量盐酸或NaCl
C [右侧电极发生氧化反应生成O,该电极为阳极,则b极为电源的正极,A项错误;电
2
解池中阳离子向阴极移动,则固体电解质中H+由阳极向阴极移动,B项错误; 阴极上OX发
生还原反应生成GC,电极反应式为OX+4H++4e-===GC+HO,C项正确;阳极电解液中
2
添加适量盐酸或NaCl,Cl-在阳极放电生成有毒气体Cl,易污染环境,D项错误。]
2
15.(1)(2020·全国卷Ⅱ,26(1))氯气是制备系列含氯化合物的主要原料,可采用如图所示
的装置来制取。装置中的离子膜只允许______离子通过,氯气的逸出口是________(填标号)。
(2)(2020·全国卷Ⅱ,28(3))CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现
4 2
两种分子的耦合转化,其原理如下图所示:①阴极上的反应式为______________________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为________。
4 2
解析 (1)根据图示,电解食盐水制备氯气时,阳极产生氯气,从a口逸出,阴极产生OH
-,为了防止阴极产生的OH-与阳极产生的Cl 反应,中间的离子交换膜只允许Na+通过,即
2
为阳离子交换膜;(2)①根据图示,阴极反应物为CO,电极反应式为CO+2e-===CO+O2-;
2 2
②阳极反应式为6CH+5O2--10e-===CH CH+2C H+5HO;根据电子守恒,6CH~10e-
4 3 3 2 4 2 4
~5CO,消耗的CH 与CO 体积之比为6∶5。
2 4 2
答案 (1)Na+ a (2)①CO+2e-===CO+O2- ②6∶5
2
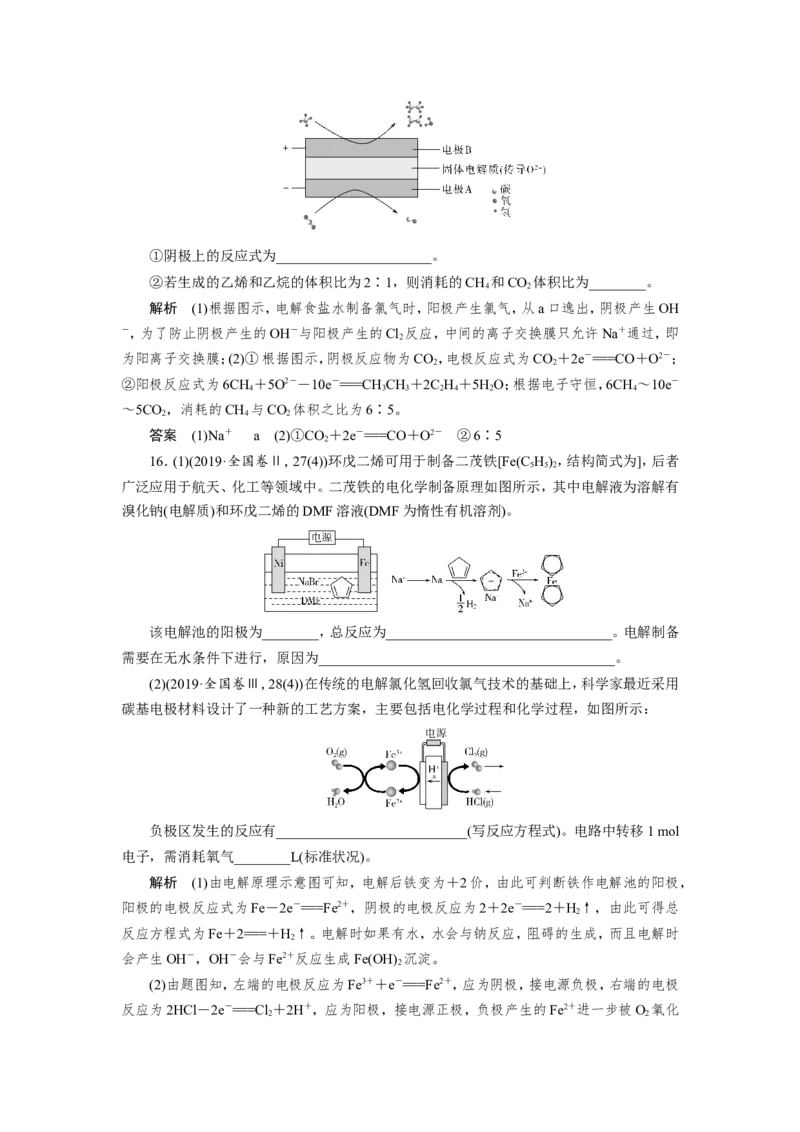
16.(1)(2019·全国卷Ⅱ,27(4))环戊二烯可用于制备二茂铁[Fe(C H),结构简式为],后者
5 5 2
广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有
溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
该电解池的阳极为________,总反应为________________________________。电解制备
需要在无水条件下进行,原因为__________________________________________。
(2)(2019·全国卷Ⅲ,28(4))在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用
碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如图所示:
负极区发生的反应有___________________________(写反应方程式)。电路中转移1 mol
电子,需消耗氧气________L(标准状况)。
解析 (1)由电解原理示意图可知,电解后铁变为+2价,由此可判断铁作电解池的阳极,
阳极的电极反应式为Fe-2e-===Fe2+,阴极的电极反应为2+2e-===2+H↑,由此可得总
2
反应方程式为Fe+2===+H↑。电解时如果有水,水会与钠反应,阻碍的生成,而且电解时
2
会产生OH-,OH-会与Fe2+反应生成Fe(OH) 沉淀。
2
(2)由题图知,左端的电极反应为Fe3++e-===Fe2+,应为阴极,接电源负极,右端的电极
反应为2HCl-2e-===Cl+2H+,应为阳极,接电源正极,负极产生的Fe2+进一步被O 氧化
2 2生成Fe3+,则4Fe2++O+4H+===4Fe3++2HO;由此可知,每消耗1 mol O ,需转移4 mol电
2 2 2
子,则转移1 mol电子时,应消耗 mol O,标准状况下, mol O 的体积为 mol×22.4 L/mol
2 2
=5.6 L。
答案 (1)Fe电极 Fe+2===+H↑[或Fe+2C H===Fe(C H) +H↑] 水会阻碍中间
2 5 6 5 5 2 2
物Na的生成;水会电解生成OH-,进一步与Fe2+反应生成Fe(OH)
2
(2)Fe3++e-===Fe2+,4Fe2++O+4H+===4Fe3++2HO 5.6
2 2