文档内容
1.下列说法错误的是 ( )
A.卤化氢中,HF的沸点最高,是由于HF分子间存在氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
C.HO的沸点比HF的沸点高,是由于水中氢键键能大
2
D.氨气极易溶于水与氨气分子和水分子间形成氢键有关
2.偶极矩是电荷量与正、负电荷中心间的距离的乘积。用偶极矩可判断分子的极性:一般
来说极性分子的偶极矩不为零;非极性分子的偶极矩为零。下列分子中偶极矩不为零的是(
)
A.BeCl B.BF C.PCl D.CH
2 3 3 4
3.下列化合物中含有2个手性碳原子的是( )
A.
B.
C.
D.
4.下列微粒中含有配位键的是( )
①HO+ ②NH ③[Cu(H O) ]2+
3 2 4
④[Fe(SCN) ]3- ⑤CuCl ⑥CH ⑦NH
6 4 3
A.①②③④⑤ B.①③⑥
C.④⑤⑦ D.②④⑥
5.(2020·海南,7)向CuSO 溶液中滴加氨水至过量,下列叙述正确的是( )
4
A.先出现沉淀,后沉淀溶解变为无色溶液
B.离子方程式为Cu2++4NH ·H O===[Cu(NH )]2++4HO
3 2 3 4 2C.Cu2+与NH 中的氮原子以π键结合
3
D.NH 分子中∠HNH为109°28′
3
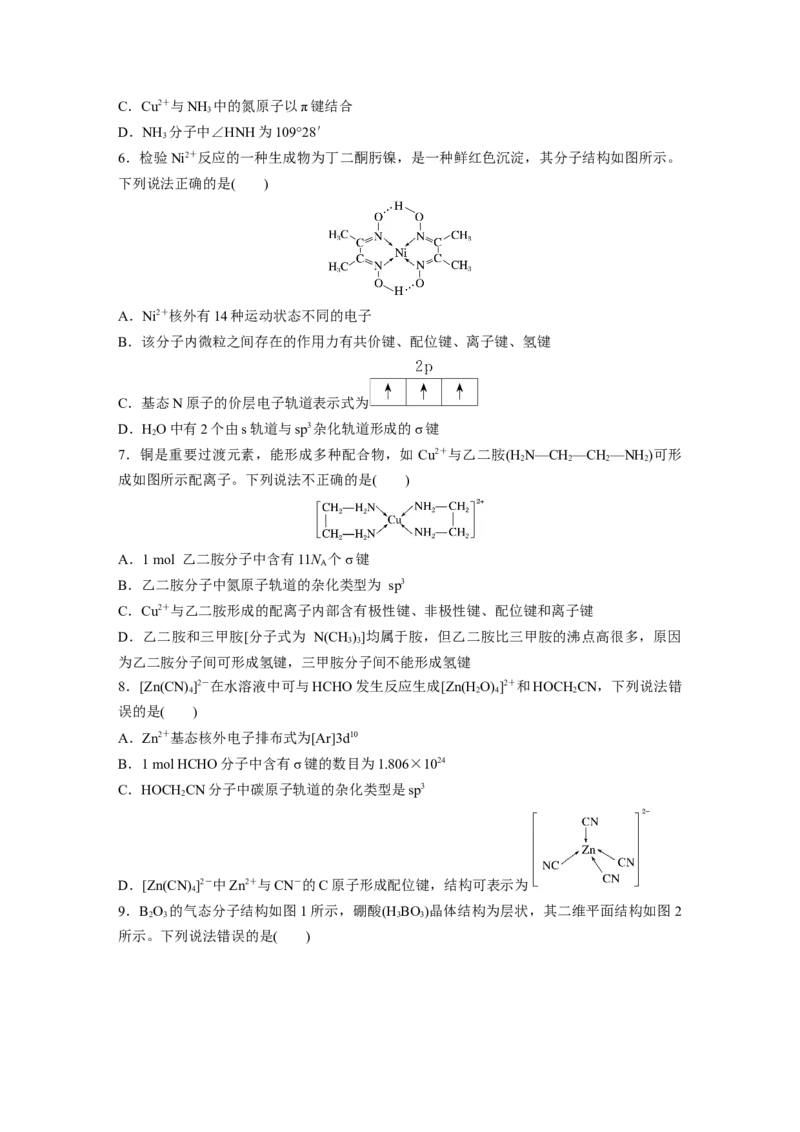
6.检验Ni2+反应的一种生成物为丁二酮肟镍,是一种鲜红色沉淀,其分子结构如图所示。
下列说法正确的是( )
A.Ni2+核外有14种运动状态不同的电子
B.该分子内微粒之间存在的作用力有共价键、配位键、离子键、氢键
C.基态N原子的价层电子轨道表示式为
D.HO中有2个由s轨道与sp3杂化轨道形成的σ键
2
7.铜是重要过渡元素,能形成多种配合物,如 Cu2+与乙二胺(H N—CH —CH—NH )可形
2 2 2 2
成如图所示配离子。下列说法不正确的是( )
A.1 mol 乙二胺分子中含有11N 个σ键
A
B.乙二胺分子中氮原子轨道的杂化类型为 sp3
C.Cu2+与乙二胺形成的配离子内部含有极性键、非极性键、配位键和离子键
D.乙二胺和三甲胺[分子式为 N(CH )]均属于胺,但乙二胺比三甲胺的沸点高很多,原因
3 3
为乙二胺分子间可形成氢键,三甲胺分子间不能形成氢键
8.[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成[Zn(HO) ]2+和HOCH CN,下列说法错
4 2 4 2
误的是( )
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1 mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH CN分子中碳原子轨道的杂化类型是sp3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
4
9.B O 的气态分子结构如图1所示,硼酸(H BO)晶体结构为层状,其二维平面结构如图2
2 3 3 3
所示。下列说法错误的是( )A.两分子中B原子分别采用sp杂化、sp2杂化
B.硼酸晶体中层与层之间存在范德华力
C.1 mol H BO 晶体中含有6 mol氢键
3 3
D.硼原子可提供空轨道,硼酸电离的方程式为HBO+HO[B(OH) ]-+H+
3 3 2 4
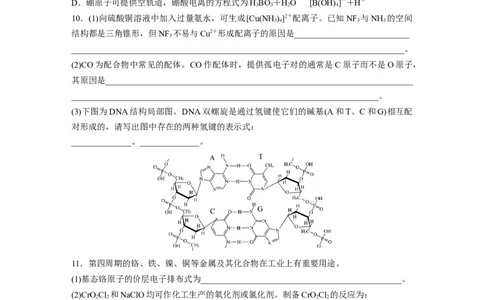
10.(1)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH )]2+配离子。已知NF 与NH 的空间
3 4 3 3
结构都是三角锥形,但NF 不易与Cu2+形成配离子的原因是___________________________
3
______________________________________________________________________________。
(2)CO为配合物中常见的配体。CO作配体时,提供孤电子对的通常是C原子而不是O原子,
其原因是________________________________________________________________________
________________________________________________________________________。
(3)下图为DNA结构局部图。DNA双螺旋是通过氢键使它们的碱基(A和T、C和G)相互配
对形成的,请写出图中存在的两种氢键的表示式:
______________、______________。
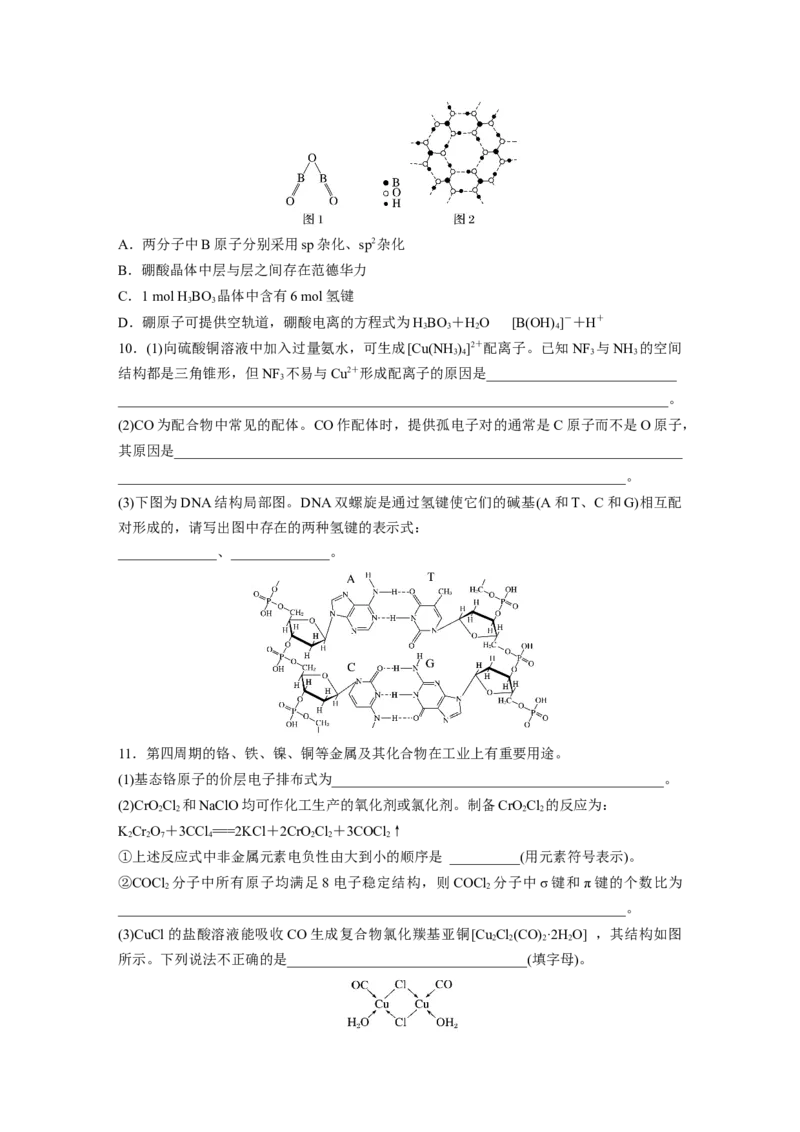
11.第四周期的铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)基态铬原子的价层电子排布式为_______________________________________________。
(2)CrO Cl 和NaClO均可作化工生产的氧化剂或氯化剂。制备CrOCl 的反应为:
2 2 2 2
KCr O+3CCl ===2KCl+2CrOCl+3COCl ↑
2 2 7 4 2 2 2
①上述反应式中非金属元素电负性由大到小的顺序是 __________(用元素符号表示)。
②COCl 分子中所有原子均满足8电子稳定结构,则COCl 分子中σ键和π键的个数比为
2 2
________________________________________________________________________。
(3)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu Cl(CO) ·2H O] ,其结构如图
2 2 2 2
所示。下列说法不正确的是__________________________________(填字母)。A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和HO作为配体
2
D.CO与N 的价层电子总数相同,其结构为C≡O
2
12.(1)配位化学创始人维尔纳发现,取 CoCl ·6NH (黄色)、CoCl ·5NH (紫红色)、
3 3 3 3
CoCl ·4NH (绿色)和CoCl ·4NH (紫色)四种化合物各1 mol,分别溶于水,加入足量硝酸银溶
3 3 3 3
液,立即产生氯化银,沉淀的量分别为3 mol、2 mol、1 mol和1 mol。
①请根据实验事实用配合物的形式写出它们的化学式。
CoCl ·6NH ______________________________________________________________________
3 3
__,
CoCl ·4NH (绿色和紫色)________________。
3 3
②上述配合物中,中心离子的配位数都是__________________________________________。
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应在有的教材中
用方程式FeCl +3KSCN===Fe(SCN) +3KCl表示。经研究表明,Fe(SCN) 是配合物,Fe3+
3 3 3
与SCN-不仅能以1∶3的个数比配合,还可以以其他个数比配合,请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供________,SCN-提供________,二者通过配位键结合。
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色,
含该离子的配合物的化学式是____________。