文档内容
第 34 讲 分子的性质 配合物与超分子
[复习目标] 1.理解分子的极性。2.掌握范德华力的含义及对物质性质的影响。 3.理解氢键
的含义, 能列举存在氢键的物质, 并能解释氢键对物质性质的影响。4.理解配位键的含义。
5.了解超分子的概念。
考点一 键的极性与分子极性
1.键的极性
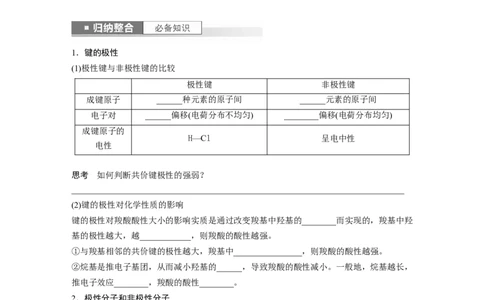
(1)极性键与非极性键的比较
极性键 非极性键
成键原子 ______种元素的原子间 ______元素的原子间
电子对 ______偏移(电荷分布不均匀) ________偏移(电荷分布均匀)
成键原子的
H—Cl 呈电中性
电性
思考 如何判断共价键极性的强弱?
______________________________________________________________________________
(2)键的极性对化学性质的影响
键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟基的________而实现的,羧基中羟
基的极性越大,越____________,则羧酸的酸性越强。
①与羧基相邻的共价键的极性越大,羧基中________________,则羧酸的酸性越强。
②烷基是推电子基团,从而减小羟基的______,导致羧酸的酸性减小。一般地,烷基越长,
推电子效应________,羧酸的酸性________。
2.极性分子和非极性分子
(1)概念
极性分子:分子的正电中心和负电中心______,键的极性的向量和________零。
非极性分子:分子的正电中心和负电中心________,键的极性的向量和________零。
(2)极性分子和非极性分子的判断方法
①A—A型分子一定是非极性分子、A—B型分子一定是极性分子。
②判断AB 型分子极性的两条经验规律
n
a.中心原子A化合价的绝对值等于该元素原子最外层电子数,则为非极性分子,反之则为
极性分子。b.中心原子A没有孤电子对,则为非极性分子,反之则为极性分子。
一、有关羧酸酸性强弱的判断及归因分析
1.试比较下列有机酸的酸性强弱。
①CFCOOH ②CCl COOH ③CHCl COOH
3 3 2
④CHClCOOH ⑤CHCOOH
2 3
⑥CHCHCOOH
3 2
____________________________________________________________________________
2.酸性:氟乙酸大于氯乙酸的原因是___________________________________________
___________________________________________________________________________。
3.酸性:甲酸大于乙酸的原因是______________________________________________
__________________________________________________________________________。
二、分子极性的判断
4.下列分子P 、C 、 Cl 、NO、HO 、NO 、SO 、CHCl 、CS 、C H 、SO 、 BF 、
4 60 2 2 2 2 2 2 2 2 2 2 3 3
HCN 、 HCHO 、 PCl 、 PCl 属 于 极 性 分 子 的 是
5 3
___________________________________________
____________________________________________________________________________;
属于非极性分子的是____________________________________________________________。
考点二 分子间作用力
1.分子间作用力
(1)范德华力、氢键的对比
范德华力 氢键
H与N、O、F等电负性很大
作用微粒 分子或原子(稀有气体分子)
的原子
分类 分子内氢键和分子间氢键
特征 ____方向性和饱和性 ____饱和性和方向性
强度 共价键>______>_______
①组成和结构相似的物质,
相对分子质量______,范德 X—H…Y强弱与X和Y的电
影响其强度的因素
华力越大; 负性有关
②分子的极性______,范德华力越大
对物质性质的影响 主要影响物理性质(如熔、沸点)
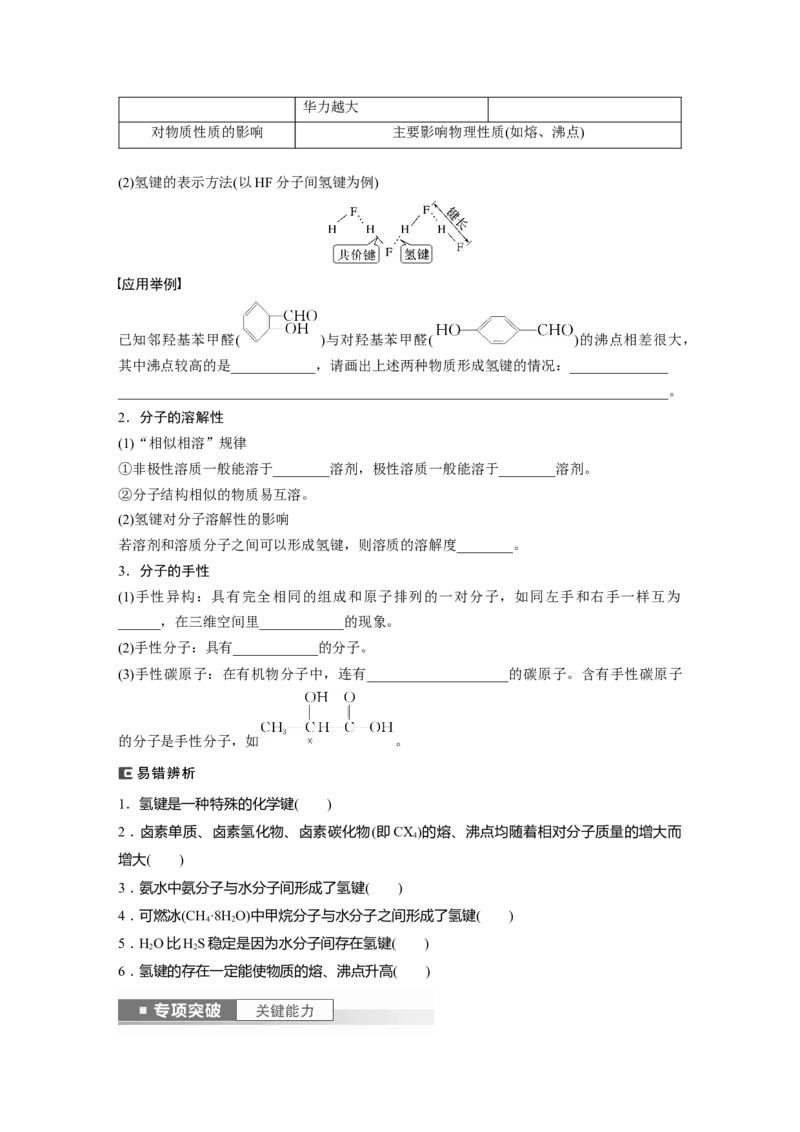
(2)氢键的表示方法(以HF分子间氢键为例)
应用举例
已知邻羟基苯甲醛( )与对羟基苯甲醛( )的沸点相差很大,
其中沸点较高的是____________,请画出上述两种物质形成氢键的情况:______________
______________________________________________________________________________。
2.分子的溶解性
(1)“相似相溶”规律
①非极性溶质一般能溶于________溶剂,极性溶质一般能溶于________溶剂。
②分子结构相似的物质易互溶。
(2)氢键对分子溶解性的影响
若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度________。
3.分子的手性
(1)手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为
______,在三维空间里____________的现象。
(2)手性分子:具有____________的分子。
(3)手性碳原子:在有机物分子中,连有____________________的碳原子。含有手性碳原子
的分子是手性分子,如 。
1.氢键是一种特殊的化学键( )
2.卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而
4
增大( )
3.氨水中氨分子与水分子间形成了氢键( )
4.可燃冰(CH·8H O)中甲烷分子与水分子之间形成了氢键( )
4 2
5.HO比HS稳定是因为水分子间存在氢键( )
2 2
6.氢键的存在一定能使物质的熔、沸点升高( )一、范德华力、氢键的存在
1.液氨、液氯、清洗剂、萃取剂等重点品种使用企业和白酒企业,应加强储罐区、危化品
库房、危化品输送等的管理,确保化工生产安全。下列说法正确的是( )
A.液氨中只存在范德华力
B.液氨分子间作用力强,所以其稳定性大于PH
3
C.液氯挥发导致人体吸入后中毒,是因为液氯分子中的共价键键能较小
D.萃取剂CCl 的沸点高于CH 的沸点
4 4
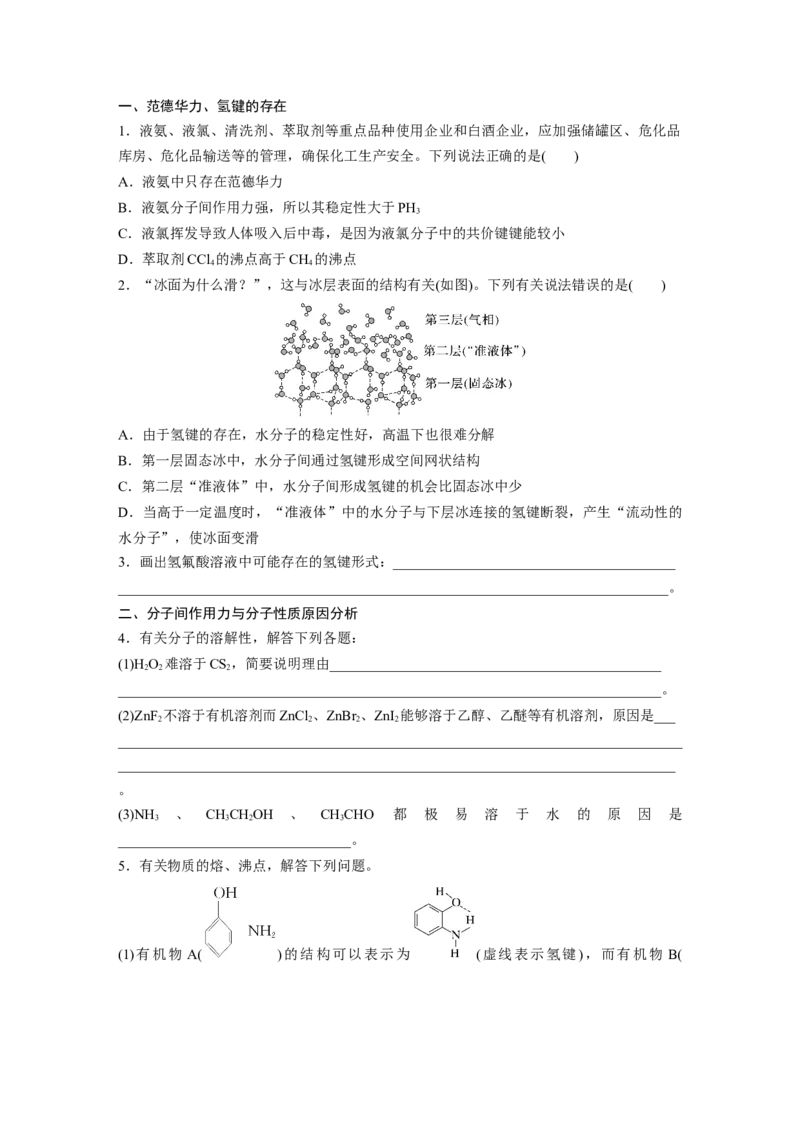
2.“冰面为什么滑?”,这与冰层表面的结构有关(如图)。下列有关说法错误的是( )
A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性的
水分子”,使冰面变滑
3.画出氢氟酸溶液中可能存在的氢键形式:________________________________________
______________________________________________________________________________。
二、分子间作用力与分子性质原因分析
4.有关分子的溶解性,解答下列各题:
(1)H O 难溶于CS,简要说明理由_______________________________________________
2 2 2
_____________________________________________________________________________。
(2)ZnF 不溶于有机溶剂而ZnCl、ZnBr 、ZnI 能够溶于乙醇、乙醚等有机溶剂,原因是___
2 2 2 2
________________________________________________________________________________
_______________________________________________________________________________
。
(3)NH 、 CHCHOH 、 CHCHO 都 极 易 溶 于 水 的 原 因 是
3 3 2 3
_________________________________。
5.有关物质的熔、沸点,解答下列问题。
(1)有机物 A( )的结构可以表示为 (虚线表示氢键),而有机物 B()只能形成分子间氢键。工业上用水蒸气蒸馏法将A和B进行分离,首先被蒸出的
成分是____,原因是:
______________________________________________________________________________。
(2)苯胺( )与甲苯( )的相对分子质量相近,但苯胺的熔点
(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(111 ℃),原因是
__________________________________。
(3)如图为 S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
8
________________________________________________________________________。
(4)在CO 低压合成甲醇反应(CO +3H===CHOH+HO)所涉及的4种物质中,沸点从高到
2 2 2 3 2
低的顺序为________________,原因是____________________________________________。
考点三 配合物、超分子
1.配位键
(1)形成:由一个原子单方面提供____________而另一个原子接受孤电子对形成的共价键,
即“电子对给予—接受”键被称为________。
(2)表示方法:常用“____”来表示配位键,箭头指向接受孤电子对的原子,如NH可表示
为______________,在NH中,虽然有一个N—H形成过程与其他3个N—H形成过程不同,
但是一旦形成之后,4个共价键就完全________。
2.配位化合物
(1)概念:金属离子或原子(称为中心离子或原子)与某些____________(称为配体或配位体)以
________结合形成的化合物。
(2)形成条件
中心离子或原子:有空轨道,一般是带正电的金属离子,特别是过渡金属离子,如Fe3+、
Cu2+、Zn2+、Ag+等,但也有电中性的原子等。
配位体:其中的配位原子(配位体中直接同中心离子或原子配合的原子)有孤电子对。配位体
可以是分子,如CO、NH 、HO等,也可以是离子,如F-、Cl-、Br-、I-、CN-、SCN
3 2-、OH-等。
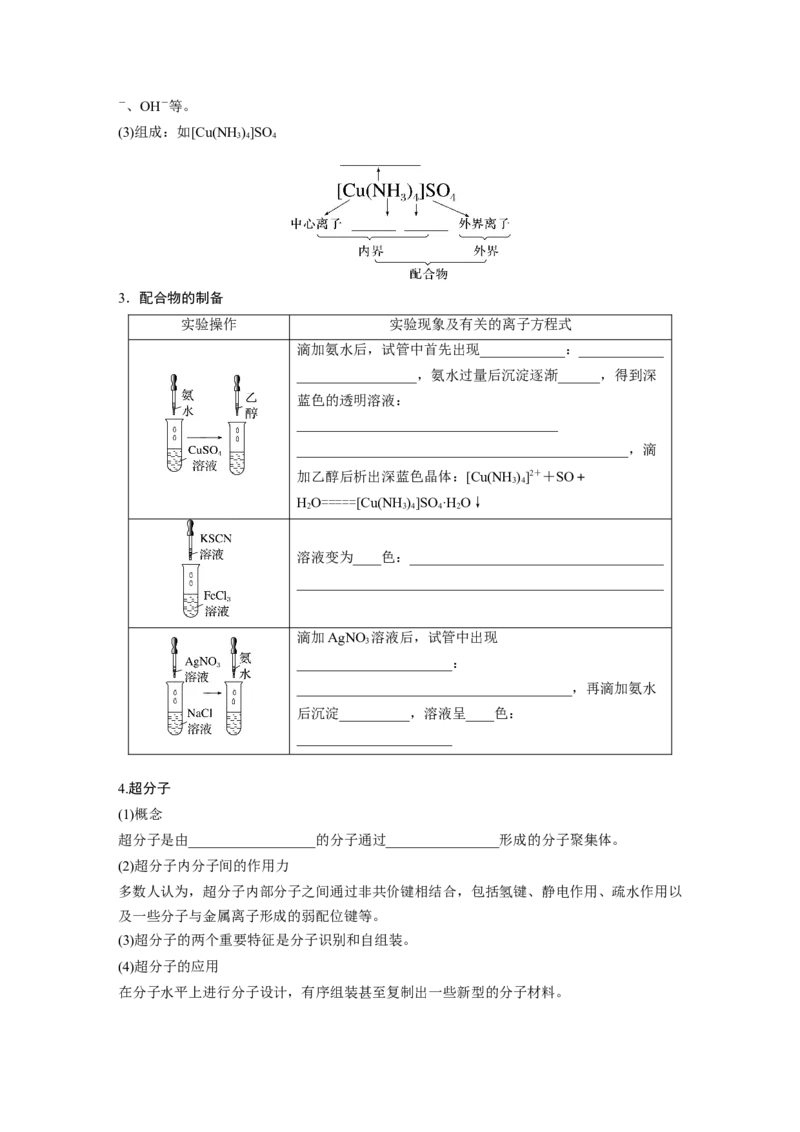
(3)组成:如[Cu(NH )]SO
3 4 4
3.配合物的制备
实验操作 实验现象及有关的离子方程式
滴加氨水后,试管中首先出现____________:____________
_________________,氨水过量后沉淀逐渐______,得到深
蓝色的透明溶液:
_____________________________________
_______________________________________________,滴
加乙醇后析出深蓝色晶体:[Cu(NH )]2++SO+
3 4
HO=====[Cu(NH )]SO ·H O↓
2 3 4 4 2
溶液变为____色:____________________________________
____________________________________________________
滴加AgNO 溶液后,试管中出现
3
______________________:
_______________________________________,再滴加氨水
后沉淀__________,溶液呈____色:
______________________
4.超分子
(1)概念
超分子是由__________________的分子通过________________形成的分子聚集体。
(2)超分子内分子间的作用力
多数人认为,超分子内部分子之间通过非共价键相结合,包括氢键、静电作用、疏水作用以
及一些分子与金属离子形成的弱配位键等。
(3)超分子的两个重要特征是分子识别和自组装。
(4)超分子的应用
在分子水平上进行分子设计,有序组装甚至复制出一些新型的分子材料。1.配位键实质上是一种特殊的共价键( )
2.提供孤电子对的微粒既可以是分子,也可以是离子( )
3.有配位键的化合物就是配位化合物( )
4.配位化合物都很稳定( )
5.在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
6.Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
一、配合物
1.关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
2.(2022·济南调研)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,
难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是( )
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,生成深蓝色的配离子[Cu(NH )]2+
3 4
C.配位化合物中只有配位键
D.在配离子[Cu(NH )]2+中,Cu2+给出孤电子对,NH 提供空轨道
3 4 3
3.(2023·烟台质检)过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为
这方面的研究无论是理论上还是工业应用上都有重要意义。氯化铁溶液用于检验食用香精乙
酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示。下列有关该配离子的说法正确
的是( )
A.1 mol该配离子中含有π键的个数是6×6.02×1023
B.该配离子中碳原子的杂化类型均为sp2杂化
C.该配离子含有的非金属元素中电负性最大的是碳
D.该配离子中含有的化学键有离子键、共价键、配位键
4.回答下列问题:(1)将白色CuSO 粉末溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的
4
配 离 子 , 请 写 出 生 成 此 配 离 子 的 离 子 方 程 式 :
__________________________________________,蓝色溶液中的阳离子内存在的全部化学键
类型有__________。1 mol该阳离子中含σ键个数为________。
(2)CuSO ·5H O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式
4 2
(必须将配位键表示出来):________________________________________________________。
(3)向CuSO 溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝
4
色溶液,继续向其中加入极性较小的乙醇可以析出深蓝色的[Cu(NH )]SO ·H O晶体。下列
3 4 4 2
说法不正确的是_________(填字母)。
a.[Cu(NH )]SO 的组成元素中电负性最大的是N元素
3 4 4
b.CuSO 晶体及[Cu(NH )]SO ·H O中S原子的杂化方式均为sp3
4 3 4 4 2
c.[Cu(NH )]SO 所含有的化学键有离子键、共价键和配位键
3 4 4
d.NH 分子内的H—N—H键角大于HO分子内的H—O—H 键角
3 2
e.SO的空间结构为正四面体形
f.[Cu(NH )]2+中,N原子是配位原子
3 4
g.NH 分子中氮原子的杂化轨道类型为sp2
3
二、超分子
5.下列关于超分子的说法中,不正确的是( )
A.超分子是由两种或两种以上的分子必须通过氢键相互作用形成的分子聚集体
B.将C 加入一种空腔大小适配C 的“杯酚”中会形成超分子
60 60
C.碱金属离子虽然不是分子,但冠醚在识别碱金属离子时,形成的也是超分子
D.超分子的重要特征是自组装和分子识别
6.冠醚是一种超分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯并-18-冠-6
与K+形成的配离子的结构如图所示。下列说法错误的是( )
冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子
B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种
D.一个配离子中配位键的数目为6
7.利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配C 的“杯酚”中
60 70 60 70 60进行分离的流程如图。下列说法错误的是( )
A.第二电离能:C