文档内容
第 62 讲 有机合成推断及合成路线设计
复习目标 1.根据合成路线图学会推断有机物的结构,判断反应条件及熟练书写化学方程
式。2.根据信息能设计有机化合物的合成路线。
考点一 有机合成路线的设计
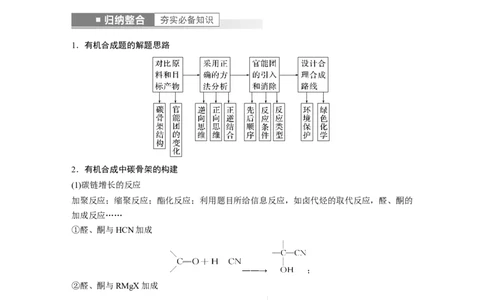
1.有机合成题的解题思路
2.有机合成中碳骨架的构建
(1)碳链增长的反应
加聚反应;缩聚反应;酯化反应;利用题目所给信息反应,如卤代烃的取代反应,醛、酮的
加成反应……
①醛、酮与HCN加成
――→ ;
②醛、酮与RMgX加成
―→ ;
③醛、酮的羟醛缩合(其中至少一种有α-H)
――→ ;
④苯环上的烷基化反应+R—Cl――→ +HCl;
⑤卤代烃与活泼金属作用
2CHCl+2Na―→CH—CH+2NaCl。
3 3 3
(2)碳链减短的反应
①烷烃的裂化反应;
②利用题目所给信息反应,如烯烃、炔烃的氧化反应,羧酸及其盐的脱羧反应……
(3)常见由链成环的方法
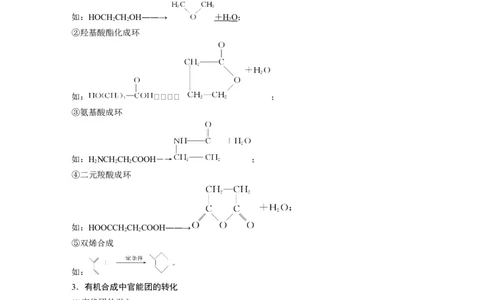
①二元醇成环
如:HOCH CHOH――→ + H O;
2 2 2
②羟基酸酯化成环
如: ;
③氨基酸成环
如:HNCH CHCOOH―→ ;
2 2 2
④二元羧酸成环
如:HOOCCH CHCOOH――→
2 2
⑤双烯合成
如:
3.有机合成中官能团的转化
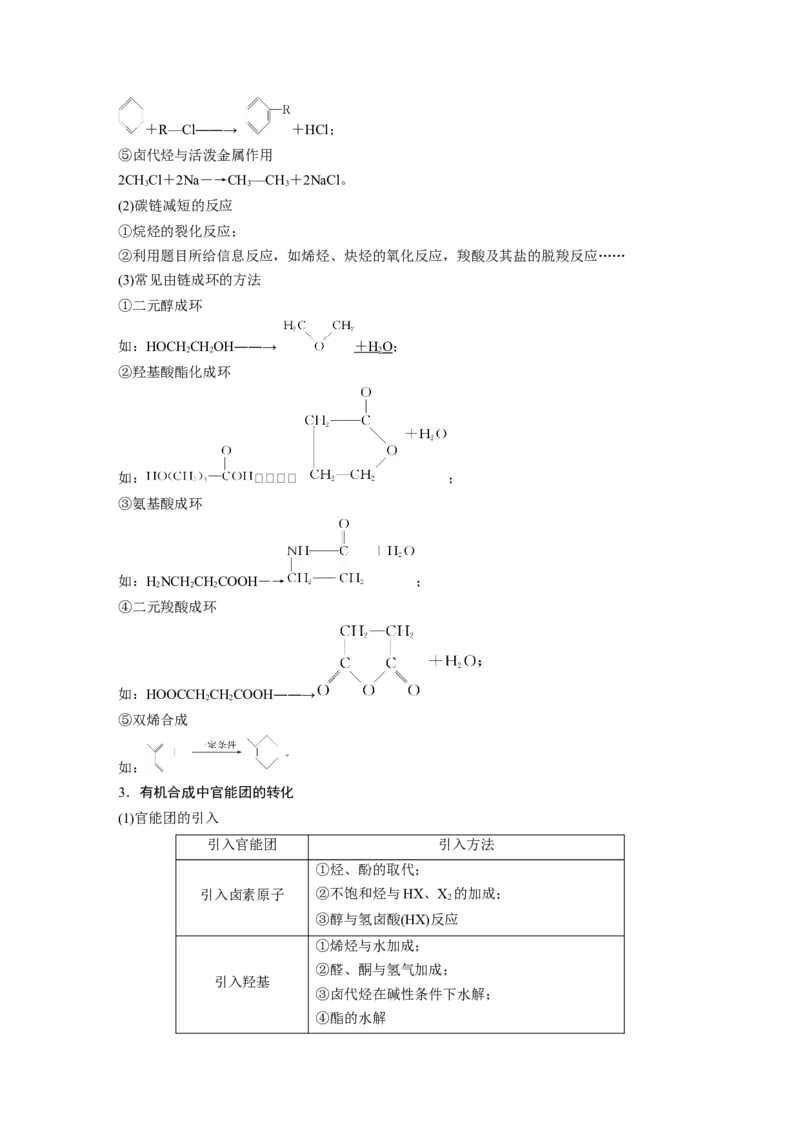
(1)官能团的引入
引入官能团 引入方法
①烃、酚的取代;
引入卤素原子 ②不饱和烃与HX、X 的加成;
2
③醇与氢卤酸(HX)反应
①烯烃与水加成;
②醛、酮与氢气加成;
引入羟基
③卤代烃在碱性条件下水解;
④酯的水解①某些醇或卤代烃的消去;
引入碳碳双键 ②炔烃不完全加成;
③烷烃裂化
①醇的催化氧化;
引入碳氧双键 ②连在同一个碳上的两个羟基脱水;
③含碳碳三键的物质与水加成
①醛基氧化;
引入羧基
②酯、肽、蛋白质、羧酸盐的水解
(2)官能团的消除
①通过加成反应可以消除不饱和键(碳碳双键、碳碳三键、苯环等);
②通过消去、氧化或酯化反应等消除羟基;
③通过加成或氧化反应等消除醛基;
④通过水解反应消除酯基、肽键、卤素原子。
(3)官能团的改变
①利用官能团的衍生关系进行衍变,如
R—CHOHR—CHO――→R—COOH;
2
②通过某种化学途径使一个官能团变为两个,如
CHCHOH――→CH==CH――→Cl—CH —CHCl――→HO—CH —CH—OH;
3 2 2 2 2 2 2 2
③通过某种手段改变官能团的位置,如
。
4.官能团的保护与恢复
(1)碳碳双键:在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后
再利用消去反应转变为碳碳双键。
HOCH CH==CHCH OH――→HOCH CHCHClCH OH――――→ ―――
2 2 2 2 2
―→ HOOC—CH = = CH—COOH 。
(2)酚羟基:在氧化其他基团前可以用NaOH溶液或CHI保护。
3
(3)醛基:在氧化其他基团前可以用乙醇(或乙二醇)加成保护。
① ――→ ――→② ――――――――→ ――→
(4)氨基:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
――――→ ――――→
(5)醇羟基、羧基可以成酯保护。
一、根据已知信息设计合成路线
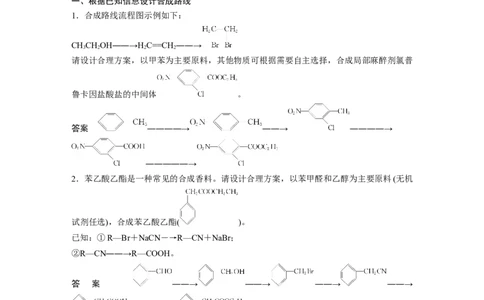
1.合成路线流程图示例如下:
CHCHOH――→HC==CH――→
3 2 2 2
请设计合理方案,以甲苯为主要原料,其他物质可根据需要自主选择,合成局部麻醉剂氯普
鲁卡因盐酸盐的中间体 。
答案 ――――→ ――→ ――――→
―――――→
2.苯乙酸乙酯是一种常见的合成香料。请设计合理方案,以苯甲醛和乙醇为主要原料(无机
试剂任选),合成苯乙酸乙酯( )。
已知:①R—Br+NaCN―→R—CN+NaBr;
②R—CN――→R—COOH。
答 案 ――→ ――→ ――→ ――→
―――――→
3.染料中间体DSD酸的结构可表示为 。请选用甲苯和其他
合适的试剂,并设计合理方案合成DSD酸(本合成过程反应条件可不写)。
已知:① ――――――――→ ;
② ――――――→ ;(弱碱性,苯胺易氧化)
③ ――→
答案 ―――――→ ――――→
――→ ―――――→
4.以CH==CHCH OH为主要原料(其他无机试剂任选)设计CH==CHCOOH的合成路线流
2 2 2
程图(已知CH==CH 可被氧气催化氧化为 ),通过此题的解答,总结设计有机合成路线需
2 2
注意的情况(至少写2条):
。
答 案
CH==CHCH OH――→CHCHClCH OH――→CHCHClCOOH――→CH==CHCOONa――
2 2 3 2 3 2
→CH==CHCOOH;选择合适的反应条件、要注意官能团的保护
2
解析 以CH==CHCH OH为主要原料合成CH==CHCOOH,CH==CHCH OH可先和HCl
2 2 2 2 2
发生加成反应,保护碳碳双键,再利用强氧化剂将醇羟基氧化为羧基,最后结合卤代烃的消
去引入碳碳双键;在选择合成路线时,需要选择合适的反应条件,同时注意官能团的保护,
上述流程中用强氧化剂氧化羟基生成羧基时需要防止碳碳双键被氧化,故需要先保护碳碳双
键。
二、类比转化关系图提取信息设计合成路线
5.化合物G是重要的药物中间体,以有机物 A为原料制备G,其合成路线如下:
参考上述合成线路,写出以1-丙醇、丙二酸二甲酯(CHOOCCH COOCH )、尿素[CO(NH)]
3 2 3 2 2为起始原料制备 的合成线路(其他试剂任选)。
答案
解 析 参 考 流 程 信 息 知 , 可 将 CHCHCHOH 转 化 为 CHCHBrCH , 再 与
3 2 2 3 3
CHOOCCH COOCH 发生取代反应生成 ,接着与尿素发生取代反应得到目标产物,
3 2 3
合成路线见答案。
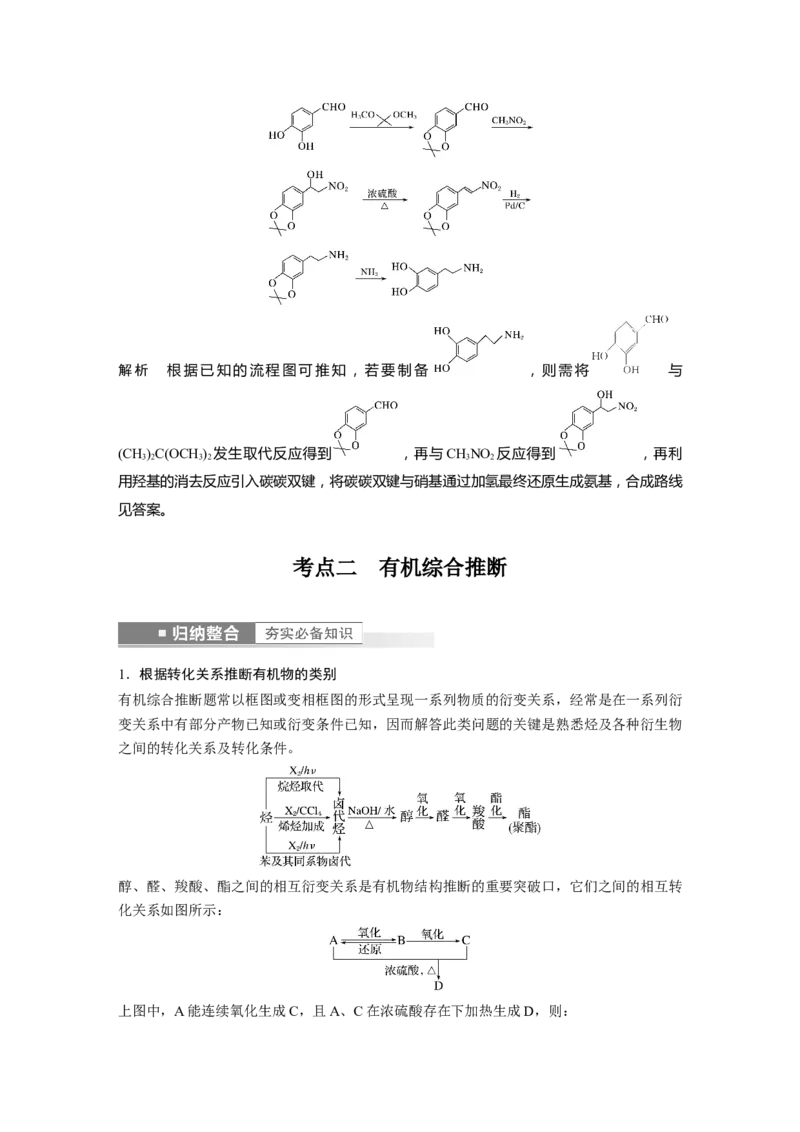
6.沙罗特美是一种长效平喘药,其合成的部分路线如图:
请写出以 、(CH)C(OCH ) 、CHNO 为原料制备 的合成路线流
3 2 3 2 3 2
程图(无机试剂任用,合成路线流程图示例见本题题干)。
答案解析 根据已知的流程图可推知,若要制备 ,则需将 与
(CH)C(OCH ) 发生取代反应得到 ,再与CHNO 反应得到 ,再利
3 2 3 2 3 2
用羟基的消去反应引入碳碳双键,将碳碳双键与硝基通过加氢最终还原生成氨基,合成路线
见答案。
考点二 有机综合推断
1.根据转化关系推断有机物的类别
有机综合推断题常以框图或变相框图的形式呈现一系列物质的衍变关系,经常是在一系列衍
变关系中有部分产物已知或衍变条件已知,因而解答此类问题的关键是熟悉烃及各种衍生物
之间的转化关系及转化条件。
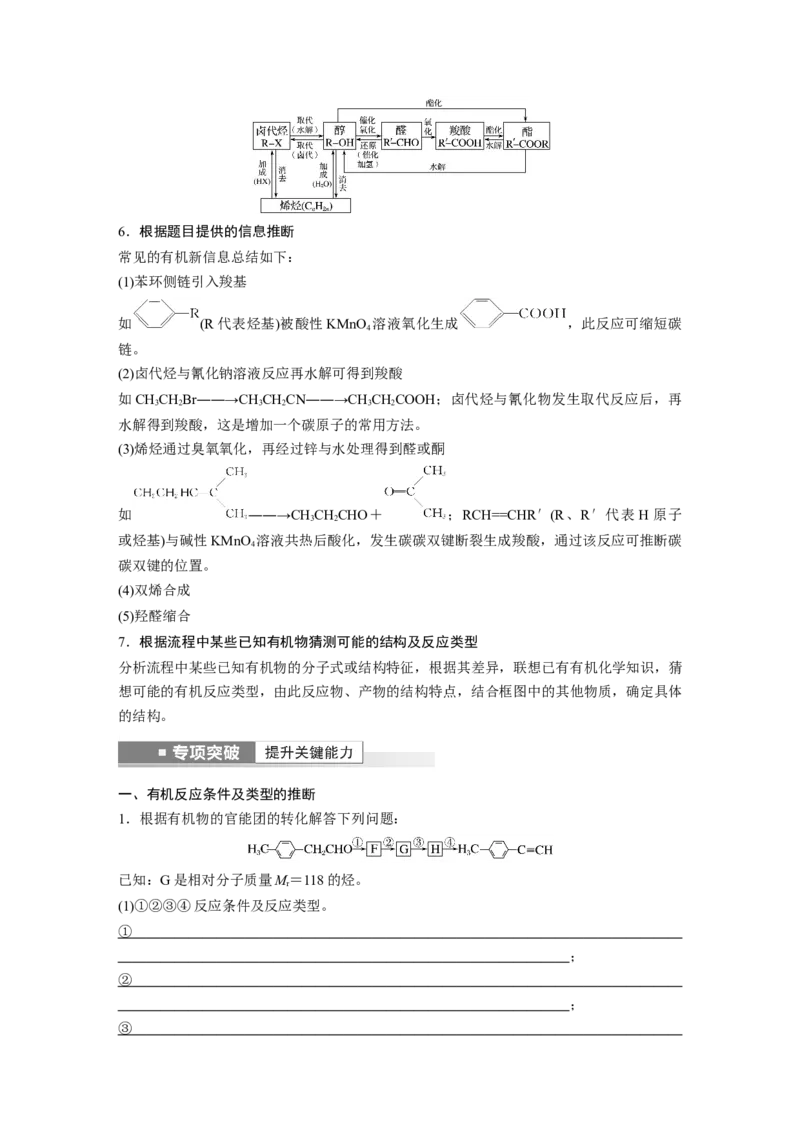
醇、醛、羧酸、酯之间的相互衍变关系是有机物结构推断的重要突破口,它们之间的相互转
化关系如图所示:
上图中,A能连续氧化生成C,且A、C在浓硫酸存在下加热生成D,则:①A为醇,B为醛,C为羧酸,D为酯。
②A、B、C三种物质中碳原子数相同,碳骨架结构相同。
③A分子中含 — CH OH 结构。
2
2.根据试剂或特征现象推知官能团的种类
熟记下列特征现象与官能团的关系。
(1)使溴的四氯化碳溶液褪色,则表示该物质中可能含有“ ”或“ — C ≡ C— ”等结
构。
(2)使KMnO (H+)溶液褪色,则该物质中可能含有“ ”“ — C ≡ C— ”或“ — CHO ”
4
等结构或为苯的同系物。
(3)遇FeCl 溶液发生显色反应,或加入饱和溴水出现白色沉淀,则该物质中含有酚羟基。
3
(4)遇浓硝酸变黄,则表明该物质是含有苯环结构的蛋白质。
(5)遇I 变蓝则该物质为淀粉。
2
(6)加入新制的Cu(OH) ,加热有砖红色沉淀生成或加入银氨溶液加热有银镜生成,表示含有
2
—CHO。
(7)加入Na放出H,表示含有 — OH 或 — COOH 。
2
(8)加入NaHCO 溶液产生气体,表示含有 — COOH 。
3
3.根据有机反应中定量关系推断官能团的数目
(1)烃和卤素单质的取代:取代 1 mol 氢原子,消耗1 mol卤素单质(X )。
2
(2) 的加成:与H、Br 、HCl、HO等加成时按物质的量之比为1∶1加成。
2 2 2
(3)含—OH的有机物与Na反应时:2 mol —OH生成1 mol H 。
2
(4)1 mol —CHO对应2 mol Ag或1 mol —CHO对应1 mol Cu O(注意:HCHO中相当于有
2
2个—CHO)。
(5)物质转化过程中相对分子质量的变化
①RCHOH―→RCHO―→RCOOH
2
M M-2 M+14
②RCHOH―――――→CHCOOCH R
2 3 2
M M+42
③RCOOH―――――→RCOOCH CH
2 3
M M+28
(关系式中M代表第一种有机物的相对分子质量)
4.根据反应条件推断反应类型
热点强化18 3.常见反应条件与反应类型的关系。
5.根据官能团的衍变推断反应类型6.根据题目提供的信息推断
常见的有机新信息总结如下:
(1)苯环侧链引入羧基
如 (R代表烃基)被酸性KMnO 溶液氧化生成 ,此反应可缩短碳
4
链。
(2)卤代烃与氰化钠溶液反应再水解可得到羧酸
如CHCHBr――→CHCHCN――→CHCHCOOH;卤代烃与氰化物发生取代反应后,再
3 2 3 2 3 2
水解得到羧酸,这是增加一个碳原子的常用方法。
(3)烯烃通过臭氧氧化,再经过锌与水处理得到醛或酮
如 ――→CHCHCHO+ ;RCH==CHR′(R、R′代表H原子
3 2
或烃基)与碱性KMnO 溶液共热后酸化,发生碳碳双键断裂生成羧酸,通过该反应可推断碳
4
碳双键的位置。
(4)双烯合成
(5)羟醛缩合
7.根据流程中某些已知有机物猜测可能的结构及反应类型
分析流程中某些已知有机物的分子式或结构特征,根据其差异,联想已有有机化学知识,猜
想可能的有机反应类型,由此反应物、产物的结构特点,结合框图中的其他物质,确定具体
的结构。
一、有机反应条件及类型的推断
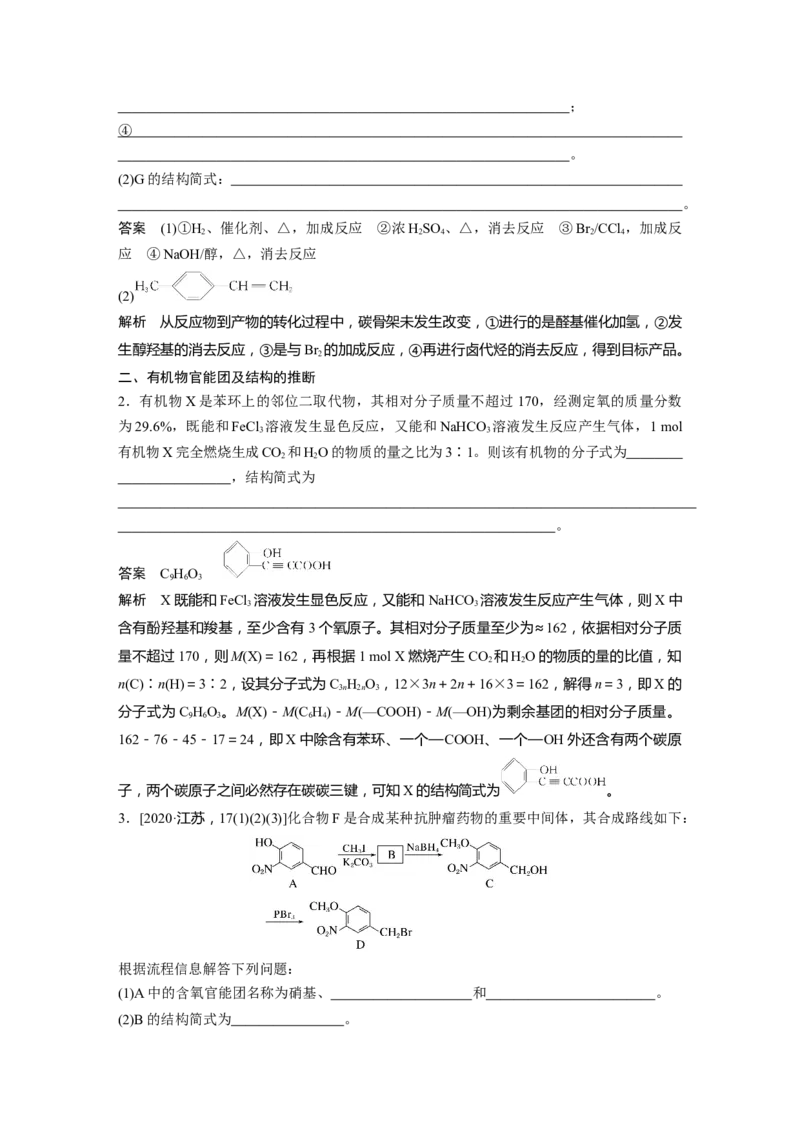
1.根据有机物的官能团的转化解答下列问题:
已知:G是相对分子质量M=118的烃。
r
(1)①②③④反应条件及反应类型。
①
;
②
;
③;
④
。
(2)G的结构简式:
。
答案 (1)①H 、催化剂、△,加成反应 ②浓HSO 、△,消去反应 ③Br /CCl ,加成反
2 2 4 2 4
应 ④NaOH/醇,△,消去反应
(2)
解析 从反应物到产物的转化过程中,碳骨架未发生改变,①进行的是醛基催化加氢,②发
生醇羟基的消去反应,③是与Br 的加成反应,④再进行卤代烃的消去反应,得到目标产品。
2
二、有机物官能团及结构的推断
2.有机物X是苯环上的邻位二取代物,其相对分子质量不超过 170,经测定氧的质量分数
为29.6%,既能和FeCl 溶液发生显色反应,又能和NaHCO 溶液发生反应产生气体,1 mol
3 3
有机物X完全燃烧生成CO 和HO的物质的量之比为3∶1。则该有机物的分子式为
2 2
,结构简式为
。
答案 C HO
9 6 3
解析 X既能和FeCl 溶液发生显色反应,又能和NaHCO 溶液发生反应产生气体,则X中
3 3
含有酚羟基和羧基,至少含有3个氧原子。其相对分子质量至少为≈162,依据相对分子质
量不超过170,则M(X)=162,再根据1 mol X燃烧产生CO 和HO的物质的量的比值,知
2 2
n(C)∶n(H)=3∶2,设其分子式为C H O ,12×3n+2n+16×3=162,解得n=3,即X的
3n 2n 3
分子式为C HO 。M(X)-M(C H)-M(—COOH)-M(—OH)为剩余基团的相对分子质量。
9 6 3 6 4
162-76-45-17=24,即X中除含有苯环、一个—COOH、一个—OH外还含有两个碳原
子,两个碳原子之间必然存在碳碳三键,可知X的结构简式为 。
3.[2020·江苏,17(1)(2)(3)]化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:
根据流程信息解答下列问题:
(1)A中的含氧官能团名称为硝基、 和 。
(2)B的结构简式为 。(3)C→D的反应类型为 。
答案 (1)醛基 (酚)羟基 (2) (3)取代反应
解析 (2)A→B发生取代反应,结合C的结构简式可知A→B是酚羟基中H原子被—CH 代
3
替,所以B的结构简式为 。(3)C→D是醇羟基被Br原子代替,反应类型为
取代反应。
考点三 有机综合大题的常考类型
一、结构已知型
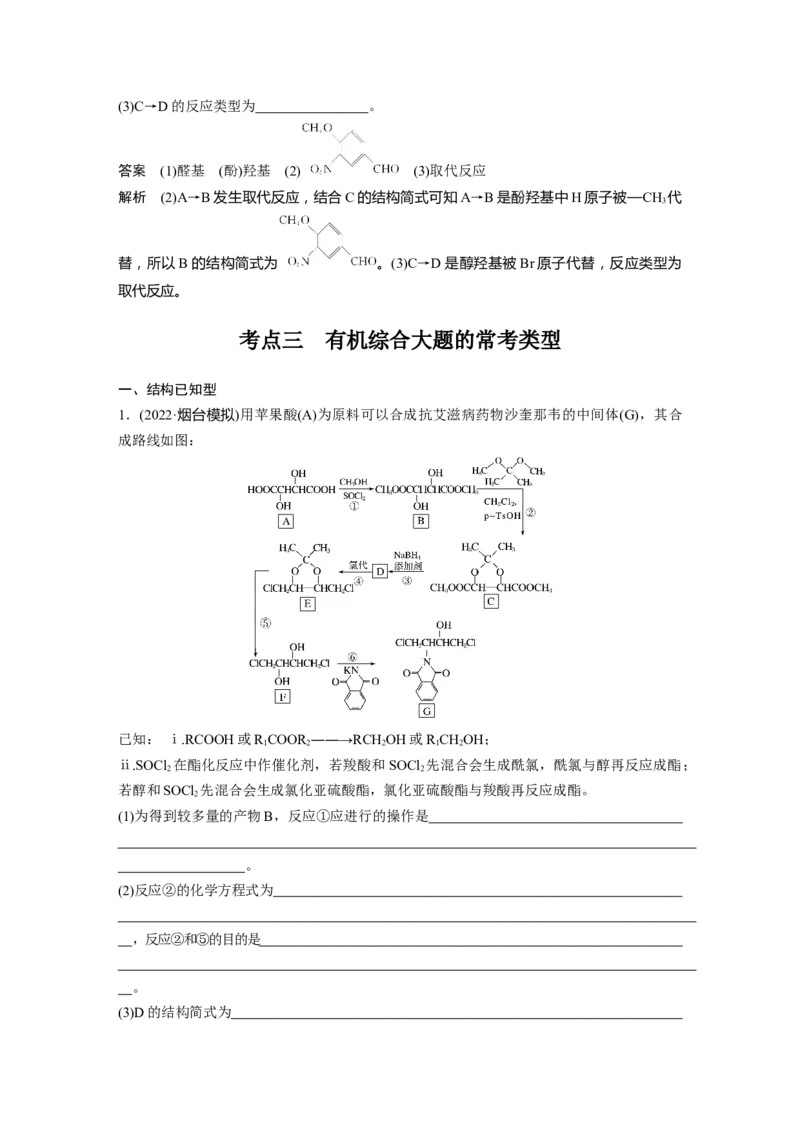
1.(2022·烟台模拟)用苹果酸(A)为原料可以合成抗艾滋病药物沙奎那韦的中间体(G),其合
成路线如图:
已知: ⅰ.RCOOH或R COOR ――→RCHOH或R CHOH;
1 2 2 1 2
ⅱ.SOCl 在酯化反应中作催化剂,若羧酸和SOCl 先混合会生成酰氯,酰氯与醇再反应成酯;
2 2
若醇和SOCl 先混合会生成氯化亚硫酸酯,氯化亚硫酸酯与羧酸再反应成酯。
2
(1)为得到较多量的产物B,反应①应进行的操作是
。
(2)反应②的化学方程式为
,反应②和⑤的目的是
。
(3)D的结构简式为,
G的分子式为 。
(4)M为C的同分异构体,M可由含有苯环的有机物N加氢还原苯环得到。N的分子中有五
个取代基,1 mol N 能与4 mol NaOH反应,但只能与2 mol NaHCO 反应,N分子中有4种
3
不同化学环境的氢原子。则M的结构简式为
。
(5)以 为原料合成 ,写出能获得更多目标产物的较优合成路线(其他
试剂任选)。
答案 (1)先将SOCl 与甲醇混合反应后,再加入苹果酸进行反应
2
(2) + ――→ +
2CHOH
3
保护两个羟基不被氯代
(3) C H NO Cl
12 11 3 2
(4) 、
(5) ――→ ――→ ―――→
解析 (1)苹果酸A为 ,若A先和SOCl 混合则A上的羟基会参与反应,根
2
据产物B的结构 可知反应后依然存在两个羟基,所以要得到较多的B,
就应先将SOCl 与甲醇混合反应后,再加入苹果酸进行反应减少副产物。
2(3)C为 ,根据反应条件以及反应信息,可推断D的结构简式为
。
(4)M为C的同分异构体,所以M分子式为C H O ,M可由含有苯环的有机物N加氢还原
9 14 6
苯环得到,所以N的分子式为C HO,不饱和度为6。1 mol N只能与2 mol NaHCO 反应,
9 8 6 3
说明一个N的分子中有2个—COOH,一个苯环和2个羧基已经占有了6个不饱和度,而1
mol N能与4 mol NaOH反应,说明除2个羧基外还有两个酚羟基,N有五个取代基,分子
中有
4种不同化学环境的氢原子,所以是高度对称的结构,所以 N可能为 或
。则M的结构简式为 或 。
解答这类问题的关键是认真分析每步转化中反应物和产物的结构,弄清官能团发生什么改变、
转化的条件以及碳原子个数是否发生变化。结合教材中典型物质的性质,规范解答关于有机
物的命名、反应类型的判断、有机化学方程式的书写、同分异构体结构简式的书写,最后模
仿已知有机物的转化过程,对比原料的结构和最终产物的结构,设计构造目标碳骨架、官能
团的合成路线。
二、半推半知型
2.(2022·昆明寻甸一中高三模拟)化合物M是一种药物中间体。实验室以烃A为原料制备M
的合成路线如图所示。请回答下列问题:已知:① ―――――→R COOH+R COR ;
1 2 3
②R CHCOOR +R COOR ――――→ +R OH(R 、R 、R 、R 均表示烃基)。
1 2 2 3 4 4 1 2 3 4
(1)A的核磁共振氢谱中有 组吸收峰;B的结构简式为
。
(2)C的化学名称为 ;D中所含官能团的名称为 。
(3)C→D所需的试剂和反应条件为 ;E→F的反应类型为
。
(4)F→M的化学方程式为
。
(5)同时满足下列条件的M的同分异构体有 种(不考虑立体异构)。
①五元环上连有2个取代基;
②能与NaHCO 溶液反应生成气体;
3
③能发生银镜反应。
(6)参照上述合成路线和信息,以 1-甲基环戊烯为原料(无机试剂任选),设计制备
的合成路线。
答案 (1)1
(2)1-氯环己烷 碳碳双键
(3)NaOH乙醇溶液、加热 酯化反应(或取代反应)
(4)
(5)6
(6)
解析 (5) M为 ,同时满足:①五元环上连有2个取代基;②能与NaHCO 溶
3
液反应生成气体,说明含有羧基;③能发生银镜反应,说明含有醛基,满足条件的 M的同
分异构体有 、 、 、 、 、 ,一共6种。
解答这类问题的关键是以已知一个或几个有机物为突破口,抓住特征条件(特殊性质或特征
反应,关系条件能告诉有机物间的联系,类别条件可给出物质的范围和类别)。再从突破口
向外发散,用正推和逆推、两边推中间相结合的方法,推出其他各有机物的结构简式,然后
结合设问分析相关物质的官能团、反应方程式及反应类型。
1.[2021·全国乙卷,36(2)(4)(5)(6)(7)]卤沙唑仑W是一种抗失眠药物,在医药工业中的一种
合成方法如下:
回答下列问题:
(2)写出反应③的化学方程式:
。
(4)反应④中,Y的结构简式为
。
(5)反应⑤的反应类型是
。
(6)C的同分异构体中,含有苯环并能发生银镜反应的化合物共有 种。
(7)写出W的结构简式:
。
答案 (2) + +NaOH――→ +NaCl+HO
2(4) (5)取代反应 (6)10 (7)
解析 (2)反应③为 与 在氯化锌和氢氧化钠的作用下,发生取代反应生成
。
(4)D为 ,E为 ,根据结构特点及反应特征,可推出Y为 。
(5)E 为 , F 为 , 根 据 结 构 特 点 , 可 知 与
发生取代反应生成F。
(6)C为 ,含有苯环且能发生银镜反应的同分异构体中含有醛基、碳氟键、碳氯键,
即苯环上含有三个不同的取代基,可能出现的结构有 、 、 、
、 、 、 、 、 ,故其同分异构体共有
10种。
2.[2021·全国甲卷,36(2)(4)(5)(6)(7)]近年来,以大豆素(化合物C)为主要成分的大豆异黄酮
及其衍生物,因其具有优良的生理活性而备受关注。大豆素的合成及其衍生化的一种工艺路
线如图:回答下列问题:
(2)1 mol D反应生成E至少需要 mol氢气。
(4)由E生成F的化学方程式为
。
(5)由G生成H分两步进行:反应1)是在酸催化下水与环氧化合物的加成反应,则反应2)的
反应类型为 。
(6)化合物B的同分异构体中能同时满足下列条件的有 (填字母)。
a.含苯环的醛、酮
b.不含过氧键(—O—O—)
c.核磁共振氢谱显示四组峰,且峰面积比为3∶2∶2∶1
A.2个 B.3个 C.4个 D.5个
(7)根据上述路线中的相关知识,以丙烯为主要原料用不超过三步的反应设计合成
。
答案 (2)2
(4) ――→ +HO
2
(5) 取 代 反 应 (6)C (7) ――→ ―――――――→ ――――→
解 析 (2)D 为 , 与 氢 气 发 生 加 成 反 应 生 成,碳碳双键及酮羰基都发生了加成反应,所以1 mol D反应生
成E至少需要2 mol氢气。
(5)由G生成H分两步进行:反应1)是在酸催化下水与环氧化合物的加成反应,则反应2)是
将酯基水解生成羟基,反应类型为取代反应。
(6)化合物B为 ,同分异构体中能同时满足下列条件:a.含苯环的醛、酮;
b.不含过氧键(—O—O—);c.核磁共振氢谱显示四组峰,且峰面积比为3∶2∶2∶1,说明为
醛或酮,而且含有甲基,根据要求可以写出: 、 、
、 ,故有4种。
课时精练
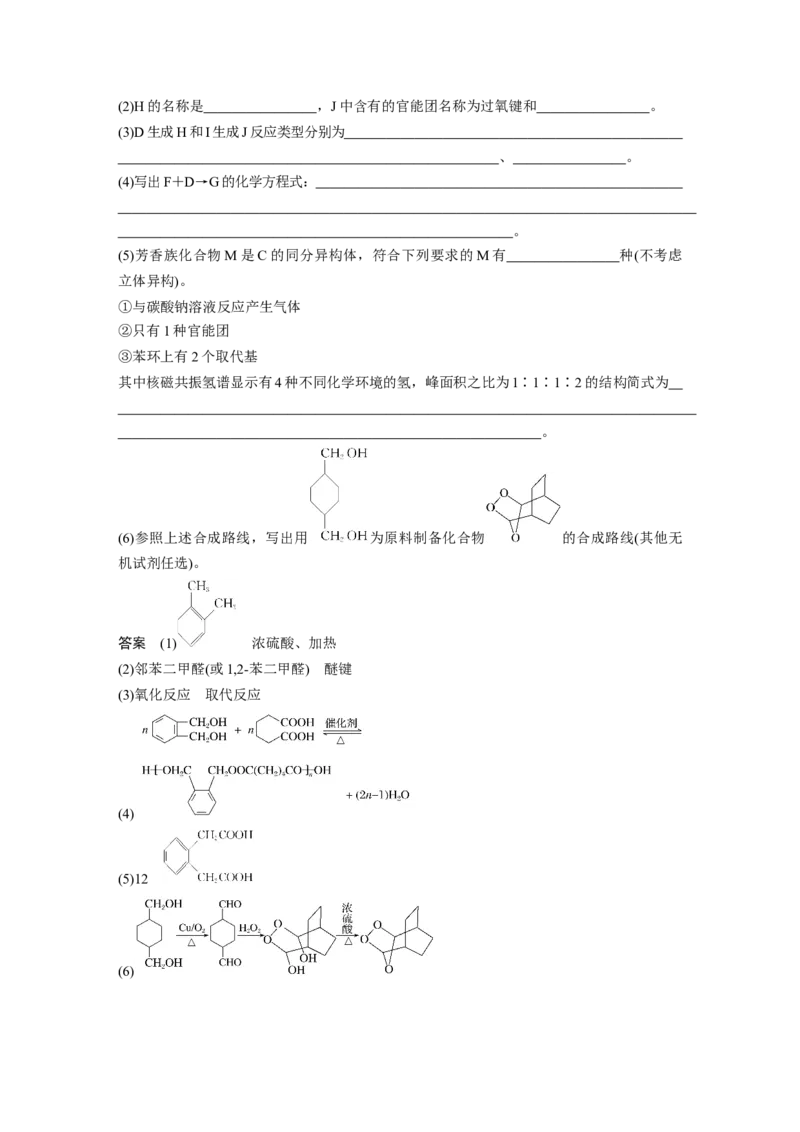
1.高聚物G是一种合成纤维,由A与E为原料制备J和G的一种合成路线如下:
已知:①酯能被LiAlH 还原为醇;
4
② 。
回答下列问题:
(1)A的结构简式为 ,B生成C的反应条件为 。(2)H的名称是 ,J中含有的官能团名称为过氧键和 。
(3)D生成H和I生成J反应类型分别为
、 。
(4)写出F+D→G的化学方程式:
。
(5)芳香族化合物M是C的同分异构体,符合下列要求的M有 种(不考虑
立体异构)。
①与碳酸钠溶液反应产生气体
②只有1种官能团
③苯环上有2个取代基
其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积之比为1∶1∶1∶2的结构简式为
。
(6)参照上述合成路线,写出用 为原料制备化合物 的合成路线(其他无
机试剂任选)。
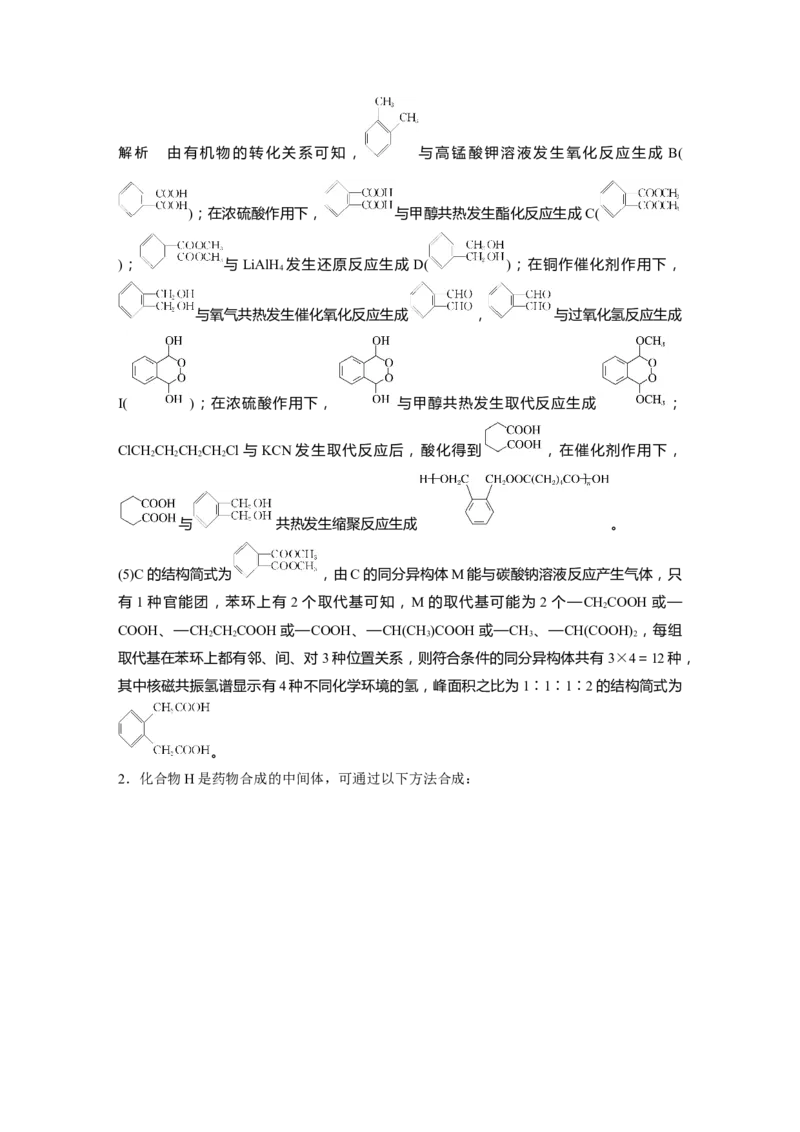
答案 (1) 浓硫酸、加热
(2)邻苯二甲醛(或1,2-苯二甲醛) 醚键
(3)氧化反应 取代反应
(4)
(5)12
(6)解析 由有机物的转化关系可知, 与高锰酸钾溶液发生氧化反应生成 B(
);在浓硫酸作用下, 与甲醇共热发生酯化反应生成C(
); 与 LiAlH 发生还原反应生成 D( );在铜作催化剂作用下,
4
与氧气共热发生催化氧化反应生成 , 与过氧化氢反应生成
I( );在浓硫酸作用下, 与甲醇共热发生取代反应生成 ;
ClCH CHCHCHCl 与 KCN 发生取代反应后,酸化得到 ,在催化剂作用下,
2 2 2 2
与 共热发生缩聚反应生成 。
(5)C的结构简式为 ,由C的同分异构体M能与碳酸钠溶液反应产生气体,只
有 1 种官能团,苯环上有 2 个取代基可知,M 的取代基可能为 2 个—CHCOOH 或—
2
COOH、—CHCHCOOH或—COOH、—CH(CH )COOH或—CH 、—CH(COOH) ,每组
2 2 3 3 2
取代基在苯环上都有邻、间、对3种位置关系,则符合条件的同分异构体共有 3×4=12种,
其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积之比为1∶1∶1∶2的结构简式为
。
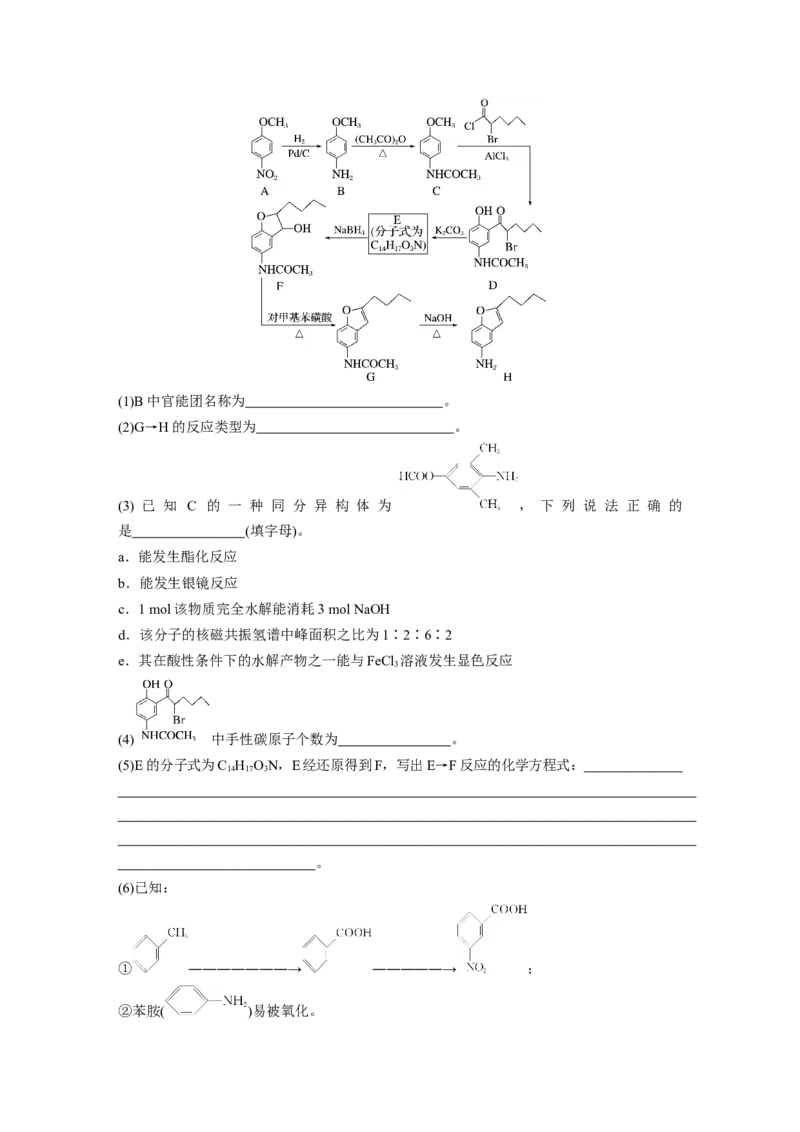
2.化合物H是药物合成的中间体,可通过以下方法合成:(1)B中官能团名称为 。
(2)G→H的反应类型为 。
(3) 已 知 C 的 一 种 同 分 异 构 体 为 , 下 列 说 法 正 确 的
是 (填字母)。
a.能发生酯化反应
b.能发生银镜反应
c.1 mol该物质完全水解能消耗3 mol NaOH
d.该分子的核磁共振氢谱中峰面积之比为1∶2∶6∶2
e.其在酸性条件下的水解产物之一能与FeCl 溶液发生显色反应
3
(4) 中手性碳原子个数为 。
(5)E的分子式为C H ON,E经还原得到F,写出E→F反应的化学方程式:
14 17 3
。
(6)已知:
① ―――――――→ ―――――→ ;
②苯胺( )易被氧化。请以甲苯和(CHCO) O为原料制备 ,写出制备的合成路线流程图(无机试剂任
3 2
选)。
答案 (1)醚键、氨基 (2)水解反应 (3)bde (4)1
(5)
(6) ――――→ ――→ ―――――→ ――――――→
解析 (3)已知C的一种同分异构体为 不含羧基也不含羟基,不能发生酯
化反应,a错误;分子结构中左边HCOO—能发生银镜反应,b正确;酯基水解消耗1 mol
NaOH,水解后的产物有酚羟基,再消耗1 mol NaOH,故1 mol该物质完全水解能消耗2
mol NaOH,c错误;该物质水解后得到1个酚羟基,可以和FeCl 溶液发生显色反应,e正
3
确。
(5)E的分子式为C H ON,F的分子式为C H ON,E的分子式比F少2个H,且E经还
14 17 3 14 19 3
原得到 F,所以 E 的结构简式为 ,E 和氢气反应生成 F,化学方程式为
。
3.苯并环己酮是合成萘( )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一
种路线如图所示:已知:
回答下列问题:
(1)萘环上的碳原子的编号如(a)式,根据系统命名法,(b)式可称为2-硝基萘,则化合物(c)的
名称应是 。
(2)有机物 含有的官能团是 (填名称),X 的结构简式
是 。
(3)步骤Ⅲ的反应类型是 ,步骤Ⅳ的反应类型是 。
(4)反应Ⅱ的化学方程式是
。
(5)1-乙基萘的同分异构体中,属于萘的取代物的有 种(不含1-乙基萘)。W
也是1-乙基萘的同分异构体,它是含一种官能团的苯的取代物,核磁共振氢谱显示W有3
种不同化学环境的氢,峰面积之比为1∶1∶2,W的结构简式为
。
(6)写出用CHCOCH 和CHMgBr为原料制备 的合成路线(其他试剂任选)。
3 3 3
答案 (1)1,6-二甲基萘 (2)碳碳双键、碳溴键 C HMgBr (3)取代反应 消去反应
2 5
(4)
(5)11(6)
解析 (1)根据萘环上的碳原子的编号可知,甲基分别取代了1号和6号碳上的氢原子,所以
化合物(c)的名称是1,6-二甲基萘。
(2)有机物 含有的官能团是碳碳双键和碳溴键;通过分析知,X为C HMgBr。
2 5
(4)Y 为 , 反 应 Ⅱ 为 醇 的 消 去 反 应 , 则 反 应 Ⅱ 的 化 学 方 程 式 是
。
(5)属于萘的取代物的同分异构体如果有一个取代基,为乙基,有2个位置(包含1-乙基萘),
如果有2个取代基,为2个甲基,可以处于同一苯环上,确定一个甲基位置,另外甲基位置
如图所示: , 有4种,若处于不同苯环上,确定一个甲基位置,另外甲
基位置如图所示: , ,有6种,不包括1-乙基萘,符合条件的同分异
构体有2+4+6-1=11种;W也是1-乙基萘的同分异构体,它是含一种官能团的苯的取代
物,则含有3个碳碳双键,核磁共振氢谱显示W有三种不同化学环境的氢原子,具有高对
称性,且个数比为 1∶1∶2,含有 3 个—CH==CH 且处于间位,其结构简式为
2
。
(6)以CHCOCH 、CHMgBr为原料合成 , 可由CH==C(CH)
3 3 3 2 3 2
和溴发生加成反应得到,CH==C(CH) 可由(CH)COH发生消去反应得到,(CH)COH可
2 3 2 3 3 3 3
由CHCOCH 、CHMgBr反应得到,合成路线见答案。
3 3 34.阿司匹林 是一种用途很广的消炎镇痛药物。可以通过以下方法合成:
已知:
3CHCOOH+PCl ―→3CHCOCl+HPO
3 3 3 3 3
请回答下列问题:
(1)阿司匹林中的含氧官能团有 (写名称),反应①的反应类型为
。
(2)通过水杨酸还可制得香料E和高分子化合物G:
①请写出A→E反应的化学方程式:
。
②已知G是一种聚酯,请写出其结构简式:
。
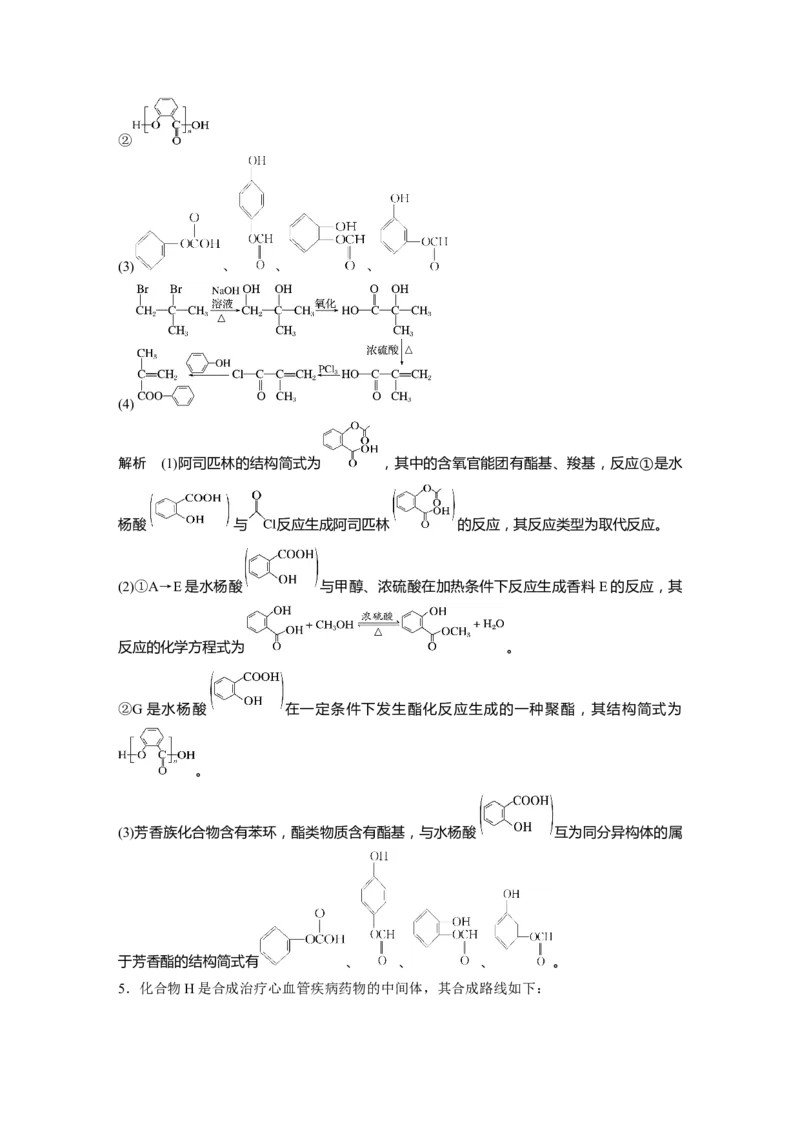
(3)写出水杨酸所有属于芳香酯的同分异构体的结构简式:
。
(4)结合题中信息,以苯酚、异丁烯为原料(其他无机原料自选)合成聚合物 的
流程路线如下:
请完善合成流程省略部分。
答案 (1)酯基、羧基 取代反应
(2)①②
(3) 、 、 、
(4)
解析 (1)阿司匹林的结构简式为 ,其中的含氧官能团有酯基、羧基,反应①是水
杨酸 与 反应生成阿司匹林 的反应,其反应类型为取代反应。
(2)①A→E是水杨酸 与甲醇、浓硫酸在加热条件下反应生成香料E的反应,其
反应的化学方程式为 。
②G是水杨酸 在一定条件下发生酯化反应生成的一种聚酯,其结构简式为
。
(3)芳香族化合物含有苯环,酯类物质含有酯基,与水杨酸 互为同分异构体的属
于芳香酯的结构简式有 、 、 、 。
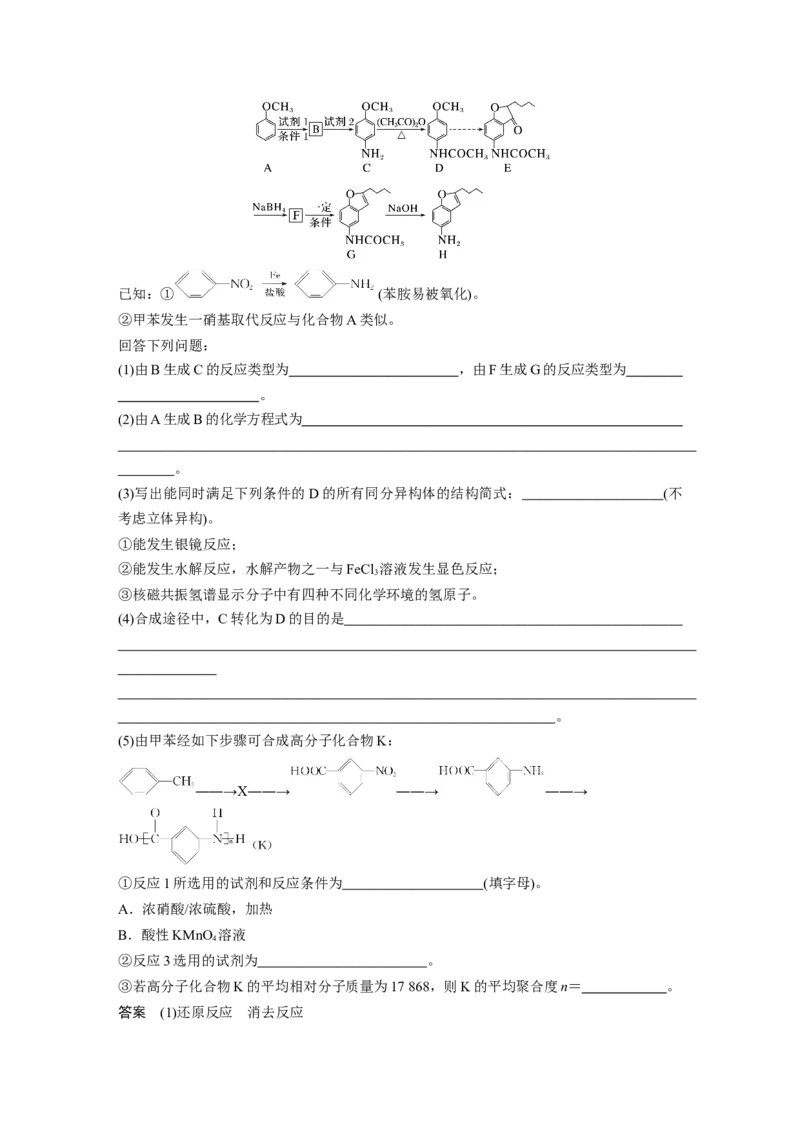
5.化合物H是合成治疗心血管疾病药物的中间体,其合成路线如下:已知:① (苯胺易被氧化)。
②甲苯发生一硝基取代反应与化合物A类似。
回答下列问题:
(1)由B生成C的反应类型为 ,由F生成G的反应类型为
。
(2)由A生成B的化学方程式为
。
(3)写出能同时满足下列条件的D的所有同分异构体的结构简式: (不
考虑立体异构)。
①能发生银镜反应;
②能发生水解反应,水解产物之一与FeCl 溶液发生显色反应;
3
③核磁共振氢谱显示分子中有四种不同化学环境的氢原子。
(4)合成途径中,C转化为D的目的是
。
(5)由甲苯经如下步骤可合成高分子化合物K:
――→X――→ ――→ ――→
①反应1所选用的试剂和反应条件为 (填字母)。
A.浓硝酸/浓硫酸,加热
B.酸性KMnO 溶液
4
②反应3选用的试剂为 。
③若高分子化合物K的平均相对分子质量为17 868,则K的平均聚合度n= 。
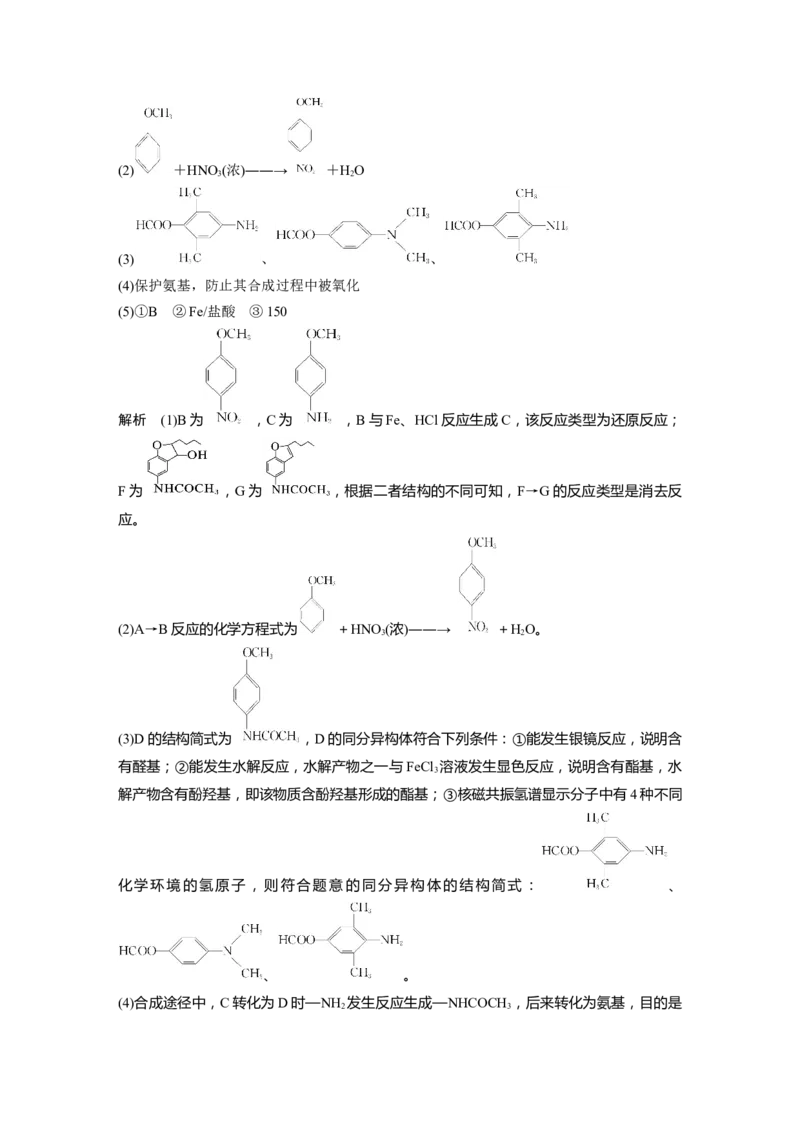
答案 (1)还原反应 消去反应(2) +HNO(浓)――→ +HO
3 2
(3) 、 、
(4)保护氨基,防止其合成过程中被氧化
(5)①B ②Fe/盐酸 ③150
解析 (1)B为 ,C为 ,B与Fe、HCl反应生成C,该反应类型为还原反应;
F为 ,G为 ,根据二者结构的不同可知,F→G的反应类型是消去反
应。
(2)A→B反应的化学方程式为 +HNO(浓)――→ +HO。
3 2
(3)D的结构简式为 ,D的同分异构体符合下列条件:①能发生银镜反应,说明含
有醛基;②能发生水解反应,水解产物之一与FeCl 溶液发生显色反应,说明含有酯基,水
3
解产物含有酚羟基,即该物质含酚羟基形成的酯基;③核磁共振氢谱显示分子中有4种不同
化学环境的氢原子,则符合题意的同分异构体的结构简式: 、
、 。
(4)合成途径中,C转化为D时—NH 发生反应生成—NHCOCH ,后来转化为氨基,目的是
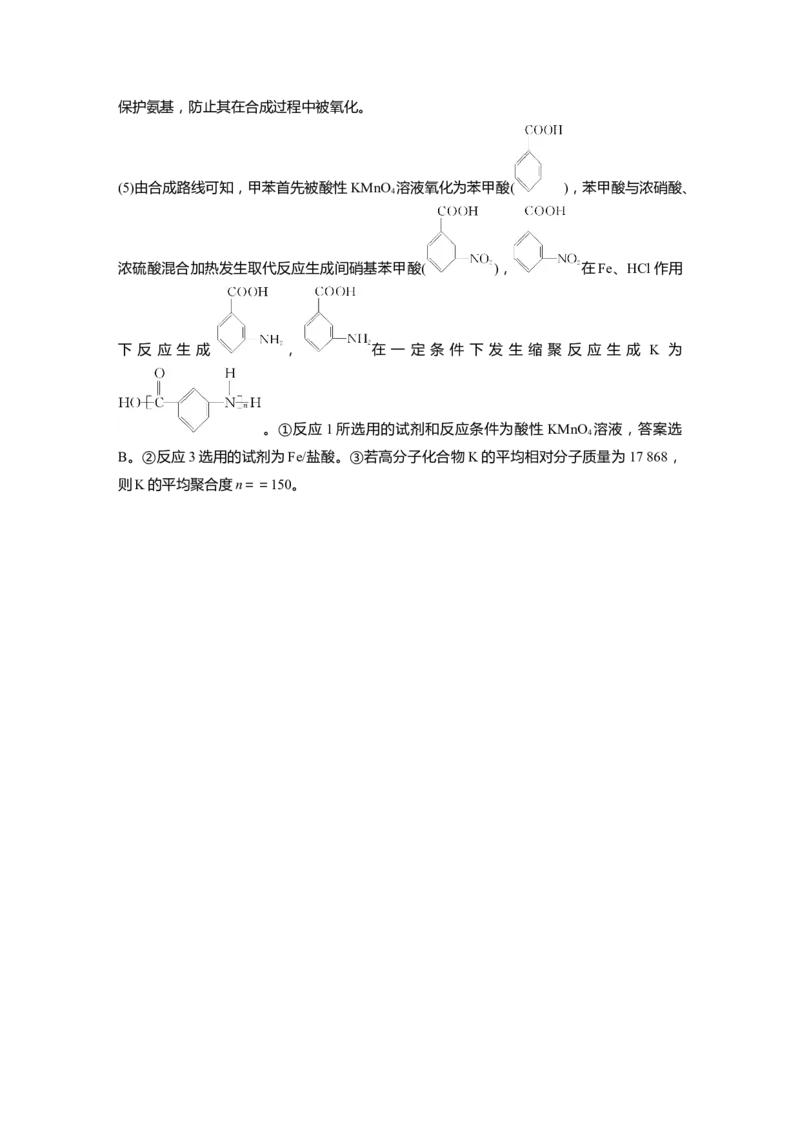
2 3保护氨基,防止其在合成过程中被氧化。
(5)由合成路线可知,甲苯首先被酸性KMnO 溶液氧化为苯甲酸( ),苯甲酸与浓硝酸、
4
浓硫酸混合加热发生取代反应生成间硝基苯甲酸( ), 在Fe、HCl作用
下 反 应 生 成 , 在 一 定 条 件 下 发 生 缩 聚 反 应 生 成 K 为
。①反应1所选用的试剂和反应条件为酸性 KMnO 溶液,答案选
4
B。②反应3选用的试剂为Fe/盐酸。③若高分子化合物K的平均相对分子质量为17 868,
则K的平均聚合度n==150。