文档内容
1.下列是我国古代常见的操作方法,其中加点部分的操作原理与化学实验中的分离除杂方
法的原理相似的是( )
① ② ③ ④
凡煮汤,欲微火, 海陆取卤,日晒火
经月而出蒸烤之…… 凡渍药酒,皆须细
令小沸……箅渣取
煎,煮海熬波,卤水
终乃得酒可饮 切……便可漉出
液 成盐
A.过滤、蒸馏、萃取、蒸发
B.过滤、蒸发、萃取、蒸馏
C.蒸发、萃取、蒸馏、过滤
D.萃取、蒸馏、过滤、蒸发
2.(2023·海口市模拟)《天工开物——作咸篇》有如下记载:“潮波浅被地,不用灰压。候
潮一过,明日天晴,半日晒出盐霜,疾趋扫起煎炼。”下列说法正确的是( )
A.“煎炼”所得物质俗称“烧碱”
B.“作咸”过程涉及“蒸馏”操作
C.“作咸”在实验室完成会用到蒸发皿、酒精灯
D.该记载过程中涉及氧化还原反应
3.下列气体去除杂质的方法中,不能实现其目的的是( )
气体(杂质) 方法
A SO (H S) 通过酸性高锰酸钾溶液
2 2
B Cl(HCl) 通过饱和的食盐水
2
C N(O ) 通过灼热的铜丝网
2 2
D NO(NO ) 通过氢氧化钠溶液
2
4.下列各物质含少量杂质,除去这些杂质选用的试剂或操作方法正确的是( )
序号 物质 杂质 选用的试剂或操作方法
① KNO 溶液 KOH 加入FeCl 溶液,并过滤
3 3
② FeSO 溶液 CuSO 加入过量铁粉,并过滤
4 4
③ H 2 CO 2 通过盛NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶
④ NaNO 固体 CaCO 溶解、过滤、蒸发
3 3
A.①②③④ B.①③④
C.②③④ D.①②③
5.下列叙述正确的是( )
A.用装置Ⅰ分离乙酸乙酯与饱和碳酸钠溶液
B.用装置Ⅱ蒸干硫酸亚铁溶液制备FeSO ·7H O
4 2
C.用装置Ⅲ将硫酸铜溶液蒸发浓缩、冷却结晶,得到胆矾晶体
D.用装置Ⅳ分离Cl 与KI溶液反应生成的碘
2
6.在从碘水中萃取碘的实验中,下列说法正确的是( )
A.萃取剂要求不溶于水,且比水更容易使碘溶解
B.注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.实验室如果没有四氯化碳,可以用酒精代替
7.(2018·海南,7)下列分离方法正确的是( )
A.回收水溶液中的I:加入乙醇,分液、蒸发
2
B.回收含有KCl的MnO :加水溶解,过滤、干燥
2
C.除去氨气中的水蒸气:通过盛有PO 的干燥管
2 5
D.除去乙醇中的水:加入无水氯化钙,蒸馏
8.某溶液含有较多的NaSO 和少量的Fe (SO ) 。若用该溶液制取芒硝(Na SO ·10H O),可
2 4 2 4 3 2 4 2
供选择的操作有:①加适量HSO 溶液,②加金属Na,③结晶,④加过量NaOH溶液,⑤
2 4
加强热脱结晶水,⑥过滤。正确的操作步骤是( )
A.②⑥③ B.④⑥①③
C.④⑥③⑤ D.②⑥①③⑤
9.(2023·郑州高三模拟)下列实验不能达到实验目的的是( )
选项 实验 实验目的
A 将含有HCl杂质的CO 通入饱和NaCO 溶液中 除去CO 中的HCl
2 2 3 2
将一定量的KNO 和NaCl的混合液加热并浓缩
3
B 分离出NaCl晶体
至有晶体析出,趁热过滤
C 将含有少量HCl、HO(g)的H 通过盛有碱石灰 除去H 中少量的HCl、
2 2 2的干燥管 HO(g)
2
将含有少量HO(g)的NH 通过盛有碱石灰的干
2 3
D 除去NH 中的HO(g)
3 2
燥管
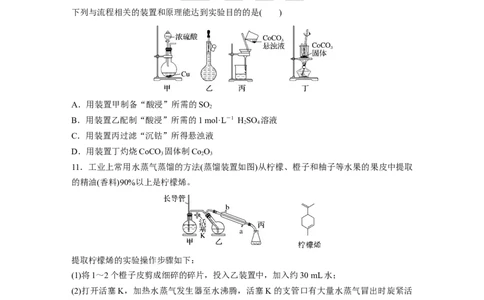
10.(2023·宁德高三模拟)以含钴废渣(主要成分为CoO、Co O,还含有Al O、ZnO等杂质)为
2 3 2 3
原料制备Co O 的实验流程如下。
2 3
下列与流程相关的装置和原理能达到实验目的的是( )
A.用装置甲制备“酸浸”所需的SO
2
B.用装置乙配制“酸浸”所需的1 mol·L-1 HSO 溶液
2 4
C.用装置丙过滤“沉钴”所得悬浊液
D.用装置丁灼烧CoCO 固体制Co O
3 2 3
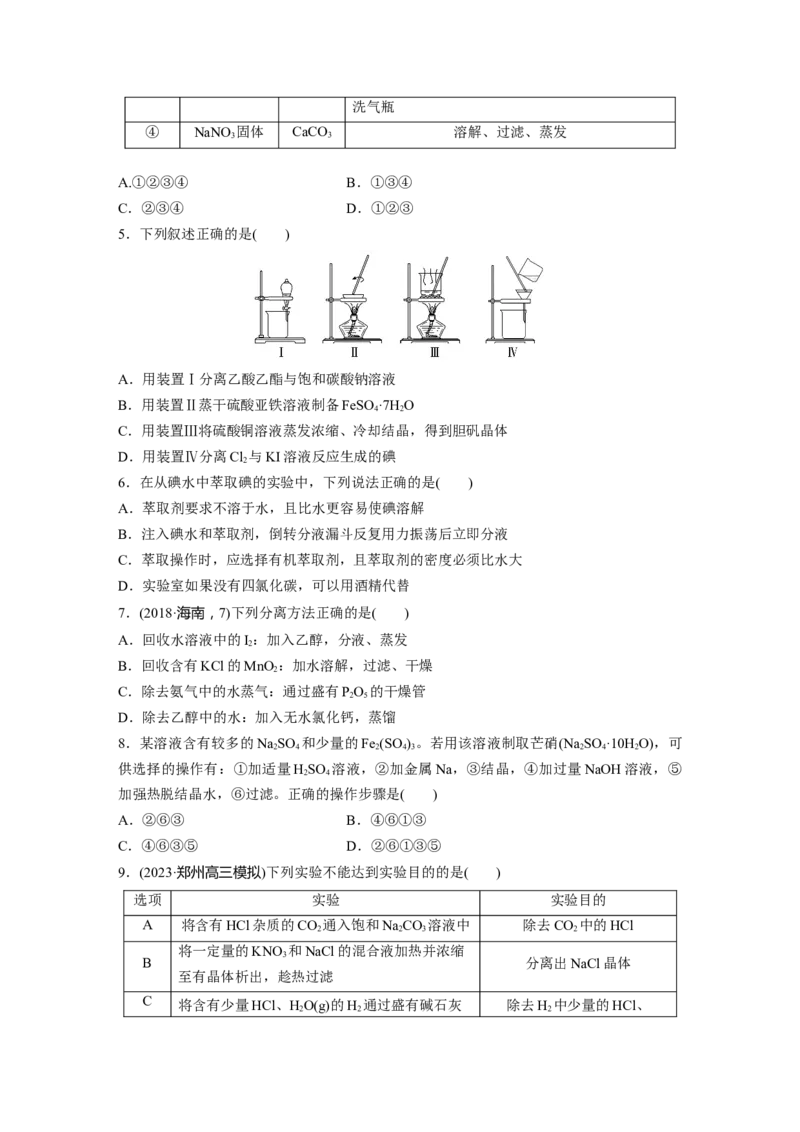
11.工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从柠檬、橙子和柚子等水果的果皮中提取
的精油(香料)90%以上是柠檬烯。
提取柠檬烯的实验操作步骤如下:
(1)将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水;
(2)打开活塞K,加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧活
塞K,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是( )
A.当馏出液无明显油珠、澄清透明时,说明蒸馏完成
B.蒸馏结束后,为防止倒吸,立即停止加热
C.长导管作安全管,能平衡气压,防止由于导管堵塞引起爆炸
D.要得到纯精油,还需要进行萃取、分液、蒸馏操作
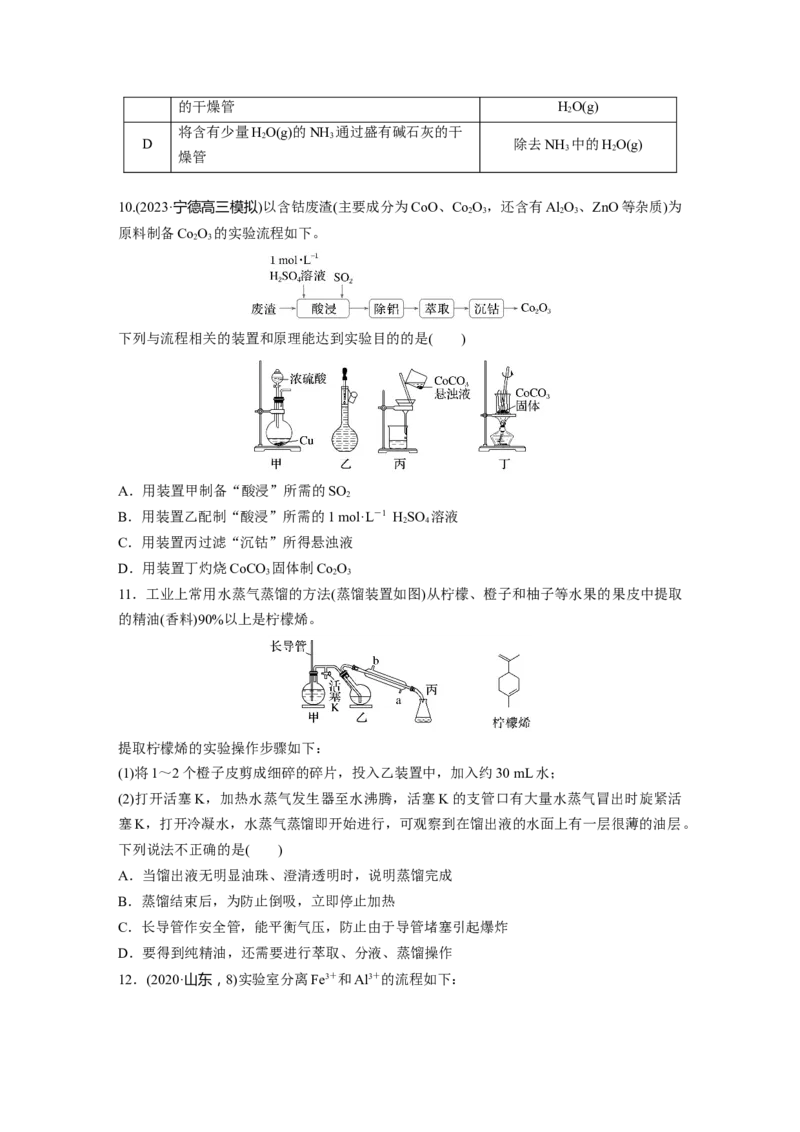
12.(2020·山东,8)实验室分离Fe3+和Al3+的流程如下:已知Fe3+在浓盐酸中生成黄色配离子[FeCl ]-,该配离子在乙醚(Et O,沸点34.5 ℃)中生成
4 2
缔合物EtO·H+·[FeCl ]-。下列说法错误的是( )
2 4
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
13.二草酸合铜(Ⅱ)酸钾晶体{K [Cu(C O)]·2H O}制备流程如下:
2 2 4 2 2
(已知:HC O=====CO↑+CO↑+HO)
2 2 4 2 2
制备CuO:CuSO 溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤。
4
(1)用双层滤纸过滤的原因是______________________________________________________
______________________________________________________________________________。
(2)用蒸馏水洗涤氧化铜时,如何证明氧化铜已洗涤干净:____________________________。
14.某工厂排放的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO。某研
究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br),他们设计了如下流程图。
2
已知加入试剂a后废液中发生的反应的化学方程式是Cl +2KBr===2KCl+Br 。试剂b需要
2 2
从以下试剂中选择:①饱和NaCO 溶液、②饱和KCO 溶液、③KOH溶液、④BaCl 溶液、
2 3 2 3 2
⑤Ba(NO ) 溶液、⑥稀盐酸。请根据以上流程,回答下列问题:
3 2
(1)操作①②③④⑤的名称依次是____________(填字母)。
A.萃取、过滤、分液、过滤、蒸发结晶
B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶
D.萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+、Mg2+、SO,选出试剂b所代表的试剂,按滴加顺序依次是
______________________________________________________________________(填序号)。(3)调至pH=7发生反应的化学方程式为___________________________________________
______________________________________________________________________________。
(4)检测SO已沉淀完全的实验方法为_____________________________________________
______________________________________________________________________________。