文档内容
INCLUDEPICTURE "F:\\方正文件\\2019 文
件\\课件\\2020 版 创新设计 高考总复习
化 学 人 教 版 \\ 第 三 章 .tif" \*
MERGEFORMATINET
第1讲 钠及其化合物
【2020·备考】
最新考纲:1.了解钠及其重要化合物的制备方法。2.掌握钠及其重要化合物的主要
性质。3.掌握钠及其重要化合物的应用。
核心素养:1.宏观辨识与微观探析:认识物质的多样性,能从钠元素的原子结构认
识钠的性质,理解“结构决定性质”的内涵。2.科学探究与创新意识:能发现和提
出有探究价值的有关钠及其化合物性质的探究方案,进行实验探究。考点一 钠的主要性质及其应用
(频数:★☆☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查钠的重要性质,特别是钠与盐溶液的反应要重点掌握,另外钠的用
途及保存也常在考题中出现,要引起关注 。
1.钠的物理性质
颜色 密度 熔点 硬度
银白色,有 ρ(水)大于 ρ(钠)
小于 100 ℃ 质地柔软
金属光泽 大于 ρ(煤油)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
钠的质地柔软,取用钠进行有关反应时,可以用小刀切割除去氧化膜。
2.从钠原子的原子结构认识钠的化学性质——还原性
(1)与非金属单质(如O 、Cl )的反应
2 2
O
2
Cl : 2Na + Cl INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新
2 2
设计 高考总复习 化学 人教版 \ \ 反应点燃 .TIF" \* MERGEFORMATINET
2NaCl
(2)与水反应①离子方程式: 2Na + 2H O == =2Na + + 2OH - + H ↑。
2 2
②与滴加酚酞的水反应的现象及解释
(3)与盐酸反应
离子方程式: 2Na + 2H + == =2Na + + H ↑。
2
(4)钠与盐反应
①钠与盐溶液反应
如 Na 投入 CuSO 溶液中,反应的离子方程式为 2Na + 2H O + Cu 2 + == =2Na + +
4 2
Cu(OH) ↓ + H ↑。
2 2
②钠与熔融盐反应:
4Na+TiCl =====Ti+4NaCl
4
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.钠与酸及能显酸性的金属盐溶液反应时,由于溶液中H+浓度较大,最后钠可能
在液面上燃烧。
2.钠与盐的饱和溶液反应时,由于溶剂H O减少,盐溶液中会有晶体析出。
2
3.钠的制取、保存及用途
(1)制取:化学方程式为 2NaCl( 熔融 ) ===== 2Na + Cl ↑。
2
(2)保存:密封保存,通常保存在石蜡油或煤油中。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
因为CCl 的密度比钠的大,钠不能保存在 CCl 中,另外常考的试剂保存还有:
4 4NaOH溶液(用橡胶塞)、氯水、浓硝酸(棕色试剂瓶、玻璃塞)、氢氟酸(塑料瓶)等。
(3)用途:
①钠、钾合金(液态)可用于原子反应堆的导热剂;
②金属钠还可用于钛、锆、铌、钽等金属的冶炼;
③用作电光源,制作高压钠灯。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
用金属钠冶炼金属时,是钠与熔融盐反应,不能与水溶液反应,如:
4Na+TiCl =====4NaCl+Ti;
4
Na+KCl=====NaCl+K↑(制取金属钾,因为钾的沸点比钠的低,使钾成为钾蒸气
而逸出)。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)烧碱、纯碱均属于碱,不能盛放在玻璃试剂瓶中(×)
(2)在氧气中加热时,金属钠剧烈燃烧,生成淡黄色的固体Na O (√)
2 2
(3)金属钠在石棉网上加热时,先熔化成银白色小球,然后剧烈燃烧,产生黄色火焰
(√)
(4)金属钠着火时,可用泡沫灭火器或干燥的沙土灭火(×)
(5)钠与水反应的离子方程式为2Na+2H O===2Na++2OH-+H ↑(√)
2 2
(6)实验完毕后剩余的金属钠不能随意丢弃,应放回原试剂瓶(√)
2.(教材改编题)取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是
________(填序号)。
①金属先熔化 ②在空气中燃烧,放出黄色火花 ③燃烧后得白色固体 ④燃烧
时火焰为黄色 ⑤燃烧后生成淡黄色固体物质
答案 ①④⑤(1)填写空白;
(2)属于物理变化的有________(填序号),属于化学变化的有________(填序号)。
答案 (1)Na O NaOH 溶液 Na CO
2 2 3
(2)③ ①②④⑤
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·郑州模拟)下列叙述中不正确的是( )
A.钠在反应TiCl +4Na Ti+4NaCl中作还原剂
4
B.用镊子从煤油中取出金属钠,切下绿豆粒大小的钠,小心放入装满水的烧杯中,
观察钠与水反应的现象
C.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,观察到火焰呈黄色, 一定含
有Na+,可能含有K+
D.金属Na表面自然形成的氧化层不能保护内层金属不被空气氧化
解析 钠与TiCl 反应作还原剂,A正确;应将钠表面的煤油用滤纸吸干且烧杯中
4
不能装满水(否则会迸溅出液体),B错误;钠元素的焰色为黄色,而钾元素的焰色
为紫色,而且黄色会掩盖紫色,所以不能判断是否含有钾元素,C正确;金属Na表
面自然形成的氧化层不能保护内层金属不被空气氧化,D正确。
答案 B
2.将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是()
①MgSO 溶液 ②Na SO 稀溶液 ③饱和澄清石灰水
4 2 4
④Ca(HCO ) 溶液 ⑤CuSO 溶液 ⑥饱和NaCl溶液
3 2 4
A.①④⑤⑥ B.③④⑤⑥
C.②④⑤⑥ D.①③④⑥
解析 2Na+2H O===2NaOH+H ↑,①中Mg2++2OH-===Mg(OH) ↓;③中反
2 2 2
应消耗水,溶液温度升高,Ca(OH) 的溶解度降低,析出Ca(OH) 沉淀;④中Ca2++
2 2
HCO+OH-===CaCO ↓+H O;⑤生成的Cu(OH) 是蓝色沉淀,不符合题意;⑥水
3 2 2
减少,c(Na+)增大,使NaCl(s) Na+(aq)+Cl-(aq)平衡向左移动。
答案 D
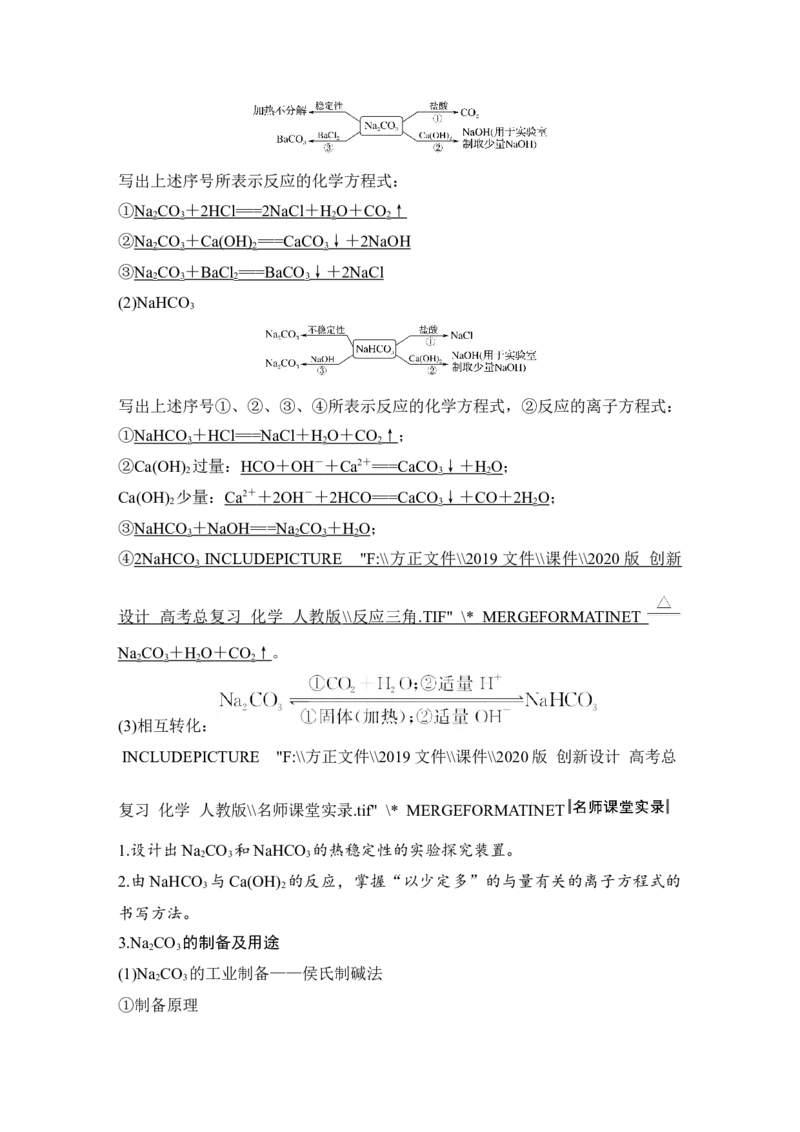
3.(2019·宁德联考)如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少
量无水CuSO 与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,据此
4
判断下列说法中不正确的是( )
A.上述反应是置换反应
B.上述反应说明钠比铜活泼
C.上述反应证明钠可以从CuSO 溶液中置换出铜
4
D.加热且无水条件下,Na可以与CuSO 反应并生成Cu
4
解析 实验在无水条件下进行,有红色物质生成,说明熔融的钠将硫酸铜中的铜
置换出来并且放出热量,属于置换反应,钠作还原剂,硫酸铜作氧化剂,说明钠比
铜活泼,故A、B项正确;若钠与CuSO 溶液混合,则钠先与水反应生成氢氧化钠,
4
氢氧化钠再与硫酸铜反应生成氢氧化铜,不会置换出铜单质,故C错误;根据以上
分析,在无水条件下,Na可以与CuSO 反应并生成Cu,故D正确。
4
答案 C【思维建模】
钠与盐溶液反应的思维模板
[微练] 写出下列反应的离子方程式
①将Na投入到Ca(HCO ) 溶液中,反应后生成正盐溶液
3 2
2Na + Ca 2 + + 2HCO == =CaCO ↓ + 2N a + + CO + H ↑。
3 2
②将Na投入到NH HCO 溶液中,有刺激性气味气体放出
4 3
2Na + NH + HCO == =2Na + + CO + NH ↑ + H ↑。
3 2
[B组 考试能力过关]
4. 下列说法正确的是( )
A.(2017·江苏化学,6A)钠与水反应:Na+2H O===Na++2OH-+H ↑
2 2
B.(2016·浙江理综,8A)钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
C.(2015·广东理综,10A)23 g Na与足量H O反应完全后可生成N 个H 分子
2 A 2
D.(2013·新课标全国Ⅱ,10B)钠与CuSO 溶液反应:2Na+Cu2+===Cu↓+2Na+
4
答案 B
5.(2018·海南化学,17)某小组在实验室中探究金属钠与二氧化碳的反应。回答下
列问题:
(1)选用如图所示装置及药品制取CO 。打开弹簧夹,制取CO 。为了得到干燥、纯
2 2
净的CO ,产生的气流应依次通过盛有________、________的洗气瓶(填试剂名称)。
2
反 应 结 束 后 , 关 闭 弹 簧 夹 , 可 观 察 到 的 现 象 是
____________________________________________________________________。
不能用稀硫酸代替稀盐酸,其原因是______________________________________。
(2)金属钠与二氧化碳反应的实验步骤及现象如下表:步骤 现象
将一小块金属钠在燃烧匙中点燃,迅速
产生大量白烟,集气瓶底部有黑色固体
伸入盛有CO 的集气瓶中。充分反应,
2 产生,瓶壁上有白色物质产生
放置冷却
在集气瓶中加入适量蒸馏水,振荡、过
滤纸上留下黑色固体,滤液为无色溶液
滤
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于 2支试管中,向一支试管
中滴加1滴酚酞溶液,溶液变红,加过量CaCl 红色褪去:向第二支试管中滴加澄
2
清石灰水,溶液变浑浊。据此推断,白色物质的主要成分是________(填标号)。
A.Na O B.Na O
2 2 2
C.NaOH D.Na CO
2 3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此
推断黑色固体是________。
③ 本 实 验 中 金 属 钠 与 二 氧 化 碳 反 应 的 化 学 方 程 式 为
____________________________________________________________________。
答案 (1)饱和碳酸氢钠溶液 浓硫酸 产生的气体使干燥管内盐酸液面下降,与
碳酸钙脱离接触,反应停止 生成的硫酸钙覆盖在碳酸钙表面,阻止反应进一步
进行
(2)①D
②碳(C)
③4Na+3CO =====2Na CO +C
2 2 3考点二 氧化钠、过氧化钠
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查过氧化钠的性质,特别是过氧化钠与CO 和H O的定性和定量分析
2 2
另外过氧化钠与其他水溶液的反应,以及过氧化钠的用途也常在考题中出现,要
引起注意 。
1.氧化钠和过氧化钠的比较
物质 氧化钠(Na O) 过氧化钠(Na O )
2 2 2
色态 白色固体 淡黄色固体
类别 碱性氧化物 过氧化物(非碱性氧化物)
氧的价态 - 2 - 1
电子式
生成条件 常温 加热或点燃
不稳定 (2N a O + O
2 2
INCLUDEPICTURE "F:\\ 方正
文件 \\201 9 文件 \ \ 课件 \\202 0 版
热稳
创新设计 高考总复习 化学 人 稳定
化 定性 教版 \ \ 反应三角 .TIF " \ *
学
MERGEFORMATINET
性 2Na 2 O 2 )
质 与水反应 Na O + H O == =2NaOH 2Na 2 O 2 + 2H 2 O == =4NaOH
2 2 + O ↑
2
2Na O + 2CO == =
2 2 2
与CO 反应 Na O + CO == =Na CO
2 2 2 2 3
2Na CO + O
2 3 2
与酸反应 Na O + 2HCl == =2NaCl + H O 2Na O +4HCl===
2 2 2 2(盐酸) 4NaCl+2H O+O ↑
2 2
主要性质 具有碱性氧化物通性 具有强氧化性
强氧化剂、漂白剂、供氧
主要用途 用于制取少量Na O 、烧碱
2 2 剂、消毒剂
2.Na O 的强氧化性与还原性
2 2
从元素化合价角度分析Na O 的性质
2 2
(1)强氧化性的五个表现
(2)遇KMnO 等强氧化剂时,表现出还原性,氧化产物为O 。
4 2
(3)遇CO 、H O、H+则发生自身的氧化还原反应。
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.Na O 的电子式为 ,晶体中阴、阳离子个数比为
2 2
1∶2而不是1∶1。
2.Na O 具有强氧化性,但Na O 与水、CO 反应时,水中的氢与CO 中的碳都处于
2 2 2 2 2 2
最高价态,不能被氧化,反应为Na O 自身的氧化还原反应。
2 2
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)1 mol Na O 固体中含离子总数为4N (×)
2 2 A
(2)7.8 g过氧化钠含有的共用电子对数为0.2N (×)
A(3)Na O 在与CO 的反应中既是氧化剂,又是还原剂(√)
2 2 2
(4)将足量过氧化钠投入紫色石蕊溶液中,溶液先变蓝色后褪色,同时有气泡产生
(√)
(5)Na O 在潮湿的空气中放置一段时间,变成白色粘稠物的原因是 2Na O +
2 2 2 2
2CO ===2Na CO +O (×)
2 2 3 2
2.(教材改编题)[RJ必修1·P “实验3-5”改编]下列对过氧化钠的叙述中,正确
55
的是( )
A.过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
B.过氧化钠能与水反应,所以过氧化钠可以作气体的干燥剂
C.过氧化钠与二氧化碳反应产生氧气,故可用于呼吸面具中
D.过氧化钠与二氧化碳反应时,过氧化钠只作氧化剂
答案 C
3.(思维探究题)比较下列四组反应,回答下列问题。
一组:①Na O +CO ②Na O +SO
2 2 2 2 2 2
二组:③Na O +FeCl (溶液) ④Na O +FeCl (溶液)
2 2 3 2 2 2
三组:⑤NaOH溶液滴入紫色石蕊试液中 ⑥Na O 固体加入到紫色石蕊试液中
2 2
问题:(1)写出①、②两反应的化学方程式。
(2)判断③、④反应中可能发生的现象,为什么?
(3)判断⑤、⑥反应中可能发生的现象?
答案 (1)①2Na O +2CO ===2Na CO +O
2 2 2 2 3 2
②Na O +SO ===Na SO
2 2 2 2 4
(2)③、④反应均会有红褐色沉淀生成并有气体放出。④中气体明显少于③中气体,
FeCl 与NaOH反应生成Fe(OH) ,Fe(OH) 是不溶性的红褐色沉淀;④中Fe2+具有
3 3 3
强还原性,易被Na O 氧化并生成Fe(OH) ,Na O 与溶液中的水剧烈反应会有O
2 2 3 2 2 2
产生。
(3)⑤溶液变蓝,⑥溶液先变蓝后褪色。原因是Na O 与H O反应生成NaOH,呈碱
2 2 2
性,同时Na O 又有漂白性。
2 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET[A组 基础知识巩固]
1.(2019·湖南联考)下列说法正确的是( )
A.Na O 遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
2 2
B.Na O 与CO 反应生成0.1 mol O 时转移电子0.2 mol
2 2 2 2
C.Na O 用于呼吸面具,活性炭用于防毒面具,两者原理相同
2 2
D.向饱和烧碱溶液中加入2 g Na O ,充分反应完后,溶液中c(Na+)不变
2 2
解析 Na O 遇到湿润的紫色石蕊试纸,它最终能氧化石蕊使其褪色,A项错误;
2 2
由2Na O +2CO ===2Na CO +O 及Na O 中氧元素的化合价为-1价知,每生成
2 2 2 2 3 2 2 2
1 mol O 时会转移2 mol 电子,B项正确;Na O 用于呼吸面具是能与水或CO 反
2 2 2 2
应产生O ,活性炭用于防毒面具是吸附有毒气体,C错误;Na O 与水反应时能放
2 2 2
出大量的热,使溶液温度升高,NaOH的溶解度增大,导致溶液中c(Na+)增大,D
项错误。
答案 B
2. 已 知 硫 酸 亚 铁 溶 液 中 加 入 Na O 时 发 生 反 应 : 4Fe2 + + 4Na O +
2 2 2 2
6H O===4Fe(OH) ↓+O ↑+8Na+。下列说法正确的是( )
2 3 2
A.该反应中氧化剂是Na O ,还原剂是FeSO
2 2 4
B.若Fe2+失去4 mol电子,生成氧气的体积约为22.4 L
C.4 mol Na O 参加反应,共得到6 mol电子
2 2
D.反应过程中可以看到白色沉淀先转化为灰绿色后转化为红褐色
解析 该反应中 Fe2+失电子作还原剂,Na O 中的氧元素既得电子又失电子,
2 2
Na O 既作氧化剂又作还原剂,A错误;未指明温度和压强,无法计算生成的氧气
2 2
的体积,B错误;该反应中转移6e-,且只有Na O 中的氧元素得电子,4 mol Na O
2 2 2 2
参加反应,共得到6 mol电子,C正确;反应过程中Fe2+直接被氧化生成Fe3+,形
成Fe(OH) 沉淀,反应过程中无Fe(OH) 生成,D错误。
3 2
答案 C
3.现有一定量含有Na O杂质的Na O 试样,用如图所示实验装置测定Na O 试样
2 2 2 2 2
的纯度。(可供选用的反应物只有CaCO 固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸
3
馏水)回答下列问题:
(1)装置A中液体试剂选用_________________________________________。
(2)装置B的作用是_________________________________________________,
装置E中碱石灰的作用是______________________________________________。
(3)装置D中发生反应的化学方程式为_________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状
况),则Na O 试样的纯度为________。
2 2
解析 (1)A是用来制取二氧化碳的装置,碳酸钙和硫酸反应时,生成的硫酸钙微
溶于水,会覆盖在碳酸钙的表面,使反应不能继续进行,所以用盐酸而不用硫酸来
反应,故装置A中液体试剂选用6 mol·L-1盐酸。
(2)碳酸钙和盐酸反应生成的二氧化碳中含有氯化氢气体,可用饱和碳酸氢钠溶液
来除去;装置E中碱石灰的作用是吸收二氧化碳,防止二氧化碳对氧气的体积测
量造成干扰。
(3)装置D中含有氧化钠和过氧化钠,CO 分别与它们发生反应。
2
(4)根据反应 2Na O +2CO ===2Na CO +O ,反应结束后测得气体体积为 224
2 2 2 2 3 2
mL(标准状况),即生成的氧气的物质的量为=0.01 mol,则过氧化钠的物质的量为
0.02 mol,故试样中过氧化钠的纯度为×100%=78%。
答案 (1)6 mol·L-1盐酸
(2)除去气体中的HCl 吸收装置D中反应剩余的CO
2
(3)2Na O +2CO ===2Na CO +O 、Na O+CO ===Na CO
2 2 2 2 3 2 2 2 2 3
(4)78%
【练后归纳】
Na O 与H O、CO 反应的定量关系
2 2 2 2
当Na O 与CO 、H O反应时,物质的量关系为2Na O ~O ~
电子转移关系 2 2 2 2 2 2 2
2e-,n(e-)=n(Na O )=2n(O )
2 2 2
若CO 、水蒸气(或两混合气体)通过足量Na O ,气体体积的
气体体积变化关系 2 2 2
减少量是原来气体体积的,等于生成氧气的量,ΔV=V(O )=
2V
CO 、水蒸气分别与足量Na O 反应时,固体相当于吸收了
2 2 2
CO 中的“CO”、水蒸气中的“H ”,所以固体增加的质量
固体质量变化关系 2 2
Δm(CO )=28 g·mol-1×n(CO ),Δm(H O)=2 g·mol-
2 2 2
1×n(H O)
2
[B组 考试能力过关]
4.判断正误(正确的打“√”,错误的打“×”)。
(1)(2018·海南化学,5A)Na O 可与CO 反应放出氧气,可用于制作呼吸面具(√)
2 2 2
(2)(2017·北京理综,8A)二氧化碳使Na O 固体变白,二氧化碳气体被还原(×)
2 2
(3)(2015·全国卷Ⅰ)过氧化钠与水反应时,生成 0.1 mol O 转移的电子数为
2
0.2N (√)
A
(4)(2015·全国卷Ⅱ)CO 通过Na O 粉末后固体质量增重(√)
2 2 2
(5)(2015·山东高考)向CuSO 溶液中加入Na O 的离子方程式为2Na O +2Cu2++
4 2 2 2 2
2H O===4Na++2Cu(OH) ↓+O ↑(√)
2 2 2
(6)(2015·四川高考)标准状况下,5.6 L CO 与足量 Na O 反应转移的电子数为
2 2 2
0.5N (×)
A
5.(2016·江苏化学,18)过氧化钙(CaO ·8H O)是一种在水产养殖中广泛使用的供
2 2
氧剂。
(1)Ca(OH) 悬浊液与H O 溶液反应可制备CaO ·8H O。
2 2 2 2 2
Ca(OH) +H O +6H O===CaO ·8H O
2 2 2 2 2 2
反 应 时 通 常 加 入 过 量 的 Ca(OH) , 其 目 的 是
2
_____________________________________________________________________
____________________________________________________________________。
(2)向池塘水中加入一定量的 CaO ·8H O 后,池塘水中浓度增加的离子有
2 2
________(填序号)。
A.Ca2+ B.H+
C.CO D.OH-
解析 (1)Ca(OH) 过量,促进H O 吸收,提高H O 的利用率。(2)CaO ·8H O溶于
2 2 2 2 2 2 2
水与水反应生成Ca(OH) 和O ,增加了Ca2+和OH-。
2 2
答案 (1)提高H O 的利用率
2 2(2)AD
考点三 两种重要的钠盐:碳酸钠、碳酸氢钠
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查碳酸钠和碳酸氢钠的性质,特别是碳酸钠和碳酸氢钠与盐酸的反应
要从定性、定量、图像等多方面掌握,另外有关碳酸钠和碳酸氢钠的实验探究也要
加以关注!
1.Na CO 和NaHCO 的物理性质
2 3 3
名称 碳酸钠 碳酸氢钠
化学式 Na CO NaHCO
2 3 3
俗名 纯碱或苏打 小苏打
颜色、状态 白色粉末 细小白色晶体
水中易溶,比Na CO
2 3
水溶性 易溶于水
的溶解度小
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.NaHCO 的溶解度较小,将CO 通入到饱和Na CO 溶液时,开始无明显现象,后
3 2 2 3
有沉淀析出。
2.能从NaHCO 的溶解度角度分析侯氏制碱法。
3
2.Na CO 和NaHCO 的化学性质
2 3 3
(1)Na CO
2 3写出上述序号所表示反应的化学方程式:
①Na CO + 2HC l == =2NaC l + H O + CO ↑
2 3 2 2
②Na CO + Ca(OH ) == =CaCO ↓ + 2NaOH
2 3 2 3
③Na CO + BaC l == =BaCO ↓ + 2NaC l
2 3 2 3
(2)NaHCO
3
写出上述序号①、②、③、④所表示反应的化学方程式,②反应的离子方程式:
①NaHCO + HC l == =NaC l + H O + CO ↑;
3 2 2
②Ca(OH) 过量: HCO + OH - + Ca 2 + == =CaCO ↓ + H O;
2 3 2
Ca(OH) 少量: Ca 2 + + 2OH - + 2HCO == =CaCO ↓ + CO + 2H O;
2 3 2
③NaHCO + NaOH == =N a CO + H O;
3 2 3 2
④2NaHCO INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新
3
设计 高考总复习 化学 人教版 \ \ 反应三角 .TIF " \* MERGEFORMATINET
Na CO + H O + CO ↑。
2 3 2 2
(3)相互转化:
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.设计出Na CO 和NaHCO 的热稳定性的实验探究装置。
2 3 3
2.由NaHCO 与Ca(OH) 的反应,掌握“以少定多”的与量有关的离子方程式的
3 2
书写方法。
3.Na CO 的制备及用途
2 3
(1)Na CO 的工业制备——侯氏制碱法
2 3
①制备原理把二氧化碳通入氨的氯化钠饱和溶液中,使溶解度较小的碳酸氢钠从溶液中析出,
过滤得到碳酸氢钠晶体,碳酸氢钠受热分解生成碳酸钠。
②反应的化学方程式
a. NaCl + NH + CO + H O == =NaHCO ↓ + NH Cl;
3 2 2 3 4
b.2NaHCO INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设
3
计 高考总复习 化学 人教版 \ \ 反应三角 .TIF " \* MERGEFORMATINET
Na CO + CO ↑ + H O。
2 3 2 2
(2)Na CO 、NaHCO 的用途
2 3 3
①Na CO 是一种非常重要的化工原料,在玻璃、肥皂、合成洗涤剂、造纸、纺织、石
2 3
油、冶金、食品等工业中有着广泛的应用。
②NaHCO 是焙制糕点所用的发酵粉的主要成分之一;在医疗上,它是治疗胃酸过
3
多的一种药剂。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
Na CO 和NaHCO 的用途较易混淆,在掌握时应从原理上加以区别,而不是死记
2 3 3
硬背。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)用试管加热碳酸氢钠固体时,使试管口竖直向上(×)
(2)分别加热Na CO 和NaHCO 固体,试管内壁均有水珠出现,则说明两种物质均
2 3 3
受热分解(×)
(3)苏打是面包发酵粉的主要成分之一(×)
(4)NaHCO 溶液中加入稀盐酸:CO+2H+===H O+CO ↑(×)
3 2 2
(5)用酚酞溶液可鉴别饱和食盐水与饱和纯碱溶液(√)
2.(教材课后习题改编)用适当的方法除杂(括号内为杂质)
物质 方法
Na CO (NaHCO )固体粉末 ________
2 3 3Na CO (NaHCO )溶液 ________
2 3 3
NaHCO (Na CO )溶液 ________
3 2 3
答案 加热 加适量NaOH溶液 通入足量的CO
2
3.(思维探究题)请设计实验方案,用50 mL 2 mol·L-1 NaOH溶液和足量的CO 气
2
体,制取50 mL 1 mol·L-1的Na CO 溶液。
2 3
答案 将50 mL NaOH溶液,等分成两份,一份通入过量的CO ,然后与另一份混
2
合。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.下列离子方程式书写正确的是( )
A.NaHCO 溶液中加入稀HCl:CO+2H+===CO ↑
3 2
B.碳酸钠溶液显碱性:CO+H O HCO+OH-
2
C.Na O 溶于水产生O :Na O +H O===2Na++2OH-+O ↑
2 2 2 2 2 2 2
D.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO+OH-===CO+H O
2
解析 A项HCO不能完全电离,不能拆成离子,错;C项氧原子不守恒,错;D项
忽视了CO与Ca2+生成CaCO 沉淀。
3
答案 B
2.(2018·黑龙江鹤岗一中期末)Na CO 和NaHCO 是常见的两种钠盐,它们广泛应
2 3 3
用于生产和生活中。下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
A.小苏打能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过
多症,但不适合胃溃疡病人
B.NaHCO 能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头
3
C.可以用澄清石灰水来鉴别Na CO 溶液和NaHCO 溶液
2 3 3
D.往Na CO 饱和溶液中通入CO 气体,可获得NaHCO 沉淀
2 3 2 3
解析 小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学
方程式为NaHCO +HCl===NaCl+H O+CO ↑,胃溃疡病人不能服用小苏打类
3 2 2药物来治疗,因为反应产生的二氧化碳气体会造成胃部胀气,易造成胃穿孔,A项
正确;NaHCO 与酸反应生成二氧化碳气体,使得馒头或面包松软多孔,B项正确;
3
Na CO 和NaHCO 溶液都能与澄清石灰水反应生成CaCO 白色沉淀,所以不能用
2 3 3 3
澄清石灰水来鉴别,C项错误;Na CO 比NaHCO 易溶于水,所以在饱和Na CO
2 3 3 2 3
溶液中通入CO 气体可得到NaHCO 沉淀,D项正确。
2 3
答案 C
3.(2018·株洲模拟)为鉴别K CO 和NaHCO 两种白色固体,有4位同学分别设计
2 3 3
了下列四种不同的方法,其中不可行的是( )
A.分别加入1 mol·L-1的盐酸,看气泡产生的快慢
B.分别取样在试管中加热,将可能产生的气体通入澄清石灰水中,观察有无白色
浑浊
C.分别取样配成溶液,滴加Ba(OH) 溶液,观察有无白色沉淀
2
D.分别配成溶液、做焰色反应实验,观察火焰的颜色
解析 A项,因K CO 与盐酸反应分步进行,先生成碳酸氢钾,盐酸过量时才生成
2 3
气体,故可行;B项,K CO 受热不分解,NaHCO 受热分解产生CO ,故可行;C项
2 3 3 2
二者与Ba(OH) 溶液反应都产生白色沉淀BaCO ,故不可行;D项,钾的焰色为紫
2 3
色(透过蓝色钴玻璃观察),钠的焰色为黄色,可行。
答案 C
【规律方法】
测定纯碱中Na CO 质量分数的两种方法
2 3
发生反应Na CO +H SO ===Na SO +H O+CO ↑,依据CO 的体积
气体法 2 3 2 4 2 4 2 2 2
确定Na CO 的物质的量,进而确定纯碱中Na CO 的质量分数
2 3 2 3
发生反应Na CO +BaCl ===BaCO ↓+2NaCl,依据BaCO 沉淀的质
沉淀法 2 3 2 3 3
量,确定Na CO 的物质的量,进而确定纯碱中Na CO 的质量分数
2 3 2 3
[B组 考试能力过关]
4.正误判断,正确的打“√”,错误的打“×”。
(1)(2018·江苏化学3A)NaHCO 受热易分解,可用于制胃酸中和剂(×)
3
(2)(2017·北京理综,8A)二氧化碳使Na O 固体变白,二氧化碳气体被还原(×)
2 2(3)(2016·天津理综,1B)碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效。(×)
(4)(2015·全国卷Ⅱ,10C)钠在空气中燃烧可生成多种氧化物,23 g Na燃烧转移电
子为1N (√)
A
(5)(2015·全国卷Ⅱ,13A)将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产
生气泡(×)
(6)(2014·新课标全国卷Ⅰ,8A)用热的烧碱溶液洗去油污,是因为Na CO 可直接
2 3
与油污反应(×)
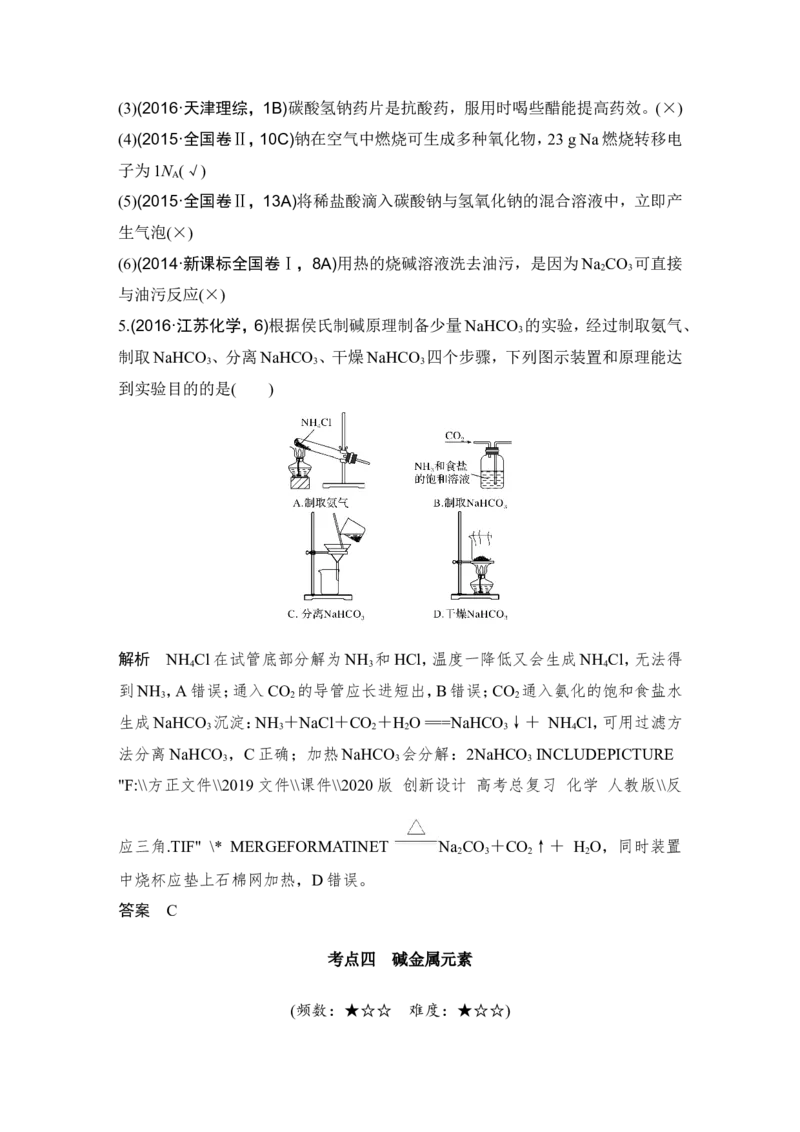
5.(2016·江苏化学,6)根据侯氏制碱原理制备少量NaHCO 的实验,经过制取氨气、
3
制取NaHCO 、分离NaHCO 、干燥NaHCO 四个步骤,下列图示装置和原理能达
3 3 3
到实验目的的是( )
解析 NH Cl在试管底部分解为NH 和HCl,温度一降低又会生成NH Cl,无法得
4 3 4
到NH ,A错误;通入CO 的导管应长进短出,B错误;CO 通入氨化的饱和食盐水
3 2 2
生成NaHCO 沉淀:NH +NaCl+CO +H O ===NaHCO ↓+ NH Cl,可用过滤方
3 3 2 2 3 4
法分离NaHCO ,C正确;加热NaHCO 会分解:2NaHCO INCLUDEPICTURE
3 3 3
"F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反
应三角.TIF" \* MERGEFORMATINET Na CO +CO ↑+ H O,同时装置
2 3 2 2
中烧杯应垫上石棉网加热,D错误。
答案 C
考点四 碱金属元素
(频数:★☆☆ 难度:★☆☆)INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点属于钠及其重要化合物的知识拓展,同时也属于元素周期律的应用,应从元
素周期律的递变规律上认识其性质的相似性和差异性,另外还应掌握焰色反应在
物质鉴别中的应用。
1.从结构角度认识碱金属的相似性、递变性与特殊性
(1)相似性和递变性
相似性 递变性(由Li→Cs)
电子层数逐渐增多,核电荷数
原子结构 最外层均为1个电子
逐渐增大,原子半径逐渐增大
都具有较强的金属性,最高正
元素性质 金属性逐渐增强
价均为+1价
(除Cs外)都呈银白色,密度较 密度逐渐增大(钾反常),熔、沸
物理性质
小,熔、沸点较低 点逐渐降低
单
质
性
还原性逐渐增强,与O 反应越
化学性质 都具有较强的还原性 2
质
来越剧烈,产物越来越复杂
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①物理性质:参照钠的物理性质学习Li、K、Cs等。
②化学性质:从原子结构讨论和参照钠的化学性质学习Li、K、Cs等。
(2)特殊性
①碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
②碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石
蜡中。
③一般情况下,碱金属所形成的盐均溶于水,并且在一定温度下,酸式盐比正盐的
溶解度大(但NaHCO 的溶解度比Na CO 的小)。
3 2 3④试剂瓶中的药品取出后,一般不能放回原瓶,但金属Na、K等需立即放回原瓶。
⑤锂与O 反应与钠不同,只生成Li O,而不生成Li O 。
2 2 2 2
2.牢记两种元素的焰色反应
(1)焰色反应:很多金属或它们的化合物在灼烧时都会使火焰呈现特殊颜色的现象
(2)操作步骤
铂丝――→无色――→待测物――→观察火焰颜色――→铂丝――→无色。
(3)常见元素焰色反应的颜色
钠元素:黄色;钾元素:紫色(透过蓝色钴玻璃观察)。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.焰色反应是物理变化,是金属元素的性质,既可以是单质,也可以是化合物。
2.用稀盐酸清洗的原因:生成金属氯化物,而金属氯化物在高温时可挥发。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)碱金属元素随核电荷数递增,原子半径依次增大,还原性增强(√)
(2)从锂到铯都能够与水反应生成碱和H (√)
2
(3)金属锂常用于制造锂电池,这跟它还原性强、密度小有关(√)
(4)用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液(×)
(5)所有金属及其化合物灼烧时火焰均有颜色(×)
2.(教材基础知识填空)用“>”或“<”填空:
(1)还原性:Li________Na________K。
(2)单质的熔点:Li________Na________K。
(3)碱性:LiOH________NaOH________KOH。
(4)与水反应的剧烈程度:Li________Na________K。
答案 (1)< < (2)> > (3)< < (4)< <
3.(思维探究题)已知铷是37号元素,质量数是85。回答下列问题:
(1)关于铷的结构和性质,判断正确的是________(填序号)。
①与水反应比钠剧烈 ②它的原子半径比钠小 ③它的氧化物暴露在空气中易吸
收CO ④它的阳离子最外层电子数和镁离子相同 ⑤化学反应中它是常见还原
2剂
(2)氢化铷与水反应可放出氢气,则下列叙述正确的是________(填字母)。
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子核外有两个电子
答案 (1)①③④⑤ (2)D
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.有关碱金属的叙述正确的是( )
A.随核电荷数的增加,碱金属单质的熔点逐渐降低,密度逐渐增大
B.碱金属单质的金属性很强,均易与Cl 、O 、N 等发生反应
2 2 2
C.Cs CO 加热时不能分解为CO 和Cs O
2 3 2 2
D.无水硫酸铯的化学式为Cs SO ,它不易溶于水
2 4
解析 钾的密度小于钠的密度,这是碱金属单质密度依次增大的一个特例;碱金
属中除锂外,均不与N 直接反应;由Na CO 加热不分解,可得出Cs CO 加热也不
2 2 3 2 3
分解;Cs与Na同为碱金属元素,性质相似,由Na SO 易溶于水,可得出Cs SO 也
2 4 2 4
易溶于水。
答案 C
2.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,根据碱金属元素性质
的递变规律预测其性质,其中不正确的是( )
A.在碱金属元素中它具有最大的原子半径
B.钫在空气中燃烧时,只生成化学式为Fr O的氧化物
2
C.它的氢氧化物的化学式为FrOH,这是一种极强的碱
D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸
解析 根据同主族元素性质的递变规律,从金属锂到金属钫随原子序数的递增,原子半径逐渐增大,元素的金属性逐渐增强,最高价氧化物对应的水化物的碱性
逐渐增强,与水反应的剧烈程度逐渐增强,与氧气反应的产物越来越复杂,可以产
生过氧化物、超氧化物甚至臭氧化物等。
答案 B
3.下列有关焰色反应实验操作注意事项的说法正确的是( )
①钾元素的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确
C.仅有⑤不正确 D.全对
解析 由于焰色反应是通过观察火焰颜色来检验元素是否存在的方法,所以实验
时所用火焰和所用金属丝在灼烧时都不应该有很明显的颜色,否则将无法观察到
被检验元素的真实焰色反应情况;观察钾的火焰颜色时要透过蓝色钴玻璃,目的
是滤去黄光,避免钠的干扰。
答案 D
[B组 考试能力过关]
4.(2015·天津理综,2)下列关于物质或离子检验的叙述正确的是( )
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水CuSO ,粉末变蓝,证明原气体中含有水蒸气
4
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO
2
解析 A项,在溶液中加KSCN,溶液显红色,说明一定含有Fe3+ ,不能证明是否
含有Fe2+,错误;B项,气体通过无水硫酸铜,粉末变蓝,是因为白色的无水硫酸铜
与水反应生成了蓝色的CuSO ·5H O,所以可证明原气体中含有水蒸气,正确;C
4 2
项,灼烧白色粉末,火焰呈黄色,说明原粉末中一定含有Na+ ,不能确定有无K+,
若要进一步确认可透过蓝色的钴玻璃滤去黄光后进行观察,如果火焰呈紫色,则
含有K+ ,否则不含K+,错误;D项,若为SO 气体也有相同的现象,所以不能确
2
定该气体一定是CO ,错误。
2答案 B
5.(2017·海南化学,16)锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回
答下列问题:
(1)用碳酸锂和________反应可制备氯化锂,工业上可由电解LiClKCl的熔融混合
物 生 产 金 属 锂 , 阴 极 上 的 电 极 反 应 式 为
_____________________________________________________________________。
(2) 不可 使用二氧化 碳灭 火器 扑灭因金属 锂引起 的火 灾,其原 因是
____________________________________________________________________。
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂
酸 锂 与 硬 脂 酸 钠 、 硬 脂 酸 钾 可 采 用 的 实 验 方 法 和 现 象 分 别 是
_____________________________________________________________________
_____________________________________________________________________
。
(4)LiPF 易溶于有机溶剂,常用作锂离子电池的电解质。LiPF 受热易分解,其热分
6 6
解产物为PF 和________。
5
解析 (1)碳酸锂与盐酸反应生成LiCl,由电解LiCl-KCl的熔融混合物产生金属
锂,阴极上锂离子得到电子。
(2)Li是活泼的金属,与二氧化碳反应。(3)阳离子不同、焰色反应不同。(4)在LiPF
6
和PF 中磷的化合价都是+5价,因而该分解反应为非氧化还原反应,根据原子守
5
恒,即可确定另一氟化物的化学式为LiF。
答案 (1)盐酸 Li++e-===Li
(2)Li与二氧化碳反应
(3)焰色反应,观察到黄色的为硬脂酸钠,透过蓝色钴玻璃观察到紫色的为硬脂酸
钾 (4)LiF
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET[A级 全员必做题]
1.钠及其化合物与人们的生活密切相关,某同学对其认识不正确的是( )
A.碳酸氢钠常用于治疗胃酸过多症
B.热的纯碱可去除油污
C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
D.金属钠着火时,使用泡沫灭火器来灭火
解析 D项,Na燃烧生成的Na O 能与CO 反应生成O ,因此金属钠着火时不能
2 2 2 2
用泡沫灭火器灭火,应用沙土掩埋法灭火。
答案 D
2.(2018·江西宜春三中期中)利用焰色反应,人们在烟花中有意识地加入特定金属
元素,使焰火更加绚丽多彩。下列说法中正确的是( )
A.非金属单质燃烧时火焰均为无色
B.NaCl与Na CO 灼烧时火焰颜色相同
2 3
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
解析 某些非金属单质燃烧时的火焰也有颜色,例如H 在氧气中燃烧产生淡蓝色
2
火焰,在氯气中燃烧产生苍白色火焰,A项错误;焰色反应为金属元素的性质,与
元素的存在形式(化合态或游离态)无关,同种金属元素的火焰颜色相同,B项正确
只有观察钾元素的焰色反应时才需要透过蓝色钴玻璃,防止钠元素的黄光造成干
扰,C项错误;焰色反应是某些金属或它们的化合物在无色火焰中灼烧时,火焰呈
现特征颜色的反应,是元素的性质,而不是单质的性质,D项错误。
答案 B
3.如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发
现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则烧杯内
的物质是( )
A.过氧化钠 B.氧化钠C.钠 D.钾
解析 Na O 、Na、K与水反应均有气体生成,均会使U形管内液面左边低于右边,
2 2
A、C、D不符合题意;Na O与水反应放热但没有气体生成,则U形管内液体慢慢
2
右移,待恢复到原温度后又使U形管内两液面相平。
答案 B
4.下列叙述中不正确的是( )
A.钠在反应TiCl +4Na===Ti+4NaCl中作还原剂
4
B.NaOH应密封保存,以防分解变质
C.盛放KOH溶液的试剂瓶不能用磨口玻璃塞
D.当足量的CO 通入饱和NaOH溶液中,会有固体析出
2
解析 NaOH密封保存,目的是防止空气中的CO 与之反应而变质。
2
答案 B
5.下列关于Na CO 、NaHCO 的说法正确的是( )
2 3 3
A.受热时Na CO 较NaHCO 更不稳定,更易分解产生CO
2 3 3 2
B.等质量的Na CO 、NaHCO 与足量盐酸反应,前者产生的CO 更多
2 3 3 2
C.常温下相同物质的量浓度的Na CO 、NaHCO 溶液,前者碱性更强
2 3 3
D.向Na CO 、NaHCO 溶液中分别滴加澄清石灰水,前者产生白色沉淀,后者无沉
2 3 3
淀
解析 NaHCO 与Na CO 相比较,NaHCO 不稳定,加热易分解;与足量盐酸反应
3 2 3 3
时,设质量都是1 g,利用n=和Na CO ~CO ,NaHCO ~CO 可计算出二者产生
2 3 2 3 2
的CO 的物质的量分别是mol、mol;CO水解程度比HCO大,则Na CO 碱性强;
2 2 3
NaHCO 与Na CO 都可与Ca(OH) 反应生成沉淀。
3 2 3 2
答案 C
6.(2019·河北冀州中学月考)过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质
时可燃烧。下列有关说法不正确的是( )
A.Na O 与CO 反应时,Na O 是氧化剂,CO 是还原剂
2 2 2 2 2 2
B.熔融过氧化钠时不可使用石英坩埚
C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性
D.过氧化钠与二氧化硫反应时可生成硫酸钠
解析 Na O 与H O、CO 反应时,都是Na O 自身发生的歧化反应,故A项错误;
2 2 2 2 2 2石英的主要成分是SiO ,而Na O 能与SiO 反应生成Na SiO ,故熔融过氧化钠时
2 2 2 2 2 3
不可使用石英坩埚,B项正确;Na O 具有强氧化性,而C、Al、SO 均具有还原性,
2 2 2
故Na O 可与C、Al、SO 发生氧化还原反应,可将 C氧化成CO ,将Al氧化成
2 2 2 2
Al O ,将SO 氧化成Na SO ,所以C项和D项均正确。
2 3 2 2 4
答案 A
7.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是(
)
选项 陈述Ⅰ 陈述Ⅱ 判断
Na CO 能与澄清石灰
碳酸钠、碳酸氢钠能用澄清石 2 3 Ⅰ对,
A 水反应生成白色沉淀,
灰水鉴别
Ⅱ对,有
而NaHCO 不能
3
向Na O 的水溶液中滴入酚酞 Na O 与水反应生成氢 Ⅰ对,
B 2 2 2 2
变红色 氧化钠 Ⅱ错,无
高压钠灯发出透雾性强 Ⅰ对,
C 金属钠具有强还原性
的黄光
Ⅱ对,有
酚酞溶液在碳酸钠溶液中的颜
Ⅰ对,
D 色比在同温同浓度的碳酸氢钠 CO水解程度大于HCO
溶液中深 Ⅱ对,有
解析 A项,因二者与澄清石灰水反应都会有白色沉淀生成,陈述Ⅰ、Ⅱ均不正确,
它们不能用澄清石灰水鉴别;B项,陈述Ⅰ应为先变红后褪色,错,陈述Ⅱ对;C项
两个陈述无因果关系。
答案 D
8.如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正确的是( )
3
A.a通入CO ,然后b通入NH ,c中放碱石灰
2 3
B.b通入NH 然后a通入CO ,c中放碱石灰
3 2
C.a通入NH ,然后b通入CO ,c中放蘸稀硫酸的脱脂棉
3 2
D.b通入CO ,然后a通入NH ,c中放蘸稀硫酸的脱脂棉
2 3
解析 由于CO 在水中的溶解度比较小,而NH 极易溶于水,所以在实验中要先
2 3通入溶解度较大的NH ,再通入CO ,由于NH 极易溶于水,在溶于水时极易发生
3 2 3
倒吸现象,所以通入NH 的导气管的末端不能伸入到溶液中,即a先通入NH ,然
3 3
后b通入CO ,A、B、D均错误;因为NH 是碱性气体,所以过量的NH 要用稀硫
2 3 3
酸来吸收,故答案选C。
答案 C
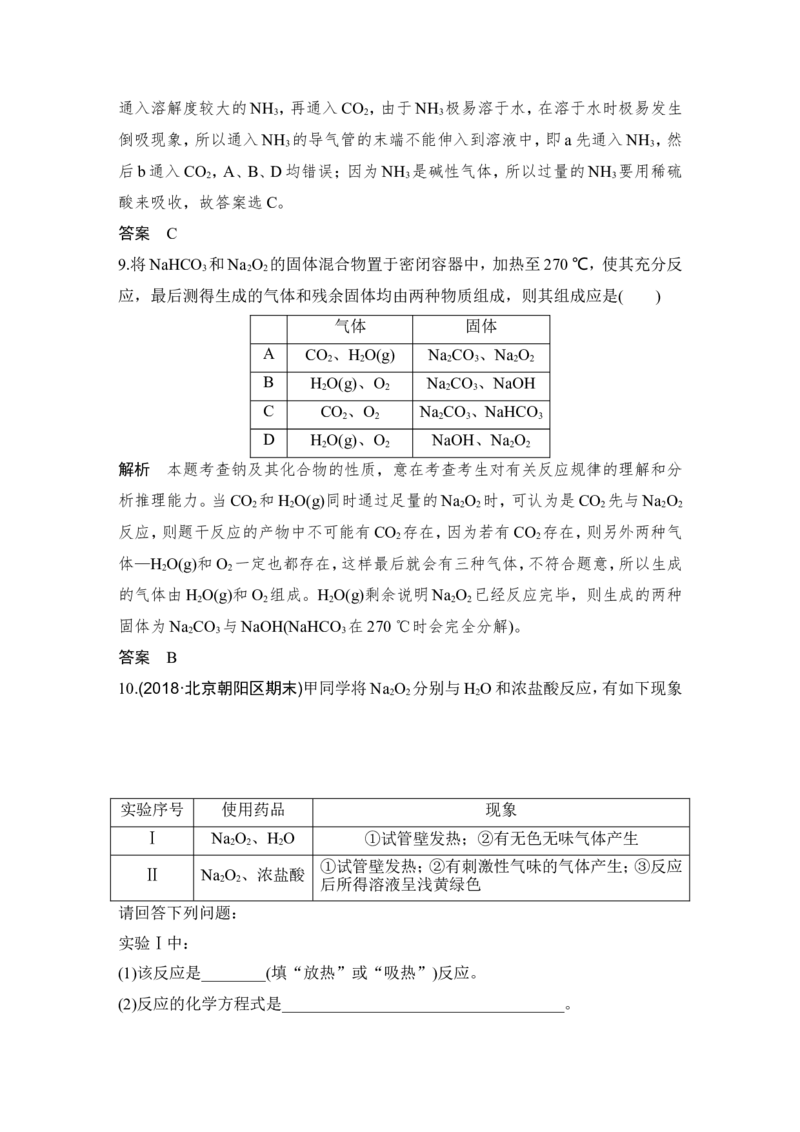
9.将NaHCO 和Na O 的固体混合物置于密闭容器中,加热至270 ℃,使其充分反
3 2 2
应,最后测得生成的气体和残余固体均由两种物质组成,则其组成应是( )
气体 固体
A CO 、H O(g) Na CO 、Na O
2 2 2 3 2 2
B H O(g)、O Na CO 、NaOH
2 2 2 3
C CO 、O Na CO 、NaHCO
2 2 2 3 3
D H O(g)、O NaOH、Na O
2 2 2 2
解析 本题考查钠及其化合物的性质,意在考查考生对有关反应规律的理解和分
析推理能力。当CO 和H O(g)同时通过足量的Na O 时,可认为是CO 先与Na O
2 2 2 2 2 2 2
反应,则题干反应的产物中不可能有CO 存在,因为若有CO 存在,则另外两种气
2 2
体—H O(g)和O 一定也都存在,这样最后就会有三种气体,不符合题意,所以生成
2 2
的气体由H O(g)和O 组成。H O(g)剩余说明Na O 已经反应完毕,则生成的两种
2 2 2 2 2
固体为Na CO 与NaOH(NaHCO 在270 ℃时会完全分解)。
2 3 3
答案 B
10.(2018·北京朝阳区期末)甲同学将Na O 分别与H O和浓盐酸反应,有如下现象
2 2 2
实验序号 使用药品 现象
Ⅰ Na O 、H O ①试管壁发热;②有无色无味气体产生
2 2 2
①试管壁发热;②有刺激性气味的气体产生;③反应
Ⅱ Na O 、浓盐酸
2 2 后所得溶液呈浅黄绿色
请回答下列问题:
实验Ⅰ中:
(1)该反应是________(填“放热”或“吸热”)反应。
(2)反应的化学方程式是___________________________________。(3)证明无色无味气体是氧气的方法是________________________________
________________________________________________________________。
实验Ⅱ中:
(4)根据现象②、③,推测生成的气体中可能含有 Cl ,产生Cl 的化学方程式是
2 2
____________________________________________________________________。
(5)若往“浅黄绿色溶液”中加入FeCl 溶液,立即产生与实验Ⅰ相同的气体,原因
3
是________________________________________________________________。
解析 (1)试管壁发热,说明反应是放热反应。
(2)过氧化钠与水反应生成氢氧化钠和氧气,化学方程式为 2Na O +
2 2
2H O===4NaOH+O ↑。
2 2
(3)检验氧气的方法是将带火星的木条放在试管口,木条复燃,则证明是氧气。
(4)有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色,说明生成的气体是氯
气,过氧化钠氧化浓盐酸生成氯气,化学方程式为 Na O +4HCl(浓)===2NaCl+
2 2
Cl ↑+2H O。
2 2
(5)随反应的进行,浓盐酸变稀盐酸,而稀盐酸与Na O 可发生复分解反应生成过
2 2
氧化氢,所以溶液中存在的过氧化氢在氯化铁催化作用下产生氧气。
答案 (1)放热
(2)2Na O +2H O===4NaOH+O ↑
2 2 2 2
(3)将带火星的木条放在试管口,木条复燃,则证明是氧气
(4)Na O +4HCl(浓)===2NaCl+Cl ↑+2H O
2 2 2 2
(5)浅黄绿色溶液中存在H O ,加入的FeCl 使H O 分解速率加快,立即产生氧气
2 2 3 2 2
11.(上海卷)钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN )受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若
3
产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________g。
(2)钠—钾合金可在核反应堆中用作热交换液。5.05 g钠—钾合金溶于200 mL水生
成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式。
解析 (1)解法一:叠氮化钠受撞击分解的化学方程式为2NaN ===2Na+3N ↑
3 2由此可知生成标准状况下40.32 L氮气时需要NaN 的质量为××65 g·mol-1=78
3
g。
解法二:根据氮元素守恒有n(NaN )=n(N )=×=1.2 mol,m(NaN )=1.2 mol×65
3 2 3
g·mol-1=78 g。
答案 (1)78 (2)①c(OH-)= mol·L-1=0.75 mol·L-1
②设上述合金中含a mol钠、b mol钾,则
解得a=0.050 b=0.10
该钠—钾合金化学式为NaK 。
2
[B级 拔高选做题]
12.(2018·湖南两校月考)①氧化钠、②氢氧化钠、③过氧化钠、④亚硫酸钠,1 mol
上述固体物质长期放置于空气中,下列说法正确的是( )
A.质量增加的情况是②>①>③>④
B.质量增加的情况是①>③>④>②
C.上述物质都发生了氧化还原反应
D.过氧化钠在反应中转移了2 mol电子
解析 Na O~Na CO 1 mol Na O 长期放置于空气中质量增加 44 g;NaOH~
2 2 3, 2
Na CO 1 mol NaOH 长期放置于空气中质量增加 13 g;Na O ~Na CO 1 mol
2 3, 2 2 2 3,
Na O 长期放置于空气中质量增加28 g;Na SO ~Na SO ,1 mol Na SO 长期放置
2 2 2 3 2 4 2 3
于空气中质量增加16 g,故A项错误,B项正确;Na O和NaOH未发生氧化还原
2
反应,C项错误;1 mol过氧化钠在反应中转移了1 mol电子,D项错误。
答案 B
13.由Na O 、Na CO 、NaHCO 、NaCl中的某几种组成的混合物,向其中加入足量
2 2 2 3 3
的盐酸有气体放出。将气体通过足量的NaOH溶液,气体体积减少一部分。将上述
混合物在空气中加热,有气体放出,下列判断正确的是( )
A.混合物中一定不含Na CO 、NaCl
2 3
B.混合物中一定有Na O 、NaHCO
2 2 3
C.无法确定混合物中是否含有NaHCO
3
D.混合物中一定不含Na O 、NaCl
2 2
解析 混合粉末加盐酸有气体产生说明其中可能有Na O 、Na CO 、NaHCO ,又
2 2 2 3 3由于气体通过足量的NaOH溶液后体积减小,说明气体中同时含有O 和CO ,则
2 2
原混合粉末中肯定存在Na O ,还可能有Na CO 或NaHCO 中的一种或两种,将
2 2 2 3 3
原混合粉末在空气中加热有气体放出,说明NaHCO 肯定存在,但Na CO 和NaCl
3 2 3
不能确定是否存在。
答案 B
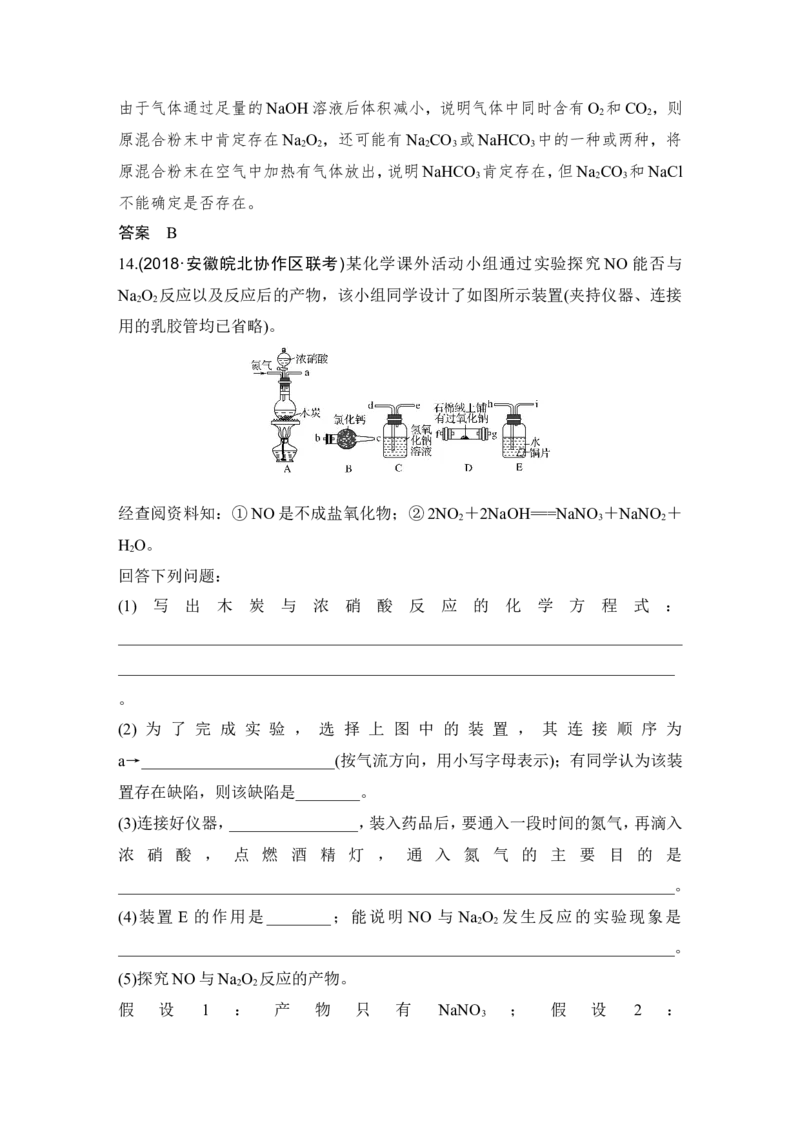
14.(2018·安徽皖北协作区联考)某化学课外活动小组通过实验探究 NO 能否与
Na O 反应以及反应后的产物,该小组同学设计了如图所示装置(夹持仪器、连接
2 2
用的乳胶管均已省略)。
经查阅资料知:①NO是不成盐氧化物;②2NO +2NaOH===NaNO +NaNO +
2 3 2
H O。
2
回答下列问题:
(1) 写 出 木 炭 与 浓 硝 酸 反 应 的 化 学 方 程 式 :
______________________________________________________________________
_____________________________________________________________________
。
(2) 为 了 完 成 实 验 , 选 择 上 图 中 的 装 置 , 其 连 接 顺 序 为
a→________________________(按气流方向,用小写字母表示);有同学认为该装
置存在缺陷,则该缺陷是________。
(3)连接好仪器,________________,装入药品后,要通入一段时间的氮气,再滴入
浓 硝 酸 , 点 燃 酒 精 灯 , 通 入 氮 气 的 主 要 目 的 是
_____________________________________________________________________。
(4)装置 E 的作用是________;能说明 NO 与 Na O 发生反应的实验现象是
2 2
_____________________________________________________________________。
(5)探究NO与Na O 反应的产物。
2 2
假 设 1 : 产 物 只 有 NaNO ; 假 设 2 :
3_________________________________________;
假设3:产物为NaNO 和NaNO 的混合物。
3 2
为验证反应产物,该小组同学准确称取反应后的固体3.50 g,用煮沸并冷却后的蒸
馏水配成 100.00 mL 溶液,取 10.00 mL 溶液于锥形瓶中,用 0.100 0 mol·L-1
KMnO 溶液(硫酸酸化)滴定,共消耗KMnO 溶液20 mL。滴定过程中发生反应的
4 4
离子方程式为________________________________________________,反应产物
中NaNO 的质量分数为________(保留四位有效数字)。
2
解析 (5)根据关系式,设NO的物质的量为n,
2MnO ~ 5NO
2 mol 5 mol
0.002 mol n
求得n=0.005 mol
则NaNO 的质量分数为×100%≈98.57%。
2
答案 (1)C+4HNO (浓) INCLUDEPICTURE "F:\\方正文件\\2019 文件\\课件\
3
\2020 版 创 新 设 计 高 考 总 复 习 化 学 人 教 版 \\ 反 应 三 角 .TIF" \*
MERGEFORMATINET CO ↑+4NO ↑+2H O
2 2 2
(2)h→i→d→e→b→c→f或g 缺少尾气处理装置
(3)检验装置的气密性 排出装置中的空气,防止NO被空气中的O 氧化为NO
2 2
(4)制备NO D中固体由淡黄色变为白色
(5)产物只有NaNO 2MnO+5NO+6H+===5NO+2Mn2++3H O 98.57%
2 2