文档内容
1.绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小
组对绿矾的一些性质进行探究。回答下列问题:
Ⅰ.测定绿矾中结晶水含量
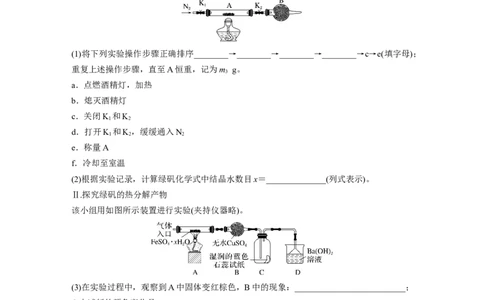
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K 和K)(设为装置A)称重,记为m
1 2 1
g。将样品装入石英玻璃管中,再次将装置A称重,记为m g。按如图连接好装置进行实验。
2
(1)将下列实验操作步骤正确排序________→________→________→________→c→e(填字母);
重复上述操作步骤,直至A恒重,记为m g。
3
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K 和K
1 2
d.打开K 和K,缓缓通入N
1 2 2
e.称量A
f.冷却至室温
(2)根据实验记录,计算绿矾化学式中结晶水数目x=______________(列式表示)。
Ⅱ.探究绿矾的热分解产物
该小组用如图所示装置进行实验(夹持仪器略)。
(3)在实验过程中,观察到A中固体变红棕色,B中的现象:__________________________;
C中试纸的颜色变化是___________________________________________________________。
(4)D中有白色沉淀生成,该沉淀的化学式为_________________________________________
______________。有同学认为还应该增加一个实验,取 D中沉淀,加入一定量的盐酸以确
定其组成,从而确定 FeSO ·xHO 的分解产物,你认为是否必要?______(填“是”或
4 2
“ 否 ” ) , 请 说 明 你 的 理 由 :
_______________________________________________________________
_______________________________________________________________________________
。
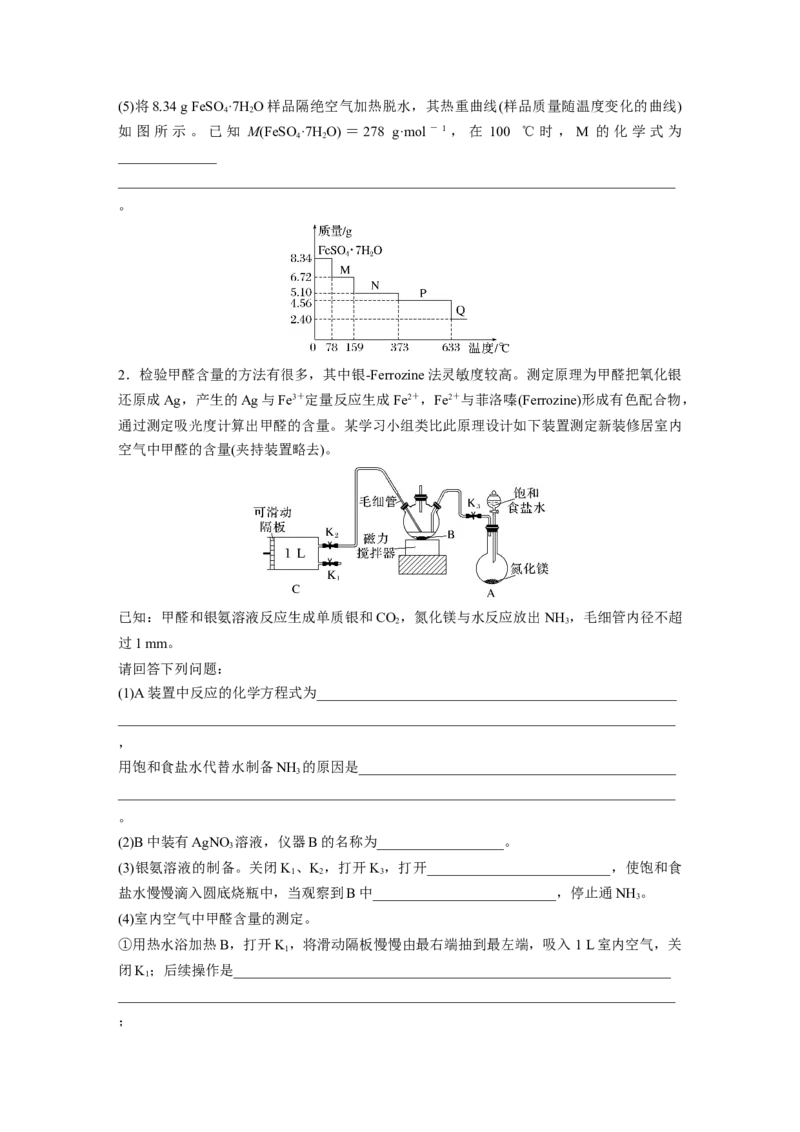
Ⅲ.测定绿矾热分解时的温度与剩余固体质量关系(5)将8.34 g FeSO ·7H O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)
4 2
如图所示。已知 M(FeSO ·7H O) =278 g·mol -1,在 100 ℃时, M 的化学式为
4 2
______________
_______________________________________________________________________________
。
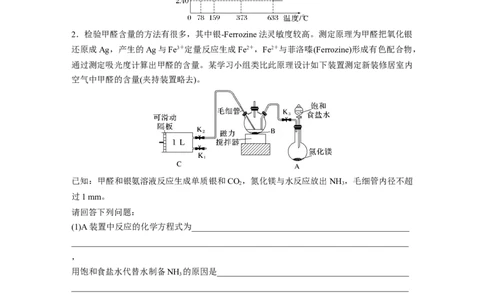
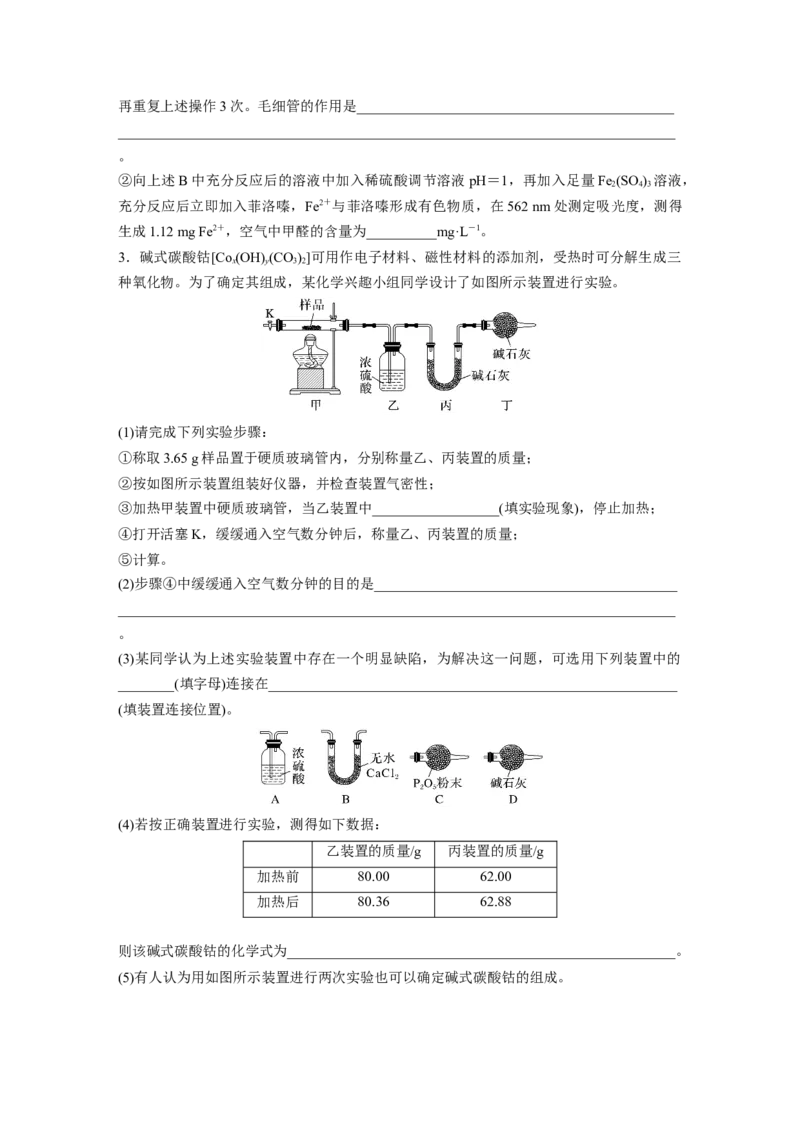
2.检验甲醛含量的方法有很多,其中银-Ferrozine法灵敏度较高。测定原理为甲醛把氧化银
还原成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,
通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如下装置测定新装修居室内
空气中甲醛的含量(夹持装置略去)。
已知:甲醛和银氨溶液反应生成单质银和CO ,氮化镁与水反应放出NH ,毛细管内径不超
2 3
过1 mm。
请回答下列问题:
(1)A装置中反应的化学方程式为___________________________________________________
_______________________________________________________________________________
,
用饱和食盐水代替水制备NH 的原因是_____________________________________________
3
_______________________________________________________________________________
。
(2)B中装有AgNO 溶液,仪器B的名称为__________________。
3
(3)银氨溶液的制备。关闭K 、K ,打开K ,打开__________________________,使饱和食
1 2 3
盐水慢慢滴入圆底烧瓶中,当观察到B中__________________________,停止通NH 。
3
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K,将滑动隔板慢慢由最右端抽到最左端,吸入1 L室内空气,关
1
闭K;后续操作是______________________________________________________________
1
_______________________________________________________________________________
;再重复上述操作3次。毛细管的作用是_____________________________________________
_______________________________________________________________________________
。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe (SO ) 溶液,
2 4 3
充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562 nm处测定吸光度,测得
生成1.12 mg Fe2+,空气中甲醛的含量为__________mg·L-1。
3.碱式碳酸钴[Co(OH)(CO)]可用作电子材料、磁性材料的添加剂,受热时可分解生成三
x y 3 2
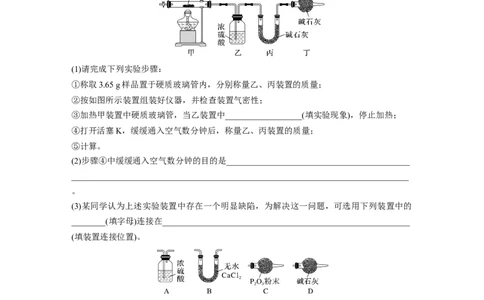
种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,分别称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检查装置气密性;
③加热甲装置中硬质玻璃管,当乙装置中__________________(填实验现象),停止加热;
④打开活塞K,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是___________________________________________
_______________________________________________________________________________
。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的
________(填字母)连接在__________________________________________________________
(填装置连接位置)。
(4)若按正确装置进行实验,测得如下数据:
乙装置的质量/g 丙装置的质量/g
加热前 80.00 62.00
加热后 80.36 62.88
则该碱式碳酸钴的化学式为_______________________________________________________。
(5)有人认为用如图所示装置进行两次实验也可以确定碱式碳酸钴的组成。实验Ⅰ:称取一定质量的样品置于Y形管a处,加入一定体积一定物质的量浓度的足量稀硫
酸于 Y 形管 b 处,量气管中盛放饱和碳酸氢钠溶液,而不用蒸馏水,其原因是
________________________________,然后通过______________________________(填操作),
引发反应,测定产生的CO 的体积(假设实验条件是在室温下)。
2
实验 Ⅱ:将实验Ⅰ中反应后的液体和足量的锌粒分别放置在另一个Y形管的a、b中,量气
管中盛装蒸馏水,此时引发反应的方式与实验Ⅰ________(填“相同”“不同”或“可相同
也可不同”),然后测定产生H 的体积(假设实验条件是在室温下)。
2
两次实验结束时,读数前,先________________,再调节量气管两侧液面持平,然后平视读
数;下列实验操作有可能会使y的值偏大的是________(填字母)。
A.实验Ⅰ读数时量气管左侧液面高于右侧液面
B.实验Ⅱ实验结束时,迅速调整两侧液面持平,立即读数
C.实验Ⅱ引发反应时将稀硫酸向锌粒倾斜
4.(2020·天津,15)为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问
4
题:
Ⅰ.甲方案
实验原理:CuSO +BaCl ===BaSO↓+CuCl
4 2 4 2
实验步骤:
(1)判断SO沉淀完全的操作为___________________________________________________
______________________________________________________________________________。
(2)步骤②判断沉淀是否洗净所选用的试剂为______________________。
(3)步骤③灼烧时盛装样品的仪器名称为____________________________________________。
(4)固体质量为w g,则c(CuSO )=__________________________________________mol·L-
4
1。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )__________(填“偏高”“偏
4
低”或“无影响”)。
Ⅱ.乙方案
实验原理:Zn+CuSO ===ZnSO+Cu
4 4
Zn+HSO ===ZnSO+H↑
2 4 4 2实验步骤:
①按图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
4
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为____________________。
(7)步骤⑥需保证体系恢复到室温的原因是__________________________________(填序号)。
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(8)Zn粉质量为a g,若测得H 体积为b mL,已知实验条件下ρ(H )=d g·L-1,则c(CuSO )
2 2 4
=_____________________________________________________________________ mol·L-1
(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )__________(填“偏高”
4
“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO 溶液的浓度:__________(填“是”或“否”)。
4