文档内容
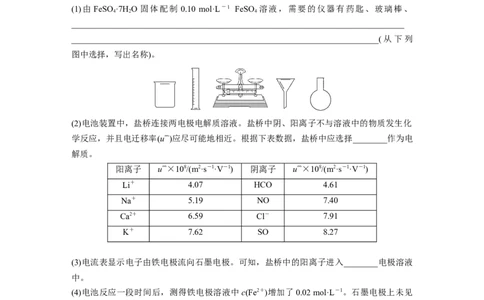
1.(2020·全国卷 Ⅰ,27)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)由 FeSO ·7H O 固体配制 0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、玻璃棒、
4 2 4
______________________________________________________________________________
________________________________________________________________________(从下列
图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化
学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电
解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)
Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液
中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见
Fe析出。可知,石墨电极溶液中c(Fe2+)=____________________________。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为__________________,铁电极的电
极反应式为__________________。因此,验证了 Fe2+氧化性小于________,还原性小于
______________________________________________________________________________。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡
4 2 4 3
一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是_______________________
______________________________________________________________________________。
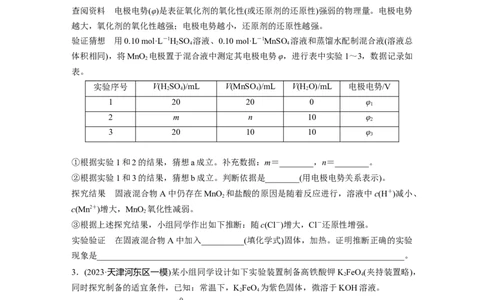
2.(2023·广州模拟)某小组从电极反应的角度研究物质氧化性和还原性的变化规律。(1)实验室以MnO 和浓盐酸为原料制取氯气的化学方程式为MnO +4HCl(浓)=====MnCl +
2 2 2
2HO+Cl↑。该反应的氧化产物是________。将该反应设计成原电池,氧化反应为2Cl--
2 2
2e-===Cl↑,还原反应为________________________________________________________。
2
(2)当氯气不再逸出时,固液混合物A中仍存在MnO 和盐酸。小组同学分析认为随着反应的
2
进行,MnO 的氧化性和Cl-的还原性均减弱,为此进行探究。
2
实验任务 探究离子浓度对MnO 氧化性的影响
2
提出猜想
猜想a:随c(H+)减小,MnO 的氧化性减弱。
2
猜想b:随c(Mn2+)增大,MnO 的氧化性减弱。
2
查阅资料 电极电势(φ)是表征氧化剂的氧化性(或还原剂的还原性)强弱的物理量。电极电势
越大,氧化剂的氧化性越强;电极电势越小,还原剂的还原性越强。
验证猜想 用0.10 mol·L-1HSO 溶液、0.10 mol·L-1MnSO 溶液和蒸馏水配制混合液(溶液总
2 4 4
体积相同),将MnO 电极置于混合液中测定其电极电势φ,进行表中实验1~3,数据记录如
2
表。
实验序号 V(H SO )/mL V(MnSO )/mL V(H O)/mL 电极电势/V
2 4 4 2
1 20 20 0 φ
1
2 m n 10 φ
2
3 20 10 10 φ
3
①根据实验1和2的结果,猜想a成立。补充数据:m=________,n=________。
②根据实验1和3的结果,猜想b成立。判断依据是________(用电极电势关系表示)。
探究结果 固液混合物A中仍存在MnO 和盐酸的原因是随着反应进行,溶液中c(H+)减小、
2
c(Mn2+)增大,MnO 氧化性减弱。
2
③根据上述探究结果,小组同学作出如下推断:随c(Cl-)增大,Cl-还原性增强。
实验验证 在固液混合物A中加入__________(填化学式)固体,加热。证明推断正确的实验
现象是________________________________________________________________________。
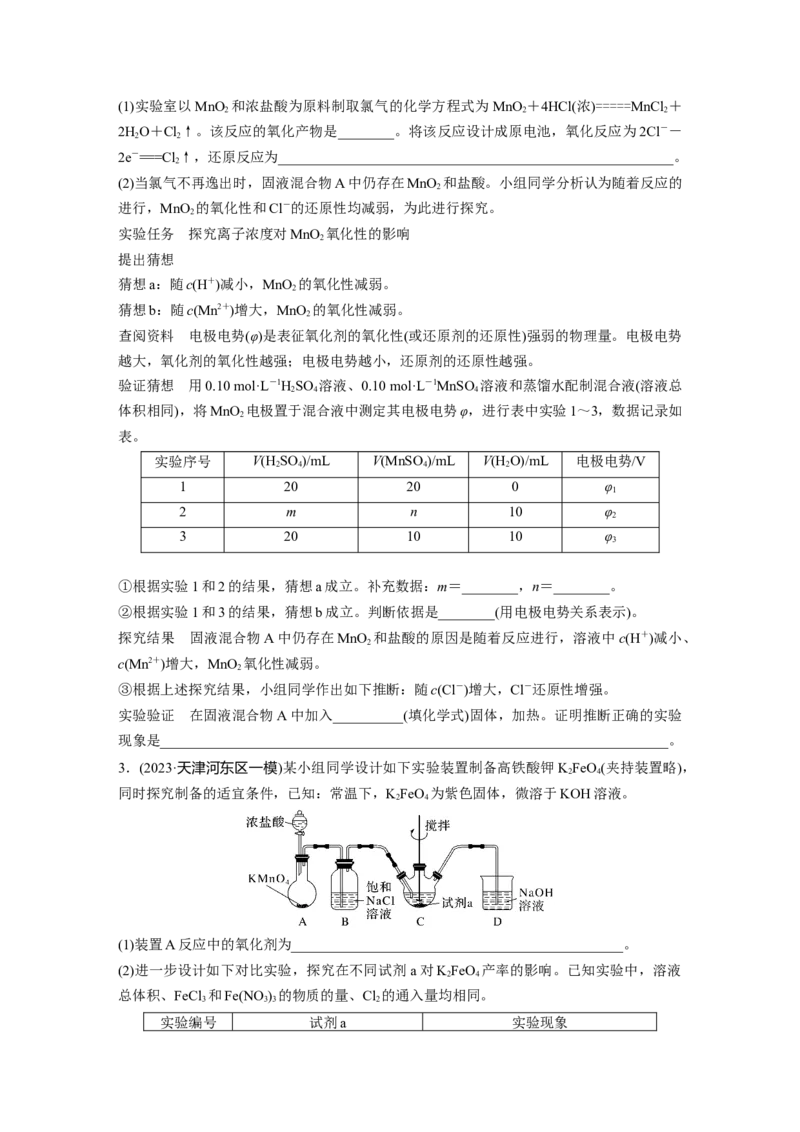
3.(2023·天津河东区一模)某小组同学设计如下实验装置制备高铁酸钾 KFeO(夹持装置略),
2 4
同时探究制备的适宜条件,已知:常温下,KFeO 为紫色固体,微溶于KOH溶液。
2 4
(1)装置A反应中的氧化剂为_______________________________________________。
(2)进一步设计如下对比实验,探究在不同试剂 a对KFeO 产率的影响。已知实验中,溶液
2 4
总体积、FeCl 和Fe(NO ) 的物质的量、Cl 的通入量均相同。
3 3 3 2
实验编号 试剂a 实验现象ⅰ FeCl 溶液和少量KOH 无明显现象
3
ⅱ FeCl 溶液和过量KOH 得到紫色溶液,无紫色固体
3
ⅲ Fe(NO ) 溶液和过量KOH 得到深紫色溶液,有紫色固体
3 3
①对比实验ⅰ与ⅱ现象,提出假设;“实验ⅱ溶液碱性较强,增强+3价铁的还原性”,验
证此假设的实验装置如图所示:
当通入Cl ,电压表示数为V ;再向右侧烧杯中加入的试剂为________,电压表示数为V ;
2 1 2
且观察V________(填“>”“<”或“=”)V ,证明上述假设成立。
1 2
②配平实验ⅲ中反应的离子方程式:
Fe3++Cl+FeO+Cl-+
2
③实验ⅱ中KFeO 的产率比实验ⅲ的低,其原因可能是_____________________________
2 4
______________________________________________________________________________。
(3)随着反应的发生,装置B中不断有白色片状固体产生。
①结合化学用语解释该现象:____________________________________________________
______________________________________________________________________________。
②若拆除装置B,而使KFeO 的产率降低的原因是_________________________________
2 4
______________________________________________________________________________。
(4)向实验ⅱ所得紫色溶液中继续通入Cl ,溶液紫色变浅,KFeO 的产率降低。可能原因是
2 2 4
通入的Cl 消耗了KOH,写出该反应的离子方程式:________________________________。
2
(5)综上可知制备KFeO,所需的适宜条件是_______________________________________。
2 4
4.某小组为探究Mg与NH Cl溶液的反应机理,常温下进行以下实验。实验中所取镁粉质
4
量均为0.5 g,分别加入选取的实验试剂中,资料:①CHCOONH 溶液呈中性。②Cl-对该
3 4
反应几乎无影响。
实验 实验试剂 实验现象
反应缓慢,有少量气泡产生(经检验为
1 5 mL蒸馏水
H)
2
剧烈反应,产生刺激性气味气体和灰白
2 5 mL 1.0 mol·L-1 NH Cl溶液(pH=4.6)
4
色难溶固体
(1)经检验实验2中刺激性气味气体为NH ,检验方法是_____________________________。
3
用排水法收集一小试管产生的气体,经检验小试管中气体为H。
2
(2)已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO 溶液后无明显浑浊。将洗涤后的固体溶于稀HNO,再滴
3 3
加 AgNO 溶液,出现白色沉淀。推测沉淀中含有________,灰白色固体可能是
3
____________(填化学式)。
(3)甲同学认为实验2比实验1反应剧烈的原因是NH Cl溶液中c(H+)大,与Mg反应快。用
4
化学用语解释NH Cl溶液显酸性的原因是__________________________________________
4
______________________________________________________________________________。
(4)乙同学通过实验3证明甲同学的说法不合理。
实验 实验装置
3
①试剂X是____________________________________________________________________。
②由实验3获取的证据为________________________________________________________。
(5)为进一步探究实验2反应剧烈的原因,进行实验4。
实验 实验试剂 实验现象
4 5 mL NH Cl乙醇溶液 有无色无味气体产生(经检验为H)
4 2
依据上述实验,可以得出Mg能与NH反应生成H。乙同学认为该方案不严谨,需要补充的
2
实验方案是____________________________________________________________________
______________________________________________________________________________。
(6)由以上实验可以得出的结论是__________________________________________________
________________________________________________________________________。