文档内容
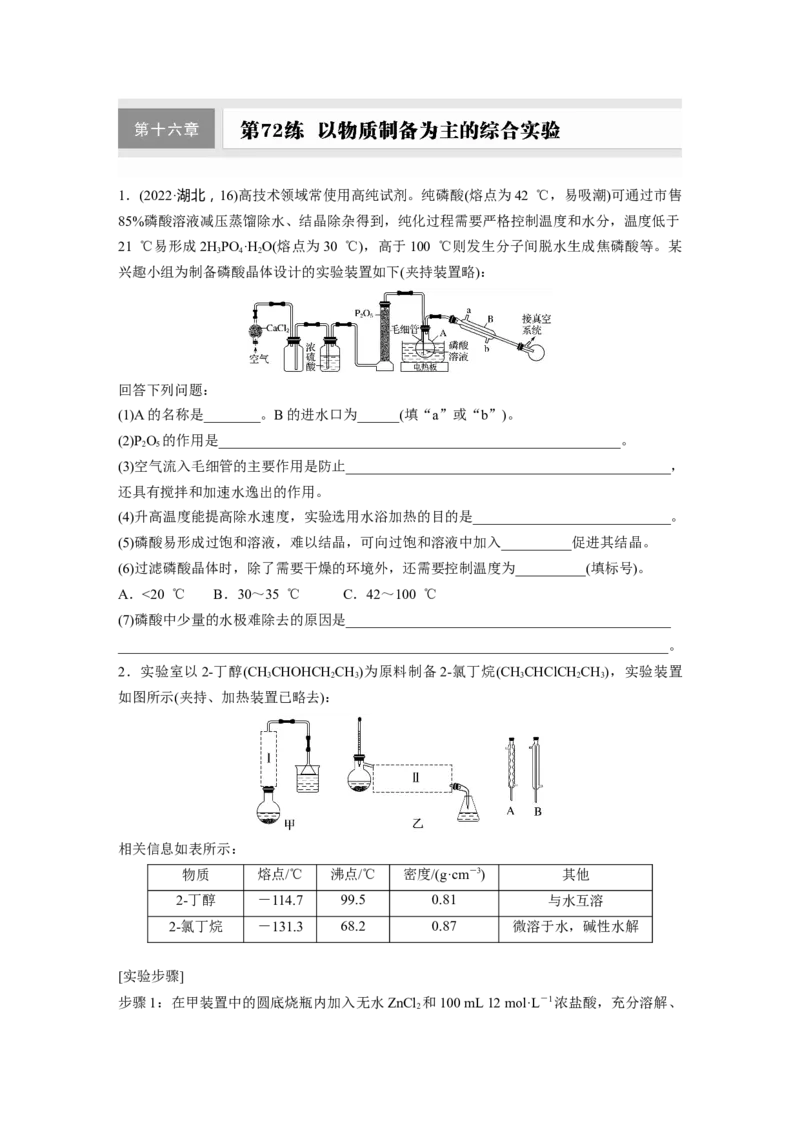
1.(2022·湖北,16)高技术领域常使用高纯试剂。纯磷酸(熔点为42 ℃,易吸潮)可通过市售
85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于
21 ℃易形成2HPO ·H O(熔点为30 ℃),高于100 ℃则发生分子间脱水生成焦磷酸等。某
3 4 2
兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):
回答下列问题:
(1)A的名称是________。B的进水口为______(填“a”或“b”)。
(2)P O 的作用是_________________________________________________________。
2 5
(3)空气流入毛细管的主要作用是防止______________________________________________,
还具有搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是____________________________。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入__________促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为__________(填标号)。
A.<20 ℃ B.30~35 ℃ C.42~100 ℃
(7)磷酸中少量的水极难除去的原因是______________________________________________
______________________________________________________________________________。
2.实验室以2-丁醇(CHCHOHCH CH)为原料制备2-氯丁烷(CHCHClCH CH),实验装置
3 2 3 3 2 3
如图所示(夹持、加热装置已略去):
相关信息如表所示:
物质 熔点/℃ 沸点/℃ 密度/(g·cm-3) 其他
2-丁醇 -114.7 99.5 0.81 与水互溶
2-氯丁烷 -131.3 68.2 0.87 微溶于水,碱性水解
[实验步骤]
步骤1:在甲装置中的圆底烧瓶内加入无水ZnCl 和100 mL 12 mol·L-1浓盐酸,充分溶解、
2冷却,再加入45.68 mL 2-丁醇,加热一段时间。
步骤2:将反应混合物移至乙装置的蒸馏烧瓶内,蒸馏并收集115 ℃以下的馏分。
步骤3:从馏分中分离出有机相,进行系列操作,放置一段时间后过滤。
步骤4:滤液经进一步精制得产品。
回答下列问题:
(1) Ⅰ 中应放置的仪器是______________(填“A”或“B”,下同), Ⅱ 中应放置的仪器是
______________________________________________________________________________。
(2)步骤1中加入的无水ZnCl 的作用是____________________________________________
2
______________________________________________________________________________。
(3)步骤3进行系列操作的顺序是____________(填序号,可重复使用)。
①10%Na CO 溶液洗涤
2 3
②加入CaCl 固体
2
③蒸馏水洗涤
用NaCO 溶液洗涤时操作要迅速,其原因是_______________________________________。
2 3
(4)步骤4中滤液进一步精制得产品所采用的操作方法是____________(填名称)。
(5)测定实验中生成2-氯丁烷的产率。将全部产品加入足量 NaOH溶液中,加热,冷却后,
滴入稀硝酸至溶液呈酸性,再滴入足量的硝酸银溶液,得到57.40 g沉淀,则2-氯丁烷的产
率是____________________________________________________________________________。
3.(2023·辽宁,17)2-噻吩乙醇(M=128)是抗血栓药物氯吡格雷的重要中间体,其制备方法
r
如下:
Ⅰ.制钠砂。向烧瓶中加入300 mL液体A和4.60 g金属钠,加热至钠熔化后,盖紧塞子,振
荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10 ℃,加入25 mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10 ℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30 min。
Ⅳ.水解。恢复室温,加入70 mL水,搅拌30 min;加盐酸调pH至4~6,继续反应2 h,分
液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻
4
吩和液体A后,得到产品17.92 g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择________。
a.乙醇 b.水 c.甲苯 d.液氨(2)噻吩沸点低于吡咯( )的原因是_____________________________________________
______________________________________________________________________________。
(3)步骤Ⅱ的化学方程式为________________________________________________________
______________________________________________________________________________。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是
______________________________________________________________________________
______________________________________________________________________________。
(5)步骤Ⅳ中用盐酸调节pH的目的是______________________________________________
______________________________________________________________________________。
(6)下列仪器在步骤Ⅴ中无需使用的是____________________(填名称);无水MgSO 的作用
4
为
______________________________________________________________________________。
(7)产品的产率为____________(用Na计算,精确至0.1%)。
4.(2023·天津河东区一模)实验室利用红磷(P)与Cl 反应可制取少量PCl 或PCl 。
2 3 5
物质 熔点/℃ 沸点/℃ 性质
PCl -112 75.5 遇水生成HPO 和HCl,与O 反应生成POCl
3 3 3 2 3
PCl — 约100 ℃升华 遇水生成HPO 和HCl,与红磷反应生成PCl
5 3 4 3
Ⅰ.利用如图所示装置制取少量PCl (部分夹持装置已略去)。
3
(1)组装好装置,在放入试剂前应先__________________________________________。
(2)A中发生反应的离子方程式为__________________________________________________
______________________________________________________________________________。
(3)B中所装试剂为________(填字母)。
A.饱和碳酸氢钠溶液 B.饱和氯化钠溶液
C.氢氧化钠溶液 D.浓硫酸
(4)实验开始前,打开 K 通入一段时间氮气来除去装置中的空气,除去空气的目的是
1______________________________________________________________________________
______________________________________________________________________________;
除去装置A、B中空气的具体方法是______________________________________________
______________________________________________________________________________。
(5)除去产物中PCl 杂质的化学方程式是___________________________________________
5
______________________________________________________________________________。
Ⅱ.测定产品中PCl 的质量分数
3
实验步骤:
①迅速称取m g产品,加水反应后配成100 mL溶液。
②取上述溶液10.00 mL,向其中加入V mL c mol·L-1碘水(足量),充分反应。
1 1
③向②所得溶液中加入几滴淀粉溶液,逐滴滴加c mol·L-1的NaSO 溶液并振荡,当溶液
2 2 2 3
恰好由蓝色变为无色时,记录所消耗NaSO 溶液的体积。
2 2 3
④重复②、③操作3次,平均消耗NaSO 溶液V mL。
2 2 3 2
(6)第①步溶于水反应的化学方程式是______________________________________________
______________________________________________________________________________。
(7)逐滴滴加NaSO 溶液使用的仪器是____________________________________________
2 2 3
________(已知:HSO 是弱酸)。
2 2 3
(8)根据上述数据测得该产品中PCl 的质量分数为______________________。(已知:HPO
3 3 3
+I+HO===HPO +2HI,I+2NaSO===2NaI+NaSO)
2 2 3 4 2 2 2 3 2 4 6