文档内容
考点 10 硫及其化合物
(核心考点精讲)
一、3年真题考点分布
考点内容 考题统计
2023浙江1月4题,3分;2022江苏卷4题,3分;2021湖南卷2
硫及其氧化物的性质及其应
题,3分;2021河北卷4题,3分;2021山东卷8题,2分;2021
用
北京卷6题,4分
2023全国新课标卷11题,6分;2022山东卷2题,2分;2022广
硫酸性质及SO 2-的检验
4 东卷5题,2分;2021全国乙卷8题,6分
2023湖南卷10题,4分;2023浙江1月5题,3分;2023全国乙
卷11题,6分;2022全国甲卷13题,6分;2022浙江6月10
不同价态含硫物质的转化
题,2分;2022湖北卷8题,3分;2021全国乙卷9题,6分;
2021天津卷4题,4分;2021辽宁卷8题;3分
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,
本考点的考查,单独命题的不多,大多结合其他元素化合物及氧化还原反应等知识,以实验题、工艺
流程题、化学反应原理综合题等形式为背景,考题注重与生产、生活实际联系,将物质的循环利用、保护
环境等观念渗透到考题中,以体现“科学态度与社会责任”的化学核心素养。
【备考策略】
1.从物质类别及价态变化角度认识硫及其化合物的性质以及相互转化;
2.对硫及其化合物的知识进行综合实验设计,能分析、解释有关实验现象,作出评价;
3.理论联系实际,关注硫及其化合物对环境产生的影响并解决实际问题。
【命题预测】
预测2024年高考会结合生产、生活实际,以硫元素及其化合物之间的转化关系为载体,考查物质的制
备、性质的探究等,高考也可能会结合绿色化学、环境保护等思想来命题,以凸显对化学学科素养“科学
态度与社会责任”的检测。
考法 1 硫的存在和性质
一、硫单质的性质及应用
资料收集整理【淘宝店铺:向阳百分百】1.硫元素的存在形态
2.硫单质的物理性质
硫单质俗称硫黄,是一种淡黄色固体;不溶于水,微溶于酒精,易溶于 CS ;有多种同素异形体,如
2
单斜硫、斜方硫等。
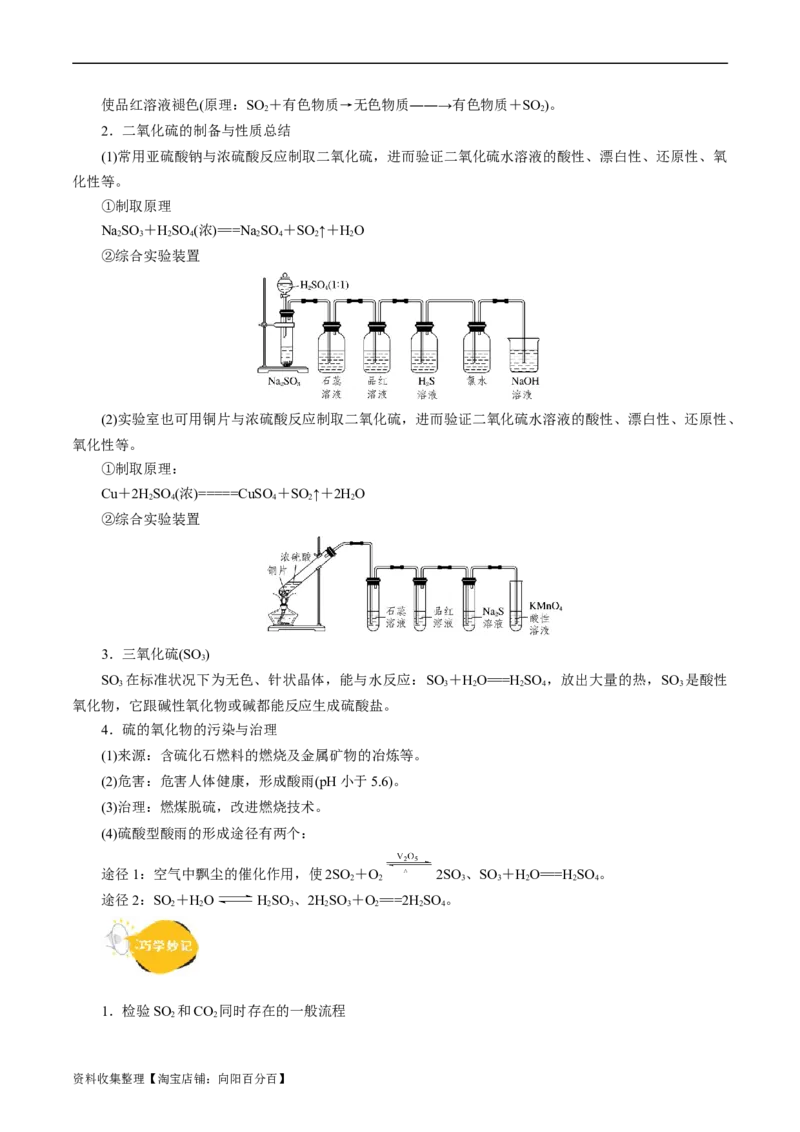
3.从化合价的角度认识硫单质的化学性质
(1)S的氧化性
S与Fe、Cu、Hg反应的化学方程式依次为Fe+S=====FeS、2Cu+S=====Cu S、S+Hg===HgS(此反
2
应适用于除去室内洒落的Hg)。
(2)S的还原性
①S与O 反应的化学方程式为S+O=====SO ,在空气中燃烧火焰为淡蓝色。
2 2 2
②与强氧化剂反应(如浓硫酸)的化学方程式为S+2HSO (浓)=====3SO ↑+2HO。
2 4 2 2
(3)S与NaOH溶液反应的化学方程式为3S+6NaOH=====2NaS+NaSO +3HO,该反应中硫既是氧
2 2 3 2
化剂,又是还原剂,此反应可用于除去试管内黏附的S。
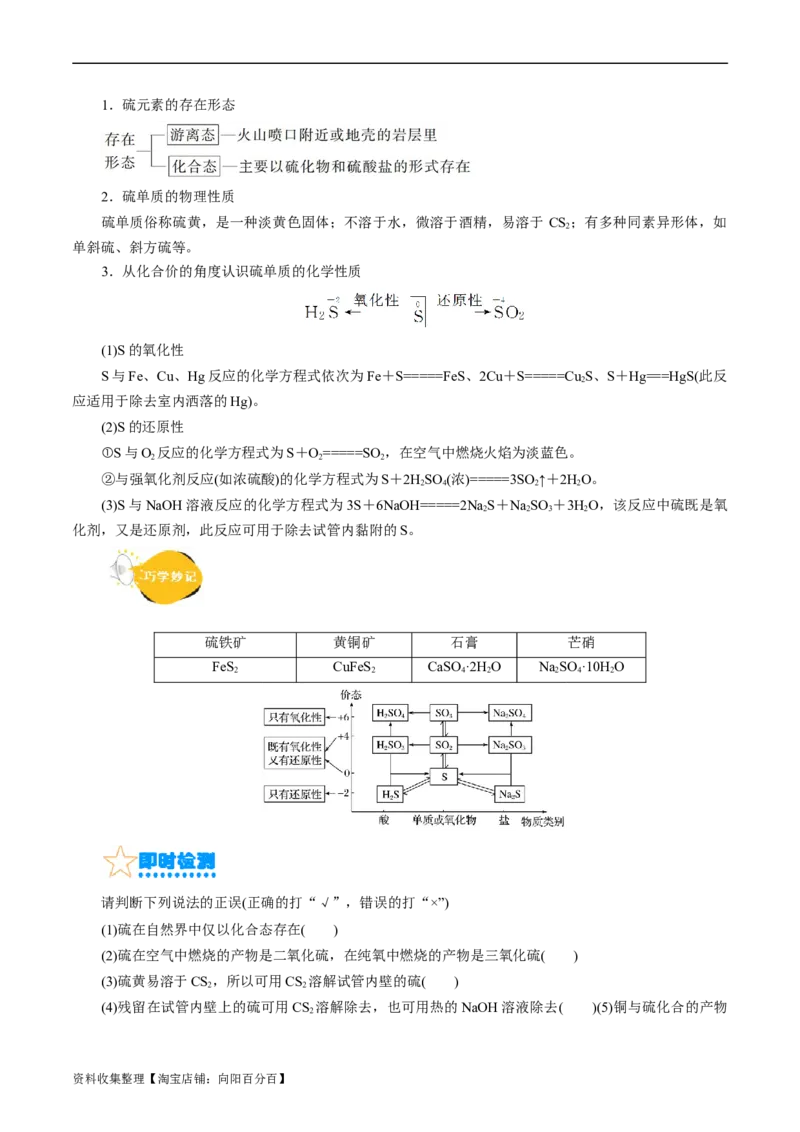
硫铁矿 黄铜矿 石膏 芒硝
FeS CuFeS CaSO·2H O NaSO ·10H O
2 2 4 2 2 4 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)硫在自然界中仅以化合态存在( )
(2)硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫( )
(3)硫黄易溶于CS,所以可用CS 溶解试管内壁的硫( )
2 2
(4)残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去( )(5)铜与硫化合的产物
2
资料收集整理【淘宝店铺:向阳百分百】是CuS( )
(6)硫单质与变价金属反应时一般生成低价态的金属硫化物( )
(7)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理( )
(8)单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO ( )
2 3
(9)富含硫黄的矿物在工业上可用于制造硫酸( )
(10)改燃煤为燃气,可以减少废气中SO 等有害物质的排放量,是治理“雾霾”等灾害天气的一种措
2
施( )
(11)向煤中加入适量石灰石,使煤燃烧产生的SO 最终生成CaSO,可减少对大气的污染( )
2 3
(12)大量燃烧化石燃料排放的废气中含SO ,从而使雨水的pH<5.6形成酸雨( )
2
(13)硫和氮的氧化物是形成酸雨的主要物质( )
答案:(1)× (2) × (3)√ (4)√ (5)× (6)√ (7)√ (8) × (9)√ (10)× (11)√ (12)√ (13) √
例1 在下列反应中硫元素只表现氧化性的是( )
A.2Al+3S=====Al S
2 3
B.S+2HSO (浓)=====2HO+3SO ↑
2 4 2 2
C.HS=====H+S
2 2
D.3S+6NaOH=====2NaS+NaSO +3HO
2 2 3 2
【答案】A
【解析】A项,该反应中S的化合价由0价变为-2价,所以只体现氧化性,正确;B项,该反应中S
的化合价由0价、+6价变为+4价,所以S体现还原性和氧化性,错误;C项,该反应中S的化合价由-
2价变为0价,所以S只体现还原性,错误;D项,该反应中S的化合价由0价变为-2价、+4价,所以
S体现氧化性和还原性,错误。
例2 已知硫有多种同素异形体,其中一种同素异形体的分子式为S。下列关于S 的说法中,正确的
8 8
是( )
A.1个这种硫分子的质量为256 g,是硫原子质量的8倍
B.在标准状况下,1mol S 的体积约为22.4 L
8
C.1mol S 和1molH O所含分子数相同
8 2
D.1 molS 与N 个HO所含原子数相同
8 A 2
【答案】C
【解析】S 在标准状态下为固体,1mol S 中含N 个S 分子和8N 个S原子。
8 8 A 8 A
对点1 据我国古代第一部药物学专著《神农本草经》记载:“石硫黄(即硫黄)能化金银钢铁,奇物”,
所得产物不可能是( )
A.Au S B.Ag S C.CuS D.FeS
2 2
资料收集整理【淘宝店铺:向阳百分百】【答案】C
【解析】S单质的氧化性比较弱,只能将变价金属氧化为低价态的物质,所以S分别与Au、Ag、Fe
反应时依次生成Au S、Ag S、FeS,选项A、B、D正确;S氧化Cu应该生成低价的Cu S,C项错误。
2 2 2
对点2 硫元素最常见和最稳定的一种同素异形体是黄色的正交α-型,1912年E.Beckmann由硫在碘
中的冰点降低法测得它含有S 分子。1891年,M.R.Engel用浓盐酸和硫代硫酸盐的饱和溶液在0℃下作用
8
首次制得了一种菱形的 -硫,后来证明含有S 分子。下列说法正确的是( )
6
A.S 和S 分子都是由S原子组成,所以它们是一种物质
6 8
B.S 和S 分子分别与铁粉反应,所得产物不同
6 8
C.S 和S 分子分别与过量的氧气反应可以得到SO
6 8 3
D.等质量的S 和S 分子分别与足量的KOH反应,消耗KOH的物质的量相同
6 8
【答案】D
【解析】A项,S 和S 分子都是由S原子组成,它们是不同的物质,互为同素异形体,故A错误;B
6 8
项,S 和S 是硫元素的不同单质,化学性质相似,因此它们分别与铁粉反应,所得产物相同,故B错误;
6 8
C项,不管氧气过量还是少量,S 和S 分子分别与氧气反应可以得到SO ,故C错误;D项,等质量的S
6 8 2 6
和S 分子,其硫原子的物质的量相同,因此它们分别与足量的 KOH反应,消耗KOH的物质的量相同,故
8
D正确。故选D。
考法 2 硫的氧化物
1.二氧化硫(SO )
2
(1)物理性质
二氧化硫是无色、有刺激性气味的有毒气体,是大气污染物之一;易溶于水,通常状况下,1体积水
溶解约40体积SO 。
2
(2)化学性质
(1)具有酸性氧化物的通性
(2)具有还原性,能被Cl、Br 、I、HO、KMnO 等氧化剂氧化。
2 2 2 2 2 4
①SO 与卤水反应:SO +X+2HO===2HX+HSO (X为Cl、Br、I)。
2 2 2 2 2 4
②使FeCl 溶液由棕黄色变为浅绿色。
3
③2SO +O 2SO 。
2 2 3
(3)具有氧化性
与HS反应:SO +2HS===3S↓+2HO。
2 2 2 2
(4)具有漂白性
资料收集整理【淘宝店铺:向阳百分百】使品红溶液褪色(原理:SO +有色物质→无色物质――→有色物质+SO )。
2 2
2.二氧化硫的制备与性质总结
(1)常用亚硫酸钠与浓硫酸反应制取二氧化硫,进而验证二氧化硫水溶液的酸性、漂白性、还原性、氧
化性等。
①制取原理
NaSO +HSO (浓)===Na SO +SO ↑+HO
2 3 2 4 2 4 2 2
②综合实验装置
(2)实验室也可用铜片与浓硫酸反应制取二氧化硫,进而验证二氧化硫水溶液的酸性、漂白性、还原性、
氧化性等。
①制取原理:
Cu+2HSO (浓)=====CuSO +SO ↑+2HO
2 4 4 2 2
②综合实验装置
3.三氧化硫(SO )
3
SO 在标准状况下为无色、针状晶体,能与水反应:SO +HO===H SO ,放出大量的热,SO 是酸性
3 3 2 2 4 3
氧化物,它跟碱性氧化物或碱都能反应生成硫酸盐。
4.硫的氧化物的污染与治理
(1)来源:含硫化石燃料的燃烧及金属矿物的冶炼等。
(2)危害:危害人体健康,形成酸雨(pH小于5.6)。
(3)治理:燃煤脱硫,改进燃烧技术。
(4)硫酸型酸雨的形成途径有两个:
途径1:空气中飘尘的催化作用,使2SO +O 2SO 、SO +HO===H SO 。
2 2 3 3 2 2 4
途径2:SO +HO HSO 、2HSO +O===2H SO 。
2 2 2 3 2 3 2 2 4
1.检验SO 和CO 同时存在的一般流程
2 2
资料收集整理【淘宝店铺:向阳百分百】SO 和CO 都能使澄清的石灰水变浑浊,检验二者同时存在的一般流程为
2 2
流程设计 检验SO 除去SO 检验SO 是否除尽⇒检验CO
2 2 2 2
选用试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清的石灰水
⇒ ⇒4
预期现象 退色 退色 不退色 变浑浊
注意:有时为简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,用较浓的酸性KMnO 溶
2 2 4
液,现象是酸性KMnO 溶液颜色变浅,但不退成无色。
4
2.三类漂白剂的区别
类型 原理 举例 特点 备注
HClO 、 NaClO 、
将有机色质内部“生色团”破 不可逆、持 无选
氧化型 Ca(ClO) 、 NaO 、
2 2 2
坏掉 久 择性
HO、O 等
2 2 3
与有机色质内部“生色团” 可逆、不持 有选
加合型 SO
2
“化合”成无色物质 久 择性
吸附
吸附型 将有色物质吸附而退色 活性炭 物理变化
色素
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)SO 有漂白性,所以SO 可使溴水退色( )
2 2
(2)SO 气体通入BaCl 溶液产生白色沉淀BaSO( )
2 2 3
(3)SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好( )
2 2
(4)SO 、漂白粉、活性炭、NaO 都能使红墨水退色,其原理相同( )
2 2 2
(5)SO 具有氧化性,可用于漂白纸浆( )
2
(6)将SO 通入溴水中证明SO 具有漂白性( )
2 2
(7)SO 和SO 都是酸性氧化物,二者的水溶液都是强酸( )
2 3
(8)标准状况下,2.24 L SO 中含有硫原子数为N ( )
3 A
(9)将SO 通入紫色石蕊溶液中先变红后褪色( )
2
(10)SO 具有氧化性,可用于漂白纸浆( )
2
(11)SO 中少量的HCl可通过饱和NaHSO 溶液除去( )
2 3
答案:(1)× (2)× (3)× (4)× (5)× (6)√ (7)× (8)× (9)× (10)× (11)√
例1 有关二氧化硫的说法错误的是( )
A.SO 通入NaSO 或NaHCO 溶液均能发生反应
2 2 3 3
B.SO 能使品红溶液褪色是因为它的氧化性
2
C.用酒精灯加热已被SO 褪色的品红溶液,可恢复原来的红色
2
资料收集整理【淘宝店铺:向阳百分百】D.SO 和O 混合后在催化剂存在的条件下加热,可生成三氧化硫
2 2
【答案】B
【解析】二氧化硫溶于水形成亚硫酸,亚硫酸与亚硫酸的正盐可生成酸式盐,亚硫酸的酸性比碳酸的
酸性强,故它还能与碳酸氢盐反应:SO +HO+NaSO ===2NaHSO ,SO +NaHCO ===NaHSO +CO 。
2 2 2 3 3 2 3 3 2
二氧化硫具有漂白性,它的漂白原理是由于二氧化硫和品红结合生成无色的不稳定化合物,它的漂白原理
与次氯酸的漂白原理不同。给被二氧化硫褪色的品红加热,无色不稳定的化合物分解,品红又恢复红色。
二氧化硫和氧气的反应必须在有催化剂存在的条件下加热才能进行,所以A、C、D正确。
例2 (2023·山东省威海市二模)向酸化的KI溶液中通入SO ,溶液变黄并出现浑浊,发生反应Ⅰ:
2
SO +4H++4I-=2I +S↓+2H O,继续通入SO ,溶液变为无色,发生反应Ⅱ:I+SO+2H O=SO 2-+4H++2I-。下
2 2 2 2 2 2 2 4
列说法错误的是( )
A.SO 、I 的氧化性强弱与外界条件有关
2 2
B.每生成0.1mol SO 2-,整个过程中转移0.4mol电子,同时消耗0.2mol KI
4
C.该过程的总反应为:3SO +2H O=2SO 2-+S↓+4H+
2 2 4
D.该反应过程中KI作催化剂
【答案】B
【解析】A项,由题干反应I可知SO 的氧化性强于I,由反应Ⅱ可知,I 的氧化性强于SO ,故可说
2 2 2 2
明SO 、I 的氧化性强弱与外界条件有关,A正确;B项,每生成0.1mol SO 2-,由反应方程式
2 2 4
I+SO+2H O=SO 2-+4H++2I-可知,转移电子为0.2mol,同时生成0.2molI-,反应0.1molI ,而生成0.1molI
2 2 2 4 2 2
则通过反应I SO+4H++4I-=2I +S↓+2H O消耗0.2molI-,转移电子数为0.2mol,故整个过程中转移0.4mol电
2 2 2
子,不消耗KI,B错误;C项,由题干信息可知,反应I+2反应Ⅱ可得该过程的总反应为:
3SO +2H O=2SO 2-+S↓+4H+,C正确;D项,由C项分析可知,该反应过程中KI作催化剂,D正确;故选
2 2 4
B。
对点1 如图所示装置可用于收集SO 并验证其某些化学性质,下列说法正确的是( )
2
选项 试剂 现象 结论
A 酸性KMnO 溶液 溶液褪色 SO 有氧化性
4 2
B 品红溶液 溶液褪色 SO 有漂白性
2
C NaOH溶液 无明显现象 SO 与NaOH溶液不反应
2
D 紫色石蕊试液 溶液变红色后不褪色 SO 有酸性,没有漂白性
2
【答案】B
资料收集整理【淘宝店铺:向阳百分百】