文档内容
【基础知识】原电池 化学电源
考点三 化学电源及工作原理
【必备知识】
1.分类
一次电池:一次电池就是放电之后不可再充电的电池。常见的一次电池有锌锰干电池、锌银电池。
放电
二次电池:二次电池又称可充电电池或蓄电池。充电电池中能量的转化关系是:化学能 充电 电能,常
见的二次电池有铅蓄电池、镉镍电池、锂离子电池等蓄电池等
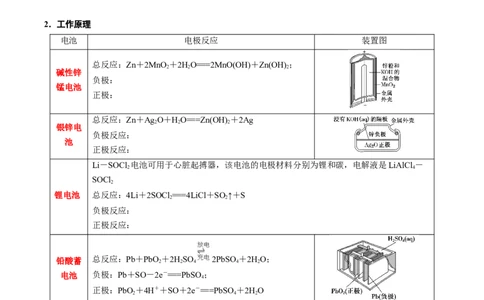
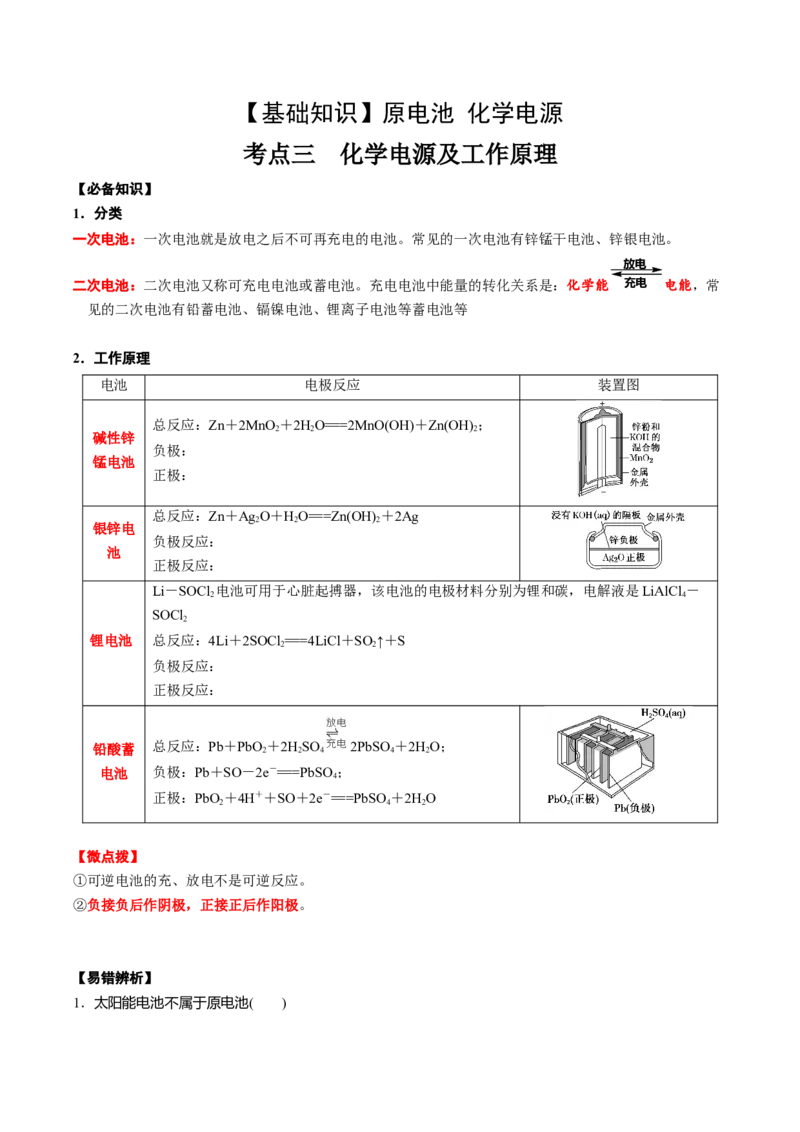
2.工作原理
电池 电极反应 装置图
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH) ;
2 2 2
碱性锌
负极:
锰电池
正极:
总反应:Zn+Ag O+HO===Zn(OH) +2Ag
2 2 2
银锌电
负极反应:
池
正极反应:
Li-SOCl 电池可用于心脏起搏器,该电池的电极材料分别为锂和碳,电解液是LiAlCl -
2 4
SOCl
2
锂电池 总反应:4Li+2SOCl ===4LiCl+SO ↑+S
2 2
负极反应:
正极反应:
铅酸蓄 总反应:Pb+PbO +2HSO 2PbSO +2HO;
2 2 4 4 2
电池 负极:Pb+SO-2e-===PbSO;
4
正极:PbO +4H++SO+2e-===PbSO+2HO
2 4 2
【微点拨】
①可逆电池的充、放电不是可逆反应。
②负接负后作阴极,正接正后作阳极。
【易错辨析】
1.太阳能电池不属于原电池( )2.可充电电池中的放电反应和充电反应互为可逆反应( )
3.铅酸蓄电池工作时,当电路中转移0.1 mol电子时,负极增重4.8 g( )(SO 2-:96)
4
【题型突破】
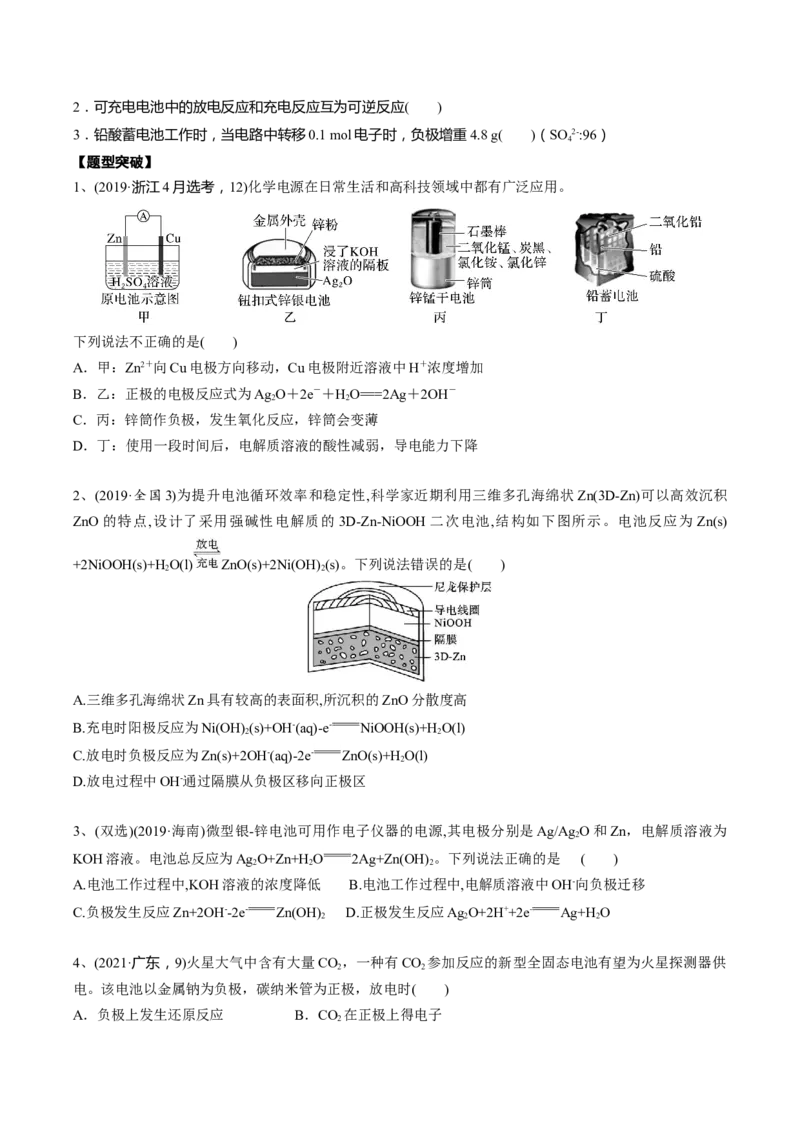
1、(2019·浙江4月选考,12)化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.乙:正极的电极反应式为Ag O+2e-+HO===2Ag+2OH-
2 2
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
2、(2019·全国3)为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D-Zn)可以高效沉积
ZnO的特点,设计了采用强碱性电解质的 3D-Zn-NiOOH二次电池,结构如下图所示。电池反应为 Zn(s)
+2NiOOH(s)+H O(l) ZnO(s)+2Ni(OH) (s)。下列说法错误的是( )
2 2
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.充电时阳极反应为Ni(OH) (s)+OH-(aq)-e- NiOOH(s)+H O(l)
2 2
C.放电时负极反应为Zn(s)+2OH-(aq)-2e- ZnO(s)+H O(l)
2
D.放电过程中OH-通过隔膜从负极区移向正极区
3、(双选)(2019·海南)微型银-锌电池可用作电子仪器的电源,其电极分别是Ag/Ag O和Zn,电解质溶液为
2
KOH溶液。电池总反应为Ag O+Zn+H O 2Ag+Zn(OH) 。下列说法正确的是 ( )
2 2 2
A.电池工作过程中,KOH溶液的浓度降低 B.电池工作过程中,电解质溶液中OH-向负极迁移
C.负极发生反应Zn+2OH--2e- Zn(OH) D.正极发生反应Ag O+2H++2e- Ag+HO
2 2 2
4、(2021·广东,9)火星大气中含有大量CO ,一种有CO 参加反应的新型全固态电池有望为火星探测器供
2 2
电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A.负极上发生还原反应 B.CO 在正极上得电子
2C.阳离子由正极移向负极 D.将电能转化为化学能
5、(2021·山东,10)以KOH溶液为离子导体,分别组成CHOH—O 、NH—O 、(CH)NNH—O 清洁燃
3 2 2 4 2 3 2 2 2
料电池,下列说法正确的是( )
A.放电过程中,K+均向负极移动 B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1 mol O 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2 L
2 2 4 2
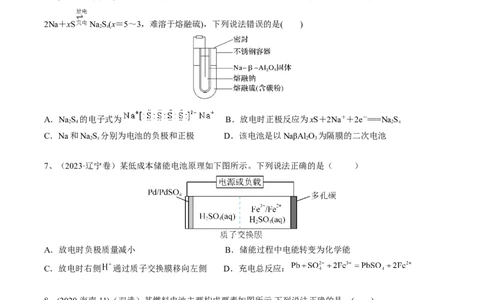
6、(2020·天津,11)熔融钠—硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为
2Na+xS NaS(x=5~3,难溶于熔融硫),下列说法错误的是( )
2 x
A.NaS 的电子式为 B.放电时正极反应为xS+2Na++2e-===Na S
2 4 2 x
C.Na和NaS 分别为电池的负极和正极 D.该电池是以NaβAl O 为隔膜的二次电池
2 x 2 3
7、(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是( )
A.放电时负极质量减小 B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧 D.充电总反应:
8、(2020·海南,11)(双选)某燃料电池主要构成要素如图所示,下列说法正确的是 ( )
A.电池可用于乙醛的制备 B.b电极为正极
C.电池工作时,a电极附近pH降低 D.a电极的反应式为O+4e-+4H+ 2HO
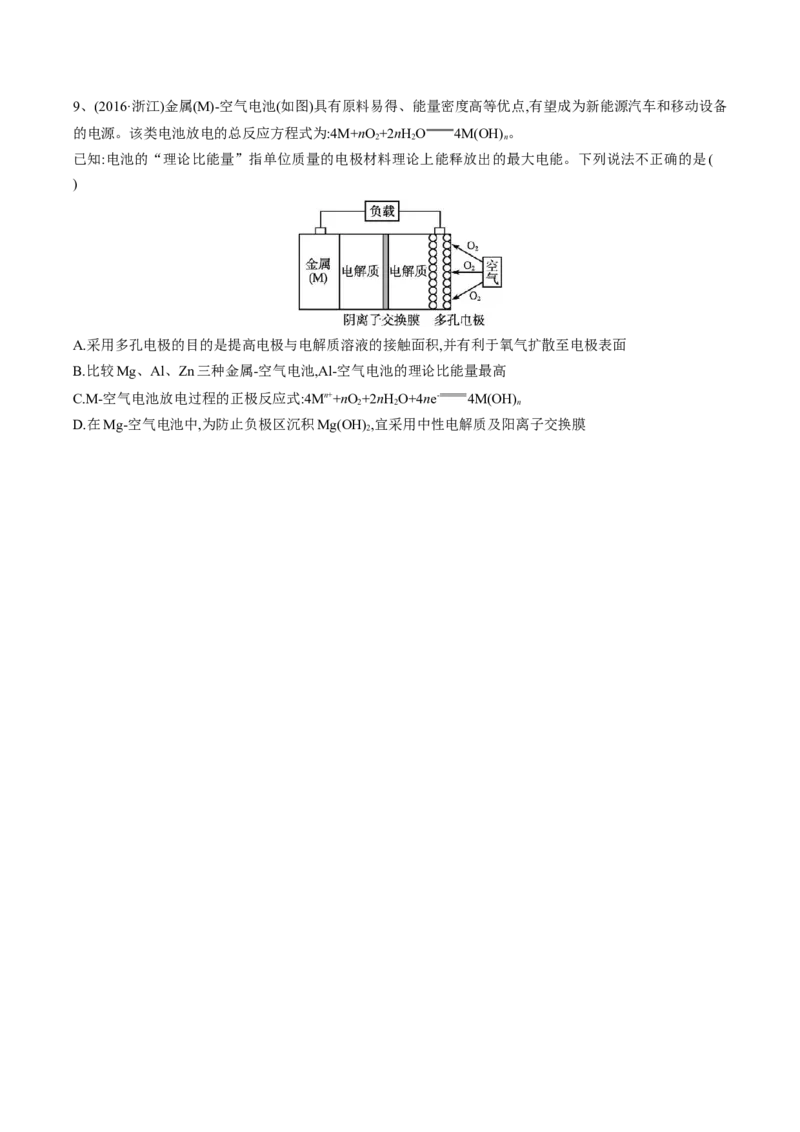
2 29、(2016·浙江)金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备
的电源。该类电池放电的总反应方程式为:4M+nO+2nHO 4M(OH) 。
2 2 n
已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是(
)
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属-空气电池,Al-空气电池的理论比能量最高
C.M-空气电池放电过程的正极反应式:4Mn++nO+2nHO+4ne- 4M(OH)
2 2 n
D.在Mg-空气电池中,为防止负极区沉积Mg(OH) ,宜采用中性电解质及阳离子交换膜
2