文档内容
考点巩固卷 07 化学反应与能量(一)
——化学反应的热效应 原电池、化学电源
考法01 反应热 焓变
考点01 化学反应的热效应 考法02 热化学方程式
(限时:20 min) 考法03 反应热的测定 燃烧热 能源
考法04 盖斯定律及应用
考法01 原电池的工作原理及应用
考法02 一次电池
考点02 原电池、化学电源
考法03 二次电池
(限时:25 min)
考法04 燃料电池
考法05 新型电源
考点01 化学反应的热效应
考法01 反应热 焓变
1.下列需要吸收热量的是( )
①Cl →2Cl
2
②2F→F
2
③SO +H O H SO
3 2 2 4
④2Na+2H O 2NaOH+H ↑
2 2
⑤KOH+CH COOH H O+CH COOK
3 2 3
高温
⑥C+H O(g) CO+H
2 2
⑦食物腐败
⑧液氨汽化A. ①⑥⑧ B. ①③⑥⑧ C. ③④⑥⑦ D. ①⑥⑦⑧
【答案】A
【解析】Cl →2Cl 需要断键,断键时吸收热量,①符合题意;2F→F 形成化学键,放出热量,②不
2 2
符 合 题 意 ; SO +H O H SO 是 放 热 反 应 , ③ 不 符 合 题 意 ;
3 2 2 4
2Na+2H O 2NaOH+H ↑ 是放热反应,④不符合题意;中和反应是放热反应,
2 2
高温
⑤不符合题意;C+H O(g) CO+H 是吸热反应,⑥符合题意;食物腐败过程中发生放热反应,
2 2
⑦不符合题意;液氨汽化会吸收大量的热,⑧符合题意。综上所述,①⑥⑧符合题意。
2.(2024·黑龙江哈尔滨六中期中)某化学反应X+Y―→Z分两步进行:①X―→M;②M+Y―→Z。其能
量变化如图所示。下列正确的是( )
A.M是总反应的催化剂
B.反应物(X和Y)的总能量低于产物(Z)的总能量
C.反应①②和总反应都是放热反应
D.总反应是原子利用率为100%的绿色化学反应
【答案】D
【解析】根据题中所给信息可知,M是反应过程中先产生又消耗掉的物质,为总反应的中间产物,A错
误;总反应为放热反应,反应物(X和Y)的总能量高于产物(Z)的总能量,B错误;反应①是吸热反应,C
错误;该反应是化合反应,原子利用率为100%,是理想的绿色化学反应,D正确。
3.CO 和CH 催化重整可制备合成气,对减缓燃料危机具有重要的意义,其反应历程示意图如下:
2 4
下列说法不正确的是( )
A.合成气的主要成分为CO和H
2
B.①→②既有碳氧键的断裂,又有碳氧键的形成
C.①→②放出能量
D.Ni在该反应中没有参与反应【答案】D
【解析】由图示可知CO 和CH 在Ni催化作用下,最终生成CO和H ,故A项正确;化学反应的过程中
2 4 2
存在反应物中键的断裂和生成物中键的形成,由图示可知①→②过程中既有碳氧键的断裂,又有碳氧键的
形成,故B项正确;①的能量总和大于②的能量总和,则①→②的过程放出能量,故 C项正确;由图示可
知CO 和CH 催化重整生成CO和H 的过程中Ni参与反应,但其质量和化学性质没有发生变化, Ni为催
2 4 2
化剂,故D项不正确。
4.H 和I 在一定条件下能发生反应:H(g)+I(g)2HI(g),1 mol H 完全反应放出a kJ热量。已知:
2 2 2 2 2
(a、b、c均大于零)
下列说法不正确的是( )
A.反应物的总能量高于生成物的总能量
B.断开1 mol H—H键和1 mol I—I键所需的能量高于断开2 mol H—I键所需的能量
C.断开2 mol H—I键所需的能量约为 kJ
D.向密闭容器中加入2 mol H 和2 mol I ,充分反应放出的热量小于2a kJ
2 2
【答案】B
【解析】已知H 和I 燃烧生成2 mol HI是一个放热反应,故反应物的总能量高于生成物的总能量,A正
2 2
确;已知H 和I 燃烧生成2 mol HI是一个放热反应,断开1 mol H—H键和1 mol I—I键所需的能量低于断
2 2
开2 mol H—I键所需的能量,B错误;根据反应热等于反应物的键能之和减去生成物的键能之和,则有-a
kJ=b kJ+c kJ-2E(H-I),则2E(H-I)=(a+b+c) kJ,断开2 mol H—I键所需的能量约为 kJ,C正确;
由于反应是一个可逆反应,向密闭容器中加入2 mol H 和2 mol I ,2 mol H 不能完全反应,故充分反应放
2 2 2
出的热量小于2a kJ,D正确。
5.化学反应的ΔH等于反应物的总键能与生成物的总键能之差。
化学键 Si—O Si—Cl H—H H—Cl Si—Si Si—C
键能/(kJ·
460 360 436 431 176 347
mol-1)
工业上高纯硅可通过下列反应制取:SiCl (g)+2H(g)=====Si(s)+4HCl(g) ΔH= kJ·mol-1。
4 2
【答案】+236
【解析】ΔH=4E(Si—Cl)+2E(H—H)-2E(Si—Si)-4E(H—Cl)=(4×360+2×436-2×176-4×431) kJ·mol-1
=+236 kJ·mol-1。
考法02 热化学方程式
6.通常人们把气态分子中1 mol化学键解离成气态原子所吸收的能量看成该化学键的键能。键能可以用
于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键吸收的能量之和与反应中形成
新化学键释放的能量之和的差。
化学键 H —H Cl—Cl H —Cl生成1 mol化学键时放出的 436 kJ 243 kJ 431 kJ
能量
根据上表中给出的数据判断,下列热化学方程式不正确的是( )
1 1
A. H (g)+ Cl (g) HCl(g) ΔH=−91.5 kJ⋅ mol−1
2 2 2 2
B. H (g)+Cl (g) 2HCl(g) ΔH=−183 kJ⋅ mol−1
2 2
1 1
C. HCl(g) H (g)+ Cl (g) ΔH=−91.5 kJ⋅ mol−1
2 2 2 2
D. 2HCl(g) H (g)+Cl (g) ΔH=+183 kJ⋅ mol−1
2 2
【答案】C
【 解 析 】 根 据 ΔH= 反 应 物 的 键 能 之 和 - 生 成 物 的 键 能 之 和 。 A项 ,
1 1
H (g)+ Cl (g) HCl(g)的
2 2 2 2
1
ΔH= ×(436 kJ⋅ mol−1+243 kJ⋅ mol−1)−431 kJ⋅ mol−1=−91.5 kJ⋅ mol−1 , 正 确 ; B项 ,
2
H (g)+Cl (g) 2HCl(g)的
2 2
ΔH=(436 kJ⋅ mol−1+243 kJ⋅ mol−1)−2×431 kJ⋅ mol−1=−183 kJ⋅ mol−1, 正 确 ; C项 ,
1 1 1 1
HCl(g) H (g)+ Cl (g)是 H (g)+ Cl (g) HCl(g) 的逆反
2 2 2 2 2 2 2 2
应 , 其 ΔH=+91.5 kJ⋅ mol−1, 错 误 ; D项 , 2HCl(g) H (g)+Cl (g)是
2 2
H (g)+Cl (g) 2HCl(g) 的逆反应,其ΔH=+183 kJ⋅ mol−1,正确。
2 2
7.(2024·齐齐哈尔高级中学模拟)已知:298 K时,相关物质的相对能量如下图所示。下列说法错误的是(
)A.CO燃烧的热化学方程式为2CO(g)+O
2
(g)⇌2CO
2
(g) ΔH=-566 kJ·mol-1
B.H 的标准燃烧热ΔH=-242 kJ·mol-1
2
C.C H 比C H 稳定
2 6 2 4
D.CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)是放热反应
【答案】B
【解析】A.CO燃烧的热化学方程式为2CO(g)+O
2
(g)⇌2CO
2
(g) ΔH=[(-393×2)-(-110×2+0)] kJ·mol
-1=-566 kJ·mol-1,A正确;B.表示H 标准燃烧热的热化学方程式为H(g)+O(g)===H O(l) ΔH=[(-
2 2 2 2
286)-(0+×0)] kJ·mol-1=-286 kJ·mol-1,B错误;C.C H 的相对能量为-84 kJ·mol-1,C H 的相对能量
2 6 2 4
为 52 kJ·mol-1,物质具有的能量越低,稳定性越强,因此 C H 比 C H 稳定,C 正确;D.CO(g)+
2 6 2 4
H
2
O(g)⇌CO
2
(g)+H
2
(g) ΔH=[(-393+0)-(-110-242)] kJ·mol-1=-41 kJ·mol-1,是放热反应,D正
确。
8.(2024·浙江杭州学军中学适应考)下列关于反应能量的说法正确的是( )
A.若反应A(g)===B(g) ΔH<0,说明物质A(g)比物质B(g)稳定,分子内共价键键能A比B大
B.若Mg(s)+CuSO (aq)===MgSO (aq)+Cu(s) ΔH=a kJ·mol-1,则a<0
4 4
C.101 kPa时,2H(g)+O(g)===2H O(g) ΔH=-Q kJ·mol-1,则H 的燃烧热为Q kJ·mol-1
2 2 2 2
D.H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则相同条件下含1 mol NaOH的氢氧化钠溶液与含
2
0.5 mol HSO 的浓硫酸混合后放出57.3 kJ的热量
2 4
【答案】B
【解析】反应A(g)===B(g) ΔH<0,焓变ΔH=生成物B(g)的能量-反应物A(g)的能量<0,所以物质A(g)
的能量比物质B(g)高,B(g)更稳定,分子内共价键键能A比B小,A错误;金属和盐发生的置换反应是放
热反应,ΔH<0,则a<0,B正确;在燃烧热的定义中,H元素的指定产物为液态水,C错误;浓硫酸溶于
水放热,二者混合放出的总热量大于57.3 kJ,D错误。
9.几种物质的能量关系如图所示。下列说法正确的是( )
A.C(s)+O(g)===CO (g)
2 2ΔH=-965.1 kJ·mol-1
B.2CO(g)+O(g)===2CO (g)
2 2
ΔH=+221.2 kJ·mol-1
C.由图可知,甲烷的燃烧热为890.3 kJ·mol-1
D.通常由元素最稳定的单质生成 1 mol纯化合物时的反应热称为该化合物的标准生成焓,由图可知,
CH(g)的标准生成焓为+74.8 kJ·mol-1
4
【答案】C
【解析】根据能量关系,无法计算出 C 和O 生成 CO 的焓变,故 A错误;根据能量关系,CO(g)+
2 2
O(g)===CO (g) ΔH=(854.5-965.1)kJ·mol-1=-110.6 kJ·mol-1,故B错误;根据图可知,甲烷的燃烧热
2 2
为890.3 kJ·mol-1,故C正确;该反应为化合反应,属于放热反应,即 CH(g)的标准生成焓为(890.3-
4
965.1)kJ·mol-1=-74.8 kJ·mol-1,故D错误。
10.根据信息书写热化学方程式。
(1)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO 用过量饱和石
2
灰水吸收可得100 g CaCO 沉淀,则乙醇燃烧的热化学方程式为____________________________。
3
(2)NaBH (s)与HO(l)反应生成NaBO (s)和氢气,在25 ℃、101 kPa下,已知每消耗3.8 g NaBH (s)放热21.6
4 2 2 4
kJ,该反应的热化学方程式是____________________________。
(3)如图是1 mol NO 和1 mol CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热
2 2 2
化学方程式:________________________________________________。
【答案】(1)C HOH(l)+3O(g)===2CO (g)+3HO(l) ΔH=-2Q kJ·mol-1
2 5 2 2 2
(2)NaBH (s)+2HO(l)===NaBO (s)+4H(g) ΔH=-216 kJ·mol-1
4 2 2 2
(3)NO (g)+CO(g)===CO (g)+NO(g)ΔH=-234 kJ·mol-1
2 2
【解析】(1)根据碳原子守恒有:C HOH~2CO ~2CaCO 。生成100 g CaCO 沉淀,则乙醇为0.5 mol,据
2 5 2 3 3
此可写出反应的热化学方程式。(2)消耗1 mol NaBH (s)放热×38 kJ=216 kJ。(3)ΔH=(134-368)kJ·mol-1=
4
-234 kJ·mol-1。
考法03 反应热的测定 燃烧热 能源
11.某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是( )A.实验(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
D.实验(c)中若用NaOH固体测定,则测定数值偏高
【答案】D
【解析】金属与酸的反应为放热反应,氢氧化钡晶体与氯化铵固体的反应为吸热反应,中和反应为放热反
应,A错误;等质量的铝片和铝粉与盐酸反应放出的热量相同,B错误;铁的导热性良好,换用铁质搅拌
棒后会有热量损失,导致测定的数值偏低,C错误;氢氧化钠固体溶于水时放热,会使测定的数值偏高,
D正确。
12.“生物质”是指由植物或动物生命体衍生得到的物质的总称。作为人类解决能源危机重要途径之一的
“生物质能”,主要指用树木、庄稼、草类等植物直接或间接提供的能量。古老的刀耕火种、烧柴做饭、
烧炭取暖等粗放方式正在被现代科学技术所改变。下面有关生物质能的说法,不正确的是( )
A.利用生物质能就是间接利用太阳能
B.生物质能是可再生的能源
C.生物质能是解决农村能源的重要途径
D.生物质能的缺点是严重污染环境
【答案】D
【解析】生物质能具有的能量是植物光合作用形成的,故A正确;生物质能,能源取之不尽、用之不竭,
是可再生能源,故B正确;农村有丰富的生物质能,生物质能是解决农村能源的重要途径,故C正确;生
物质能是一种优良的可再生能源,可代替一部分煤、天然气等燃料,有利于改善环境、节约能源、减少污
染,故D错误。
13.下列热化学方程式中ΔH的数值表示可燃物燃烧热的是( )
A.CO(g)+O(g)===CO (g) ΔH=-283 kJ· mol-1
2 2
B.CH(g)+2O(g)===CO (g)+2HO(g) ΔH=-802.3 kJ· mol-1
4 2 2 2
C.H(g)+O(g)===H O(g) ΔH=-285.8 kJ· mol-1
2 2 2
D.H(g)+Cl(g)===2HCl(g) ΔH=-184.6 kJ· mol-1
2 2
【答案】A
【解析】A项,符合燃烧热的概念,正确;B、C项,生成物中的水是气体,属于不稳定氧化物,错误;D
项,HCl不是指定产物,不符合燃烧热的概念要求,错误。
14.一些烷烃的燃烧热如下表:
化合物 燃烧热ΔH/(kJ⋅mol−1) 化合物 燃烧热ΔH/(kJ⋅mol−1)
甲烷 −890.3 正丁烷 −2 878.0
乙烷 −1 559.8 异丁烷 −2 869.6
丙烷 −2 219.9 2−甲基丁烷 −3 531.3
下列表达正确的是( )A. 乙 烷 燃 烧 的 热 化 学 方 程 式 为
2C H (g)+7O (g) 4CO (g)+6H O(l) ΔH=−1 559.8 kJ⋅ mol−1
2 6 2 2 2
B. 稳定性:正丁烷> 异丁烷
C. 正戊烷的燃烧热ΔH<−3 531.3 kJ⋅ mol−1
D. 相同质量的烷烃,碳元素的质量分数越大,燃烧放出的热量越多
【答案】C
【解析】乙烷的燃烧热ΔH=−1 559.8 kJ⋅ mol−1,说明1 mol 乙烷完全燃烧生成二氧化碳和液态水
时 会 放 出 1 559.8 kJ 的 热 量 , 所 以 正 确 的 热 化 学 方 程 式 为
2C H (g)+7O (g) 4CO (g)+6H O(l) ΔH=−3 119.6 kJ⋅ mol−1 , A项 错
2 6 2 2 2
误;由题表中数据可知,异丁烷的燃烧热ΔH 比正丁烷的燃烧热ΔH 大,则稳定性:正丁烷< 异丁烷,
B项错误;正戊烷和2− 甲基丁烷互为同分异构体,由题表中正丁烷、异丁烷的燃烧热可知,互为同分异
构体的烷烃,支链多的燃烧放热少,则正戊烷的燃烧热ΔH<−3 531.3 kJ⋅ mol−1,C项正确;由题表
中数据可知,相同质量的烷烃,氢元素的质量分数越大,燃烧放热越多,D项错误。
15.下列说法正确的是( )
A.葡萄糖的燃烧热是2800 kJ·mol-1,则C H O(s)+3O(g)===3CO (g)+3HO(l) ΔH=-1400 kJ·mol-1
6 12 6 2 2 2
B.在一定条件下将1 mol SO 和0.5 mol O 置于密闭容器中充分反应,放出热量79.2 kJ,则反应的热化学
2 2
方程式为2SO (g)+O(g)2SO (g) ΔH=-158.4 kJ·mol-1
2 2 3
C.已知稀溶液中,H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀氨水与稀盐酸溶液反应生成1
2
mol水时放出57.3 kJ的热量
D.已知HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则稀硫酸与氢氧化钠固体反应生成1 mol水时
放出的热量为57.3 kJ
【答案】A
【解析】燃烧热是指1 mol纯物质完全燃烧放出的热量,故 mol葡萄糖燃烧放出热量1400 kJ,A正确;该
反应为可逆反应,1 mol SO 和0.5 mol O 反应生成的SO 小于1 mol,故2SO (g)+O(g)2SO (g) ΔH<
2 2 3 2 2 3
-158.4 kJ·mol-1,B错误;一水合氨为弱电解质,不完全电离,电离时吸热,故稀氨水与稀盐酸反应生成
1 mol水放出的热量小于57.3 kJ,C错误;氢氧化钠固体溶于水时放热,其与稀硫酸反应生成1 mol水放出
的热量大于57.3 kJ,D错误。
考法04 盖斯定律及应用
16.盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接
的方法测定。现有如下3个热化学方程式:①Fe O (s)+3CO(g) 2Fe(s)+3CO (g) ΔH=−24.8 kJ⋅ mol−1
2 3 2
②3Fe O (s)+CO(g) 2Fe O (s)+CO (g) ΔH=−47.2 kJ⋅ mol−1
2 3 3 4 2
③Fe O (s)+CO(g) 3FeO(s)+CO (g) ΔH=+640.5 kJ⋅ mol−1
3 4 2
则CO气体还原FeO固体得到Fe固体和CO 气体的热化学反应方程式为( )
2
A. FeO+CO Fe+CO ΔH=+11 kJ⋅ mol−1
2
B. FeO(s)+CO(g) Fe(s)+CO (g) ΔH=−22 kJ⋅ mol−1
2
C. FeO(s)+CO(g) Fe(s)+CO (g) ΔH=−218.0 kJ⋅ mol−1
2
D. FeO(s)+CO(g) Fe(s)+CO (g) ΔH=+22 kJ⋅ mol−1
2
【答案】C
①×3−②−③×2
【 解 析 】 根 据 盖 斯 定 律 , 得
6
CO(g)+FeO(s) Fe(s)+CO (g) ΔH≈−218.0 kJ⋅ mol−1 ,选C。
2
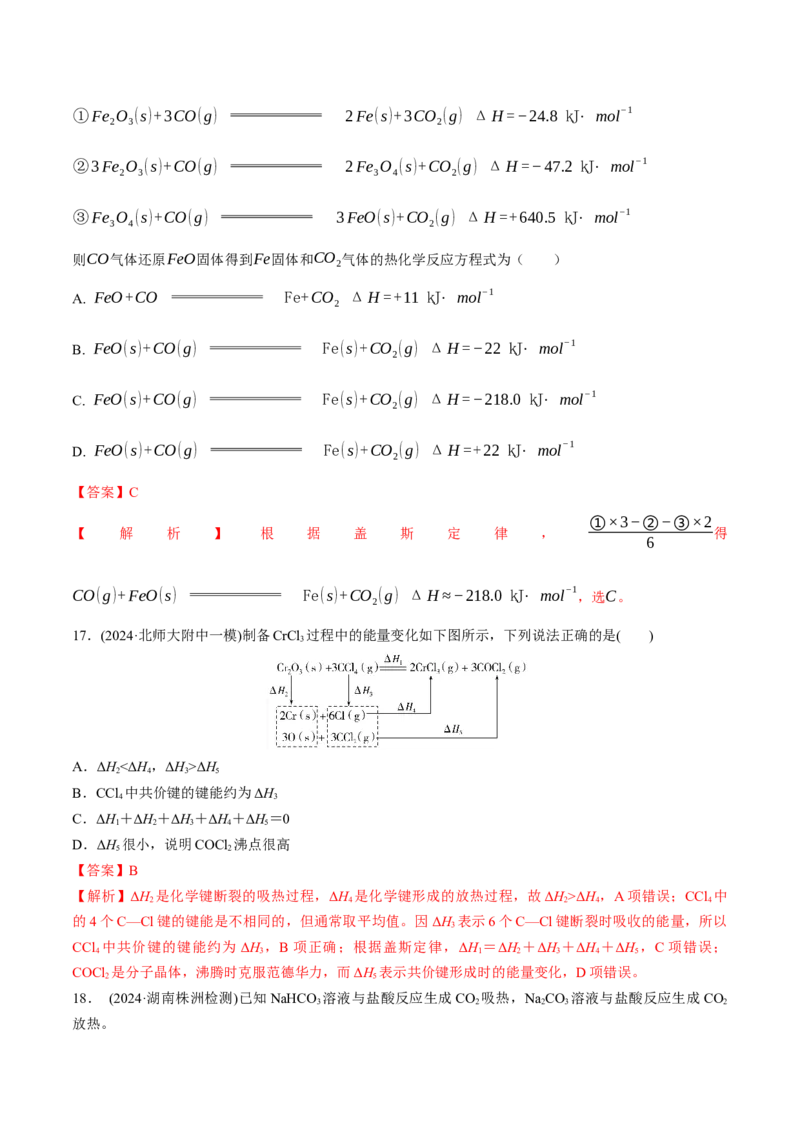
17.(2024·北师大附中一模)制备CrCl 过程中的能量变化如下图所示,下列说法正确的是( )
3
A.ΔH<ΔH,ΔH>ΔH
2 4 3 5
B.CCl 中共价键的键能约为ΔH
4 3
C.ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5
D.ΔH 很小,说明COCl 沸点很高
5 2
【答案】B
【解析】ΔH 是化学键断裂的吸热过程,ΔH 是化学键形成的放热过程,故ΔH>ΔH ,A项错误;CCl 中
2 4 2 4 4
的4个C—Cl键的键能是不相同的,但通常取平均值。因ΔH 表示6个C—Cl键断裂时吸收的能量,所以
3
CCl 中共价键的键能约为ΔH ,B项正确;根据盖斯定律,ΔH =ΔH +ΔH +ΔH +ΔH ,C项错误;
4 3 1 2 3 4 5
COCl 是分子晶体,沸腾时克服范德华力,而ΔH 表示共价键形成时的能量变化,D项错误。
2 5
18. (2024·湖南株洲检测)已知NaHCO 溶液与盐酸反应生成CO 吸热,NaCO 溶液与盐酸反应生成CO
3 2 2 3 2
放热。CO(aq)+H+(aq)===HCO(aq) ΔH
1
HCO(aq)+H+(aq)===H CO(aq) ΔH
2 3 2
HCO(aq)H O(l)+CO(g) ΔH
2 3 2 2 3
CO(g)+CO(aq)+HO(l)===2HCO(aq) ΔH
2 2 4
下列关于ΔH的判断正确的是( )
A.ΔH<0,ΔH>0
1 2
B.ΔH+ΔH>0
2 3
C.ΔH+ΔH+ΔH>0
1 2 3
D.ΔH<ΔH
1 4
【答案】B
【解析】CO(aq)+H+(aq)===HCO(aq) ΔH 和HCO(aq)+H+(aq)===H CO(aq) ΔH 均只存在化学键的形
1 2 3 2
成,形成化学键时会释放能量,所以 ΔH<0、ΔH<0,A 项错误;根据盖斯定律,将 HCO(aq)+H+
1 2
(aq)===H CO(aq) ΔH 与 HCO(aq)H O(l)+CO(g) ΔH 相加可得:HCO(aq)+H+(aq)===H O(l)+
2 3 2 2 3 2 2 3 2
CO(g) ΔH=ΔH +ΔH ,由题意可知,该反应属于吸热反应,则ΔH +ΔH>0,B项正确;根据盖斯定
2 2 3 2 3
律,将题给前三个反应相加得到:CO(aq)+2H+(aq)===H O(l)+CO(g) ΔH′=ΔH +ΔH +ΔH ,由题意可
2 2 1 2 3
知,该反应属于放热反应,则 ΔH +ΔH +ΔH<0,C 项错误;根据盖斯定律知,HCO(aq)+H+
1 2 3
(aq)===H O(l)+CO(g)的ΔH=ΔH-ΔH>0,所以ΔH>ΔH,D项错误。
2 2 1 4 1 4
19.在好氧菌和厌氧菌作用下,废液中NH能转化为N(g)和HO(l),总反应为4NH(aq)+3O(g)===2N (g)
2 2 2 2
+4H+(aq)+6HO(l) ΔH=a kJ·mol-1,示意图如下:
2
已知:反应Ⅰ为NH(aq)+2O(g)===NO(aq)+2H+(aq)+HO(l) ΔH=b kJ·mol-1
2 2 1
下列说法正确的是( )
A.两池发生的反应中氮元素的化合价均升高
B.两池中投放的废液体积相等时,NH能完全转化为N
2
C.常温常压下,反应Ⅱ中生成22.4 L N 转移的电子数为3.75N
2 A
D.反应Ⅱ为5NH(aq)+3NO(aq)===4N (g)+9HO(l)+2H+(aq) ΔH=(2a-3b)kJ·mol-1
2 2
【答案】D
【解析】反应Ⅱ在厌氧菌池中进行,则无氧气参加反应,根据盖斯定律,由总反应×2-反应Ⅰ×3可得
5NH(aq)+3NO(aq)===4N (g)+9HO(l)+2H+(aq) ΔH=(2a-3b)kJ·mol-1,所以在反应Ⅰ中氮元素的化合价
2 2
升高,在反应Ⅱ中氮元素的化合价既有升高又有降低,A项错误、D项正确;反应Ⅱ中的NO是反应Ⅰ的
产物,好氧菌池和厌氧菌池的废液体积比符合3∶5时,NH能够恰好完全转化为N ,B项错误;常温常压
2
下,气体的摩尔体积不是 22.4 L·mol-1,22.4 L 氮气的物质的量不为 1 mol,所以转移的电子数不为
3.75N ,C项错误。
A3−
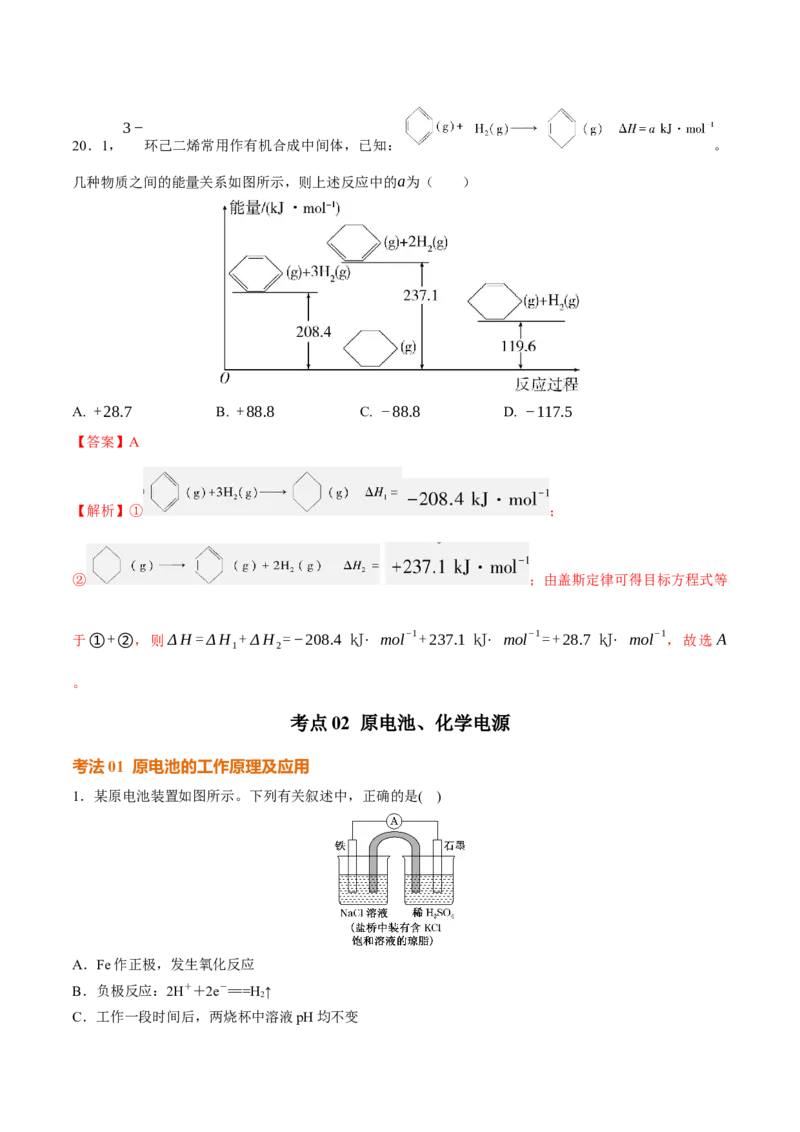
20.1, 环己二烯常用作有机合成中间体,已知: 。
几种物质之间的能量关系如图所示,则上述反应中的a为( )
A. +28.7 B. +88.8 C. −88.8 D. −117.5
【答案】A
【解析】① ;
② ;由盖斯定律可得目标方程式等
于①+②,则ΔH=ΔH +ΔH =−208.4 kJ⋅ mol−1+237.1 kJ⋅ mol−1=+28.7 kJ⋅ mol−1 ,故选A
1 2
。
考点02 原电池、化学电源
考法01 原电池的工作原理及应用
1.某原电池装置如图所示。下列有关叙述中,正确的是( )
A.Fe作正极,发生氧化反应
B.负极反应:2H++2e-===H ↑
2
C.工作一段时间后,两烧杯中溶液pH均不变D.工作一段时间后,NaCl溶液中c(Cl-)增大
【答案】D
【解析】负极是铁发生氧化反应,A错误;正极是石墨,H+在此发生还原反应,B错误;工作一段时间
后,右池中H+在石墨棒上被还原为H ,溶液的pH增大,C错误;盐桥中的Cl-移向负极,NaCl溶液中
2
c(Cl-)增大,D正确。
2.(2024·上海育才中学月考)有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验
装置
部分
a极质量减少;b b极有气体产 d极溶解;c极 电流从a极流向
实验
极质量增加 生;c极无变化 有气体产生 d极
现象
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a
C.d>a>b>c D.a>b>d>c
【答案】C
【解析】把四个实验从左到右分别编号为①②③④,则由实验①现象可知,a为负极,b为正极,金属活动
性a>b;由实验②现象可知,b可与稀硫酸反应产生H ,c不与稀硫酸反应,则金属活动性b>c;由实验③
2
现象可知,d为负极,c为正极,则金属活动性d>c;由实验④现象可知,d为负极,a为正极,则金属活动
性d>a。综上所述可知金属活动性d>a>b>c。
3.理论上能用于设计原电池的化学反应,必须是能自发进行的氧化还原反应。下列不能用于设计原电池
的化学反应是( )
A. HCl(aq)+NaOH(aq) NaCl(aq)+H O(l)
2
B. 2CH OH(l)+3O (g) 2CO (g)+4H O(l)
3 2 2 2
C. Zn(s)+CuSO (aq) ZnSO (aq)+Cu(s)
4 4
D. 2H (g)+O (g) 2H O(l)
2 2 2
【答案】A
【解析】理论上能用于设计原电池的化学反应,必须是能自发进行的氧化还原反应。HCl(aq)+NaOH(aq) NaCl(aq)+H O(l)是酸碱中和反应,故理论上不能用于设计
2
原电池,选项A符合题意。
4.(2024·广东广州一模)下列有关电化学知识的描述正确的是( )
A.锌、铜与稀硫酸组成的原电池,在工作过程中,电解质溶液的pH保持不变
B.用足量锌粒与稀硫酸反应制取H,若要增大反应速率,可以滴入几滴CuSO 溶液
2 4
C.将铁、铜用导线连接后放入浓硝酸中组成原电池,铁作负极,铜作正极,其负极反应式为 Fe-2e-
===Fe2+
D.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学
电源
【答案】B
【解析】锌、铜与稀硫酸组成的原电池,在工作过程中,H+在正极上放电生成H ,电解质溶液的pH增
2
大,A错误;用足量锌粒与稀硫酸反应制取H ,滴入几滴CuSO 溶液,Zn与Cu2+发生置换反应,锌粒表
2 4
面有Cu生成,在稀硫酸形成原电池,能增大反应速率,B正确;将铁、铜用导线连接后放入浓硝酸中组成
原电池,常温下铁遇浓硝酸发生钝化,因此铜作负极,铁作正极,其负极反应式为Cu-2e-===Cu2+,C错
误;燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为电能的化学电源,D错误。
5.镁、海水、溶解氧(石墨)可构成原电池,为水下小功率设备长时间供电,其原理如图所示。但该电
池负极存在析氢副反应和负极活性衰减等问题。下列说法不正确的是( )
A. 由于溶解氧浓度低,故需增大电极与海水的接触面积
B. 该电池正极的电极反应式为O +4H++4e− 2H O
2 2
C. 负极活性衰减的原因可能是生成的Mg(OH) 覆盖了电极
2
D. 析氢副反应可以表示为Mg+2H O Mg(OH) +H ↑
2 2 2
【答案】B
【解析】溶解氧浓度低,反应速率低,故可用增大电极与海水的接触面积的方法来提高反应速率,故A正
确;正极的电极反应式为O +2H O+4e− 4OH−,故B错误;负极的电极反应式为
2 2Mg+2OH−−2e− Mg(OH) ,生成的氢氧化镁覆盖在电极表面,阻隔电极与海水的接
2
触 , 负 极 活 性 衰 减 , 故 C 正 确 ; Mg较 活 泼 , 在 合 适 条 件 下 可 直 接 与 水 发 生 析 氢 反 应
Mg+2H O Mg(OH) +H ↑ ,故D正确。
2 2 2
考法02 一次电池
6.微型银-锌电池可用作电子仪器的电源,其电极分别是 Ag/Ag O和Zn,电解质为KOH溶液,电池总
2
反应为Ag O+Zn+HO===2Ag+Zn(OH) ,下列说法正确的是( )
2 2 2
A.电池工作过程中,KOH溶液浓度降低
B.电池工作过程中,电解液中OH-向正极迁移
C.负极发生反应Zn+2OH--2e-===Zn(OH)
2
D.正极发生反应Ag O+2H++2e-===Ag+HO
2 2
【答案】C
【解析】根据电池反应式知,Zn失电子发生氧化反应而作负极,氧化银作正极,放电时,电解质溶液中阴
离子向负极移动、阳离子向正极移动。根据电池工作原理可知,在电池工作过程中,KOH的物质的量不
变,但反应消耗水,使c(KOH)增大,A错误;电池工作过程中,电解液中 OH-向负极迁移,B错误;负
极上锌失电子发生氧化反应,电极反应式为Zn+2OH--2e-===Zn(OH) ,C正确;正极上Ag O获得电
2 2
子,发生还原反应,由于电解质溶液为碱性,不可能大量存在 H+,电极反应式为 Ag O+HO+2e-
2 2
===2Ag+2OH-,D错误。
7.(2024·新疆乌鲁木齐一模)水动力盐水灯为无电或少电的地方带来了光明,也可以在抗震救灾或者极限
情况下用于应急使用。工作时,只需要将盐水倒入灯中,就可以持续发光。该电池的工作原理如图所示,
下列叙述错误的是( )
A.合金片接LED灯的正极
B.盐水中的NaCl不参与反应
C.用铁片代替镁片,发光效果更好
D.反应一段时间后,盐水的pH增大
【答案】C
【解析】Mg是活泼金属,为负极,合金为正极,A项正确;该原电池发生的是吸氧腐蚀,正极上是 O 参
2
与反应生成OH-离子,氯化钠不参与反应,B项正确;铁的活泼性比镁弱,用铁作负极发光效果差,C项
错误;反应一段时间后,正极上发生O+4e-+2HO===4OH-,因此pH增大,D项正确。
2 2
8. 纸电池是一种有广泛应用的“软电池”,某种碱性纸电池采用薄层纸片作为载体和传导体,纸的两面
分别附着锌和二氧化锰。下列有关该纸电池的说法不合理的是( )
A.Zn为负极,发生氧化反应B.电池工作时,电子由MnO 流向Zn
2
C.正极反应:MnO +e-+HO===MnO(OH)+OH-
2 2
D.电池总反应:Zn+2MnO +2HO===Zn(OH) +2MnO(OH)
2 2 2
【答案】B
【解析】类似于碱性锌锰电池,MnO 在正极上得电子被还原生成 MnO(OH),则正极的电极反应式为
2
MnO +HO+e-===MnO(OH)+OH-,C正确;负极反应式为Zn+2OH--2e-===Zn(OH) ,结合正、负极
2 2 2
反应式及得失电子守恒可知,该电池的总反应式为Zn+2MnO +2HO===Zn(OH) +2MnO(OH),D正确。
2 2 2
9.海水电池在海洋能源领域备受关注,一种锂−海水电池构造示意图如图。下列说法错误的是( )
A. 海水起电解质溶液作用
B. N极仅发生的电极反应:2H O+2e− 2OH−+H ↑
2 2
C. 玻璃陶瓷具有传导离子和防水的功能
D. 该锂−海水电池属于一次电池
【答案】B
【解析】锂-海水电池的总反应为2Li+2H O 2LiOH+H ↑ ,M极上Li失去电子发
2 2
生氧化反应,则M极为负极,电极反应式为Li−e− Li+
,N极为正极,电极反应式为
2H O+2e− 2OH−+H ↑ ,同时氧气也可以在N 极得电子,电极反应式为
2 2
O +2H O+4e− 4OH− 。海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为
2 2
电 解 质 溶 液 , 故 A 正 确 ; 由 上 述 分 析 可 知 , N极 为 正 极 , 电 极 反 应 式 为
2H O+2e− 2OH−+H ↑ 和O +2H O+4e− 4OH− ,故B错
2 2 2 2
误;Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;该电池不可充电,属于一次电池,故D正确。
10.热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图
所示,其中作为电解质的无水LiClKCl 混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为
PbSO +2LiCl+Ca===CaCl +LiSO +Pb。下列有关说法不正确的是( )
4 2 2 4
A.负极反应式:Ca+2Cl--2e-===CaCl
2
B.放电过程中,Li+向正极移动
C.每转移0.2 mol电子,理论上生成20.7 g Pb
D.常温时,在正负极间接上电流表或检流计,指针偏转
【答案】D
【解析】Ca为原电池的负极,电极反应式为Ca+2Cl--2e-===CaCl ,故A正确;原电池中阳离子向正极
2
移动,所以放电过程中,Li+向正极移动,故B正确;根据电极反应式PbSO +2Li++2e-===LiSO +Pb,
4 2 4
可知每转移0.2 mol电子,理论上生成0.1 mol Pb,质量为20.7 g,故C正确;常温下,电解质不是熔融
态,离子不能移动,不能产生电流,因此连接电流表或检流计,指针不偏转,故D错误。
考法03 二次电池
11.(2024·湖北武汉武昌区质检)Li-O 电池比能量高,可用于汽车、航天等领域。电池反应为 2Li+
2
OLiO,放电时,下列说法不正确的是( )
2 2 2
A.Li在负极失去电子
B.O 在正极发生还原反应
2
C.阳离子由正极移向负极
D.化学能转化成电能
【答案】C
【解析】放电时为原电池,负极Li失去电子,发生氧化反应,A项正确;氧气在正极得到电子,发生还原
反应,B项正确;原电池工作时,阳离子向正极移动,即阳离子由负极移向正极,C项错误;原电池工作
时化学能转化成电能,D项正确。
12.近日,华中科技大学某课题组开发了一种可充电锌-空气/碘化物混合电池,该电池的放电过程如图所
示:下列叙述错误的是( )
A.放电时,电极B发生氧化反应
B.充电时,电极A接直流电源的正极
C.放电时,理论上每消耗65 g Zn,消耗标准状况下氧气的体积为11.2 L
D.充电时,阳极发生的电极反应之一为I--6e-+6OH-===IO+3HO
2
【答案】C
【解析】锌为活泼金属,失去电子发生氧化反应,故B为负极,A极氧气、碘酸根离子得到电子发生还原
反应,A为正极。由以上分析可知,放电时,电极B为负极,发生氧化反应,A项正确;充电时,电极A
为阳极,接直流电源的正极,B项正确;放电时,理论上每消耗65 g Zn,由于正极上碘酸根离子也会参与
反应,故消耗标准状况下氧气的体积小于 11.2 L,C项错误;充电时,阳极发生的电极反应之一为碘离子
失去电子发生氧化反应生成碘酸根离子,反应为I--6e-+6OH-===IO+3HO,D正确。
2
13.某科研团队发明了一种新型的锌离子热充电电池,可以利用人体产生的低热量充电。该电池以 Zn和
VO PC为电极材料,实现了低热量发电。放电时,VO 结合Zn2+生成ZnVO ·yHO,原理如图。下列说法
2 2 x 2 2
正确的是( )
A.分离器可以为阴离子交换膜
B.充电时,阳极电极反应式为ZnVO ·yHO+2xe-===VO+xZn2++yHO
x 2 2 2 2
C.放电时,电流从Zn极流向VO PC极
2
D.充电时,锌离子从较高温一侧移至低温一侧
【答案】D
【解析】由分析可知,分离器为阳离子交换膜,A错误;充电时,阳极电极反应式为ZnVO ·yHO-2xe-
x 2 2
===VO +xZn2++yHO,B错误;放电时,Zn为负极,VO PC极为正极,电流从VO PC极流向Zn极,C
2 2 2 2
错误;充电时,阳离子由阳极区移向阴极区,则锌离子从较高温一侧移至低温一侧,D正确。
14.LiFePO 二次电池具有安全性能高、热稳定性好等优点,应用于新能源汽车。电池反应:Li FePO +
4 1-x 4
LiC LiFePO +6C,石墨层和过渡金属氧化物为电极,离子导体由锂盐掺杂在液态的有机溶剂中形
x 6 4
成(原理如图)。下列说法错误的是( )A.放电时,电流由石墨层经外电路流向过渡金属氧化物
B.放电时,正极电极反应式:Li FePO +xLi++xe-===LiFePO
1-x 4 4
C.充电时,阴极电极反应式:xLi++6C+xe-===LiC
x 6
D.充电时,Li+向石墨层电极移动,若电路中通过1 mol 电子,质量增加7 g
【答案】A
【解析】由原理图和电池反应可知,石墨层为电池放电时的负极,过渡金属氧化物为正极,故放电时,电
流由正极流向负极,应由过渡金属氧化物流向石墨层,A错误;放电时,正极Li FePO 得电子生成
1-x 4
LiFePO ,B正确;充电时,阴极Li+得电子生成LiC ,电极反应式为xLi++6C+xe-===LiC ,C正确;
4 x 6 x 6
充电时,Li+向石墨层电极移动,若电路中通过1 mol电子,石墨层电极质量增加1 mol Li的质量,为7
g,D正确。
15.我国科学家使用更为稳定且不生长枝晶的KSn合金作负极,结合羧酸根官能化的碳纳米管(MWCNTs-
COOH)作正极,实现了高循环稳定性、低过电位的钾二氧化碳二次电池,装置如图所示,电池的总反应
为4KSn+3CO2KCO+C+4Sn。下列说法错误的是( )
2 2 3
A.放电时吸收CO,充电时释放CO
2 2
B.充电时,K+向负极移动
C.放电时,正极反应为4K++3CO+4e-===2KCO+C
2 2 3
D.充电时,阳极反应为K++Sn+e-===KSn
【答案】D
【解析】由电池总反应知,电池放电时吸收二氧化碳,充电时释放二氧化碳,A正确。充电时,为电解
池,钾离子(阳离子)向阴极(负极)移动,B正确。放电时,电池总反应中二氧化碳是氧化剂,正极反应为
“氧化剂得到电子生成还原产物”:4K++3CO +4e-===2KCO +C,C正确。充电时,阳极反应是放电
2 2 3
时正极反应的逆过程:2KCO+C-4e-===4K++3CO↑,D错误。
2 3 2
考法04 燃料电池
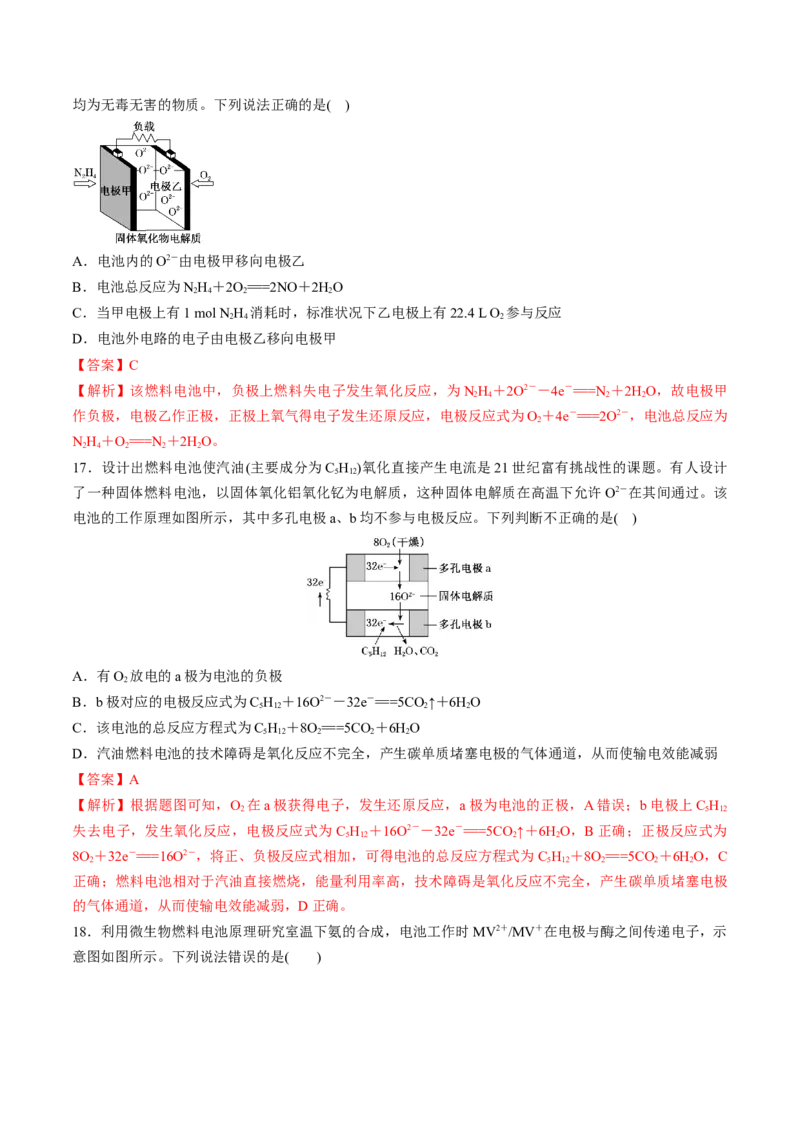
16.如图所示是一种以液态肼(N H)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该
2 4
固体氧化物电解质的工作温度高达700~900 ℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是( )
A.电池内的O2-由电极甲移向电极乙
B.电池总反应为NH+2O===2NO+2HO
2 4 2 2
C.当甲电极上有1 mol N H 消耗时,标准状况下乙电极上有22.4 L O 参与反应
2 4 2
D.电池外电路的电子由电极乙移向电极甲
【答案】C
【解析】该燃料电池中,负极上燃料失电子发生氧化反应,为NH +2O2--4e-===N +2HO,故电极甲
2 4 2 2
作负极,电极乙作正极,正极上氧气得电子发生还原反应,电极反应式为O+4e-===2O2-,电池总反应为
2
NH+O===N +2HO。
2 4 2 2 2
17.设计出燃料电池使汽油(主要成分为C H )氧化直接产生电流是21世纪富有挑战性的课题。有人设计
5 12
了一种固体燃料电池,以固体氧化铝氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过。该
电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是( )
A.有O 放电的a极为电池的负极
2
B.b极对应的电极反应式为C H +16O2--32e-===5CO ↑+6HO
5 12 2 2
C.该电池的总反应方程式为C H +8O===5CO +6HO
5 12 2 2 2
D.汽油燃料电池的技术障碍是氧化反应不完全,产生碳单质堵塞电极的气体通道,从而使输电效能减弱
【答案】A
【解析】根据题图可知,O 在a极获得电子,发生还原反应,a极为电池的正极,A错误;b电极上C H
2 5 12
失去电子,发生氧化反应,电极反应式为C H +16O2--32e-===5CO ↑+6HO,B正确;正极反应式为
5 12 2 2
8O+32e-===16O2-,将正、负极反应式相加,可得电池的总反应方程式为C H +8O===5CO +6HO,C
2 5 12 2 2 2
正确;燃料电池相对于汽油直接燃烧,能量利用率高,技术障碍是氧化反应不完全,产生碳单质堵塞电极
的气体通道,从而使输电效能减弱,D正确。
18.利用微生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示
意图如图所示。下列说法错误的是( )A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应:H+2MV2+===2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
【答案】B
【解析】由题图和题意知,电池总反应是 3H +N===2NH 。该合成氨反应在常温下进行,并形成原电池
2 2 3
产生电能,反应不需要高温、高压和催化剂,条件温和,A项正确;观察题图知,左边电极发生氧化反
应:MV+-e-===MV2+,为负极,不是阴极,B项错误;正极区N 在固氮酶作用下发生还原反应生成
2
NH ,C项正确;电池工作时,H+通过交换膜,由左侧(负极区)向右侧(正极区)迁移,D项正确。
3
19.为了强化安全管理,某油库引进一台测空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液
作电解质溶液)。下列说法不正确的是( )
A.石墨电极作正极,发生还原反应
B.铂电极的电极反应式:
C H +16HO-50e-===8CO ↑+50H+
8 18 2 2
C.H+由质子交换膜左侧向右侧迁移
D.每消耗5.6 L O ,电路中通过1 mol电子
2
【答案】D
【解析】在石墨电极,O +4e-+4H+===2HO,作正极,发生还原反应,A正确;铂电极为负极,C H
2 2 8 18
失电子生成CO 等,B正确;依据原电池原理,阳离子向正极移动,则H+由质子交换膜左侧向右侧迁移,
2
C正确;依据正极反应式,电路中通过1 mol电子时,需消耗0.25 mol O ,但未指明温度与压强,O 体积
2 2
不一定是5.6 L,D不正确。
20.一种以天然气为燃料的固体氧化物燃料电池的原理如图所示,其中YSZ为6~10%Y O 掺杂的ZrO 固
2 3 2
体电解质,下列有关叙述正确的是( )A.电子通过外电路从b极流向a极
B.b极上的电极反应式为O+2HO+4e-===4OH-
2 2
C.电路中每转移0.1 mol电子,消耗0.28 L的CH
4
D.O2-由正极通过固体电解质YSZ迁移到负极
【答案】D
【解析】该燃料电池中,通入甲烷的电极是负极、通入氧气的电极是正极,电子从a极沿导线流向b极,
故A错误;b电极上氧气得电子生成O2-,电极反应式为O +4e-===2O2-,故B错误;温度和压强未知,
2
所以无法计算甲烷体积,故C错误;电解质中阴离子向负极移动,则O2-由正极通过固体电解质YSZ迁移
到负极,故D正确。
考法05 新型电源
21. 以硝酸盐为离子导体的Na—O 电池装置与其某一电极M附近的反应机理如图所示。下列说法正确的
2
是( )
A.镍电极上发生氧化反应
B.NO是该电池的氧化剂
C.固体电解质只起到离子导体的作用
D.M的电极反应为2Na++O+2e-===Na O
2 2 2
【答案】D
【解析】金属钠为活泼金属,作负极,镍电极为正极,正极上得到电子,发生还原反应,A项错误;根据
反应机理可知,NO为该电池的催化剂,B项错误;固体电解质还能防止钠直接与氧气反应,能起到隔绝
空气的作用,C项错误;根据原理图可知,M电极的电极反应式为2Na++NO+2e-===Na O+NO,然后
2
又发生2NaO+O===2Na O 和2NO+O===2NO,总反应式为2Na++O+2e-===Na O,D项正确。
2 2 2 2 2 2 2 2
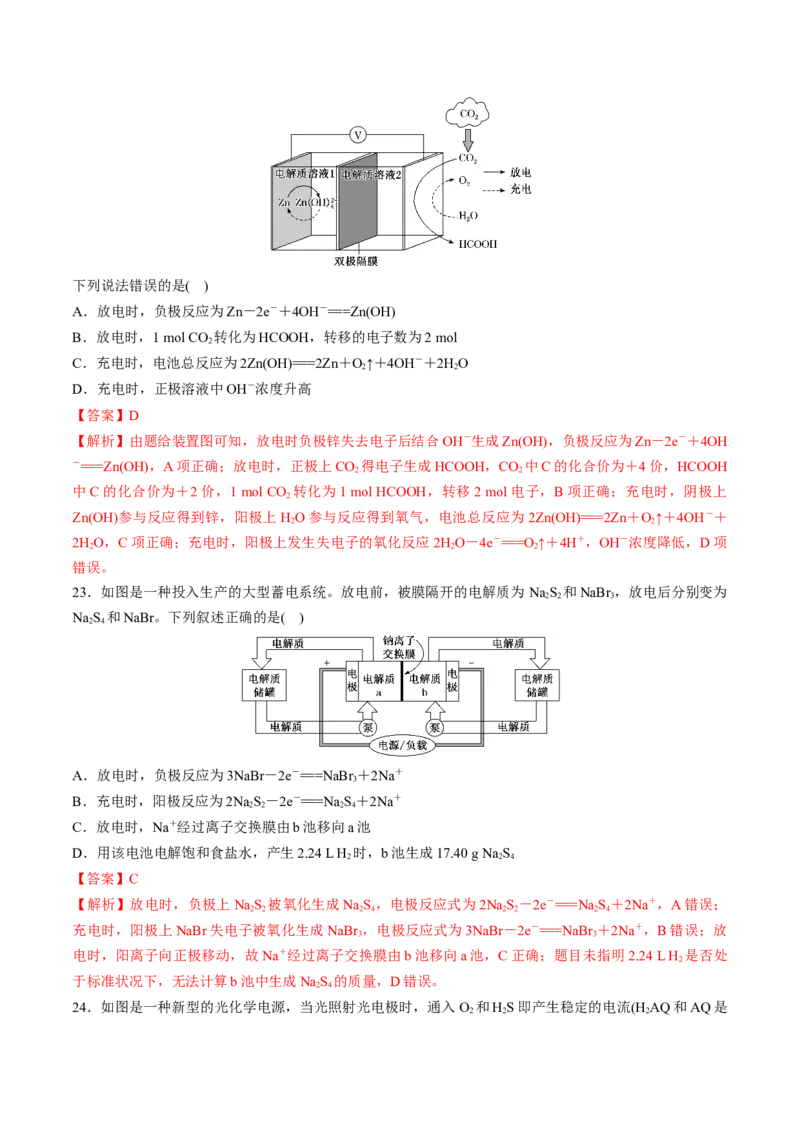
22.科学家近年发明了一种新型ZnCO 水介质电池。电池示意图如下,电极为金属锌和选择性催化材料。
2
放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
2下列说法错误的是( )
A.放电时,负极反应为Zn-2e-+4OH-===Zn(OH)
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为2Zn(OH)===2Zn+O↑+4OH-+2HO
2 2
D.充电时,正极溶液中OH-浓度升高
【答案】D
【解析】由题给装置图可知,放电时负极锌失去电子后结合OH-生成Zn(OH),负极反应为Zn-2e-+4OH
-===Zn(OH),A项正确;放电时,正极上CO 得电子生成HCOOH,CO 中C的化合价为+4价,HCOOH
2 2
中C的化合价为+2价,1 mol CO 转化为1 mol HCOOH,转移2 mol电子,B项正确;充电时,阴极上
2
Zn(OH)参与反应得到锌,阳极上HO参与反应得到氧气,电池总反应为2Zn(OH)===2Zn+O↑+4OH-+
2 2
2HO,C项正确;充电时,阳极上发生失电子的氧化反应 2HO-4e-===O ↑+4H+,OH-浓度降低,D项
2 2 2
错误。
23.如图是一种投入生产的大型蓄电系统。放电前,被膜隔开的电解质为 NaS 和NaBr ,放电后分别变为
2 2 3
NaS 和NaBr。下列叙述正确的是( )
2 4
A.放电时,负极反应为3NaBr-2e-===NaBr +2Na+
3
B.充电时,阳极反应为2NaS-2e-===Na S+2Na+
2 2 2 4
C.放电时,Na+经过离子交换膜由b池移向a池
D.用该电池电解饱和食盐水,产生2.24 L H 时,b池生成17.40 g Na S
2 2 4
【答案】C
【解析】放电时,负极上NaS 被氧化生成NaS ,电极反应式为2NaS -2e-===Na S +2Na+,A错误;
2 2 2 4 2 2 2 4
充电时,阳极上NaBr失电子被氧化生成NaBr ,电极反应式为3NaBr-2e-===NaBr +2Na+,B错误;放
3 3
电时,阳离子向正极移动,故Na+经过离子交换膜由b池移向a池,C正确;题目未指明2.24 L H 是否处
2
于标准状况下,无法计算b池中生成NaS 的质量,D错误。
2 4
24.如图是一种新型的光化学电源,当光照射光电极时,通入 O 和HS即产生稳定的电流(H AQ和AQ是
2 2 2两种有机物)。下列说法不正确的是( )
A.H+通过阳离子交换膜从正极区进入负极区
B.电源工作时发生了光能、化学能、电能间的转化
C.负极的电极反应式为2I--2e-===I
2
D.总反应为HS+O=====HO+S
2 2 2 2
【答案】A
【解析】由题意可知原电池工作时,阳离子向正极移动,故A错误;由题图可知电源工作时发生了光能、
化学能、电能间的转化,故B正确;负极的电极反应为2I--2e-===I ,故C正确;通入硫化氢和氧气,
2
分别生成硫、过氧化氢,则总反应为HS+O=====HO+S,故D正确。
2 2 2 2
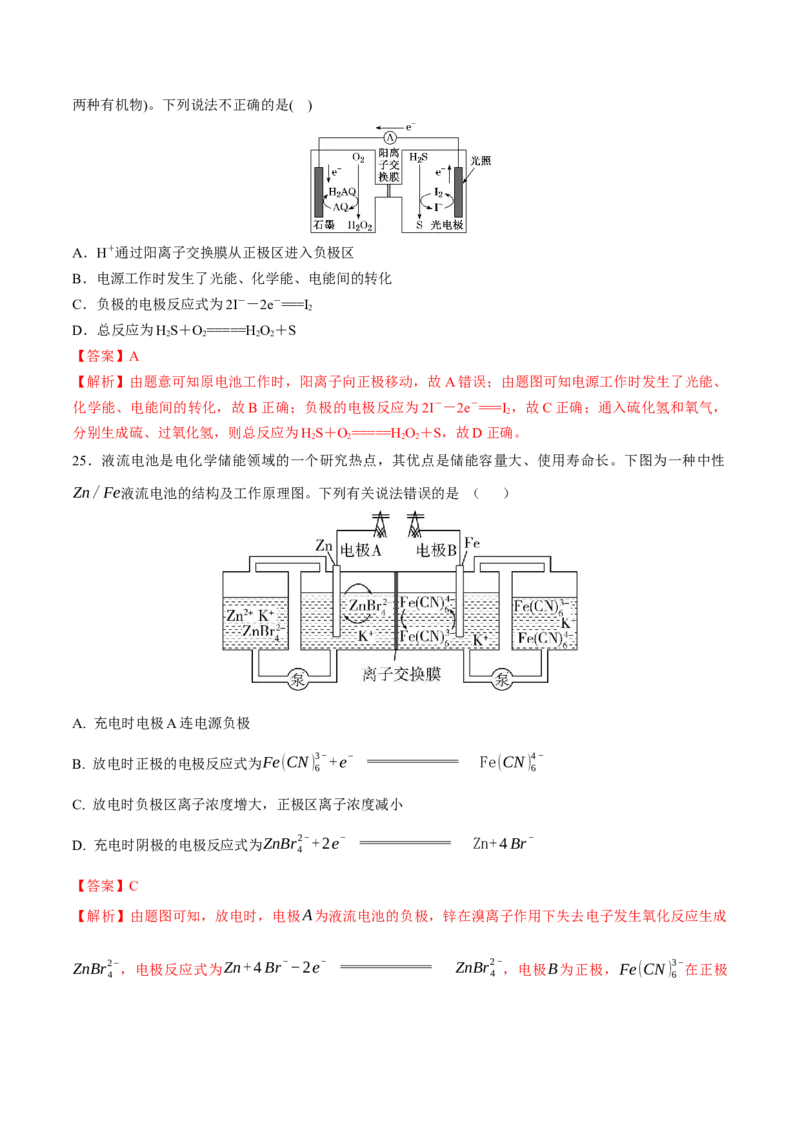
25.液流电池是电化学储能领域的一个研究热点,其优点是储能容量大、使用寿命长。下图为一种中性
Zn/Fe液流电池的结构及工作原理图。下列有关说法错误的是 ( )
A. 充电时电极A连电源负极
B. 放电时正极的电极反应式为Fe(CN) 3−+e− Fe(CN) 4−
6 6
C. 放电时负极区离子浓度增大,正极区离子浓度减小
D.
充电时阴极的电极反应式为ZnBr2−+2e− Zn+4Br−
4
【答案】C
【解析】由题图可知,放电时,电极A为液流电池的负极,锌在溴离子作用下失去电子发生氧化反应生成
ZnBr2− ,电极反应式为Zn+4Br−−2e− ZnBr2− ,电极B为正极,Fe(CN) 3− 在正极
4 4 6得到电子发生还原反应生成Fe(CN) 4− ,电极反应式为Fe(CN) 3−+e− Fe(CN) 4− ;充
6 6 6
电时,电极A连电源负极,作电解池的阴极,ZnBr2− 在阴极得到电子发生还原反应生成Zn和Br−,电极反
4
应式为ZnBr2−+2e− Zn+4Br− ,电极B与正极相连,作电解池阳极,Fe(CN) 4− 在阳
4 6
极失去电子发生氧化反应生成Fe(CN) 3− ,电极反应式为Fe(CN) 4−−e− Fe(CN) 3− 。
6 6 6
由分析可知A、B、D正确;放电时负极的电极反应式为Zn+4Br−−2e− ZnBr2−
,正
4
极的电极反应式为Fe(CN) 3−+e− Fe(CN) 4− ,负极区K+通过离子交换膜移至正极区,
6 6
负极区离子浓度减小,正极区离子浓度增大,故C错误。