文档内容
解密 06 化学反应与能量
一、单选题
1.下列反应属于吸热反应的是
A.氢气在氯气中燃烧 B.石灰石在高温下分解
C.稀硫酸与NaOH溶液反应 D.铝和氧化铁在高温下反应
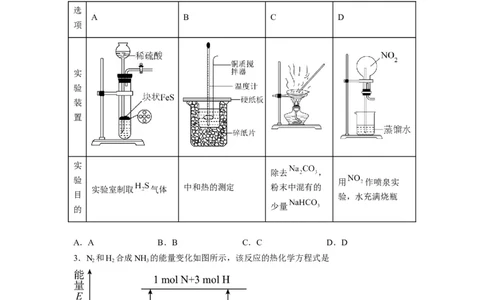
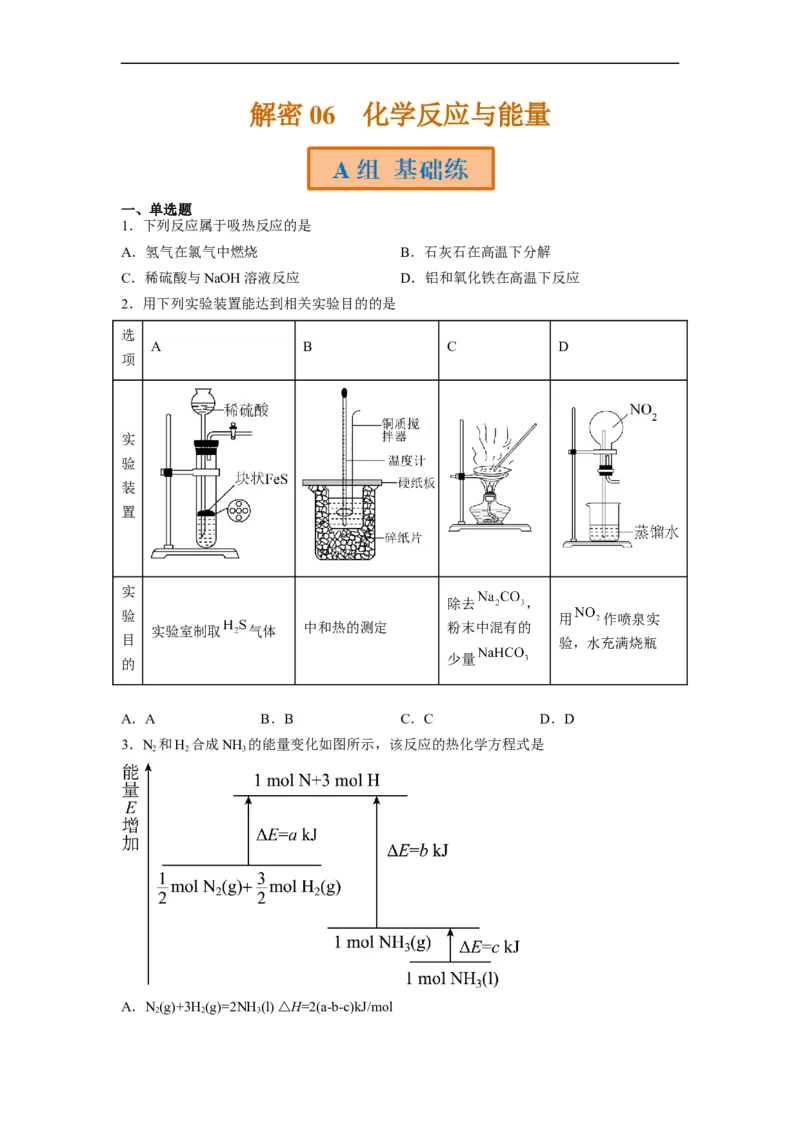
2.用下列实验装置能达到相关实验目的的是
选
A B C D
项
实
验
装
置
实
除去 ,
验 用 作喷泉实
实验室制取 气体 中和热的测定 粉末中混有的
目 验,水充满烧瓶
少量
的
A.A B.B C.C D.D
3.N 和H 合成NH 的能量变化如图所示,该反应的热化学方程式是
2 2 3
A.N(g)+3H(g)=2NH (l) △H=2(a-b-c)kJ/mol
2 2 3B.N(g)+3H(g)=2NH (g) △H=2(b-a)kJ/mol
2 2 3
C. N(g)+ H(g)=NH (l) △H=(b+c-a)kJ/mol
2 2 3
D. N(g)+ H(g)=NH (g) △H=(a+b)kJ/mol
2 2 3
4.液态CS 是一种溶剂,其燃烧热为1077 。含SeO、SO 的烟气用水吸收后,硒
2 2 2
元素全部变为单质硒。工业上制备碲用SO 还原TeCl 溶液或者以石墨为电极,电解强碱性
2 4
NaTeO 溶液。下列化学反应表示正确的是
2 3
A.用SO 水溶液吸收溴蒸气的离子方程式:
2
B.CS 燃烧的热化学方程式:CS(l)+3O (g)=CO (g)+2SO(g)
2 2 2 2 2
C.SO 还原TeCl 反应方程式:2SO +TeCl+4H O=Te+2HSO +4HCl
2 4 2 4 2 2 4
D.电解法制备碲的阴极电极方程式:
5.下列说法正确的是
A.在中性溶液中能大量共存: 、 、 、
B.含有大量 能大量共存: 、 、 、
C.已知辛烷的燃烧热为5518KJ/mol,则辛烷燃烧的热化学方程式:
,
D.已知中和热为57.3KJ/mol,则稀氨水与盐酸反应生成1mol水时放出的热量小于57.3KJ
6.下列热化学方程式中ΔH代表燃烧热的是
A.CH(g)+3/2O (g)=2HO(l)+CO(g) ΔH
4 2 2 1
B.S(s)+3/2O (g)=SO(g) ΔH
2 3 2
C.C H O(s)+6O(g)=6CO (g)+6HO(l) ΔH
6 12 6 2 2 2 3
D.2CO(g)+O(g)=2CO (g) ΔH
2 2 4
7.已知 三种气体燃烧的热化学方程式如下。下列有关说法正确的是
①
②
③
④
A.
B. 气化为 放出 热量
C.
D.乙炔燃烧的火焰温度比乙烯高,是因为其燃烧热的值比乙烯的大8.C和 在生产、生活、科技中是非常重要的燃料。已知:
①
②
下列推断正确的是
A.C(s)的摩尔燃烧焓为110.5KJ·mol-1
B.
C.
D.由②可知该反应中,反应物化学键中储存的总能量比产物化学键储存的能量高
9.周期表中ⅥA族元素及其化合物应用广泛。用硫黄熏蒸中药材的传统由来已久; 是
一种易燃的有毒气体(燃烧热为 ),是制取多种硫化物的原料;硫酸、硫酸盐
是重要化工原料;硫酰氯( )常作氯化剂或氯磺化剂。硒( )和碲( )的单质及其
化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)
为原料回收Se,以电解强碱性 溶液制备Te。下列化学反应表示正确的是
A. 的燃烧:
B. 和浓硫酸反应:
C.电解强碱性 溶液的阴极反应:
D.向 溶液中滴加足量 溶液,有白色沉淀生成:
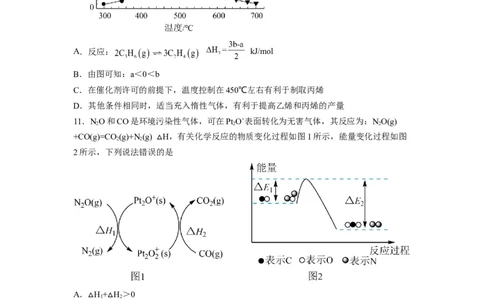
10.在丁烯(C H)催化裂解为丙烯(C H)、乙烯(C H)的反应体系中,主要发生反应的热化
4 8 3 6 2 4
学方程式为:反应I: H=a kJ/mol;反应II:
1
H=b kJ/mol。在0.1 M△Pa的恒压密闭容器中,丁烯催化裂解体系
2
中各组分平衡时的质量分△数随温度变化的关系如图所示。下列说法错误的是A.反应: kJ/mol
B.由图可知:a<0<b
C.在催化剂许可的前提下,温度控制在450℃左右有利于制取丙烯
D.其他条件相同时,适当充入惰性气体,有利于提高乙烯和丙烯的产量
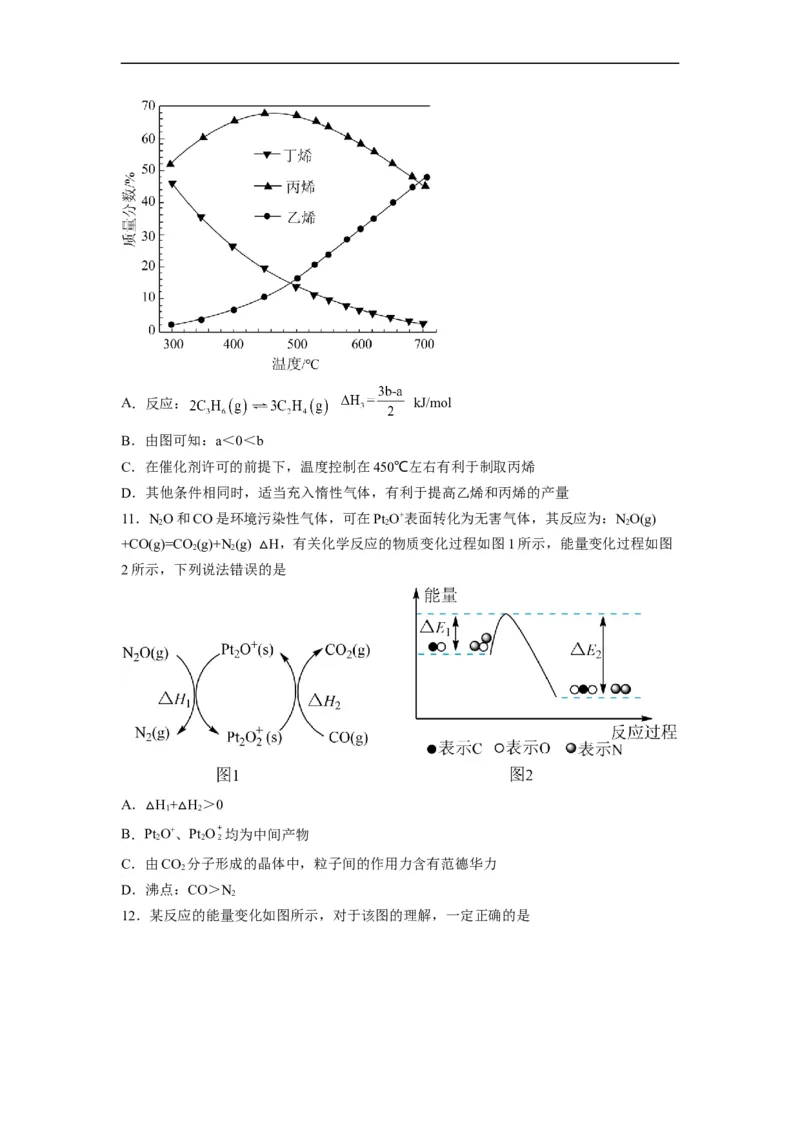
11.NO和CO是环境污染性气体,可在Pt O+表面转化为无害气体,其反应为:NO(g)
2 2 2
+CO(g)=CO (g)+N(g) H,有关化学反应的物质变化过程如图1所示,能量变化过程如图
2 2
2所示,下列说法错误的是
△
A. H+ H>0
1 2
B.P△t
2
O+、△Pt
2
O 均为中间产物
C.由CO 分子形成的晶体中,粒子间的作用力含有范德华力
2
D.沸点:CO>N
2
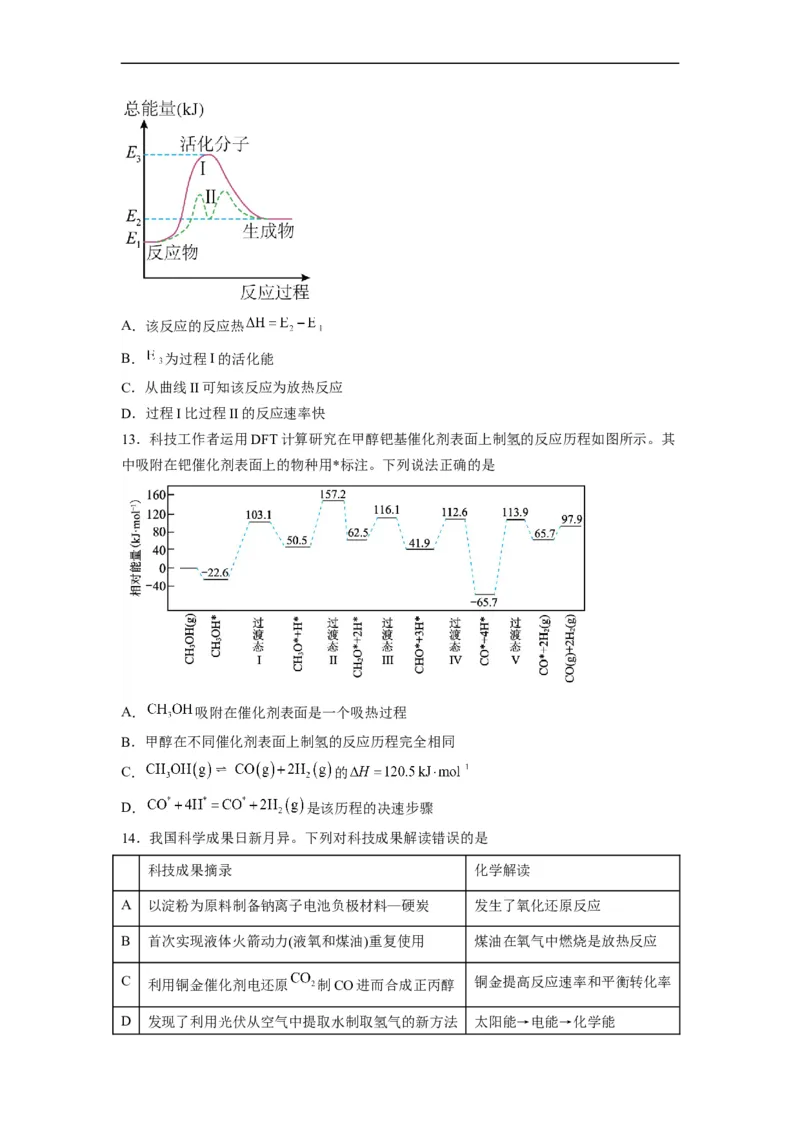
12.某反应的能量变化如图所示,对于该图的理解,一定正确的是A.该反应的反应热
B. 为过程I的活化能
C.从曲线II可知该反应为放热反应
D.过程I比过程II的反应速率快
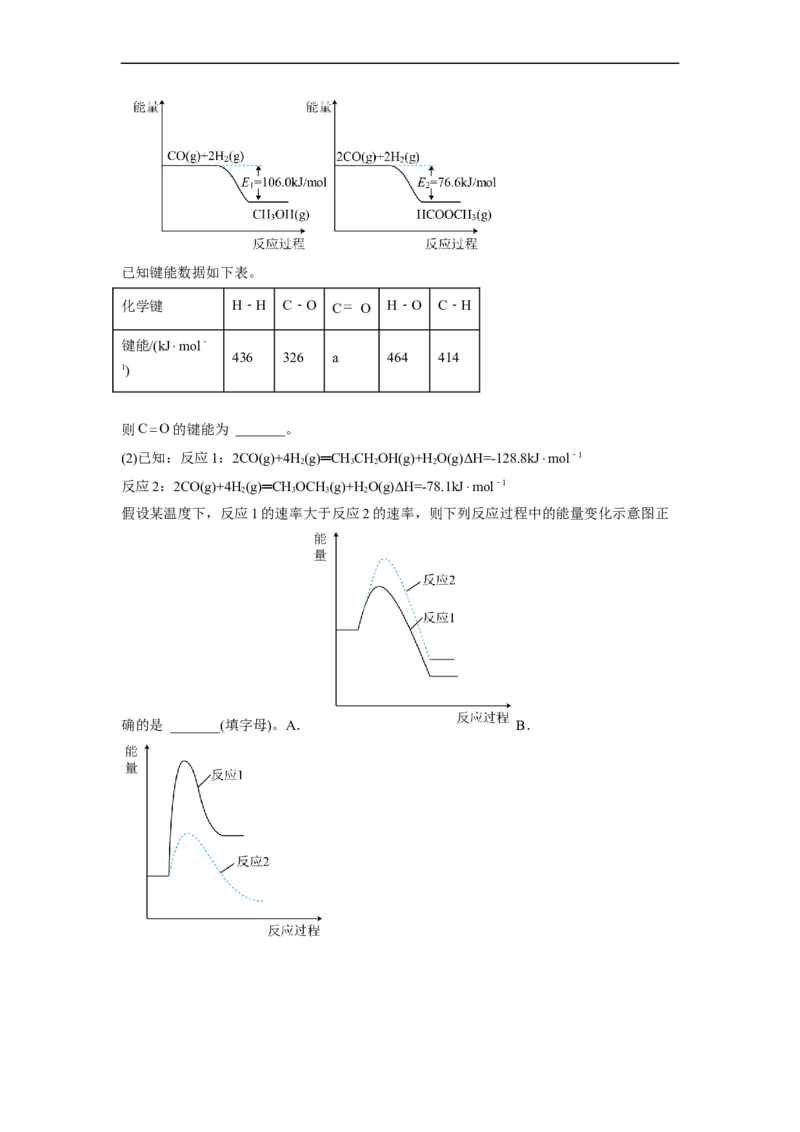
13.科技工作者运用DFT计算研究在甲醇钯基催化剂表面上制氢的反应历程如图所示。其
中吸附在钯催化剂表面上的物种用*标注。下列说法正确的是
A. 吸附在催化剂表面是一个吸热过程
B.甲醇在不同催化剂表面上制氢的反应历程完全相同
C. 的
D. 是该历程的决速步骤
14.我国科学成果日新月异。下列对科技成果解读错误的是
科技成果摘录 化学解读
A 以淀粉为原料制备钠离子电池负极材料—硬炭 发生了氧化还原反应
B 首次实现液体火箭动力(液氧和煤油)重复使用 煤油在氧气中燃烧是放热反应
C 利用铜金催化剂电还原 制CO进而合成正丙醇 铜金提高反应速率和平衡转化率
D 发现了利用光伏从空气中提取水制取氢气的新方法 太阳能→电能→化学能A.A B.B C.C D.D
15.我国正面临巨大的 减排压力。燃煤电厂是 的主要排放源,直接从燃煤烟气中
捕获 是缓解 排放危机最有效的手段。一种钙基吸收剂(主要成分为 )循环捕集
烟气中 的过程如图所示,下列说法中错误的是
A.碳酸化反应器中发生了化合反应,且为放热反应
B.生成的 附着在钙基吸收剂表面会堵塞孔隙,导致其捕集性能下降
C. 中含有 个电子
D.封存的 可以转化为甲醇等产品
二、填空题
16.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下
列问题:
(1)已知: (g)= (g)+H(g) ΔH=100.3kJ·mol−1 ①
2 1
H(g)+I (g)=2HI(g) ΔH=﹣11.0kJ·mol−1 ②
2 2 2
对于反应: (g)+I (g)= (g)+2HI(g) ③ ΔH=_______kJ·mol−1。
2 3
7近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。
因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl (s)=CuCl(s)+ Cl(g) ΔH=83kJ·mol-1
2 2 1
CuCl(s)+ O(g)=CuO(s)+ Cl(g) ΔH=-20kJ·mol-1
2 2 2CuO(s)+2HCl(g)=CuCl (s)+HO(g) ΔH=-121kJ·mol-1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2HO(g)的ΔH=_______kJ·mol-1。
2 2 2
17.回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类
化合物[Mn(L) ]( ClO ) 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能
3 4 2
量变化如图所示,已知△H= -299kJ/mol,则△H (kJ/mol )为_____________
2 1
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO 利用的
4 2 2
研究热点之一、该重整反应体系主要涉及以下反应:
(a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
(b)CO (g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
(c)CH(g) C(s)+2H(g) ∆H
4 2 3
(d)2CO(g) CO(g)+C(s) ∆H
2 4
(e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(3)用H 还原SiCl 蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,
2 4
则该反应的热化学方程式为___________________________________。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的HSO 稀溶液反应放出11.46kJ的热量。请
2 4
写出KOH的稀溶液与的HSO 稀溶液发生中和反应,表示中和热的热化学方程式为
2 4
___________________。
(5)1mol CH (g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催
4
化剂作用下,CH 可以还原SO 生成单质S(g)、HO(g)和CO,写出该反应的热化学方程式:
4 2 2 2
________________。
18.CO、CO 的回收和综合利用有利于实现“碳中和”。
2
(1)CO和H 可以合成简单有机物,已知CO、H 合成CHOH、HCOOCH 的能量变化如图
2 2 3 3
所示,计算2CHOH(g) HCOOCH (g)+2H(g)ΔH=_______。
3 3 2已知键能数据如下表。
化学键 H﹣H C﹣O C O H﹣O C﹣H
键能/(kJ⋅mol﹣
436 326 a 464 414
1)
则C O的键能为 _______。
(2)已知:反应1:2CO(g)+4H(g)═CH CHOH(g)+H O(g)ΔH=-128.8kJ⋅mol﹣1
2 3 2 2
反应2:2CO(g)+4H(g)═CH OCH (g)+HO(g)ΔH=-78.1kJ⋅mol﹣1
2 3 3 2
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正
确的是 _______(填字母)。A. B.C. D.
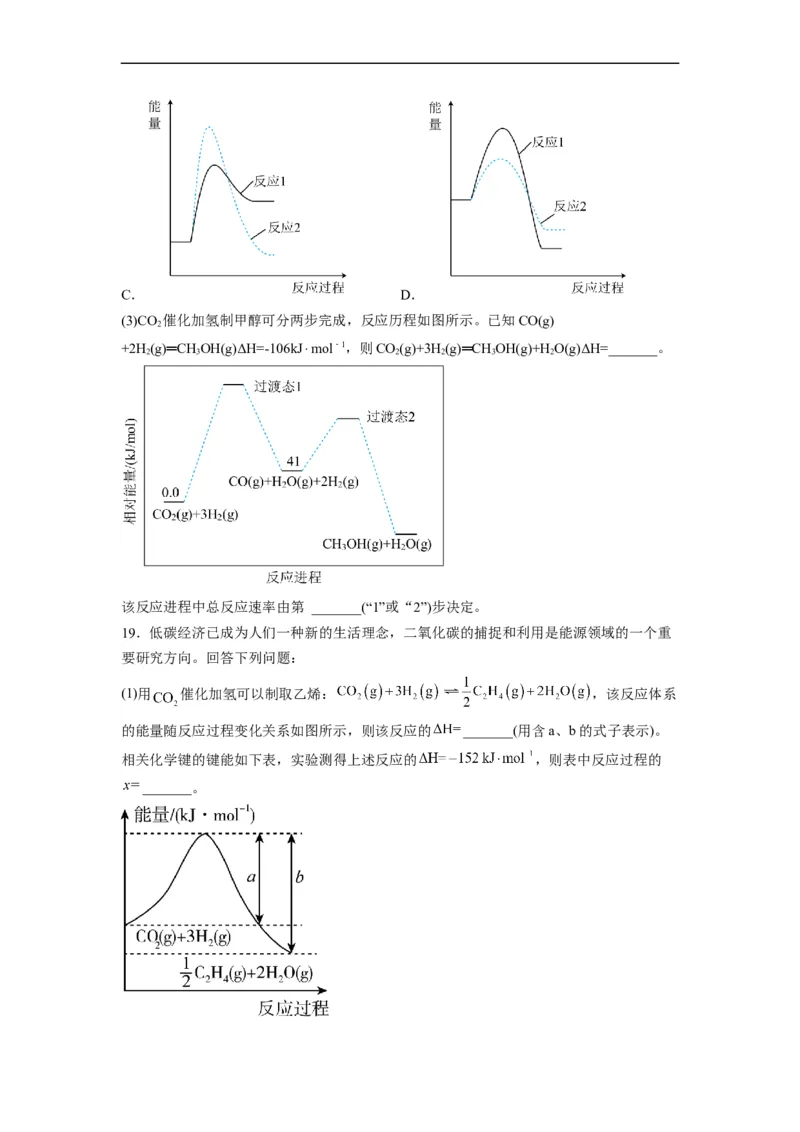
(3)CO 催化加氢制甲醇可分两步完成,反应历程如图所示。已知CO(g)
2
+2H (g)═CH OH(g)ΔH=-106kJ⋅mol﹣1,则CO(g)+3H(g)═CH OH(g)+H O(g)ΔH=_______。
2 3 2 2 3 2
该反应进程中总反应速率由第 _______(“1”或“2”)步决定。
19.低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重
要研究方向。回答下列问题:
(1)用 催化加氢可以制取乙烯: ,该反应体系
的能量随反应过程变化关系如图所示,则该反应的 _______(用含a、b的式子表示)。
相关化学键的键能如下表,实验测得上述反应的 ,则表中反应过程的
_______。化学键 C=O H-H C=C C-H H-O
键能( ) x 436 764 414 464
(2)工业上用 和 反应合成二甲醚。
已知:
则 _______ 。
(3)用 表示阿伏加德罗常数的值,在 (g)完全燃烧生成 和液态水的反应中,每有
5 个电子转移时,放出650kJ的热量。 的热值为_______。
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取C
的太阳能工艺如图。
①工艺过程中的能量转化形式为_______。
②已知“重整系统”发生的反应中 ,则 (y<8)的化学式为___,“热分解系
统”中每转移2mol电子,需消耗 __mol。Ⅰ.在50mL的圆底烧瓶中加入10.0mL正丁醇(微溶于水)、8mL冰醋酸和0.5g硫酸镍,混合
均匀后加入几粒沸石,连接装置如图所示(夹持和加热装置已略去)。
Ⅱ.反应约1h后停止加热,冷却,过滤分离出催化剂,将烧瓶中的混合物与分水器中的酯
层合并,转入分液漏斗中,用10mL饱和碳酸钠溶液洗涤至中性,再依次用饱和氯化钠溶
液、饱和氯化钙溶液洗涤,分出酯层。
Ⅲ.将分离出来的酯层倒入干燥锥形瓶中,加入1~2g无水硫酸镁,过滤,将酯层转移到干
燥的蒸馏烧瓶中,加入几粒沸石进行蒸馏,收集122~126℃的馏分。
回答下列问题:
(1)仪器A的名称为_______。
(2)写出生成乙酸正丁酯的化学方程式:_______。
(3)用10mL饱和碳酸钠溶液洗涤的目的是_______。
(4)向分液漏斗中加入饱和碳酸钠溶液洗涤时,在摇动后应进行的操作是_______。
(5)步骤Ⅲ加入无水硫酸镁的目的是_______;该步骤进行蒸馏时,应选用_______(填“直
形”“球形”或“蛇形”)冷凝管。
(6)可利用分水器中的现象判断反应已经完成,该现象是_______。
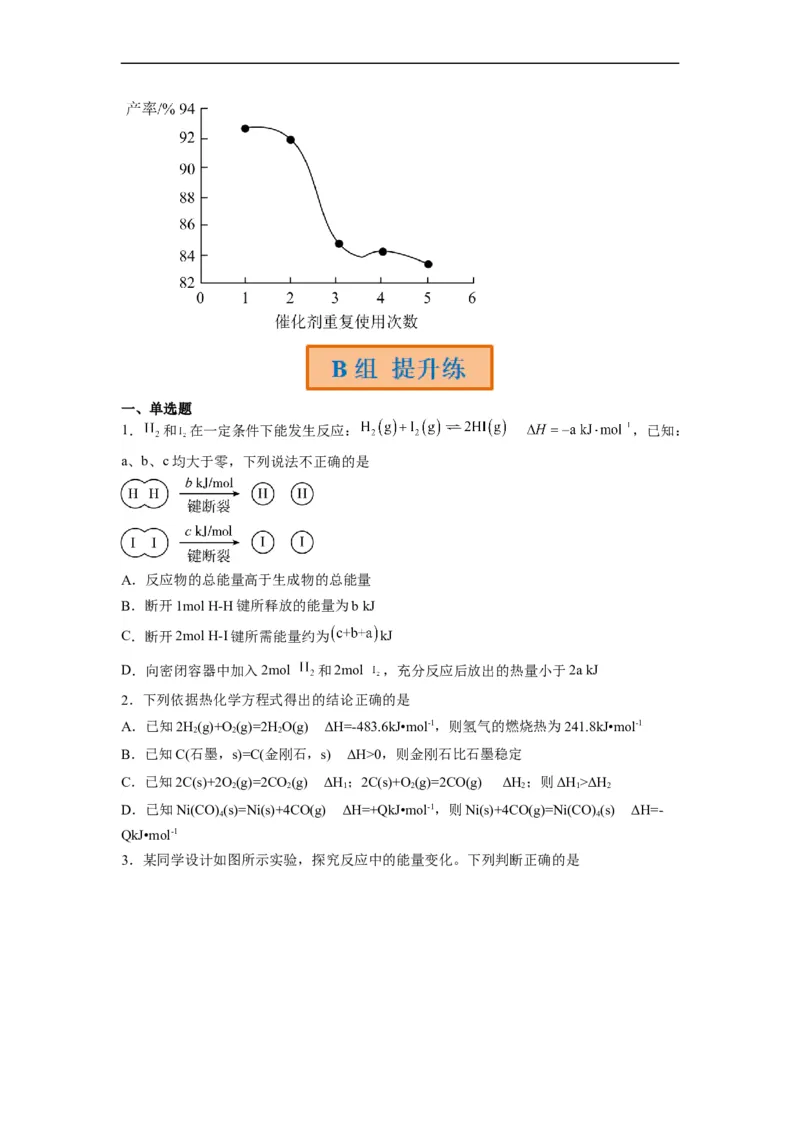
(7)本方法中用硫酸镍作催化剂的优点是硫酸镍能重复利用,催化剂重复利用次数与产率的
关系如图所示。随着重复次数的增多,产率逐渐下降的原因可能是_______。一、单选题
1. 和 在一定条件下能发生反应: ,已知:
a、b、c均大于零,下列说法不正确的是
A.反应物的总能量高于生成物的总能量
B.断开1mol H-H键所释放的能量为b kJ
C.断开2mol H-I键所需能量约为 kJ
D.向密闭容器中加入2mol 和2mol ,充分反应后放出的热量小于2a kJ
2.下列依据热化学方程式得出的结论正确的是
A.已知2H(g)+O(g)=2HO(g) ΔH=-483.6kJ•mol-1,则氢气的燃烧热为241.8kJ•mol-1
2 2 2
B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.已知2C(s)+2O(g)=2CO (g) ΔH;2C(s)+O(g)=2CO(g) ΔH;则ΔH>ΔH
2 2 1 2 2 1 2
D.已知Ni(CO) (s)=Ni(s)+4CO(g) ΔH=+QkJ•mol-1,则Ni(s)+4CO(g)=Ni(CO) (s) ΔH=-
4 4
QkJ•mol-1
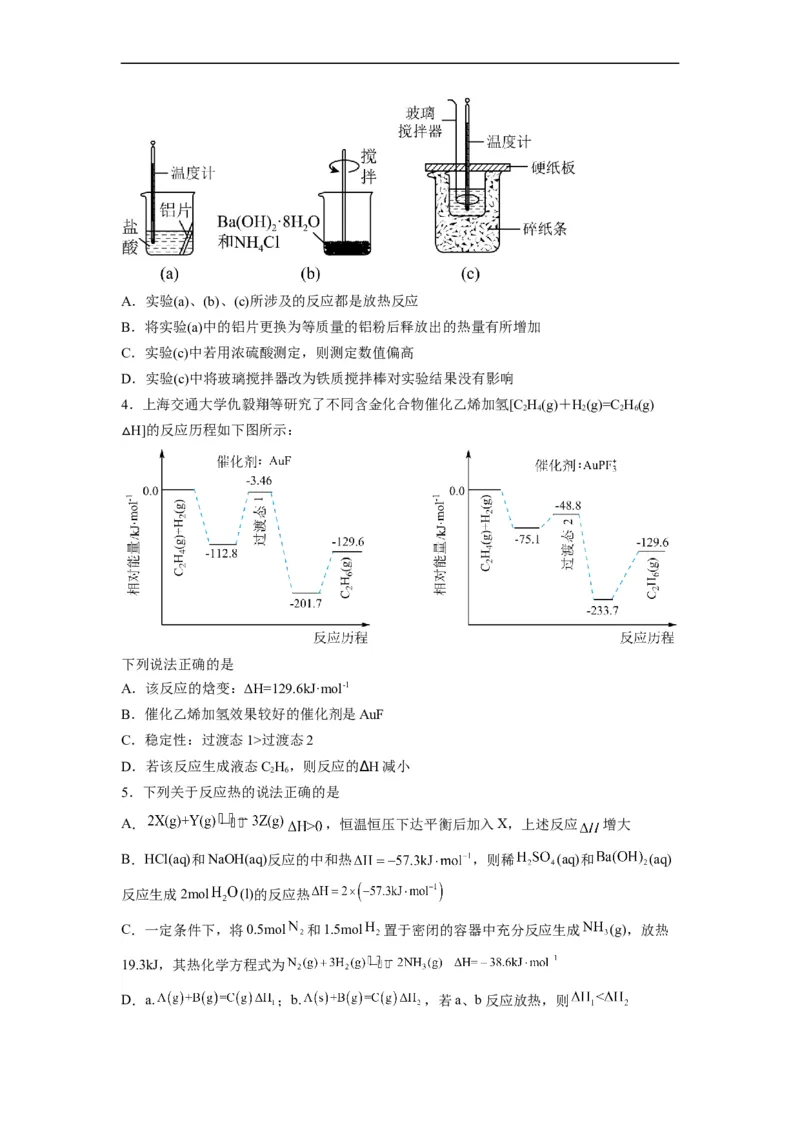
3.某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是A.实验(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中若用浓硫酸测定,则测定数值偏高
D.实验(c)中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
4.上海交通大学仇毅翔等研究了不同含金化合物催化乙烯加氢[C H(g)+H(g)=C H(g)
2 4 2 2 6
H]的反应历程如下图所示:
△
下列说法正确的是
A.该反应的焓变:ΔH=129.6kJ·mol-1
B.催化乙烯加氢效果较好的催化剂是AuF
C.稳定性:过渡态1>过渡态2
D.若该反应生成液态C H,则反应的∆H减小
2 6
5.下列关于反应热的说法正确的是
A. ,恒温恒压下达平衡后加入X,上述反应 增大
B.HCl(aq)和NaOH(aq)反应的中和热 ,则稀 (aq)和 (aq)
反应生成2mol (l)的反应热
C.一定条件下,将0.5mol 和1.5mol 置于密闭的容器中充分反应生成 (g),放热
19.3kJ,其热化学方程式为
D.a. ;b. ,若a、b反应放热,则6.下列关于中和反应反应热和燃烧热的描述中,正确的是
A.25℃,101kPa时,HSO 和Ca(OH) 反应生成1mol水放出的热量与HCl和NaOH反应
2 4 2
生成1mol水放出的热量一定相等
B.中和反应反应热的测定过程中,若隔热层隔热效果不好,会导致所测数值的绝对值偏
小
C.根据热化学方程式NH(l)+3O (g)=2NO (g)+2HO(l) H=-622kJ•mol-1,可求得NH(l)
2 4 2 2 2 2 4
的燃烧热
△
D.1gH 完全燃烧生成液态水时放出的热量即为H 的燃烧热
2 2
7.设N 为阿伏加德罗常数的值。已知反应:
A
①CH(g)+2O(g)=CO (g)+2HO(l) ΔH=a kJ·mol–1
4 2 2 2 1
②CH (g)+2O(g)=CO (g)+2HO(g) ΔH=b kJ·mol–1
4 2 2 2 2
化学键 C=O O=O C-H O-H
键能/( kJ·mol–1) 798 x 413 463
下列说法正确的是A.上表中x=
B.HO(g)=H O(l) ΔH=(a-b)kJ·mol–1
2 2
C.当有4 N 个C-H键断裂时,反应放出的热量一定为 |a| kJ
A
D.a>b且甲烷燃烧热ΔH =b kJ·mol–1
8.2022年北京冬奥会火炬采用的是碳纤维材质,燃烧的是氢能源,在奥运史上首次实现
了零碳排放。涉及氢燃烧反应的物质的汽化热(1mol纯净物由液态变为气态所需要的热量)
如下:
物质
汽化热/( ) a b c
若 的燃烧热 ,则火炬燃烧反应 的 为A.
B.
C. D.
9.根据以下3个热化学方程式:
2HS(g)+3O(g)=2SO(g)+2HO(l) H=Q kJ·mol-1
2 2 2 2 1
2H
2
S(g)+O
2
(g)=2S (s)+2H
2
O(l) ∆H=Q
2
kJ·mol-1
2H
2
S(g)+O
2
(g)=2S (s)+2H
2
O(g) ∆H=Q
3
kJ·mol-1
∆判断Q、Q、Q 三者关系正确的是
1 2 3
A.Q>Q >Q B.Q>Q >Q C.Q>Q >Q D.Q>Q >Q
1 2 3 1 3 2 3 2 1 2 1 3
10.关于反应 说法正确的是
A.反应的
B.反应中, (E表示键能,CO中为
键)
C.平衡后,保持其他条件不变,再加入少量 , 的数值不变
D.相同条件下,向容器中充入1mol 和1mol ,充分反应放出206.3kJ热量
二、填空题
11.“绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的
反应对缓解环境污染、能源危机具有重要意义。
(1)CO还原NO的反应为 。部分
化学键的键能数据如下表(CO以 键构成):
化学键
1076 945 745
①由以上数据可求得NO的键能为_______ 。
②写出两条有利于提高NO平衡转化率的措施_______。
(2)一定条件下,向某恒容密闭容器中充入 和 ,发生的反应
。
①图中能表示该反应的平衡常数K与温度T之间的变化关系曲线为_______(填“a”或
“b”),其判断依据是_______。
②若 、 ,测得在相同时间内不同温度下 的转化率如图所示,则在该时间段内,
在 时恰好达到化学平衡,此时容器内的压强与反应开始时的压强之比为_______。(3)在有氧条件下,新型催化剂M能催化 与NOx反应生成 。 与 生成 的
反应中,当生成 吋,转移的电子数为_______mol。
12.燃煤烟气中SO 和NO 是大气污染物的主要来源,脱硫脱硝技术是烟气治理技术的研
2 x
究热点。
(1)尿素/H O 溶液脱硫脱硝。尿素[CO(NH)]是一种强还原剂。60℃时在一定浓度的尿
2 2 2 2
素/H O 溶液中通入含有SO 和NO的烟气,烟气中有毒气体被一定程度吸收。尿素/H O 溶
2 2 2 2 2
液对SO 具有很高的去除效率,写出尿素和HO 溶液吸收SO ,生成硫酸铵和CO 的化学
2 2 2 2 2
方程式为____。
(2)除去烟气中的NO ,利用氢气选择性催化还原(H —SCR)是目前消除NO的理想方法。H
x 2 2
—SCR法的主反应:2NO(g)+2H (g)=N(g)+2HO(g) H
2 2 2 1
副反应:2NO(g)+H (g)=NO(g)+H O(g) H<0
2 2 2 2 △
①已知H(g)+ O(g)=HO(g) H=-241.△5kJ·mol-1
2 2 2 3
N(g)+O(g)=2NO(g) H=+180△.5kJ·mol-1
2 2 4
则 H=____kJ·mol-1。
1 △
②H —SCR在Pt—HY催化剂表面的反应机理如图所示:
△2
已知在HY载体表面发生反应的NO、O 物质的量之比为4∶1,反应中每生成1molN ,转移
2 2
的电子的物质的量为___mol。
(3)V O/炭基材料(活性炭、活性焦、活炭纤维)也可以脱硫脱硝。VO/炭基材料脱硫原理是:
2 5 2 5
SO 在炭表面被吸附,吸附态SO 在炭表面被催化氧化为SO ,SO 再转化为硫酸盐等。
2 2 3 3①VO/炭基材料脱硫时,通过红外光谱发现,脱硫开始后催化剂表面出现了VOSO 的吸收
2 5 4
峰,再通入O 后VOSO 吸收峰消失,该脱硫反应过程可描述为____。
2 4
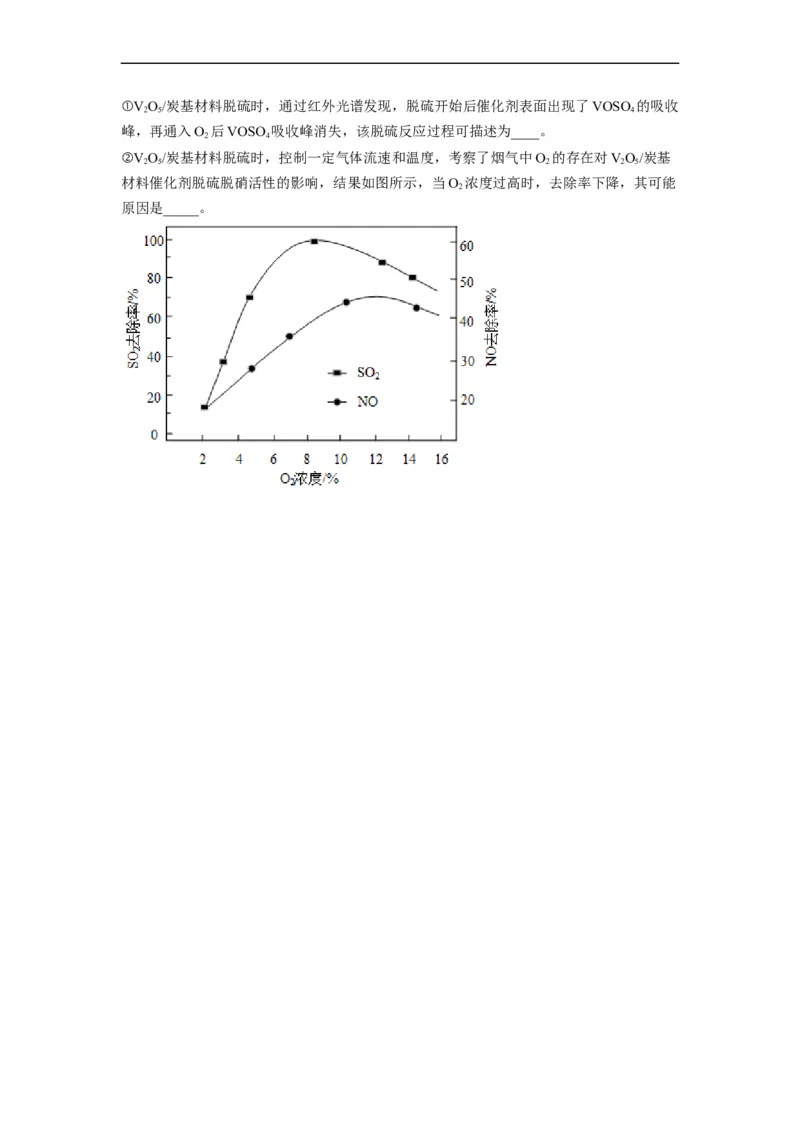
②V O/炭基材料脱硫时,控制一定气体流速和温度,考察了烟气中O 的存在对VO/炭基
2 5 2 2 5
材料催化剂脱硫脱硝活性的影响,结果如图所示,当O 浓度过高时,去除率下降,其可能
2
原因是_____。