文档内容
重难点 07 选修部分物质结构与性质选择题
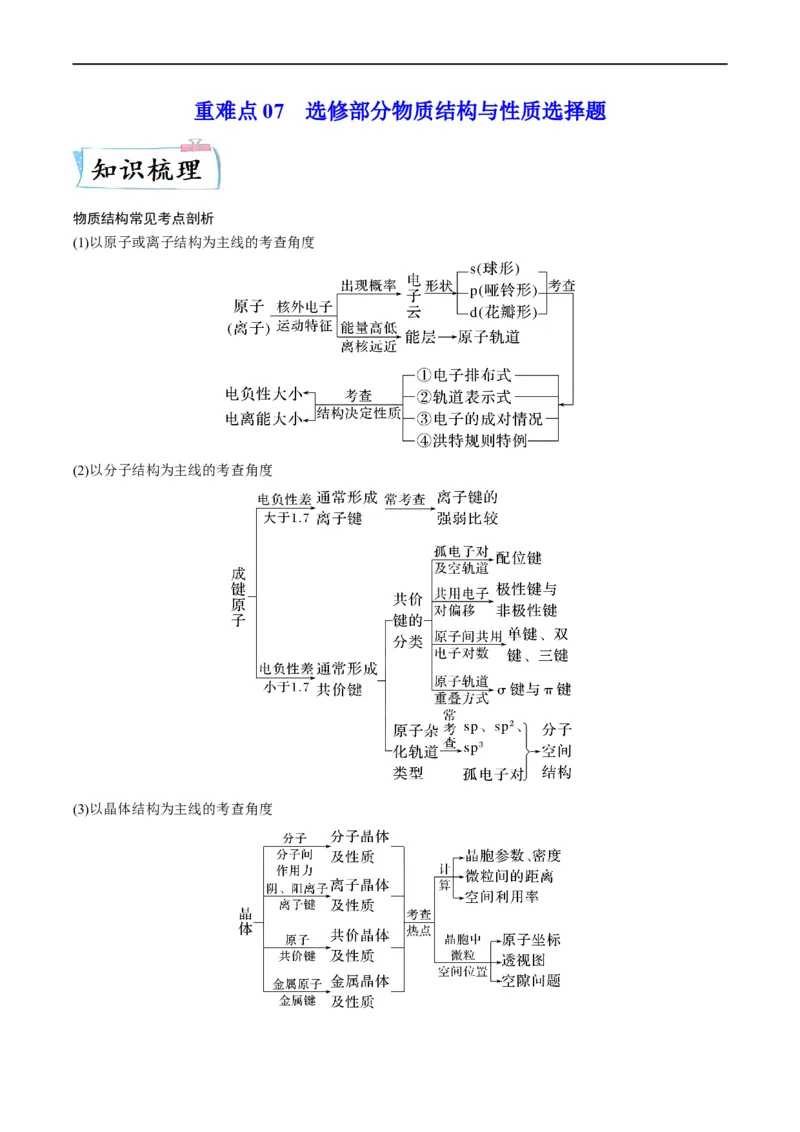
物质结构常见考点剖析
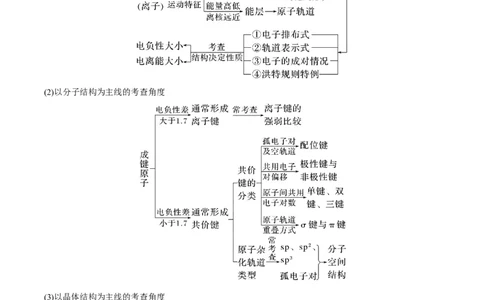
(1)以原子或离子结构为主线的考查角度
(2)以分子结构为主线的考查角度
(3)以晶体结构为主线的考查角度(建议用时:30分钟)
【真题再现】
1.(2022·湖北卷)C 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关于该碳
60
玻璃的说法错误的是
A.具有自范性 B.与C 互为同素异形体
60
C.含有sp3杂化的碳原子 D.化学性质与金刚石有差异
【答案】A
【解析】A.自范性是晶体的性质,碳玻璃为非晶态,所以没有自范性,A错误;
B.碳玻璃和C 均是由碳元素形成的不同的单质,所以是同素异形体,B正确;
60
C.碳玻璃具有高硬度,与物理性质金刚石类似,因而结构具有一定的相似性,所以含有sp3杂化的碳原子
形成化学键,C正确;
D.金刚石与碳玻璃属于同素异形体,性质差异主要表现在物理性质上,化学性质上也有着活性的差异,
D正确;
故选A。
2.(2022·湖北卷)磷酰三叠氮是一种高能分子,结构简式为OPN
。下列关于该分子的说法正确的
3 3
是
A.为非极性分子 B.立体构型为正四面体形
··
C.加热条件下会分解并放出N D.分解产物 的电子式为NMMP:O:
NPO
2 ··
【答案】C
【解析】A.磷酰三叠氮分子不是对称结构,分子中的正负电荷重心是不重合的,是极性分子,A项错误;
B.磷酰三叠氮分子含有三个P-N键及一个P=O双键,则立体构型为四面体构型,B项错误;
C.磷酰三叠氮是一种高能分子,加热条件下会分解并放出N ,C项正确;
2
D. 为共价化合物,则电子式为 ,D项错误;
NPO
答案选C。
3.(2022·山东卷)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在N-Al
键、N-Ga键。下列说法错误的是
A.GaN的熔点高于AlN B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其
相邻的原子形成3个普通共价键和1个配位键。
A.因为AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,
则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于AlN,A说错误;
B.不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正确;
C.金刚石中每个C原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故C原子
均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C说法正
确;
D.金刚石中每个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN与金
刚石互为等电子体,则其晶体中所有原子的配位数也均为4,D说法正确。
综上所述,本题选A。
4.(2022·湖北卷)Be2+和Al3+的电荷与半径之比相近,导致两元素性质相似。下列说法错误的是
A.Be2+与Al3+都能在水中与氨形成配合物
B.BeCl 和AlCl 的熔点都比MgCl 的低
2 3 2
C.BeOH 和AlOH
均可表现出弱酸性
2 3
D.Be和Al的氢化物都不能在酸中稳定存在
【答案】A
【解析】A.Al3+半径小,不能容纳6个氮原子和它配位,则不能在水中与氨形成配合物,A项错误;
B.BeCl 和AlCl 属于分子晶体,而MgCl 属于离子晶体,则BeCl 和AlCl 的熔点都比MgCl 的低,B项
2 3 2 2 3 2
正确;
C.BeOH 和AlOH
均为两性氢氧化物,则均可表现出弱酸性,C项正确;
2 3
D.Be和Al的氢化物与酸反应,生成对应的盐和氢气,则都不能在酸中稳定存在,D项正确;
答案选A。
5.(2022·湖北卷)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
A.Ca2+的配位数为6 B.与F距离最近的是K
C.该物质的化学式为KCaF
3
D.若F换为Cl-,则晶胞棱长将改变
【答案】B
【解析】A.Ca2+配位数为与其距离最近且等距离的F-的个数,如图所示,Ca2+位于体心,F-位于面心,所以Ca2+配位数为6,A正确;
2
B. 与 的最近距离为棱长的 , 与 的最近距离为棱长的1 ,所以与 距离最近的是 ,
F K 2 F Ca2+ 2 F Ca2+
B错误;
1 1
C. 位于顶点,所以 个数= 8=1,F-位于面心,F-个数= 6=3, 位于体心,所以 个数
K+ K+ 8 2 Ca2+ Ca2+
=1,综上,该物质的化学式为KCaF ,C正确;
3
D.F与Cl-半径不同,替换后晶胞棱长将改变,D正确;
故选B。
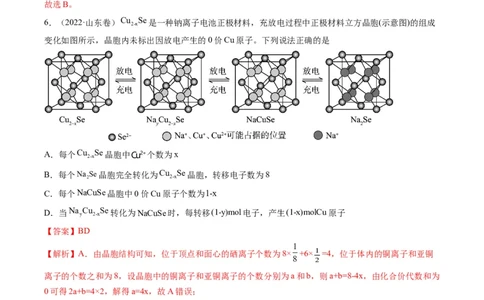
6.(2022·山东卷)Cu Se是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成
2-x
变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个Cu
2-x
Se晶胞中Cu2+个数为x
B.每个Na Se晶胞完全转化为Cu Se晶胞,转移电子数为8
2 2-x
C.每个NaCuSe晶胞中0价Cu原子个数为1-x
D.当Na
y
Cu
2-x
Se转化为NaCuSe时,每转移(1-y)mol电子,产生(1-x)molCu原子
【答案】BD
1
【解析】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6×1 =4,位于体内的铜离子和亚铜
8 2
离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代数和为
0可得2a+b=4×2,解得a=4x,故A错误;
B.由题意可知,NaSe转化为Cu Se的电极反应式为NaSe-2e-+(2-x)Cu=Cu Se+2Na+,由晶胞结构可知,
2 2-x 2 2-x
1
位于顶点和面心的硒离子个数为8× +6×1 =4,则每个晶胞中含有4个NaSe,转移电子数为8,故B正确;
8 2 2
C.由题意可知,Cu Se转化为NaCuSe的电极反应式为Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可
2-x 2-x
1
知,位于顶点和面心的硒离子个数为8× +6×1 =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数
8 2
为(4-4x),故C错误;
D.由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,所
y 2-x y 2-x
以每转移(1-y)电子,产生(1-x)mol铜,故D正确;故选BD。
【优选特训】
1.下列有关化学用语正确的是( )
A.O原子的轨道表示式为
B.氯化钠的分子式:NaCl
C.S2-的结构示意图:
D.Ca原子的电子排布式为 1s22s22p63s23p63d2
答案 C
解析 O原子的2s能级的2个电子应自旋相反,A错误;氯化钠是离子化合物,NaCl只是化学式,不是分
子式,B错误;Ca的核电荷数为20,电子排布式应是1s22s22p63s23p64s2,D错误。
2.下列叙述错误的是( )
A.所有的非金属元素都在p区
B.磷的价电子排布式为3s23p3
C.碱金属元素具有较小的电负性
D.当各原子轨道处于全充满、半充满、全空时原子较稳定
答案 A
解析 除氢元素外,所有的非金属元素都在p区,选项A错误;磷的最外层电子数为5,其价电子排布式
为3s23p3,选项B正确;碱金属易失去电子,元素的电负性很小,选项 C正确;当各原子轨道处于全充满、
半充满、全空时原子较稳定,选项D正确。
3.以下有关元素性质的说法不正确的是( )
A.具有下列价电子排布式的原子中:①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,电负性最大的是③
B.某元素X气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、
21 703,当它与氯气反应时可能生成的阳离子是X2+
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的第一电离能随原子序数增大而递
增的是④
D.具有下列电子排布式的原子中:①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2
④1s22s22p63s23p4,原子半径最大的是①
答案 A
解析 ①为铝元素,②为硅元素,③为磷元素,④为硫元素;同一周期从左到右,元素的电负性逐渐增大,
因此电负性最大的是④,A项错误;第三电离能远大于第二电离能,所以X是第ⅡA族元素,形成的阳离
子是X2+,B项正确;同一主族从上到下,元素的第一电离能逐渐减弱,①Na、K、Rb,②N、P、As,
③O、S、Se均符合此规律,同一周期从左到右,元素的第一电离能呈逐渐增大的趋势,④Na、P、Cl符
合此规律,C项正确;①为硅元素,②为氮元素,③为碳元素,④为硫元素;同一周期从左到右,原子半径逐渐减小,同一主族从上到下,原子半径逐渐增大,因此原子半径最大的为①,D项正确。
4.(2022·大连质检)下列说法正确的是( )
A.PCl 分子的空间结构是三角锥形,这是因为P原子是以sp2杂化的结果
3
B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道
C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形
D.AB 型分子的空间结构必为平面三角形
3
答案 C
解析 A项,PCl 分子的中心原子P含有3个成键电子对和1个孤电子对,为sp3杂化,空间结构为三角锥
3
形,错误;B项,能量相近的s轨道和p轨道形成杂化轨道,错误;C项,凡中心原子采取sp3杂化的分子,
其VSEPR模型都是四面体形,而分子的空间结构还与含有的孤电子对数有关,正确;D项,AB 型分子的
3
空间结构与中心原子的孤电子对数也有关,如 BF 中B原子没有孤电子对,为平面三角形,NH 中N原子
3 3
有1个孤电子对,为三角锥形,错误。
5.下列说法错误的是
A.石墨晶体中层内导电性强于层间导电性
B.基态Cr3+的最高能层中成对电子与未成对电子的数目比为8∶3
C.(CHCOO) Ni·4H O的空间构型为八面体,中心离子的配位数为6
3 2 2
D.N元素的电负性比P元素的大,可推断NCl 分子的极性比PCl 的大
3 3
【答案】D
【解析】
A.石墨晶体中层内碳原子的杂化方式为sp2杂化,碳原子间以σ键形成六元环,层内形成大π键能提供自
由移动的电子导电,而层间以分子间作用力相结合,导电能力差,则层内导电性强于层间导电性,故A正
确;
B.铬元素的原子序数为24,失去3个电子形成铬离子,基态Cr3+离子的电子排布式为1s22s22p63s23p63d3,
则最高能层N能层中成对电子与未成对电子的数目比为8∶3,故B正确;
C.由(CHCOO) Ni·4H O的空间构型为八面体,中心离子为镍离子,配位体为2个醋酸根离子和4个水分
3 2 2
子,配位数为6,故C正确;
D.氮元素的电负性大于磷元素,与氯元素的电负性差值小于磷元素,则空间构型都为三角锥形的三氯化
氮分子的极性小于三氯化磷,故D错误;
故选D。
6.下列说法错误的是
A.水分子间存在氢键,故HO比HS的稳定性强
2 2
B.原子最外层电子为ns1的元素可以形成离子化合物,也可形成共价化合物
C.N、O、S的第一电离能逐渐减小,其氢化物分子中键角逐渐减小
D.铟( In)是第五周期第ⅢA族元素,位于元素周期表p区
49
【答案】A
【解析】A.氢键是分子间的作用力,决定物质的物理性质,不会影响分子稳定性,分子稳定性是其被破坏的难易程度,和化学键有关,A项错误;
B.最外层电子为ns1的元素有: H、Li、 Na、K、Rb、Cs等,可以形成离子化合物(如NaCl) 也可形成
共价化合物(如HCl),B项正确;
C.根据同周期同主族元素性质递变规律判断,同一周期由左向右元素原子的第一电离能呈递增趋势,但
氮原子2p轨道为半充满状态,第一电离能比相邻的元素都大,同主族由上到下元素原子的第一电离能逐渐
减小,则N、O、S三种元素的第一电离能从大到小的顺序为N>O>S;N、O、S的氢化物分子都是有孤
对电子的角锥形分子。水和硫化氢有两对孤对电子,但是氧原子的电负性比硫原子大,氧原子对其携带的
两对孤对电子的吸引比硫原子大,相应的孤对电子斥力增大使键角也相应比硫化氢大,氨分子只有一对孤
对电子,排斥力比有两对孤对电子的情况小,所以键角比水和硫化氢都大,即键角大小氨>水>硫化氢,C
项正确;
D.铟( In)是一种金属元素,元素符号为In,原子序数为49,位于元素周期表第五周期ⅢA族,p区包括
49
第三主族到第七主族加上零族的元素,因此它位于p区,D项正确;
答案选A。
7.下列有关说法不正确的是( )
A.C H 中碳原子都采取的是sp3杂化
3 8
B.O、CO、N 都是非极性分子
2 2 2
C.酸性:HCO<HPO <HSO <HClO
2 3 3 4 2 4
D.SnCl 的空间结构为正四面体形
4
答案 C
解析 C H 分子中每个C原子含有4个σ键,所以每个C原子价层电子对数是4,采取sp3杂化,故A正确;
3 8
O 、N 都是以非极性键结合的双原子分子,一定为非极性分子,CO 中含有极性键,为直线形分子,结构
2 2 2
对称,为非极性分子,故B正确;非金属性:C<P<S<Cl,元素的非金属性越强,其最高价氧化物对应
水化物的酸性越强,HClO不是氯元素的最高价氧化物对应的水化物,则酸性:HClO <HCO,故C错误。
2 3
8.关于CH−N=N−CH、HNCH COOH和ONCH CH 的结构与性质,下列说法正确的是
3 3 2 2 2 2 3
A.CH−N=N−CH 有顺反异构现象
3 3
B.1mol ONCH CH 含有10mol σ键
2 2 3
C.三种物质中,氮原子杂化方式相同
D.在乙醇中溶解度,HNCH COOH低于ONCH CH,原因是前者与乙醇形成氢键
2 2 2 2 3
【答案】A
【解析】
A.CH−N=N−CH 中两个甲基可以在同一边,也可以在不同边,因此存在顺反异构现象,故A正确;
3 3
B.1个−CHCH 含有6个σ键,1个−NO 含有2个σ键,则1mol ON−CHCH 含有9mol σ键,故B错误;
2 3 2 2 2 3
C.三种物质中,CH−N=N−CH 中氮原子杂化方式为sp2杂化,HNCH COOH中氮原子杂化方式为sp3杂
3 3 2 2
化,ONCH CH 中氮原子杂化方式为sp2杂化,故C错误;
2 2 3
D.在乙醇中,HNCH COOH中HN−和−COOH能与乙醇形成分子间氢键,因此HNCH COOH溶解度高
2 2 2 2 2
于ONCH CH,故D错误。
2 2 3综上所述,答案为A。
9.通常情况下,NCl 是一种油状液体,其分子空间结构与NH 相似,下列对NCl 和NH 的有关叙述错误
3 3 3 3
的是( )
A.分子中N—Cl的键长与CCl 分子中C—Cl的键长不相等
4
B.NCl 分子是极性分子
3
C.NBr 比NCl 易挥发
3 3
D.在氨水中,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子,则NH ·H O的结构式为
3 2 3 2 3 2
答案 C
解析 C原子的原子半径大于N原子的原子半径,所以CCl 中C—Cl的键长比NCl 中N—Cl的键长长,
4 3
故A正确;NCl 分子的空间结构与氨分子相似,都是三角锥形,氨分子是极性分子,所以 NCl 分子也是
3 3
极性分子,故B正确;分子晶体中物质的熔、沸点与相对分子质量有关,相对分子质量越大其熔、沸点越
高,所以NBr 比NCl 的熔、沸点高,NCl 比NBr 易挥发,故C错误;在氨水中, NH 与HO以氢键(用
3 3 3 3 3 2
“…”表示)结合形成NH ·H O分子,则NH ·H O的结构式为 ,故D正确。
3 2 3 2
10.(2022·黄石市模拟)下列说法错误的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱与化学键强弱有关
B.三硫化磷(P S)分子结构如图: ,1 mol P S 分子中含有9 mol共价键
4 3 4 3
C.丙烯腈 分子中,碳原子的杂化方式有sp3、sp2
D.CO的结构可以表示为 ,所以CO分子中有一个π键是配位键
答案 C
解析 键能:H—F>H—Cl>H—Br>H—I,其热稳定性:HF>HCl>HBr>HI,A项正确;由题图可知,
1个PS 分子中有6个P—S、3个P—P共价键,则1 mol P S 分子中含有9 mol共价键,B项正确;由丙烯
4 3 4 3
腈的结构可知,碳原子的杂化方式有sp、sp2,C项错误。
11. 和 可反应生成乙二胺四乙酸( ),
ClCH COOH H NCH CH NH
2 2 2 2 2
乙二胺四乙酸与金属阳离子形成配合物的结构如图所示。已知含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。下列说法正确的是
A.H NCH CH NH 为非极性分子
2 2 2 2
B.ClCH COOH空间结构为平面形
2
C.H NCH CH NH 的沸点高于CH CH CH CH
2 2 2 2 3 2 2 3
D.1mol该配合物中通过螯合作用形成的配位键有4mol
【答案】C
【解析】A.H NCH CH NH 正负电荷中心不重合,属于极性分子,A项错误;
2 2 2 2
B.ClCH COOH中存在亚甲基,碳原子为sp3杂化,其空间结构不可能为平面形,B项错误;
2
C.H NCH CH NH 中存在氨基,分子之间会存在氢键,故其沸点高于CH CH CH CH ,C项正确;
2 2 2 2 3 2 2 3
D.含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物,由结构
图可知,1mol该配合物中通过螯合作用形成的配位键有6mol,D项错误;
答案选C。
12.硼砂阴离子 B 4 O 5 OH 4 2 的球棍模型如图所示,下列说法正确的是
A.B原子的杂化方式均为sp2
B.该阴离子中所存在的化学键类型有配位键、极性共价键、氢键
C.硼砂阴离子呈链状结构,则阴离子间以氢键结合
D.1、3原子之间的化学键为配位键
【答案】C
【解析】
A.形成4个B-O键的B原子杂化方式均为sp3,形成3个B-O键的B原子杂化方式均为sp2,故A错误;
B.氢键不是化学键,故B错误;
C.硼砂阴离子中含有O-H键,可以形成氢键,硼砂阴离子呈链状结构,阴离子间以氢键结合,故C正确;D.B原子一般形成3个共价键,1号B原子形成4个共价键,1、2原子之间的化学键为配位键,故D错
误;
选C。
13.C O 是一种无色无味的气体,结构式如图,可溶于水生成草酸:C O H O=HOOCCOOH。下列说
2 3 2 3 2
法正确的是
A.甲酸与草酸互为同系物
B.C O 是非极性分子
2 3
C.晶体溶点:草酸>冰>三氧化二碳>干冰
D.CO 、C O 和HOOCCOOH分子中碳原子的杂化方式均相同
2 2 3
【答案】C
【解析】A.同系物是结构相似,分子式相差若干个CH 的物质,甲酸(HCOOH)与草酸(HOOCCOOH)不符
2
合要求,不互为同系物,A错误;
B.由图可知C O 正负电中心不重合,是极性分子,B错误;
2 3
C.草酸、冰、三氧化二碳、干冰均是分子晶体,草酸分子间和HO分子间均能形成氢键,熔点会更高,
2
草酸形成的氢键数目更多,熔点在四者中最大,CO 相对分子质量比C O 低,熔点也低于C O ,所以四
2 2 3 2 3
者熔点大小为:草酸>冰>三氧化二碳>干冰,C正确;
D.CO 中碳原子的杂化方式为sp杂化,C O 中碳原子的杂化方式为sp2杂化, HOOCCOOH分子中碳原
2 2 3
子的杂化方式为sp2杂化,杂化方式不全部相同,D错误;
答案选C。
14.硅及其化合物广泛应用于光电材料领域,其中SiCl 与N-甲基咪唑( )反应可以得到M2+,
4
其结构如图所示。下列叙述错误的是
A.SiCl 的空间构型为正四面体
4
B.1个M2+中含有42个σ键。
C.H、C、N的电负性由大到小的顺序为N>C>H
D.N-甲基咪唑分子中碳原子的杂化轨道类型为sp2、sp3
【答案】B【解析】
A.SiCl 分子中Si形成4个σ键,且不存在孤电子对,其结构与甲烷相似,空间构型是正四面体,A正确;
4
B.共价单键为σ键、共价双键中含有1个σ键、1个π键,配位键为σ键,则 中含有12个
σ键,所以1个 中含有12×4+6=54个σ键,则1mol该物质中含有
54molσ键,B错误;
C.根据同一周期从左往右元素的电负性依次增强,同一主族从上往下依次减弱,故H、C、N的电负性由
大到小的顺序为N>C>H,C增强;
D.由题干信息可知,N-甲基咪唑分子中存在甲基和碳碳双键,故碳原子的杂化轨道类型为sp2、sp3,D正
确;
故答案为:B。
15.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。如图中原子1
的坐标为(,,),则原子2和3的坐标正确的是( )
A.原子2为(,0,) B.原子2为(0,,)
C.原子3为(1,0,) D.原子3为(0,0,)
答案 D
16.已知NiMg O晶体属立方晶系,晶胞边长a。将Li+掺杂到该晶胞中,可得到一种高性能的p型太阳
x 1-x
能电池材料,其结构单元如图所示。假定掺杂后的晶胞参数不发生变化,下列说法正确的是( )
A.该结构单元中O原子数为3
B.Ni和Mg间的最短距离是a
C.Ni的配位数为4
D.该物质的化学式为Li.Mg. Ni . O
05 112 238 4
答案 B解析 O原子数为12×+1=4,A错误;由图可知,Ni与Mg的最短距离为晶胞面对角线的,即=a,B正
确;由晶胞结构可知,Ni的配位数为6,C错误;晶胞中各微粒的个数为N(Li)=1×=0.5,N(Mg)=1×+2×
=1.125,N(Ni)=7×+3×=2.375,N(O)=4,因此该物质的化学式为Li.Mg. Ni . O,D错误。
05 1125 2375 4
17.我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构如图。下列说法正确的是( )
A.11BN和10BN的性质无差异
B.该晶体具有良好的导电性
C.该晶胞中含有14个B原子,4个N原子
D.N原子周围等距且最近的N原子数为12
答案 D
解析 11B和10B互为同位素,形成的化合物在化学性质上无差异,但其物理性质不同,A错误;该晶体结
构中无自由移动的电子,不具有导电性,B错误;由图可知,该晶胞含4个N原子,B原子位于晶胞的顶
点和面心上,故B原子的数量为8×+6×=4个,C错误;由晶胞示意图,1个N原子与4个B原子成键,1
个B原子可以和3个N原子成键,这些N原子距中心N原子等距且最近,总数为12个,D正确。
18.近日,科学家研究利用CaF 晶体释放出的Ca2+和F-脱除硅烷,拓展了金属氟化物材料的生物医学功能。
2
下列说法错误的是
A.F、Si和Ca,原子半径依次增大
B.SiO 与OF 的晶体类型及氧原子的杂化方式均相同
2 2
1 1 3
C.图中A处原子分数坐标为(0,0,0),则B处原子分数坐标为( , , )
4 4 4
D.脱除硅烷反应速率依赖于晶体提供自由氟离子的能力,脱硅能力BaF <CaF <MgF
2 2 2
【答案】BD
【解析】A.同周期元素,从左到右原子半径依次减小,同主族元素从上到下,原子半径依次增大,则
F、Si和Ca原子半径依次增大,故A正确;
B.OF 与 SiO 都是含有极性共价键的共价化合物,化合物中氧原子的价层电子对数都为4,杂化方式都
2 2
为sp3杂化,OF 为分子晶体、 SiO 为共价晶体,故B错误;
2 2
3
C.由晶胞结构可知,A处到B处的距离为体对角线的 ,若A处原子分数坐标为(0,0,0),则B 处原子
43 3 3
分数坐标为 , , ,故C正确;
4 4 4
D.三种金属氟化物都为离子晶体,晶体提供自由氟离子的能力越强,阴阳离子间形成的离子键越弱,钡
离子、钙离子和镁离子的电荷数相同,离子半径依次减小,则氟化钡、氟化钙、氟化镁三种晶体中的离子
键依次增强,晶体提供自由氟离子的能力依次减弱,故D错误;
故选BD。
19.X、Y为第二周期相邻的两种元素,X的最高正价与最低负价代数和为2,二者形成的固态化合物以
XY +XY - 的形式存在,下列说法错误的是
2 3
A.原子半径:X>Y
B.X、Y均属于p区元素
C.X、Y的第一电离能:XO即X>Y,A正确;
B.N的电子排布式为:1s22s22p3,O的电子排布式为:1s22s22p4,故X、Y均属于p区元素,B正确;
C.由分析可知,X为N,Y为O,根据第一电离能从左往右呈增大趋势,VA与VIA反常,则X、Y的第
一电离能:X>Y,C错误;
D.由分析可知,X为N,Y为O,非金属性N