文档内容
高频考点 51 化学实验方案的设计与评价
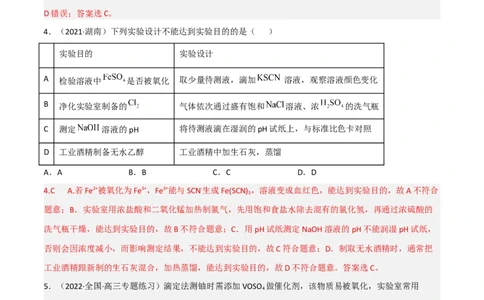
1.(2022·江苏卷)室温下,下列实验探究方案不能达到探究目的的是 ( )
选
探究方案 探究目的
项
向盛有 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新制
A 具有还原性
氯水,观察溶液颜色变化
向盛有 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察溶
B 具有漂白性
液颜色变化
C 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 的氧化性比 的强
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 是弱电解质
A.A B.B C.C D.D
1.D A.向盛有 溶液的试管中滴加几滴 溶液,无现象,振荡,再滴加几滴新制氯水,溶液变
为红色,亚铁离子被新制氯水氧化,说明 具有还原性,A正确; B.向盛有 水溶液的试管中滴加
几滴品红溶液,品红溶液褪色,振荡,加热试管,溶液又恢复红色,说明 具有漂白性, B正确;C.
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,溶液变为蓝色,说明 的氧化性比 的强,C正确;
D.用pH计测量醋酸、盐酸的pH用以证明 是弱电解质时,一定要注明醋酸和盐酸的物质的量
浓度相同,D错误。故选D。
2.(2021·山东)下列由实验现象所得结论错误的是( )
A.向NaHSO 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性
3
B.向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,证明Fe O 中含Fe(Ⅱ)
4 3 4 3 4
C.向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
2.C A.淡黄色沉淀是S,在反应过程中硫元素由NaHSO 中的+4价降低到0价,发生还原反应, 体
3现氧化性,A项不符合题意;B.酸性高锰酸钾溶液具有强氧化性,与还原性物质反应紫色才会褪去,所以
可以证明Fe O 中有还原性物质,即Fe(Ⅱ),B项不符合题意;C.在该反应中浓硝酸体现氧化性,N元素化
3 4
合价降低,生成的产物可能是NO或者NO ,NO暴露于空气中也会迅速产生红棕色气体,无法证明反应产
2
物,C项符合题意;D.先变红说明溶液显碱性,证明NaClO在溶液中发生了水解,
,后来褪色,是因为水解产生了漂白性物质HClO,D项不符合题意;故选
C。
3.(2021·江苏卷)室温下,通过下列实验探究NaHCO 、Na CO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol·L-1NaHCO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向0.1mol·L-1Na CO 溶液中通入CO ,溶液pH从12下降到约为9
2 3 2
实验4:向0.1mol·L-1Na CO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是()
A.由实验1可得出:K (H CO )>
a2 2 3
B.实验2中两溶液混合时有:c(Ca2+)·c(CO ) HY,故B项错误;C. 无论蔗糖部分水解还是完全水解,都会
产生还原糖,实验现象相同,故C项错误;D. CuS不溶解,说明CuS更难溶,因此K (ZnS) > K (CuS),故D
sp sp
项正确;故答案选D。
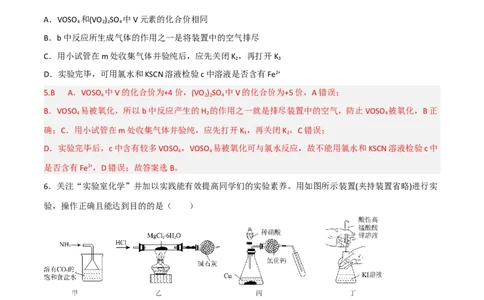
8.为实现下列实验目的,橙子辅导小组的成员们实验操作和实验现象都正确的是()
选
实验目的 实验操作 实验现象
项
证明金属性
A 少量金属Na与胆矾隔绝空气加热 有红色固体生成
Na>Cu
常温下,溶度 常温下,向盛有2滴 溶液的试管
先有白色沉淀生成,后又产
积:
B 中滴加1mL NaCl溶液,再向其中滴加
生黄色沉淀
1mL KI溶液
注射器内气体颜色加深,证
验证压强对化学
C 先将注射器充满 气体,然后将活塞往里推 明加压平衡朝生成 气体
平衡的影响
的方向移动
证明浓硫酸具有
D
强氧化性
加热浓硫酸、NaCl固体与 固体的混合物 有黄绿色气体产生A.A B.B C.C D.D
8.B A.Na性质活泼,与胆矾的结晶水反应,少量金属Na与胆矾隔绝空气加热,生成氢氧化钠和氢气,
不能得到铜,故A错误;B.向盛有2滴 0.1mol/LAgNO 溶液的试管中滴加1mL 0.1mol/LNaCl溶液,先有白
3
色AgCl沉淀生成,溶液中氯离子过量,再向其中滴1mL0.1mol/LKI溶液,Ag+与I-结合产生黄色沉淀AgI,实
现沉淀转化,可得出K (AgCl)>K (AgI),故B正确;C.先将注射器充满NO 气体,然后将活塞往里
sp sp 2
推压缩体积,观察到注射器内气体颜色先加深,后又变浅,但比开始时颜色深,先是由于体积减小,颜色
加深,后因平衡移动,颜色变浅,故C错误;D.加热浓硫酸、NaCl固体与 固体的混合物有黄绿色气
体产生,是因为浓硫酸和NaCl反应生成的HCl和MnO 反应生成Cl ,不能验证浓硫酸的强氧化性,体现了
2 2
非挥发性的浓硫酸制取挥发性酸的性质,故D错误;答案选B。
9.(双选)(2022·河南郑州·三模)海带中含有丰富的碘元素,某化学兴趣小组设计的海带提碘实验流程如
下图,下列说法中正确的是( )
A.上述流程中各步操作用到的仪器包括:
B.“氧化”时,试剂可选用O 、H O 或Br
2 2 2 2
C.上述流程包括三个氧化还原反应和三种分离操作
D.“反萃取”时,反应的离子方程式为I +2OH-=I-+IO +H O
2 2
9. AD A.上述流程中灼烧用到坩埚,萃取分液用到分液漏斗,蒸馏用到直形冷凝管和蒸馏烧瓶,过滤用
到漏斗,A正确;B.氧化过程将碘离子变成碘单质,可选用的氧化剂为O 、H O ,选Br 会引入杂质,B
2 2 2 2
错误;C.该过程中海带灼烧、氧化过程碘离子氧化成碘单质、反萃取过程中碘单质与氢氧化钠溶液反应、
酸化分离过程中生成碘单质,共4个氧化还原反应;涉及到过滤、分液、蒸馏三种分离操作,C错误;D.
根据分析,反萃取时反应的离子方程式为:I +2OH-=I-+IO-+H O,D错误;故选A D。
2 2
10.某研究性学习小组通过下列实验验证AgI沉淀的生成会使I 的氧化能力增强,可将Fe2+氧化。
2回答下列问题:
(1)由AgNO 固体配制0.1 mol·L-1的AgNO 溶液50 mL,配制好的溶液应转移到_______试剂瓶中保存。
3 3
(2)步骤1的实验现象是_______;步骤2无明显现象;步骤3最终的实验现象是溶液中生成黄色沉淀,
_______。由此可知,步骤3反应的离子方程式为_______。
(3)某同学在实验时漏掉步骤2,直接加入过量AgNO 溶液,也观察到与步骤3相同的实验现象。该同学推
3
测溶液中还有碘的离子_______(填离子符号)生成,并由此对I 氧化Fe2+产生了质疑。
2
(4)为了确证AgI的生成使I 的氧化能力增强而将Fe2+氧化,学习小组在上述实验基础上进行补充实验:分别
2
取少量的_______和步骤3试管中的上层清液于试管a和试管b中,往两支试管中加入过量的_______,观
察到的现象为_______。
10. (1)棕色细口
(2) 溶液显蓝色 蓝色褪去,溶液显黄色 2Fe2++I +2Ag+=2Fe3++2AgI↓
2
(3)
(4) 步骤2 NaOH溶液 试管a中蓝色褪去,先出现白色沉淀,白色沉淀迅速变为灰绿色,最
后变为红褐色;试管b中有白色沉淀(转变为褐色沉淀)和红褐色沉淀
解析:(1)硝酸银见光易分解,故配制好的溶液应转移到棕色细口瓶中保存。
(2)步骤1中碘水遇淀粉溶液,现象是溶液变蓝;步骤2再加入硫酸亚铁铵溶液,无明显现象,则说明亚
铁离子和碘水不发生反应;步骤3最终的实验现象是溶液中生成黄色沉淀,黄色沉淀为AgI,则碘分子中碘
化合价降低,溶液中发生氧化还原反应,碘作氧化剂,亚铁离子为还原剂,氧化产物为铁离子,故反应中
还有另一个现象——溶液蓝色褪去。由此可知,步骤3反应的离子方程式为I +2Fe2++2Ag+=2AgI↓+2Fe3+。
2
(3)实验时漏掉步骤2,直接加入过量AgNO 溶液,也观察到产生黄色沉淀AgI,说明溶液中同时存在碘
3
单质、碘离子,则有I +I- ,故推测溶液中还有碘的离子 生成。
2
(4)由于步骤2的溶液中有亚铁离子而没有铁离子,要确证AgI的生成使I 的氧化能力增强而将Fe2+氧化,
2
只要证明步骤3的溶液中存在氧化产物铁离子即可,由实验知,步骤2溶液中有碘与淀粉混合液和亚铁离
子,步骤3中加入了过量的硝酸银溶液,则上层清液中银离子与铁离子共存,所以可以用氢氧化钠溶液进行鉴别,学习小组在上述实验基础上进行补充实验:分别取少量的步骤2中的溶液和步骤3试管中的上层
清液于试管a和试管b中,往两支试管中加入过量的氢氧化钠溶液,试管a中,过量的氢氧化钠溶液消耗
了碘使之褪色,与亚铁离子反应产生氢氧化亚铁,氢氧化亚铁最终氧化为氢氧化铁,试管b中,过量的氢
氧化钠溶液与银离子反应生成白色沉淀氢氧化银(可以分解为褐色沉淀氧化银)、又与铁离子反应生成红褐
色沉淀。
11.绿矾(FeSO ·xH O)是生血片的主要成分。某研究性学习小组拟对绿矾的热分解产物进行探究。
4 2
实验猜想
猜想1:生成Fe O 、SO 、H O;
2 3 2 2
猜想2:生成Fe、Fe O 、SO 、H O;
2 3 2 2
猜想3:生成Fe O 、SO 、SO 、H O;
2 3 2 3 2
……
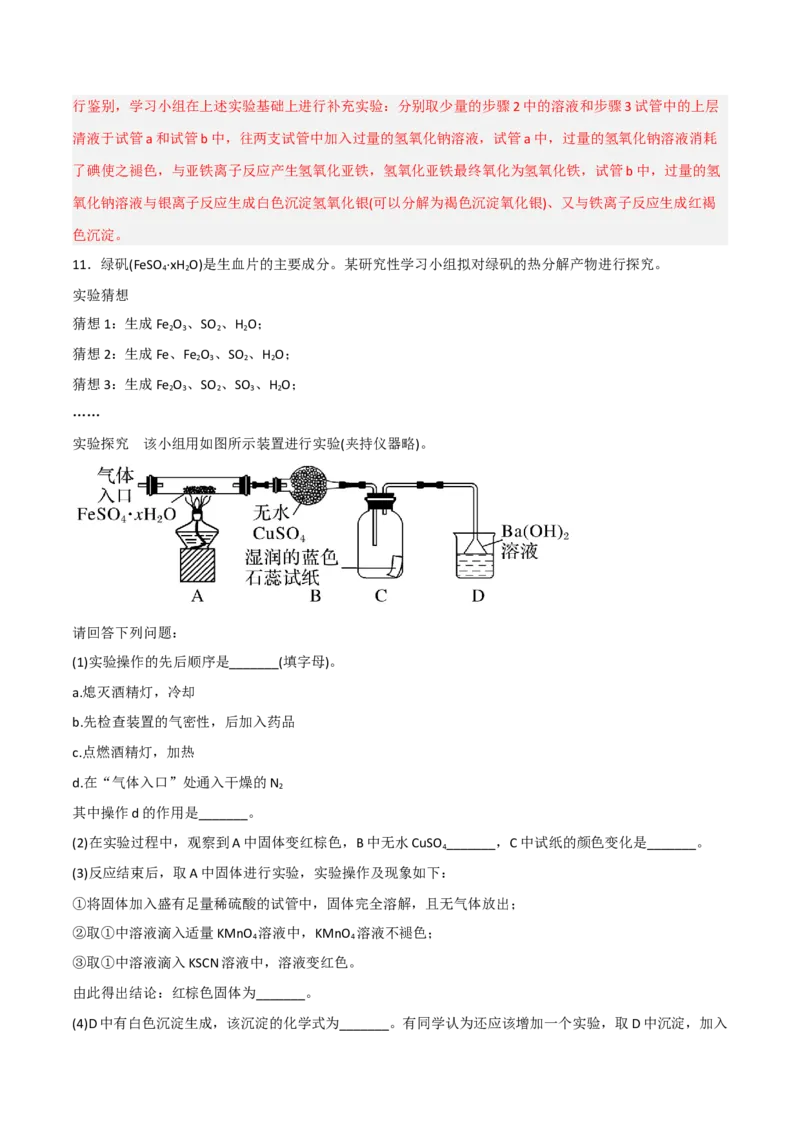
实验探究 该小组用如图所示装置进行实验(夹持仪器略)。
请回答下列问题:
(1)实验操作的先后顺序是_______(填字母)。
a.熄灭酒精灯,冷却
b.先检查装置的气密性,后加入药品
c.点燃酒精灯,加热
d.在“气体入口”处通入干燥的N
2
其中操作d的作用是_______。
(2)在实验过程中,观察到A中固体变红棕色,B中无水CuSO _______,C中试纸的颜色变化是_______。
4
(3)反应结束后,取A中固体进行实验,实验操作及现象如下:
①将固体加入盛有足量稀硫酸的试管中,固体完全溶解,且无气体放出;
②取①中溶液滴入适量KMnO 溶液中,KMnO 溶液不褪色;
4 4
③取①中溶液滴入KSCN溶液中,溶液变红色。
由此得出结论:红棕色固体为_______。
(4)D中有白色沉淀生成,该沉淀的化学式为_______。有同学认为还应该增加一个实验,取D中沉淀,加入一定量的盐酸以确定其组成,从而确定FeSO ·xH O的分解产物,你认为是否需要?说明你的理由:
4 2
_______。
实验结论
(5)硫酸亚铁晶体加热分解的化学方程式为_______。
11 .(1) bdca 排净装置内的空气,防止Fe2+被空气中的氧气氧化而干扰实验
(2) 由白色变蓝色 蓝色变红色
(3)Fe O
2 3
(4) BaSO 、BaSO 不需要;Fe元素的化合价升高,则必有S元素的化合价降低,根据原子守恒和得失
4 3
电子守恒可知,只有部分S元素的化合价降低,则进入D中的气体为SO 和SO
3 2
(5)2(FeSO ·xH O) Fe O +SO ↑+SO ↑+2xH O
4 2 2 3 2 3 2
解析:(1)该实验探究有气体生成,故首先应检查装置的气密性;Fe2+具有还原性,易被空气中的氧气氧
化,影响探究结果,故应在“气体入口”处通入干燥的N ,排净装置内的空气;然后点燃酒精灯,对样品
2
进行加热,实验结束后,熄灭酒精灯,进行冷却,故实验操作的先后顺序是bdca。
(2)加热时,FeSO ·xH O首先会失去结晶水,然后FeSO 分解。B中无水CuSO 用于检验水的生成,吸水
4 2 4 4
后固体由白色变成蓝色;C中收集到酸性气体,该气体会使湿润的蓝色石蕊试纸变红。
(3)由实验①可知,没有气体放出,可能的原因有两个:一是反应后的固体中没有单质Fe,二是固体中
有单质Fe与Fe O ,二者发生反应生成Fe2+;由实验②可知,溶液中不存在Fe2+,则可知反应后的固体中没
2 3
有单质Fe;由实验③和固体颜色可知,反应后的固体应为Fe O 。
2 3
(4)由(3)可知,Fe元素的化合价升高,则必有S元素的化合价降低,根据原子守恒和得失电子守恒可知,
只有部分S元素的化合价降低,从而可知进入D中的气体为SO 和SO ,因此D中的白色沉淀为BaSO 和
3 2 4
BaSO ,不需要再经过实验验证。
3
(5)由上述分析可知,产物为H O、Fe O 、SO 和SO ,则反应的化学方程式为2(FeSO ·xH O)
2 2 3 2 3 4 2
Fe O +SO ↑+SO ↑+2xH O。
2 3 2 3 2