文档内容
微考点 5 离子方程式的正误判断和书写
题点(一) 离子方程式的正误判断
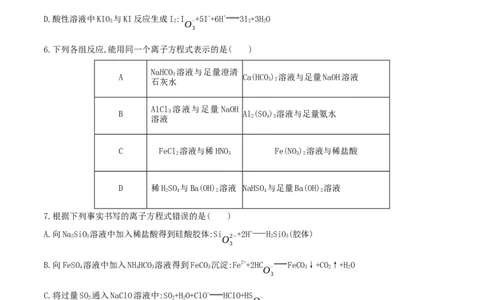
1.(2022·全国甲卷)能正确表示下列反应的离子方程式为( )
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO ↓+2H O
2 4 4 4 2
2.(双选)(2022·湖南)下列离子方程式正确的是( )
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
3.(2022·广东卷)下列关于 的化合物之间转化反应的离子方程式书写正确的是( )
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
4. (2022·潍坊高三期中)下列离子方程式正确的是( )
A.用醋酸除水垢: CaCO+2H+ Ca2++HO+CO↑
3 2 2
B.用小苏打治疗胃酸过多: HC +H+ CO↑+HO
O- 2 2
3C.向溴化亚铁溶液中通入足量氯气: 2Br-+Cl Br+2Cl-
2 2
D.向澄清石灰水中通入过量二氧化碳: Ca2++2OH-+CO CaCO↓+HO
2 3 2
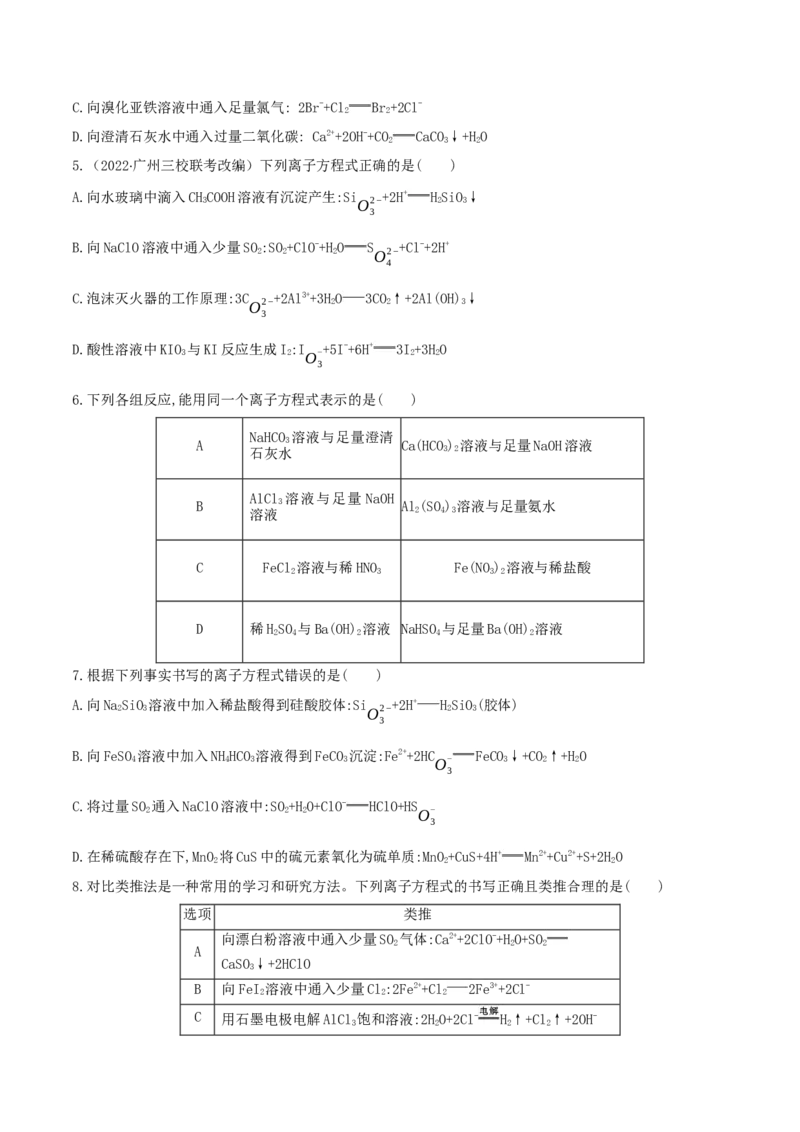
5.(2022·广州三校联考改编)下列离子方程式正确的是( )
A.向水玻璃中滴入CHCOOH溶液有沉淀产生:Si +2H+ HSiO↓
3 O2− 2 3
3
B.向NaClO溶液中通入少量SO:SO+ClO-+HO S +Cl-+2H+
2 2 2 O2−
4
C.泡沫灭火器的工作原理:3C +2Al3++3HO 3CO↑+2Al(OH)↓
O2− 2 2 3
3
D.酸性溶液中KIO 与KI反应生成I:I +5I-+6H+ 3I+3HO
3 2 O- 2 2
3
6.下列各组反应,能用同一个离子方程式表示的是( )
NaHCO 溶液与足量澄清
A 3 Ca(HCO) 溶液与足量NaOH溶液
石灰水 3 2
AlCl 溶液与足量 NaOH
B 3 Al(SO) 溶液与足量氨水
溶液 2 4 3
C FeCl 溶液与稀HNO Fe(NO) 溶液与稀盐酸
2 3 3 2
D 稀HSO 与Ba(OH) 溶液 NaHSO 与足量Ba(OH) 溶液
2 4 2 4 2
7.根据下列事实书写的离子方程式错误的是( )
A.向NaSiO 溶液中加入稀盐酸得到硅酸胶体:Si +2H+ HSiO(胶体)
2 3 O2− 2 3
3
B.向FeSO 溶液中加入NHHCO 溶液得到FeCO 沉淀:Fe2++2HC FeCO↓+CO↑+HO
4 4 3 3 O- 3 2 2
3
C.将过量SO 通入NaClO溶液中:SO+HO+ClO- HClO+HS
2 2 2 O-
3
D.在稀硫酸存在下,MnO 将CuS中的硫元素氧化为硫单质:MnO+CuS+4H+ Mn2++Cu2++S+2HO
2 2 2
8.对比类推法是一种常用的学习和研究方法。下列离子方程式的书写正确且类推合理的是( )
选项 类推
向漂白粉溶液中通入少量SO 气体:Ca2++2ClO-+HO+SO
2 2 2
A
CaSO↓+2HClO
3
B 向FeI 溶液中通入少量Cl:2Fe2++Cl 2Fe3++2Cl-
2 2 2
C 用石墨电极电解AlCl 饱和溶液:2HO+2Cl- H↑+Cl↑+2OH-
3 2 2 2D 硫酸铁净水:Fe3++3HO Fe(OH)(胶体)+3H+
2 3
题点(二)离子方程式的书写
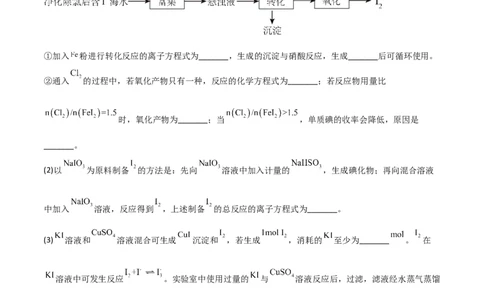
9.(2021·全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______后可循环使用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量比
时,氧化产物为_______;当 ,单质碘的收率会降低,原因是
_______。
(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再向混合溶液
中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_______。
(3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为_______ 。 在
溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水蒸气蒸馏
可制得高纯碘。反应中加入过量 的原因是_______。
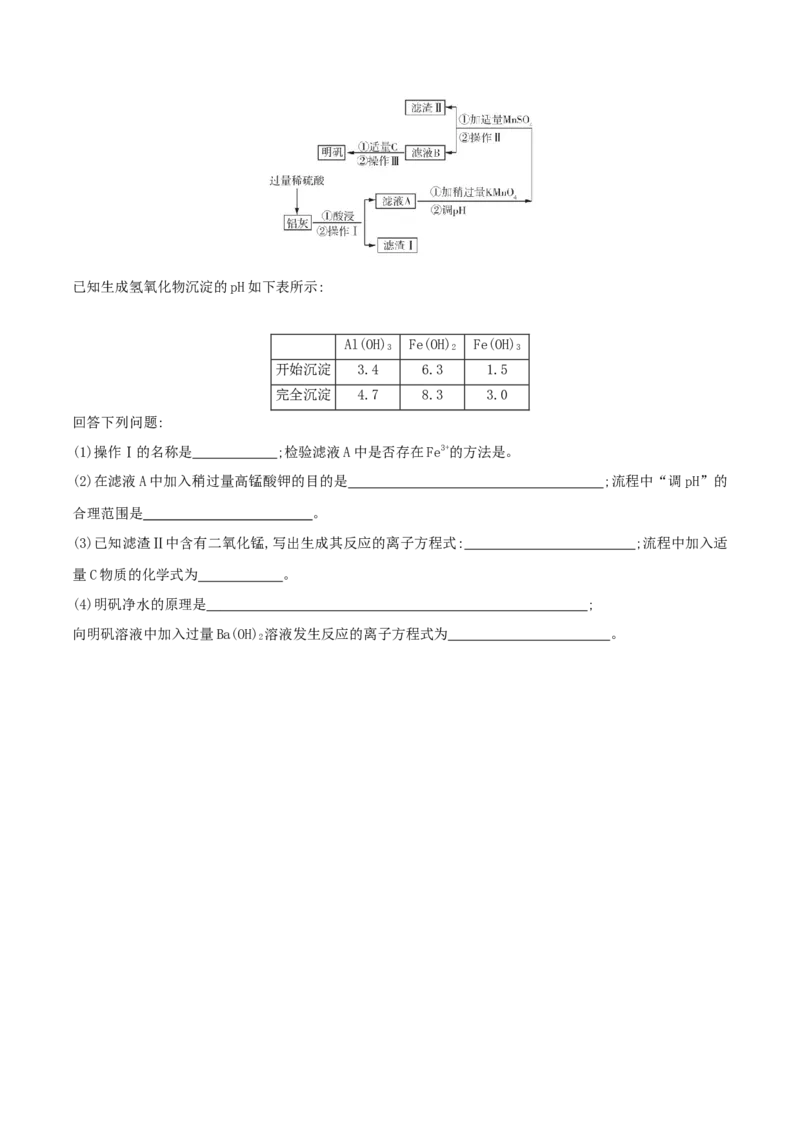
10.(2022·洛阳一中高三月考)明矾[KAl(SO)·12HO]在生产、生活中有广泛用途,利用炼铝厂的废料
4 2 2
——铝灰(含Al、AlO 及少量SiO 和FeO·xFeO)可制备明矾。工艺流程如下:
2 3 2 2 3已知生成氢氧化物沉淀的pH如下表所示:
Al(OH) Fe(OH) Fe(OH)
3 2 3
开始沉淀 3.4 6.3 1.5
完全沉淀 4.7 8.3 3.0
回答下列问题:
(1)操作Ⅰ的名称是 ;检验滤液A中是否存在Fe3+的方法是。
(2)在滤液A中加入稍过量高锰酸钾的目的是 ;流程中“调pH”的
合理范围是 。
(3)已知滤渣Ⅱ中含有二氧化锰,写出生成其反应的离子方程式: ;流程中加入适
量C物质的化学式为 。
(4)明矾净水的原理是 ;
向明矾溶液中加入过量Ba(OH) 溶液发生反应的离子方程式为 。
2